Ar-NHR-11.ppt
- Количество слайдов: 8
 АРОМАТИЧНІ АМІНИ - сполуки, в молекулах яких міститься аміногрупа, безпосередньо сполучена з атомом Карбону ароматичного ядра. Ароматичні аміни похідні амоніаку. За кількістю заміщених атомів Гідрогену в молекулі амоніаку їх поділяють на первинні (Ar–NH 2), вторинні (Аr–NH–Ar) і третинні (Ar 3 N, де Ar – ароматичний радикал, наприклад C 6 H 5– -феніл, о-, м-, п-СН 3–C 6 H 4– -о-, м-, п-толіл і т. д. ). Найпростішим первинним ароматичним аміном є анілін C 6 H 5–NH 2, вторинним – дифеніламін (C 6 H 5)2 NH, третинним – трифеніламін (C 6 H 5)3 N. Жирно-ароматичні аміни метиланілін C 6 H 5–NH–CH 3, диметиланілін C 6 H 5–N(CH 3)2. Крім того, відомі аміни з аміногрупою в бічному ланцюгу, наприклад бензиламін C 6 H 5–CH 2–NH 2. Номенклатура. За систематичною номенклатурою назви ариламінів утворюють від слова „анілін” (традиційна назва). Нумерацію атомів Карбону в ядрі починають з атома С, сполученого з NRR 1. Для жирно-ароматичних амінів перелік алкільних замісників у назві здійснюють за алфавітом, наприклад, 3 -етил-5 -метиланілін (І). Назви ароматичних ді- та триамінів утворюють від слова „бензен” шляхом додавання суфікса –амін з відповідними множними префіксами за принципом найменших локантів, наприклад бензен-1, 3 -діамін (ІІ), 4 -етил-5 -метилбензен-1, 2 -діамін (ІІІ), або 3 -метил-6 -пропілбензен-1, 2, 4 -триамін (IV): За IUPAC (1993 р. ) анілін може мати назви фенілазан і феніламін, (С 6 Н 5)2 NH дифеніламін або дифенілазан, (С 6 Н 5)3 N – трифеніламін або трифенілазан. Тривіальні назви - анілін, о-, м-, і п-толуїдини тощо). Ізомерія - структурна (орто-, мета- і пара-ізомери), положення аміногрупи в ядрі або в бічному ланцюгу, положення алкільного радикала в ядрі N:
АРОМАТИЧНІ АМІНИ - сполуки, в молекулах яких міститься аміногрупа, безпосередньо сполучена з атомом Карбону ароматичного ядра. Ароматичні аміни похідні амоніаку. За кількістю заміщених атомів Гідрогену в молекулі амоніаку їх поділяють на первинні (Ar–NH 2), вторинні (Аr–NH–Ar) і третинні (Ar 3 N, де Ar – ароматичний радикал, наприклад C 6 H 5– -феніл, о-, м-, п-СН 3–C 6 H 4– -о-, м-, п-толіл і т. д. ). Найпростішим первинним ароматичним аміном є анілін C 6 H 5–NH 2, вторинним – дифеніламін (C 6 H 5)2 NH, третинним – трифеніламін (C 6 H 5)3 N. Жирно-ароматичні аміни метиланілін C 6 H 5–NH–CH 3, диметиланілін C 6 H 5–N(CH 3)2. Крім того, відомі аміни з аміногрупою в бічному ланцюгу, наприклад бензиламін C 6 H 5–CH 2–NH 2. Номенклатура. За систематичною номенклатурою назви ариламінів утворюють від слова „анілін” (традиційна назва). Нумерацію атомів Карбону в ядрі починають з атома С, сполученого з NRR 1. Для жирно-ароматичних амінів перелік алкільних замісників у назві здійснюють за алфавітом, наприклад, 3 -етил-5 -метиланілін (І). Назви ароматичних ді- та триамінів утворюють від слова „бензен” шляхом додавання суфікса –амін з відповідними множними префіксами за принципом найменших локантів, наприклад бензен-1, 3 -діамін (ІІ), 4 -етил-5 -метилбензен-1, 2 -діамін (ІІІ), або 3 -метил-6 -пропілбензен-1, 2, 4 -триамін (IV): За IUPAC (1993 р. ) анілін може мати назви фенілазан і феніламін, (С 6 Н 5)2 NH дифеніламін або дифенілазан, (С 6 Н 5)3 N – трифеніламін або трифенілазан. Тривіальні назви - анілін, о-, м-, і п-толуїдини тощо). Ізомерія - структурна (орто-, мета- і пара-ізомери), положення аміногрупи в ядрі або в бічному ланцюгу, положення алкільного радикала в ядрі N:
 Методи добування. 1. Відновленням ароматичних нітросполук сульфідом амонію (M. M. Зінін, 1842 р. ): C 6 H 5–NO 2 + 3(NH 4)2 S → C 6 H 5–NH 2 + 2 H 2 O + 6 NH 3 +3 S. Відновлення ароматичних нітросполук можна здійснювати і залізом (стружками або ошурками) в хлоридній кислоті за наступною схемою: 2. Амонолізом галогенопохідних аренів (O. M. Енгельгардт, П. O. Лачинов, 1870 р. ). У сучасних промислових установках реакцію ведуть з надлишком амоніаку, за Т 180– 200 °С Р до 1 МПа і за наявності мідних каталізаторів: Орто- і пара-нітрохлорбензени взаємодіють з амоніаком значно легше, ніж хлорбензен, оскільки нітрогрупа підвищує реакційну здатність атома хлору. Фізичні властивості. Ариламіни – рідини або тверді речовини з характерним неприємним запахом, мало розчинні у воді. Ариламіни мають сильну фізіологічну дію на організм людини – є дуже отруйними. Електронна будова молекули аніліну. Середнє значення валентного кута атома Нітрогену досягає 120° (перебуває в sp 2 -гібридизованому стані. Тому аміногрупа в молекулі ароматичних амінів набуває плоскої конфігурації. Атом Нітрогену в молекулі аніліну дві свої sp 2 -орбіталі використовує на утворення двох σ-зв’язків з s-орбіталями двох атомів Гідрогену, а третю sp 2 -орбіталь – на утворення σзв’язку з sp 2 -гібридизованим атомом Карбону бензенового ядра. Четверта sp 2 -орбіталь амінного Нітрогену зайнята вільною парою електронів.
Методи добування. 1. Відновленням ароматичних нітросполук сульфідом амонію (M. M. Зінін, 1842 р. ): C 6 H 5–NO 2 + 3(NH 4)2 S → C 6 H 5–NH 2 + 2 H 2 O + 6 NH 3 +3 S. Відновлення ароматичних нітросполук можна здійснювати і залізом (стружками або ошурками) в хлоридній кислоті за наступною схемою: 2. Амонолізом галогенопохідних аренів (O. M. Енгельгардт, П. O. Лачинов, 1870 р. ). У сучасних промислових установках реакцію ведуть з надлишком амоніаку, за Т 180– 200 °С Р до 1 МПа і за наявності мідних каталізаторів: Орто- і пара-нітрохлорбензени взаємодіють з амоніаком значно легше, ніж хлорбензен, оскільки нітрогрупа підвищує реакційну здатність атома хлору. Фізичні властивості. Ариламіни – рідини або тверді речовини з характерним неприємним запахом, мало розчинні у воді. Ариламіни мають сильну фізіологічну дію на організм людини – є дуже отруйними. Електронна будова молекули аніліну. Середнє значення валентного кута атома Нітрогену досягає 120° (перебуває в sp 2 -гібридизованому стані. Тому аміногрупа в молекулі ароматичних амінів набуває плоскої конфігурації. Атом Нітрогену в молекулі аніліну дві свої sp 2 -орбіталі використовує на утворення двох σ-зв’язків з s-орбіталями двох атомів Гідрогену, а третю sp 2 -орбіталь – на утворення σзв’язку з sp 2 -гібридизованим атомом Карбону бензенового ядра. Четверта sp 2 -орбіталь амінного Нітрогену зайнята вільною парою електронів.
 У молекулі аніліну аміногрупа впливає на Ar ядро, а воно – на аміногрупу у вигляді двох електронних ефектів: аміногрупа виявляє –I-ефект і +М-ефект, який значно сильніший від її –I-ефекту. У зв’язку із спряженням електронна густина на атомі Нітрогену в молекулі ароматичних амінів зменшується. Внаслідок цього зменшується здатність N приєднувати протони і основні властивості ариламінів порівняно з NH 3 значно послаблюються, але за рахунок +M-ефекту аміногрупи підвищується електронна густина Ar ядра ариламінів в орто- і пара-положеннях і підвищується його активність до реакцій електрофільного заміщення. Хімічні властивості. Реакції за участі аміногрупи. 1. Кислотно-основні властивості. Ароматичні аміни виявляють основні властивості, оскільки в них на атомі Нітрогену аміногрупи є вільна пара електронів. За основністю ароматичні аміни можна розмістити в наступний ряд: NH 3 > C 6 H 5–N(Alk)2 > C 6 H 5–NHAlk > C 6 H 5–NH 2 > (C 6 H 5) 2 NH > (C 6 H 5)3 N. Отже, чим більше атомів Гідрогену у молекулі амоніаку заміщено на бензенові ядра, тим нижча основність такого ароматичного аміну. Основні властивості ароматичних амінів виявляються в реакціях з сильними кислотами, з якими вони утворюють солі. Так, анілін з хлоридною кислотою утворює легко розчинну у воді сіль – анілінгідрогенхлорид: Солі ароматичних амінів легко гідролізуються водою. Тому їх водні розчини мають кислу реакцію: Зі слабкими кислотами ароматичні аміни солей не утворюють, що свідчить про послаблення основних властивостей ароматичних амінів порівняно з амоніаком.
У молекулі аніліну аміногрупа впливає на Ar ядро, а воно – на аміногрупу у вигляді двох електронних ефектів: аміногрупа виявляє –I-ефект і +М-ефект, який значно сильніший від її –I-ефекту. У зв’язку із спряженням електронна густина на атомі Нітрогену в молекулі ароматичних амінів зменшується. Внаслідок цього зменшується здатність N приєднувати протони і основні властивості ариламінів порівняно з NH 3 значно послаблюються, але за рахунок +M-ефекту аміногрупи підвищується електронна густина Ar ядра ариламінів в орто- і пара-положеннях і підвищується його активність до реакцій електрофільного заміщення. Хімічні властивості. Реакції за участі аміногрупи. 1. Кислотно-основні властивості. Ароматичні аміни виявляють основні властивості, оскільки в них на атомі Нітрогену аміногрупи є вільна пара електронів. За основністю ароматичні аміни можна розмістити в наступний ряд: NH 3 > C 6 H 5–N(Alk)2 > C 6 H 5–NHAlk > C 6 H 5–NH 2 > (C 6 H 5) 2 NH > (C 6 H 5)3 N. Отже, чим більше атомів Гідрогену у молекулі амоніаку заміщено на бензенові ядра, тим нижча основність такого ароматичного аміну. Основні властивості ароматичних амінів виявляються в реакціях з сильними кислотами, з якими вони утворюють солі. Так, анілін з хлоридною кислотою утворює легко розчинну у воді сіль – анілінгідрогенхлорид: Солі ароматичних амінів легко гідролізуються водою. Тому їх водні розчини мають кислу реакцію: Зі слабкими кислотами ароматичні аміни солей не утворюють, що свідчить про послаблення основних властивостей ароматичних амінів порівняно з амоніаком.
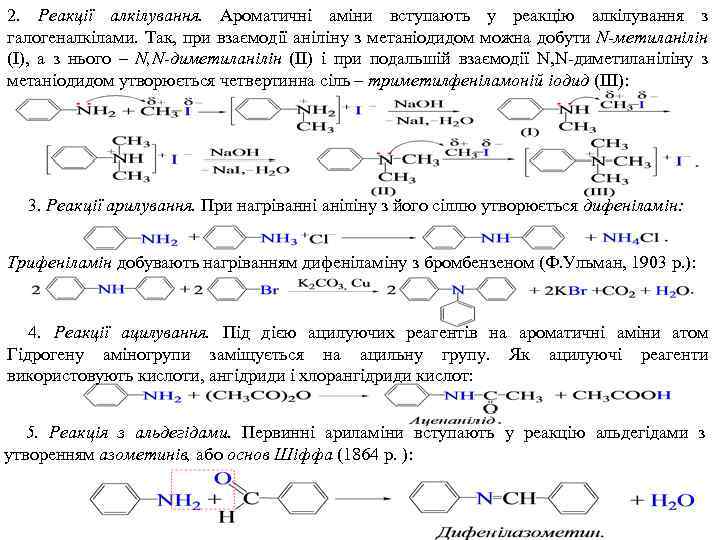 2. Реакції алкілування. Ароматичні аміни вступають у реакцію алкілування з галогеналкілами. Так, при взаємодії аніліну з метаніодидом можна добути N-метиланілін (І), а з нього – Ν, Ν-диметиланілін (ІІ) і при подальшій взаємодії N, N-диметиланіліну з метаніодидом утворюється четвертинна сіль – триметилфеніламоній іодид (ІІІ): 3. Реакції арилування. При нагріванні аніліну з його сіллю утворюється дифеніламін: Трифеніламін добувають нагріванням дифеніламіну з бромбензеном (Ф. Ульман, 1903 р. ): 4. Реакції ацилування. Під дією ацилуючих реагентів на ароматичні аміни атом Гідрогену аміногрупи заміщується на ацильну групу. Як ацилуючі реагенти використовують кислоти, ангідриди і хлорангідриди кислот: 5. Реакція з альдегідами. Первинні ариламіни вступають у реакцію альдегідами з утворенням азометинів, або основ Шіффа (1864 p. ):
2. Реакції алкілування. Ароматичні аміни вступають у реакцію алкілування з галогеналкілами. Так, при взаємодії аніліну з метаніодидом можна добути N-метиланілін (І), а з нього – Ν, Ν-диметиланілін (ІІ) і при подальшій взаємодії N, N-диметиланіліну з метаніодидом утворюється четвертинна сіль – триметилфеніламоній іодид (ІІІ): 3. Реакції арилування. При нагріванні аніліну з його сіллю утворюється дифеніламін: Трифеніламін добувають нагріванням дифеніламіну з бромбензеном (Ф. Ульман, 1903 р. ): 4. Реакції ацилування. Під дією ацилуючих реагентів на ароматичні аміни атом Гідрогену аміногрупи заміщується на ацильну групу. Як ацилуючі реагенти використовують кислоти, ангідриди і хлорангідриди кислот: 5. Реакція з альдегідами. Первинні ариламіни вступають у реакцію альдегідами з утворенням азометинів, або основ Шіффа (1864 p. ):
 6. Взаємодія ароматичних амінів з нітритною кислотою з утворенням солей діазонію: Вторинні ароматичні і жирно-ароматичні аміни з нітритною кислотою утворюють Nнітрозаміни: Третинні ариламіни утворюють ароматичні нітрозопохідні в пара- або орто-положенні до аміногрупи: Реакції за участі бензенового ядра. Оскільки NH 2 -група виявляє сильний +M-ефект, то SE–реакції (галогенування, нітрування і сульфування) відбуваються набагато легше, ніж у бензену, і проходить в орто- і пара-положеннях відносно аміногрупи. 1. Галогенування. Анілін дуже легко вступає в реакцію з бромною водою і утворює важкорозчинний 2, 4, 6 -триброманілін (якісна проба на анілін). Для одержання моноброманіліну, аміногрупу ацетилують, а потім бромують ацетанілід. Після гідролізу ацетамідної групи в пара-бромацетаніліді одержують пара-броманілін: Хлорують ацильні похідні, а хлорацетаніліди гідролізом перетворюють на орто- і парахлораніліни:
6. Взаємодія ароматичних амінів з нітритною кислотою з утворенням солей діазонію: Вторинні ароматичні і жирно-ароматичні аміни з нітритною кислотою утворюють Nнітрозаміни: Третинні ариламіни утворюють ароматичні нітрозопохідні в пара- або орто-положенні до аміногрупи: Реакції за участі бензенового ядра. Оскільки NH 2 -група виявляє сильний +M-ефект, то SE–реакції (галогенування, нітрування і сульфування) відбуваються набагато легше, ніж у бензену, і проходить в орто- і пара-положеннях відносно аміногрупи. 1. Галогенування. Анілін дуже легко вступає в реакцію з бромною водою і утворює важкорозчинний 2, 4, 6 -триброманілін (якісна проба на анілін). Для одержання моноброманіліну, аміногрупу ацетилують, а потім бромують ацетанілід. Після гідролізу ацетамідної групи в пара-бромацетаніліді одержують пара-броманілін: Хлорують ацильні похідні, а хлорацетаніліди гідролізом перетворюють на орто- і парахлораніліни:
 2. Нітрування. Ариламіни при нітруванні легко окиснюються і осмолюються. Якщо нітрування аніліну проводити нітруючою сумішшю, то крім окиснення аніліну відбувається перетворення його на іон анілінію, який орієнтує вхід нітроній-катіона в мета -положення. У промисловості мета-нітроанілін добувають відновленням метадинітробензену натрій дисульфідом: Для добування пара-нітроаніліну анілін ацетилують, ацетанілід нітрують і гідролізом перетворюють на пара-нітроанілін: 3. Сульфування аніліну розбавленою сульфатною кислотою є SE-реакцією і приводить до утворення суміші орто-і пара-анілінсульфокислот: Анілінсульфокислоти застосовують для синтезу барвників, різних похідних бензену та лікарських препаратів. Особливо велике значення має сульфанілова кислота, яку добувають за схемою:
2. Нітрування. Ариламіни при нітруванні легко окиснюються і осмолюються. Якщо нітрування аніліну проводити нітруючою сумішшю, то крім окиснення аніліну відбувається перетворення його на іон анілінію, який орієнтує вхід нітроній-катіона в мета -положення. У промисловості мета-нітроанілін добувають відновленням метадинітробензену натрій дисульфідом: Для добування пара-нітроаніліну анілін ацетилують, ацетанілід нітрують і гідролізом перетворюють на пара-нітроанілін: 3. Сульфування аніліну розбавленою сульфатною кислотою є SE-реакцією і приводить до утворення суміші орто-і пара-анілінсульфокислот: Анілінсульфокислоти застосовують для синтезу барвників, різних похідних бензену та лікарських препаратів. Особливо велике значення має сульфанілова кислота, яку добувають за схемою:
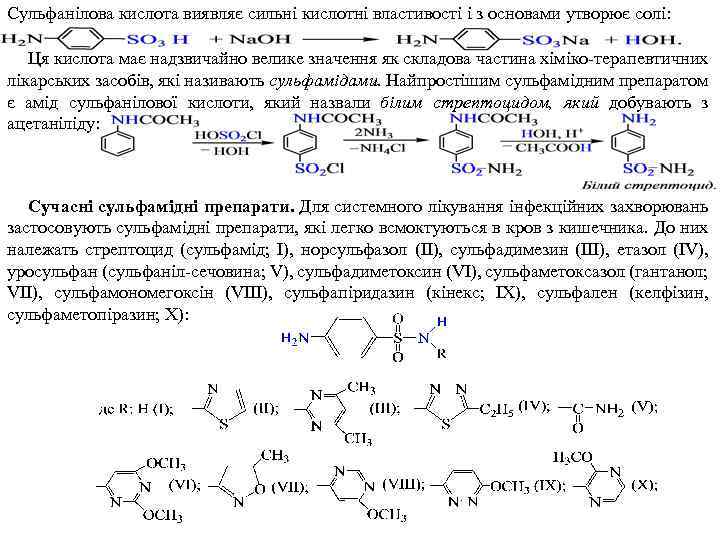 Сульфанілова кислота виявляє сильні кислотні властивості і з основами утворює солі: Ця кислота має надзвичайно велике значення як складова частина хіміко-терапевтичних лікарських засобів, які називають сульфамідами. Найпростішим сульфамідним препаратом є амід сульфанілової кислоти, який назвали білим стрептоцидом, який добувають з ацетаніліду: Сучасні сульфамідні препарати. Для системного лікування інфекційних захворювань застосовують сульфамідні препарати, які легко всмоктуються в кров з кишечника. До них належать стрептоцид (сульфамід; I), норсульфазол (II), сульфадимезин (III), етазол (IV), уросульфан (сульфаніл-сечовина; V), сульфадиметоксин (VI), сульфаметоксазол (гантанол; VII), сульфамономегоксін (VIII), сульфапіридазин (кінекс; IX), сульфален (келфізин, сульфаметопіразин; X):
Сульфанілова кислота виявляє сильні кислотні властивості і з основами утворює солі: Ця кислота має надзвичайно велике значення як складова частина хіміко-терапевтичних лікарських засобів, які називають сульфамідами. Найпростішим сульфамідним препаратом є амід сульфанілової кислоти, який назвали білим стрептоцидом, який добувають з ацетаніліду: Сучасні сульфамідні препарати. Для системного лікування інфекційних захворювань застосовують сульфамідні препарати, які легко всмоктуються в кров з кишечника. До них належать стрептоцид (сульфамід; I), норсульфазол (II), сульфадимезин (III), етазол (IV), уросульфан (сульфаніл-сечовина; V), сульфадиметоксин (VI), сульфаметоксазол (гантанол; VII), сульфамономегоксін (VIII), сульфапіридазин (кінекс; IX), сульфален (келфізин, сульфаметопіразин; X):
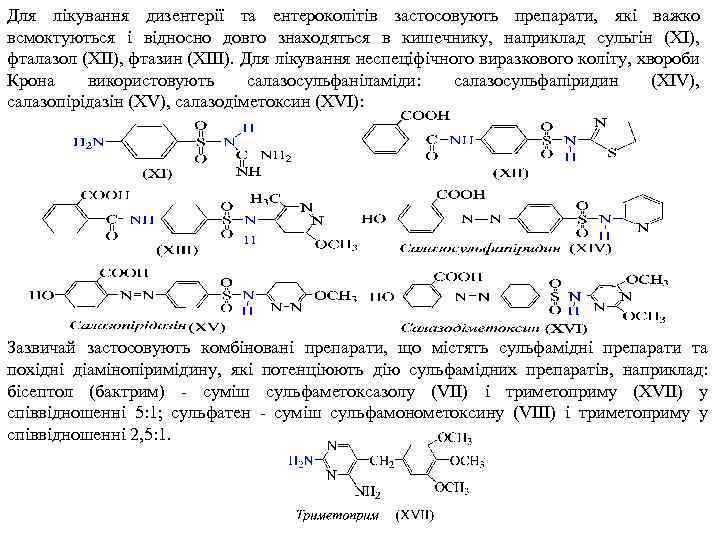 Для лікування дизентерії та ентероколітів застосовують препарати, які важко всмоктуються і відносно довго знаходяться в кишечнику, наприклад сульгін (XI), фталазол (XII), фтазин (XIII). Для лікування неспеціфічного виразкового коліту, хвороби Крона використовують салазосульфаніламіди: салазосульфапіридин (XIV), салазопірідазін (XV), салазодіметоксин (XVI): Зазвичай застосовують комбіновані препарати, що містять сульфамідні препарати та похідні діамінопіримідину, які потенціюють дію сульфамідних препаратів, наприклад: бісептол (бактрим) - суміш сульфаметоксазолу (VII) і триметоприму (XVII) у співвідношенні 5: 1; сульфатен - суміш сульфамонометоксину (VIII) і триметоприму у співвідношенні 2, 5: 1.
Для лікування дизентерії та ентероколітів застосовують препарати, які важко всмоктуються і відносно довго знаходяться в кишечнику, наприклад сульгін (XI), фталазол (XII), фтазин (XIII). Для лікування неспеціфічного виразкового коліту, хвороби Крона використовують салазосульфаніламіди: салазосульфапіридин (XIV), салазопірідазін (XV), салазодіметоксин (XVI): Зазвичай застосовують комбіновані препарати, що містять сульфамідні препарати та похідні діамінопіримідину, які потенціюють дію сульфамідних препаратів, наприклад: бісептол (бактрим) - суміш сульфаметоксазолу (VII) і триметоприму (XVII) у співвідношенні 5: 1; сульфатен - суміш сульфамонометоксину (VIII) і триметоприму у співвідношенні 2, 5: 1.


