Ароматические оксисоединения2003.ppt
- Количество слайдов: 33
 Ароматические оксисоединения Фенолы
Ароматические оксисоединения Фенолы
 Фенолы - это ароматические углеводороды, содержащие одну, две или большее количество гидроксильных групп. Кроме фенолов существуют ароматические спирты, которые содержат гидроксильную группу в боковой цепи, например: бензиловый спирт
Фенолы - это ароматические углеводороды, содержащие одну, две или большее количество гидроксильных групп. Кроме фенолов существуют ароматические спирты, которые содержат гидроксильную группу в боковой цепи, например: бензиловый спирт
 В зависимости от количества гидроксильных групп различают по атомности: • • одноатомные; двухатомные; трехатомные; четырехатомные.
В зависимости от количества гидроксильных групп различают по атомности: • • одноатомные; двухатомные; трехатомные; четырехатомные.
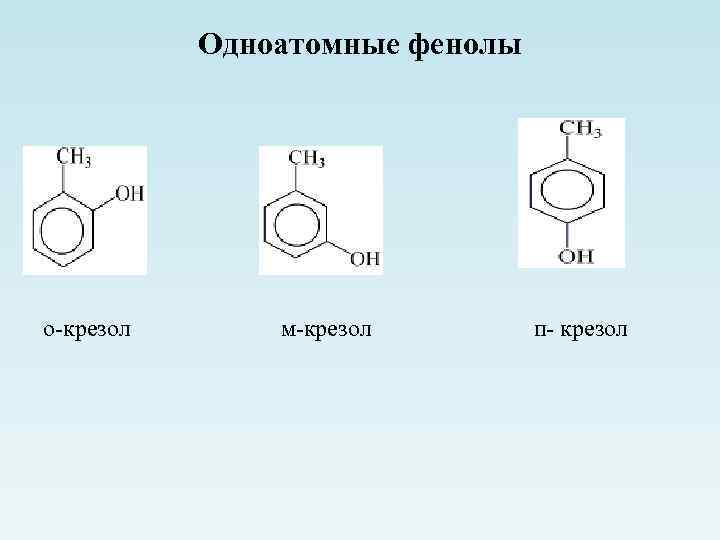 Одноатомные фенолы о-крезол м-крезол п- крезол
Одноатомные фенолы о-крезол м-крезол п- крезол
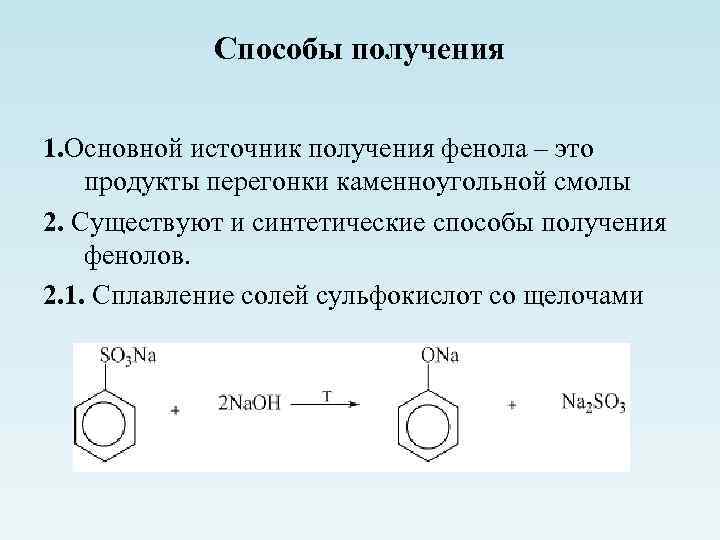 Способы получения 1. Основной источник получения фенола – это продукты перегонки каменноугольной смолы 2. Существуют и синтетические способы получения фенолов. 2. 1. Сплавление солей сульфокислот со щелочами
Способы получения 1. Основной источник получения фенола – это продукты перегонки каменноугольной смолы 2. Существуют и синтетические способы получения фенолов. 2. 1. Сплавление солей сульфокислот со щелочами
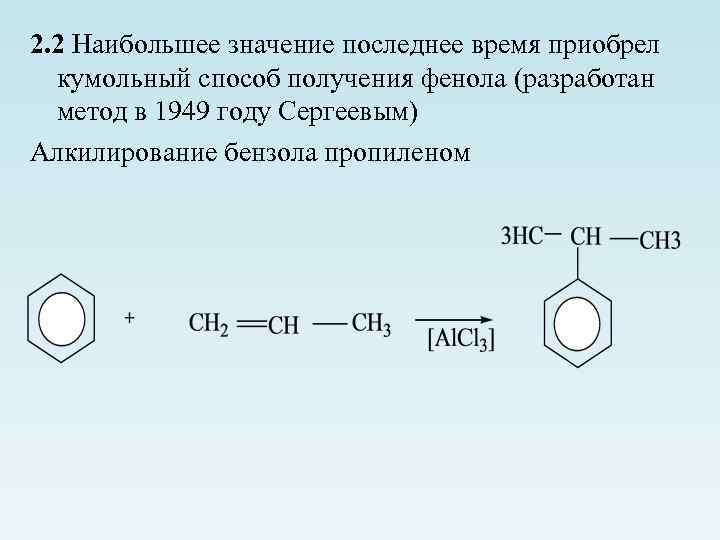 2. 2 Наибольшее значение последнее время приобрел кумольный способ получения фенола (разработан метод в 1949 году Сергеевым) Алкилирование бензола пропиленом
2. 2 Наибольшее значение последнее время приобрел кумольный способ получения фенола (разработан метод в 1949 году Сергеевым) Алкилирование бензола пропиленом
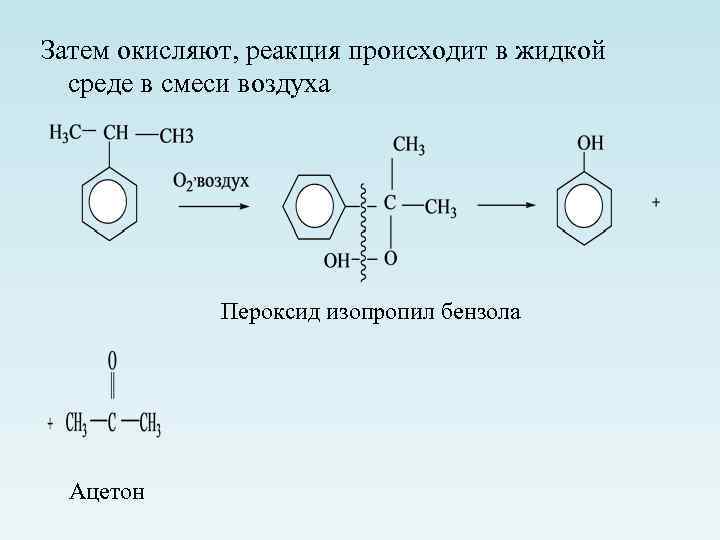 Затем окисляют, реакция происходит в жидкой среде в смеси воздуха Пероксид изопропил бензола Ацетон
Затем окисляют, реакция происходит в жидкой среде в смеси воздуха Пероксид изопропил бензола Ацетон
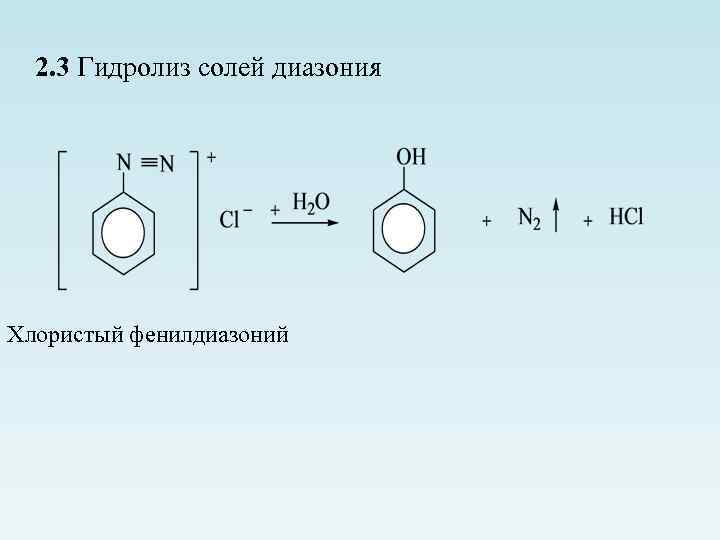 2. 3 Гидролиз солей диазония Хлористый фенилдиазоний
2. 3 Гидролиз солей диазония Хлористый фенилдиазоний
 Физические свойства Фенолы – это бесцветные кристаллические вещества, трудно растворимые в воде, обладают характерным запахом, а так же обладают сильным антисептическим действием. При попадание на кожу вызывает долго незаживающие ожоги! ЯДОВИТ!!!
Физические свойства Фенолы – это бесцветные кристаллические вещества, трудно растворимые в воде, обладают характерным запахом, а так же обладают сильным антисептическим действием. При попадание на кожу вызывает долго незаживающие ожоги! ЯДОВИТ!!!
 Химические свойства фенола определяются наличием двух функциональных групп: • гидроксильная группа; • ароматическое кольцо. Из-за взаимного влияния этих функциональных групп не все химические свойства спиртов и фенолов совпадают.
Химические свойства фенола определяются наличием двух функциональных групп: • гидроксильная группа; • ароматическое кольцо. Из-за взаимного влияния этих функциональных групп не все химические свойства спиртов и фенолов совпадают.
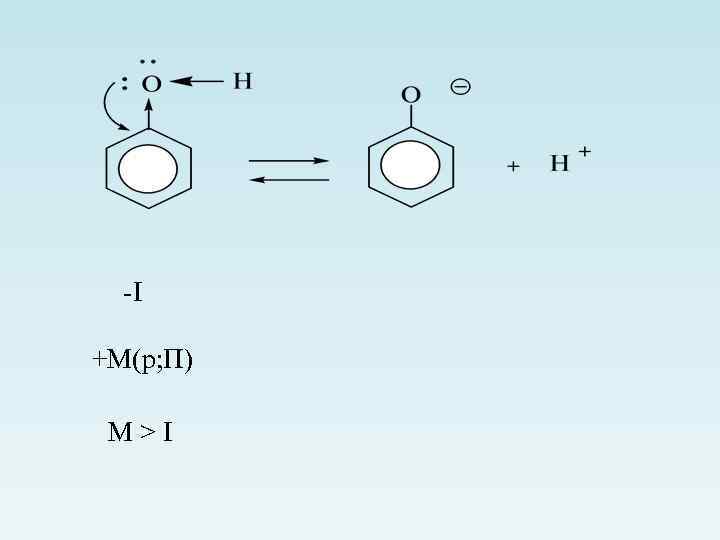 -I +М(p; П) М>I
-I +М(p; П) М>I
 С другой стороны, увеличению кислотных свойств способствует большая стабильность образующегося фенолят иона -I -М Вывод: электроно-акцепторные заместители увеличивают кислотные свойства фенолов
С другой стороны, увеличению кислотных свойств способствует большая стабильность образующегося фенолят иона -I -М Вывод: электроно-акцепторные заместители увеличивают кислотные свойства фенолов
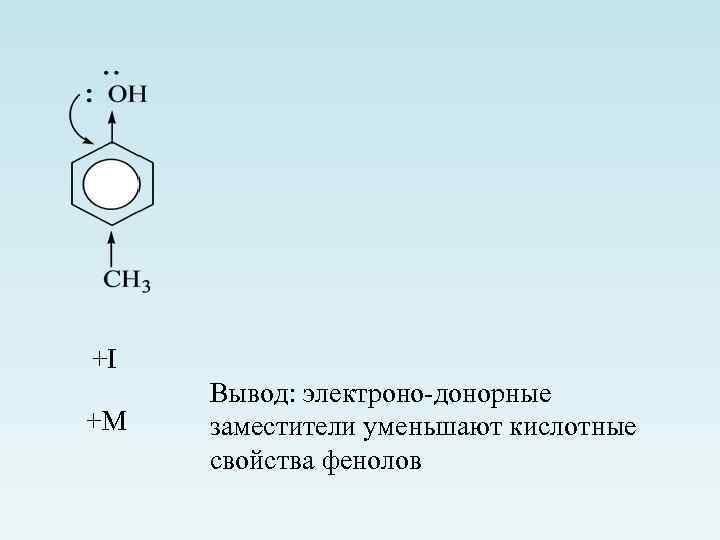 +I +М Вывод: электроно-донорные заместители уменьшают кислотные свойства фенолов
+I +М Вывод: электроно-донорные заместители уменьшают кислотные свойства фенолов
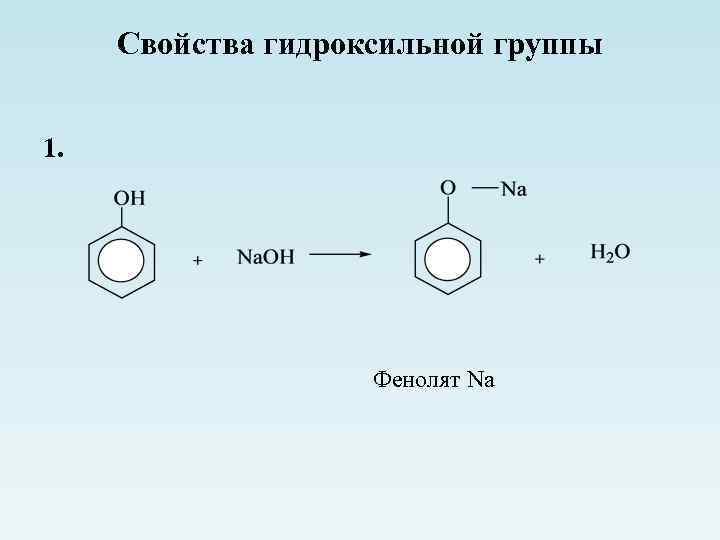 Свойства гидроксильной группы 1. Фенолят Na
Свойства гидроксильной группы 1. Фенолят Na
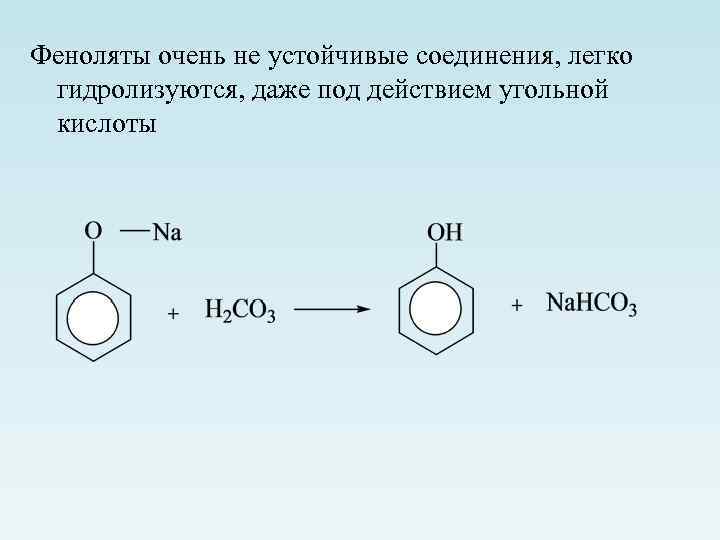 Феноляты очень не устойчивые соединения, легко гидролизуются, даже под действием угольной кислоты
Феноляты очень не устойчивые соединения, легко гидролизуются, даже под действием угольной кислоты
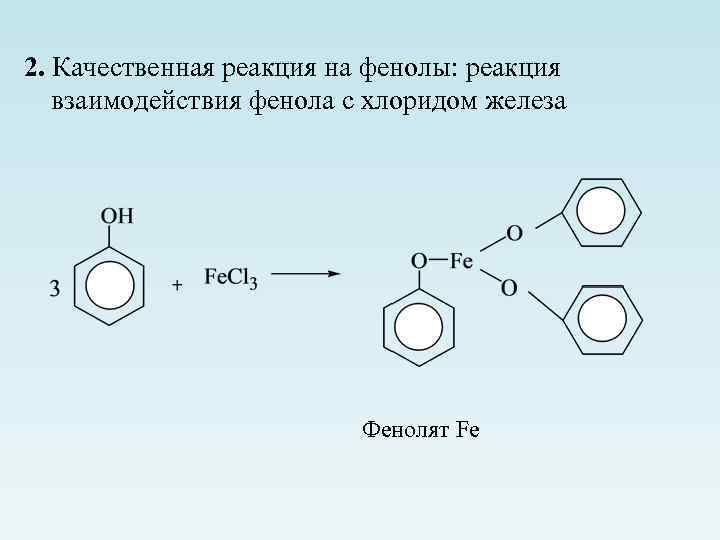 2. Качественная реакция на фенолы: реакция взаимодействия фенола с хлоридом железа Фенолят Fe
2. Качественная реакция на фенолы: реакция взаимодействия фенола с хлоридом железа Фенолят Fe
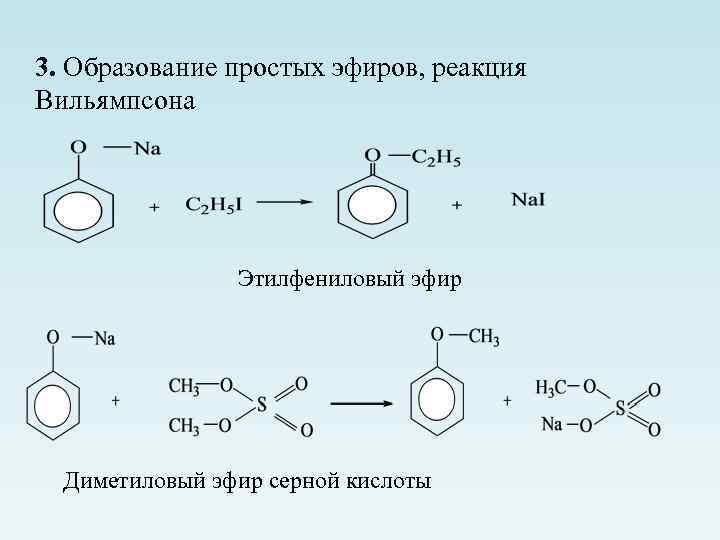 3. Образование простых эфиров, реакция Вильямпсона Этилфениловый эфир Диметиловый эфир серной кислоты
3. Образование простых эфиров, реакция Вильямпсона Этилфениловый эфир Диметиловый эфир серной кислоты
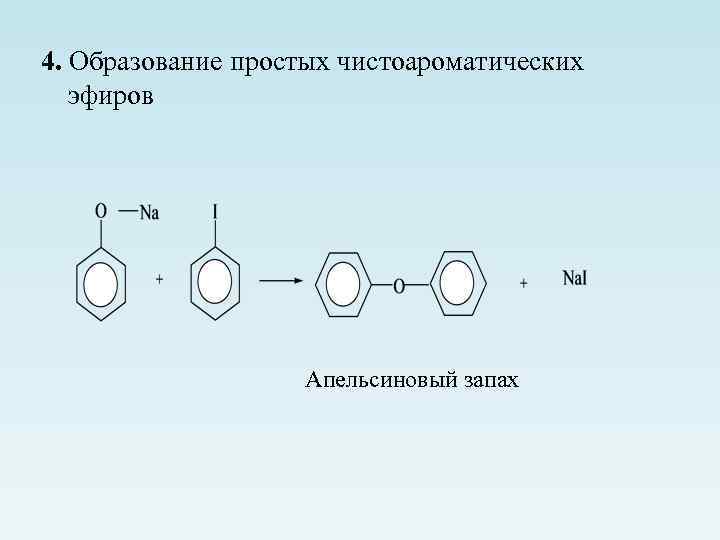 4. Образование простых чистоароматических эфиров Апельсиновый запах
4. Образование простых чистоароматических эфиров Апельсиновый запах
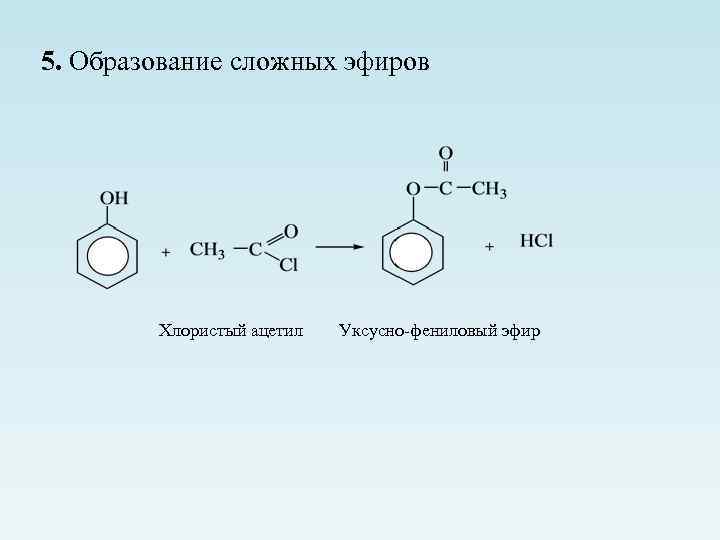 5. Образование сложных эфиров Хлористый ацетил Уксусно-фениловый эфир
5. Образование сложных эфиров Хлористый ацетил Уксусно-фениловый эфир
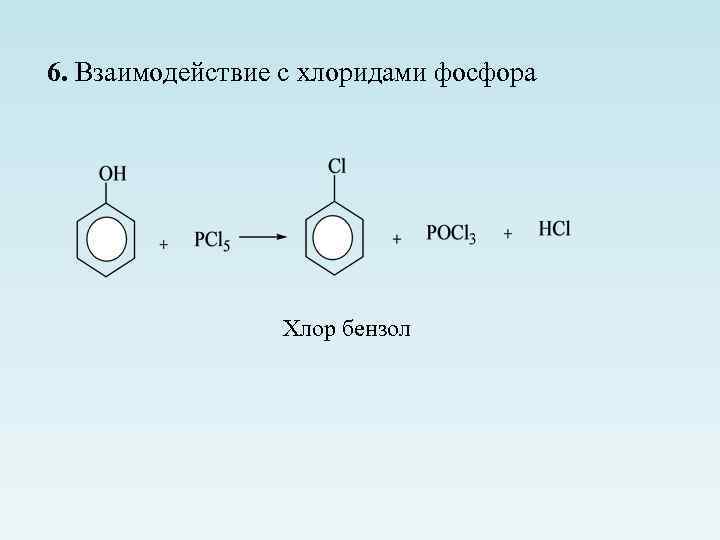 6. Взаимодействие с хлоридами фосфора Хлор бензол
6. Взаимодействие с хлоридами фосфора Хлор бензол
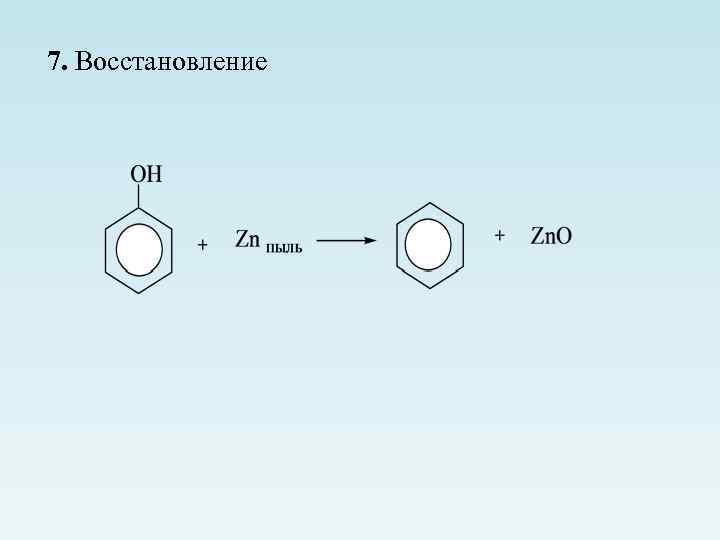 7. Восстановление
7. Восстановление
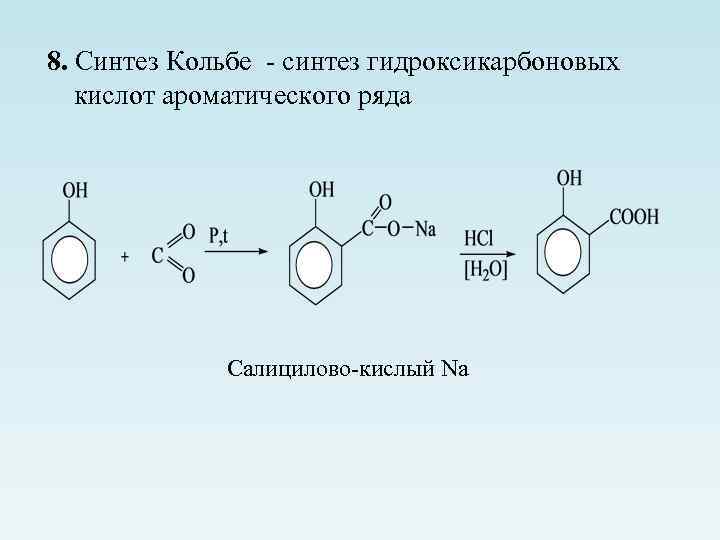 8. Синтез Кольбе - синтез гидроксикарбоновых кислот ароматического ряда Салицилово-кислый Na
8. Синтез Кольбе - синтез гидроксикарбоновых кислот ароматического ряда Салицилово-кислый Na
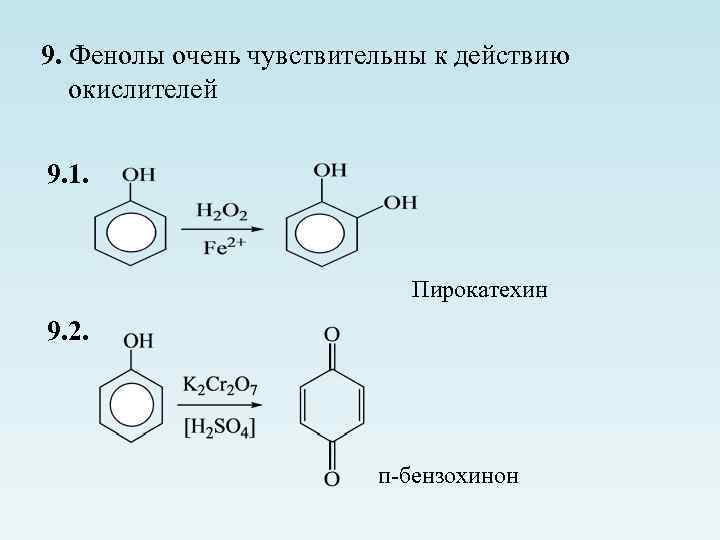 9. Фенолы очень чувствительны к действию окислителей 9. 1. Пирокатехин 9. 2. п-бензохинон
9. Фенолы очень чувствительны к действию окислителей 9. 1. Пирокатехин 9. 2. п-бензохинон
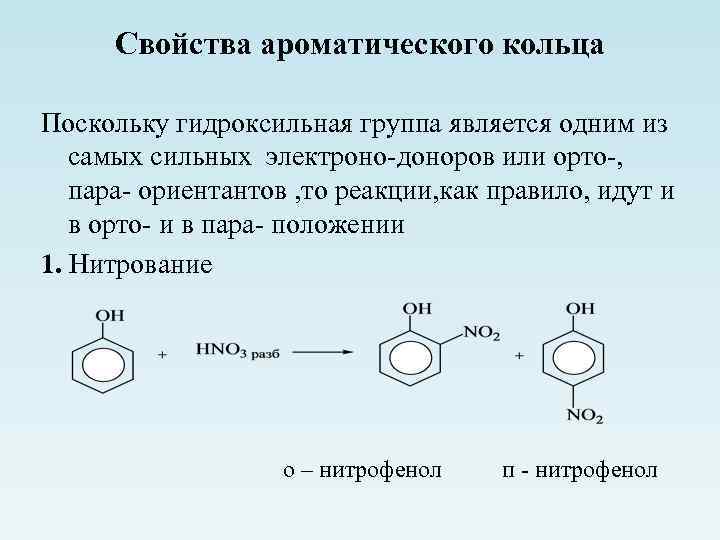 Свойства ароматического кольца Поскольку гидроксильная группа является одним из самых сильных электроно-доноров или орто-, пара- ориентантов , то реакции, как правило, идут и в орто- и в пара- положении 1. Нитрование о – нитрофенол п - нитрофенол
Свойства ароматического кольца Поскольку гидроксильная группа является одним из самых сильных электроно-доноров или орто-, пара- ориентантов , то реакции, как правило, идут и в орто- и в пара- положении 1. Нитрование о – нитрофенол п - нитрофенол
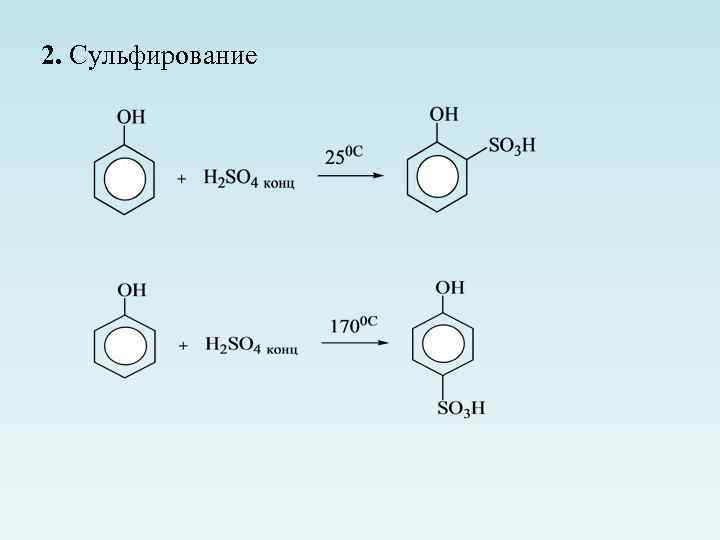 2. Сульфирование
2. Сульфирование
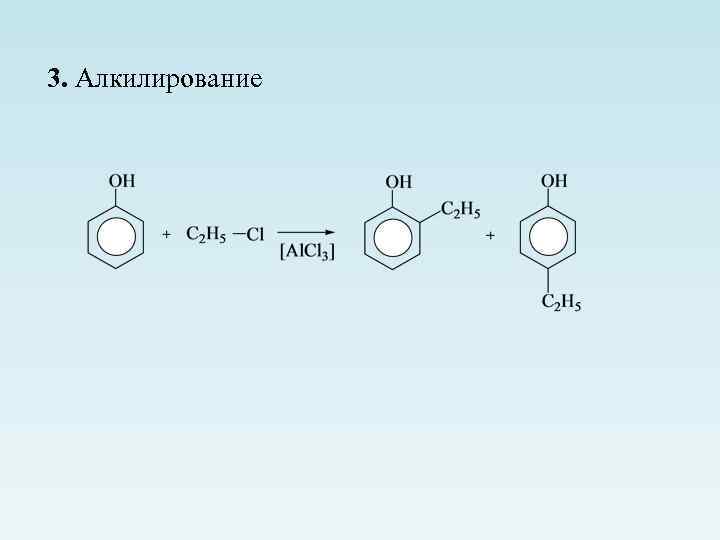 3. Алкилирование
3. Алкилирование
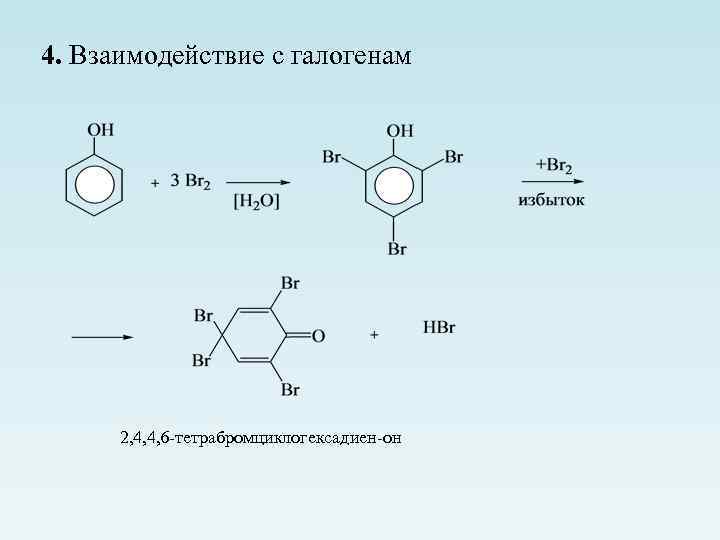 4. Взаимодействие с галогенам 2, 4, 4, 6 -тетрабромциклогексадиен-он
4. Взаимодействие с галогенам 2, 4, 4, 6 -тетрабромциклогексадиен-он
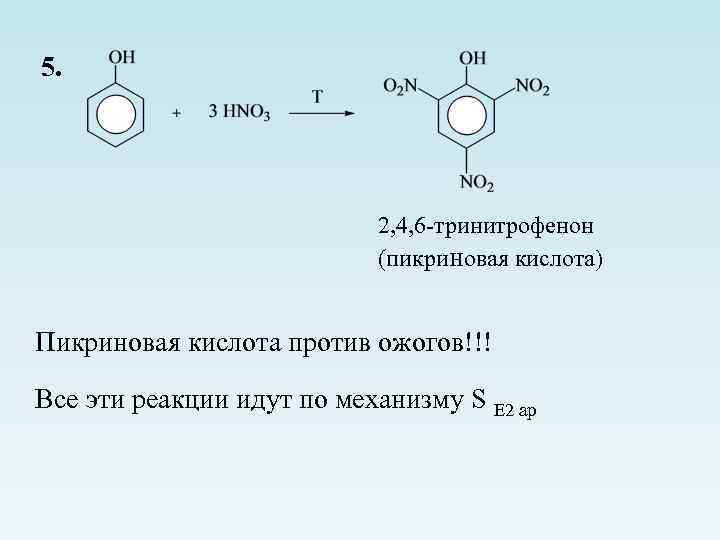 5. 2, 4, 6 -тринитрофенон (пикриновая кислота) Пикриновая кислота против ожогов!!! Все эти реакции идут по механизму S Е 2 ар
5. 2, 4, 6 -тринитрофенон (пикриновая кислота) Пикриновая кислота против ожогов!!! Все эти реакции идут по механизму S Е 2 ар
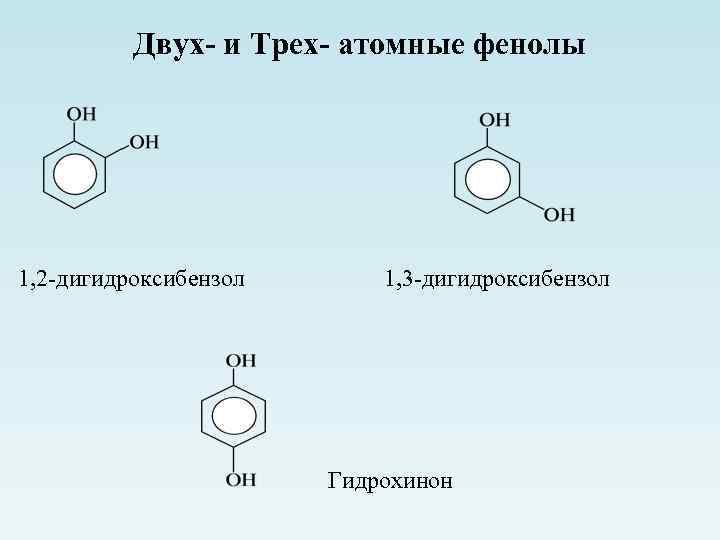 Двух- и Трех- атомные фенолы 1, 2 -дигидроксибензол 1, 3 -дигидроксибензол Гидрохинон
Двух- и Трех- атомные фенолы 1, 2 -дигидроксибензол 1, 3 -дигидроксибензол Гидрохинон
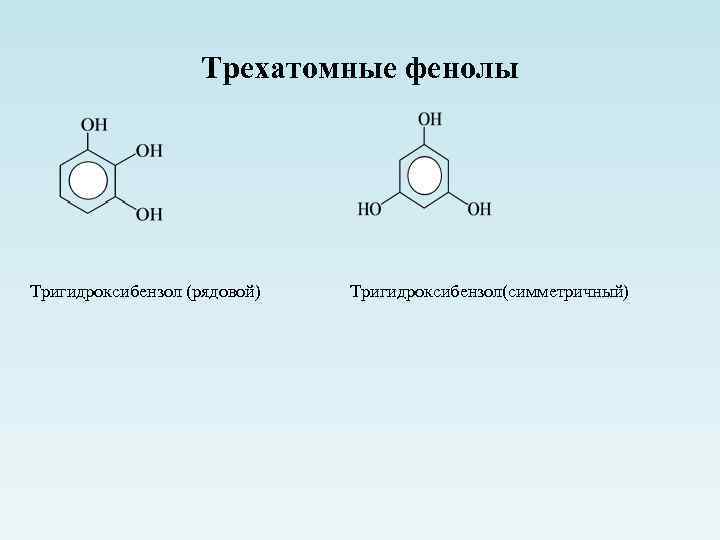 Трехатомные фенолы Тригидроксибензол (рядовой) Тригидроксибензол(симметричный)
Трехатомные фенолы Тригидроксибензол (рядовой) Тригидроксибензол(симметричный)
 Двух- и трех- атомные фенолы – кристаллические вещества, которые легко растворяются в воде. Проявляют все свойства одноатомных фенолов. Однако есть некоторые особенности в их свойствах: 1. Поскольку они содержат большее количество гидроксильных групп, то они проявляют большие кислотные свойства.
Двух- и трех- атомные фенолы – кристаллические вещества, которые легко растворяются в воде. Проявляют все свойства одноатомных фенолов. Однако есть некоторые особенности в их свойствах: 1. Поскольку они содержат большее количество гидроксильных групп, то они проявляют большие кислотные свойства.
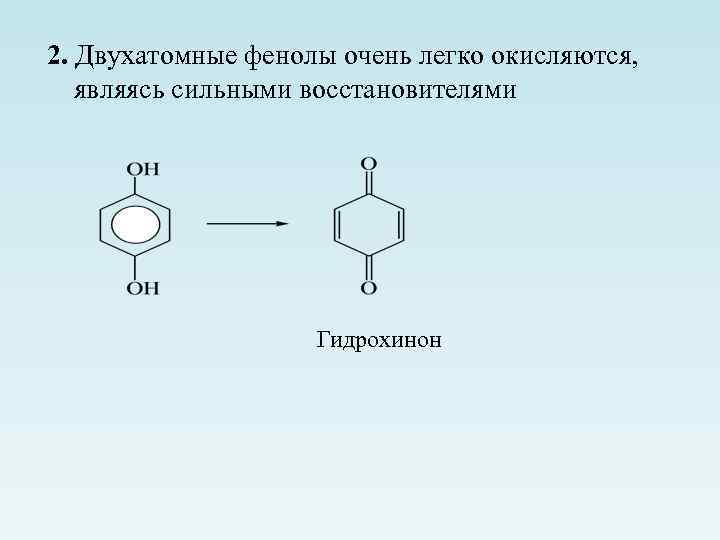 2. Двухатомные фенолы очень легко окисляются, являясь сильными восстановителями Гидрохинон
2. Двухатомные фенолы очень легко окисляются, являясь сильными восстановителями Гидрохинон
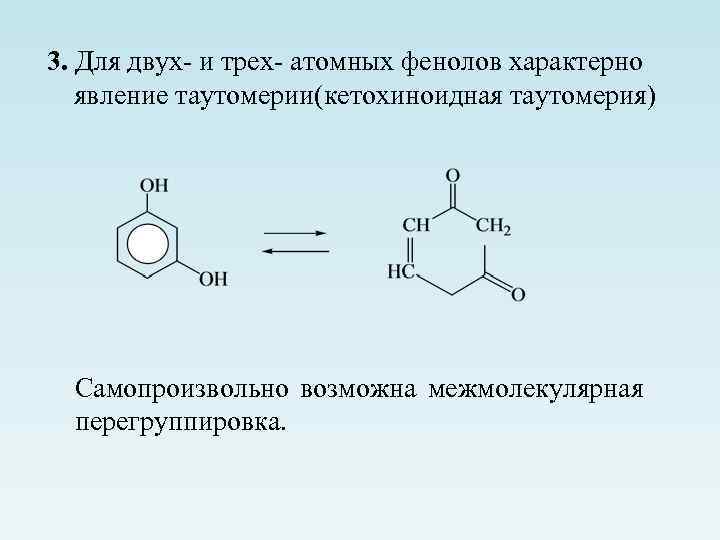 3. Для двух- и трех- атомных фенолов характерно явление таутомерии(кетохиноидная таутомерия) Самопроизвольно возможна межмолекулярная перегруппировка.
3. Для двух- и трех- атомных фенолов характерно явление таутомерии(кетохиноидная таутомерия) Самопроизвольно возможна межмолекулярная перегруппировка.


