Арены_2016.pptx
- Количество слайдов: 18

Арены (общая характеристика) Ароматические углеводороды – циклические углеводороды, в молекуле которых в качестве обязательного элемента структуры содержится одно или несколько бензольных колец
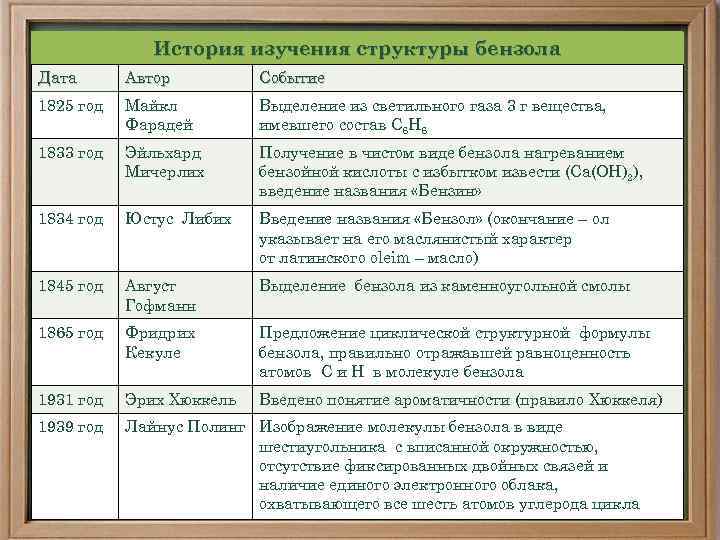
История изучения структуры бензола Дата Автор Событие 1825 год Майкл Фарадей Выделение из светильного газа 3 г вещества, имевшего состав С 6 Н 6 1833 год Эйльхард Мичерлих Получение в чистом виде бензола нагреванием бензойной кислоты с избытком извести (Са(ОН)2), введение названия «Бензин» 1834 год Юстус Либих Введение названия «Бензол» (окончание – ол указывает на его маслянистый характер от латинского оleim – масло) 1845 год Август Гофманн Выделение бензола из каменноугольной смолы 1865 год Фридрих Кекуле Предложение циклической структурной формулы бензола, правильно отражавшей равноценность атомов С и Н в молекуле бензола 1931 год Эрих Хюккель Введено понятие ароматичности (правило Хюккеля) 1939 год Лайнус Полинг Изображение молекулы бензола в виде шестиугольника с вписанной окружностью, отсутствие фиксированных двойных связей и наличие единого электронного облака, охватывающего все шесть атомов углерода цикла
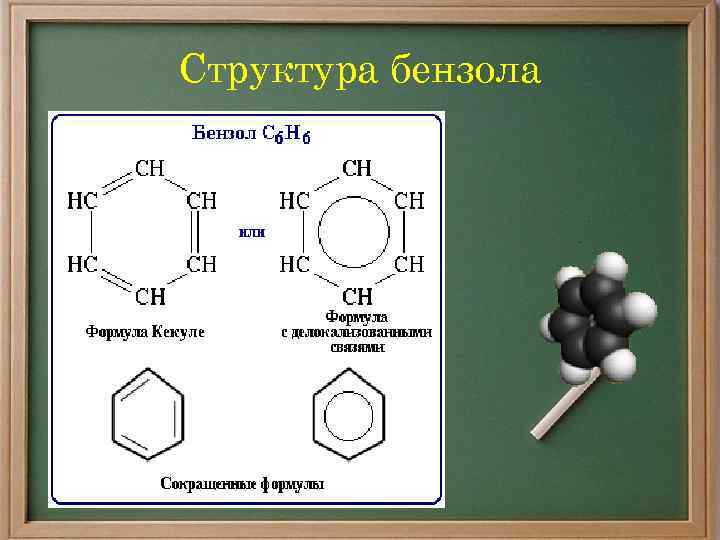
Структура бензола
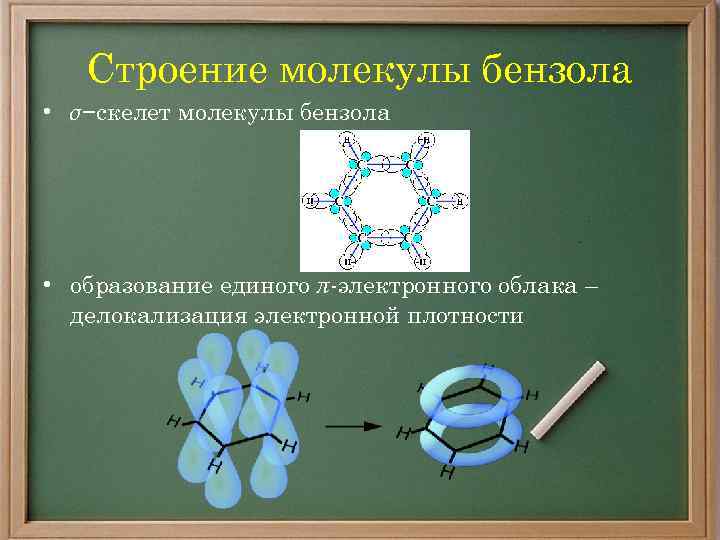
Строение молекулы бензола • σ−скелет молекулы бензола • образование единого π-электронного облака – делокализация электронной плотности
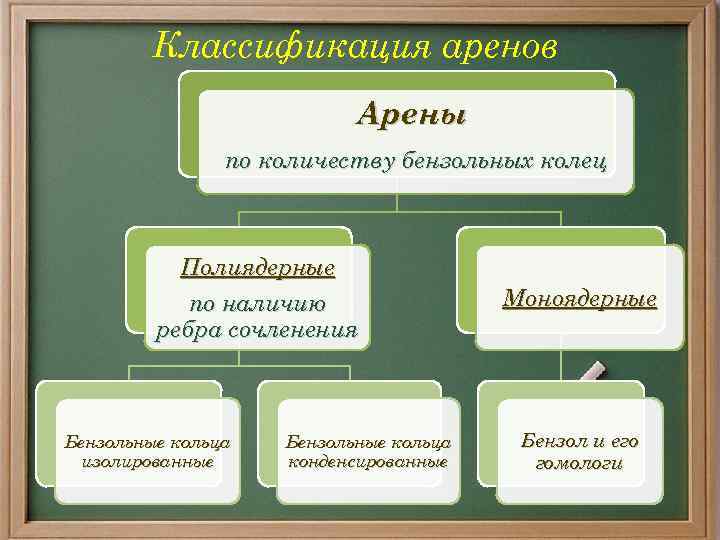
Классификация аренов Арены по количеству бензольных колец Полиядерные по наличию ребра сочленения Бензольные кольца изолированные Бензольные кольца конденсированные Моноядерные Бензол и его гомологи
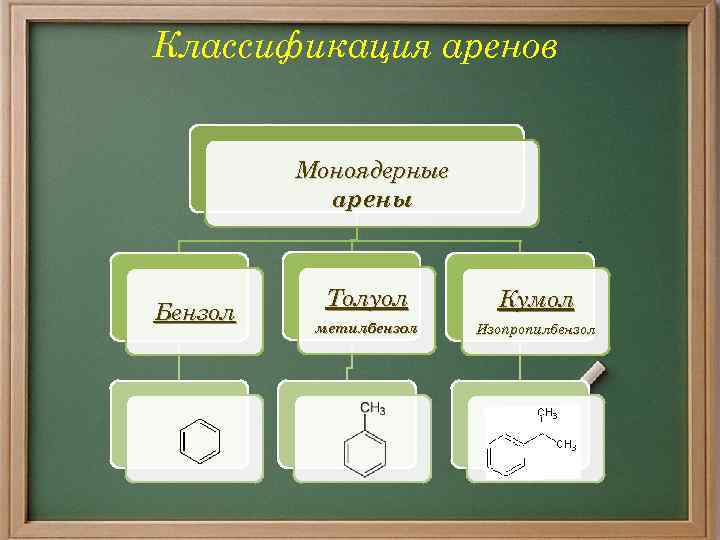
Классификация аренов Моноядерные арены Бензол Толуол Кумол метилбензол Изопропилбензол
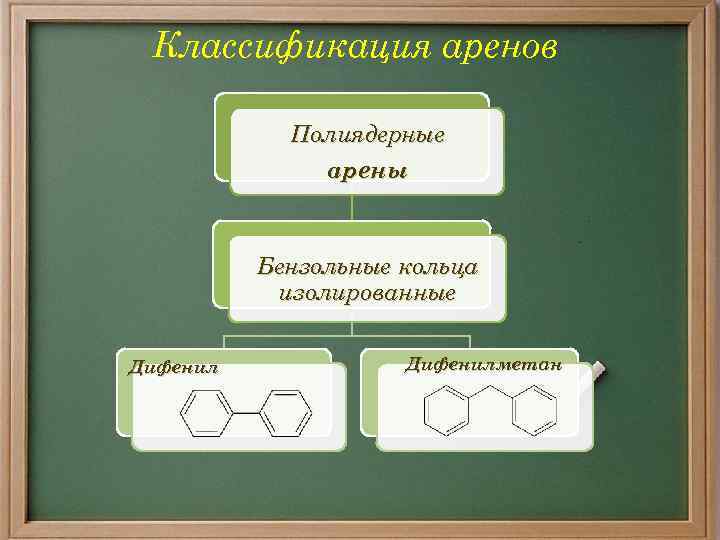
Классификация аренов Полиядерные арены Бензольные кольца изолированные Дифенилметан
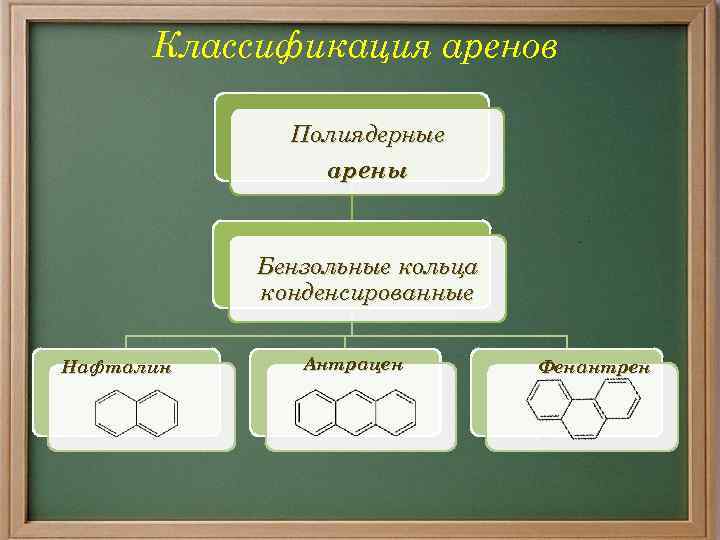
Классификация аренов Полиядерные арены Бензольные кольца конденсированные Нафталин Антрацен Фенантрен

Общая характеристика аренов ü Общая формула аренов: Cn. H 2 n− 6, где n ≥ 6; ü Простейший представитель – бензол С 6 Н 6; ü Атомы углерода в молекуле бензола – атомы sp 2−C; ü Валентный угол (∠НСС и ∠ССС) равен 120°; ü Длина С−С связи 0, 140 нм; С−Н связи 0, 108 нм; ü Направленность σ−связей − плоскостно-тригональная; ü σ−скелет молекулы бензола − плоский

Основные характеристики ароматических соединений • склонность к реакциям замещения, а не присоединения; • выигрыш в энергии по сравнении с системой несопряженных двойных связей – энергия сопряжения Eсопряжения бензола = 150 к. Дж/моль; • наличие плоскости, в которой лежат все атомы образующие ароматическую систему, единое π-электронное облако, образующееся при сопряжении, лежит над и под плоскостью ароматической системы. • правило Хюккеля: ароматичной может быть лишь система, содержащая (в кольце) 4 n+2 электронов (где n = 0, 1, 2, …).
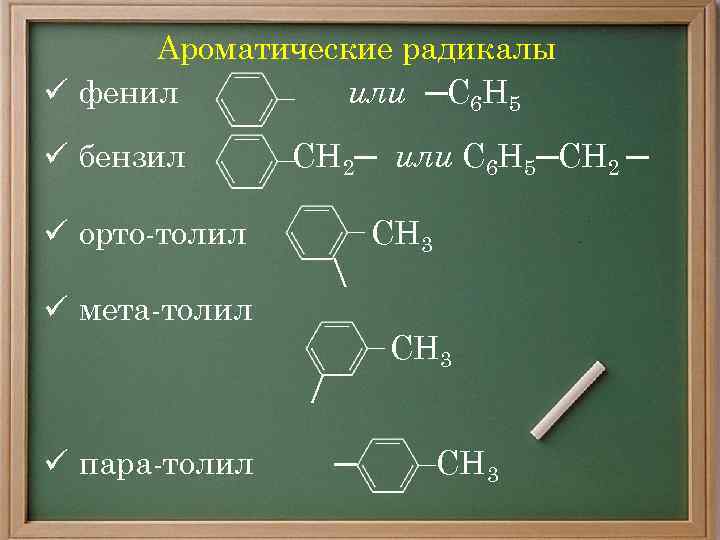
Ароматические радикалы ü фенил или ─С 6 Н 5 ü бензил СН 2─ или С 6 Н 5─СН 2 ─ ü орто-толил ü мета-толил СН 3 / ü пара-толил СН 3 ─ СН 3

Номенклатура аренов Названия гомологов бензола в качестве корня содержат слово «бензол» : метилбензол или толуол или фенилметан С 6 Н 5─СН 3 этилбензол или фенилэтан С 6 Н 5─СН 2 ─СН 3 или С 6 Н 5─С 2 Н 5 1, 2 -диметилбензол 1, 3 -диметилбензол 1, 4 -диметилбензол
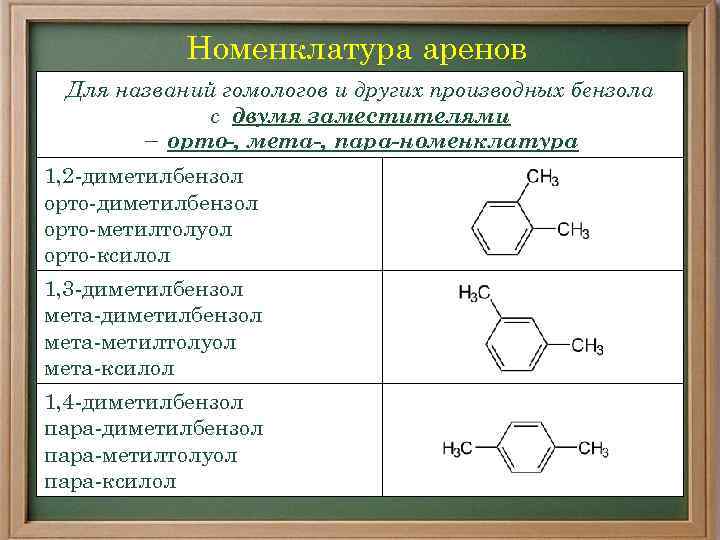
Номенклатура аренов Для названий гомологов и других производных бензола с двумя заместителями − орто-, мета-, пара-номенклатура 1, 2 -диметилбензол орто-метилтолуол орто-ксилол 1, 3 -диметилбензол мета-метилтолуол мета-ксилол 1, 4 -диметилбензол пара-метилтолуол пара-ксилол

Изомерия, гомология аренов I. Структурная изомерия 1. Изомерия углеродного скелета боковой цепи (С 9 Н 12) Пропилбензол Изопропилбензол 1 -фенилпропан 2 -фенилпропан или кумол СН 2−СН 3−СН−СН 3 2. (а) Изомерия числа или количества заместителей в цикле (С 8 Н 10) а) этилбензол 1, 2 -диметилбензол

Изомерия, номенклатура, гомология I. Структурная изомерия 2. (б) Изомерия положения заместителей в цикле (С 8 Н 10) б) пара-ксилол мета-ксилол орто-ксилол 3. Межклассовая изомерия Как правило, не приводят межклассовые изомеры аренов, хотя существует не один класс углеводородов, которые являются межклассовыми изомерами аренов, например: для бензола С 6 Н 6 гексадиин-1, 5 СН≡С─СН 2─С≡СН гексадиен-1, 5 -ин-3 или дивинилацетилен СН 2=СН−С≡С−СН=СН 2

Изомерия, номенклатура, гомология II. Пространственная изомерия 1. Геометрическая изомерия (цис-транс-изомерия) для аренов невозможна

Методы получения ароматических углеводородов 1. Алкилирование бензола и его гомологов по Фриделю-Крафтсу – метод получения гомологов бензола (химическое свойство). 2. Алкилирование бензола и его гомологов алкенами – метод получения гомологов бензола (химическое свойство)*. 3. Восстановление ароматических кетонов – метод получения гомологов бензола, в молекуле которых содержится α−метиленовое звено (α−СН 2−звено). 4. Реакция Вюрца−Фиттига – метод получения гомологов бензола, модифицированная реакция Вюрца*.

Методы получения ароматических углеводородов 5. Дегидроциклизация (ароматизация) алканов* − метод получения бензола и его гомологов. 6. Дегидрирование циклогексана и его гомологов* − метод получения бензола и его гомологов. 7. Щелочное декарбоксилирование солей ароматических карбоновых кислот* − метод получения бензола и его гомологов. 8. Синтез Зелинского – циклическая тримеризация низших алкинов* − метод получения бензола и его симметричных полизамещенных гомологов, например: 1, 3, 5 -триметилбензола.
Арены_2016.pptx