 Арены 11 ен
Арены 11 ен
 История l l l ¾ всех органических веществ Ароматические (начало XIX в. ) – имеющие приятный запах (ванилин, бензальдегид) Ароматичность – общие признаки строения и химических свойств, подобные бензолу
История l l l ¾ всех органических веществ Ароматические (начало XIX в. ) – имеющие приятный запах (ванилин, бензальдегид) Ароматичность – общие признаки строения и химических свойств, подобные бензолу
 История изучения бензола l l l Впервые получен в 1825 г. М. Фарадеем (из каменноугольной смолы) В 1834 г. – установлена молекулярная формула – С 6 Н 6 К 1930 г. – электронное строение молекулы с помощью рентгеноструктурного анализа
История изучения бензола l l l Впервые получен в 1825 г. М. Фарадеем (из каменноугольной смолы) В 1834 г. – установлена молекулярная формула – С 6 Н 6 К 1930 г. – электронное строение молекулы с помощью рентгеноструктурного анализа
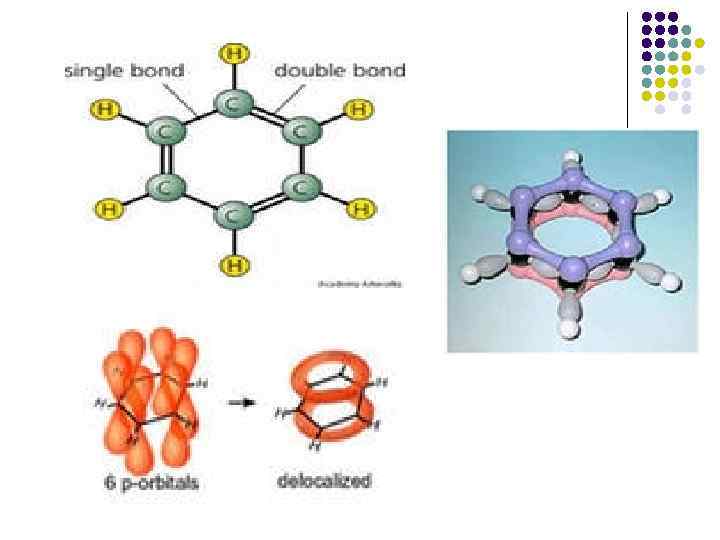
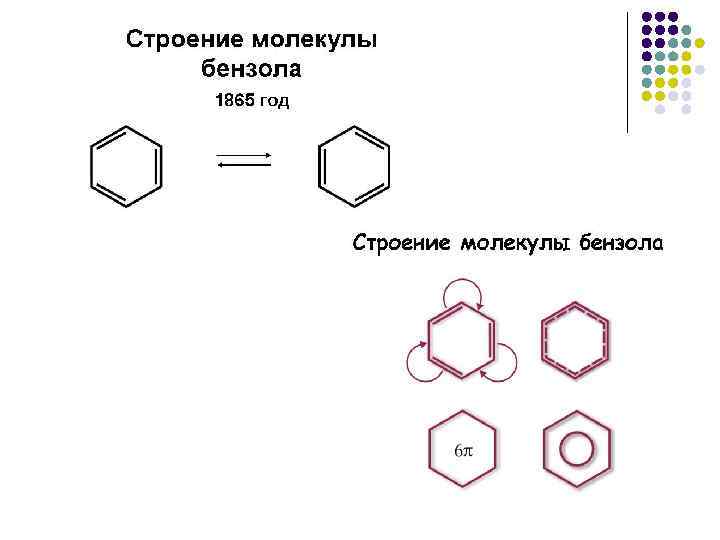
 Строение бензола l l l l Молекула плоская УС – в виде правильного 6 -угольника Валентные углы - 120˚ Атомы С – в sp 2 – гибридизации Каждый атом С – 2 сигма-связи с соседними атомами С и 1 сигма-связь с Н Негибридные орбитали всех 6 атомов С взаимно параллельны и перпендикулярны плоскости УС (бензольного кольца) р-р Сопряжение – образование общего электронного облака (выше и ниже плоскости кольца), по которому свободно перемещаются все 6 электронов, связывая 6 атомов С
Строение бензола l l l l Молекула плоская УС – в виде правильного 6 -угольника Валентные углы - 120˚ Атомы С – в sp 2 – гибридизации Каждый атом С – 2 сигма-связи с соседними атомами С и 1 сигма-связь с Н Негибридные орбитали всех 6 атомов С взаимно параллельны и перпендикулярны плоскости УС (бензольного кольца) р-р Сопряжение – образование общего электронного облака (выше и ниже плоскости кольца), по которому свободно перемещаются все 6 электронов, связывая 6 атомов С
 Следствия сопряжения l l l l Все СС связи имеют одинаковую длину (0, 140 нм) (ароматическая связь) Многоцентровая пи-связь Резонансные структуры Устойчивость бензольного кольца (гидрирование бензола – 49, 8 ккал/моль, циклогексена – 28, 8 ккал/моль, циклогексадиена – 1, 4 – 56, 7 ккал/моль) Энергия сопряжения бензола – 36, 6 ккал/моль (электроны идеально распределены среди всех атомов С, участвующих в образовании многоцентровой связи) Устойчивость пи-системы – каждый из входящих в нее электронов притягивается одновременно всеми 6 атомами С кольца Привлекательность пи-системы для электрофильных реагентов
Следствия сопряжения l l l l Все СС связи имеют одинаковую длину (0, 140 нм) (ароматическая связь) Многоцентровая пи-связь Резонансные структуры Устойчивость бензольного кольца (гидрирование бензола – 49, 8 ккал/моль, циклогексена – 28, 8 ккал/моль, циклогексадиена – 1, 4 – 56, 7 ккал/моль) Энергия сопряжения бензола – 36, 6 ккал/моль (электроны идеально распределены среди всех атомов С, участвующих в образовании многоцентровой связи) Устойчивость пи-системы – каждый из входящих в нее электронов притягивается одновременно всеми 6 атомами С кольца Привлекательность пи-системы для электрофильных реагентов
 Ароматичность l l l Это совокупность химических и физикохимических свойств, вызванных особой устойчивостью структуры Правило Хюккеля: химическое соединение обладает ароматическими свойствами, если: а) его молекула имеет циклическое строение; б) все атомы цикла – в одной плоскости; в) р-орбитали атомов цикла перекрываются друг с другом с образованием циклической системы пиэлектронов выше и ниже плоскости молекулы; г) циклическая пи-система включает 4 n+2 электронов (n=0, 1, 2, 3…) Бензол – ароматическая система (n=1)
Ароматичность l l l Это совокупность химических и физикохимических свойств, вызванных особой устойчивостью структуры Правило Хюккеля: химическое соединение обладает ароматическими свойствами, если: а) его молекула имеет циклическое строение; б) все атомы цикла – в одной плоскости; в) р-орбитали атомов цикла перекрываются друг с другом с образованием циклической системы пиэлектронов выше и ниже плоскости молекулы; г) циклическая пи-система включает 4 n+2 электронов (n=0, 1, 2, 3…) Бензол – ароматическая система (n=1)
 Ароматические соединения с конденсированными циклами l l Конденсированные – 2 бензольных кольца, имеющие 2 общих атома С Нафталин (C 10 Н 8): 2 бензольных кольца, sp 2 – гибридизация, 10 негибридных р-орбиталей перекрываются, образуя циклическую писистему, состоящую из 10 электронов (n=2) Антрацен, фенантрен(С 14 Н 10): 3 конденсированных кольца, имеют пи-систему из 14 электронов (n=3) Природные источники – каменный уголь (каменноугольная смола), нефть
Ароматические соединения с конденсированными циклами l l Конденсированные – 2 бензольных кольца, имеющие 2 общих атома С Нафталин (C 10 Н 8): 2 бензольных кольца, sp 2 – гибридизация, 10 негибридных р-орбиталей перекрываются, образуя циклическую писистему, состоящую из 10 электронов (n=2) Антрацен, фенантрен(С 14 Н 10): 3 конденсированных кольца, имеют пи-систему из 14 электронов (n=3) Природные источники – каменный уголь (каменноугольная смола), нефть
 Номенклатура производных бензола l l l l Название заместителя + «бензол» (хлорбензол, нитробензол) Тривиальные названия: толуол, анилин, фенол, бензойная кислота 3 изомера дизамещенных бензолов – приставки орто- (о-), мета(м-), пара- (п-) (о-нитротолуол, м-нитрохлорбензол, п-бромфенол) Если с бензольным кольцом связано более 2 -х заместителей, для обозначения их положения используют цифры (1, 2, 4 трибромбензол, 3 -хлор-5 -бром-нитробензол, 2, 4, 6 -трибром-анилин) Если все заместители одинаковы, то положение каждого – цифрой, чтобы заместители получили возможно наименьшие номера Если заместители разные – заместитель при С 1 – последним, а остальные – получают соответствующие номера Если одна из групп в сочетании со словом «бензол» отвечает тривиальному названию вещества, то считается, что она находится в положении 1.
Номенклатура производных бензола l l l l Название заместителя + «бензол» (хлорбензол, нитробензол) Тривиальные названия: толуол, анилин, фенол, бензойная кислота 3 изомера дизамещенных бензолов – приставки орто- (о-), мета(м-), пара- (п-) (о-нитротолуол, м-нитрохлорбензол, п-бромфенол) Если с бензольным кольцом связано более 2 -х заместителей, для обозначения их положения используют цифры (1, 2, 4 трибромбензол, 3 -хлор-5 -бром-нитробензол, 2, 4, 6 -трибром-анилин) Если все заместители одинаковы, то положение каждого – цифрой, чтобы заместители получили возможно наименьшие номера Если заместители разные – заместитель при С 1 – последним, а остальные – получают соответствующие номера Если одна из групп в сочетании со словом «бензол» отвечает тривиальному названию вещества, то считается, что она находится в положении 1.
 Физические свойства бензола l l l l Бесцветная жидкость Температура кипения - 80˚С Температура замерзания – 5, 5˚С Слабый специфический запах Практически не смешивается с водой Хорошо растворим в органических растворителях Растворяет многие органические вещества Ядовит
Физические свойства бензола l l l l Бесцветная жидкость Температура кипения - 80˚С Температура замерзания – 5, 5˚С Слабый специфический запах Практически не смешивается с водой Хорошо растворим в органических растворителях Растворяет многие органические вещества Ядовит
 Реакции присоединения бензола l l l Не обесцвечивает раствор брома Не присоединяет галогеноводороды Гидрирование: кат – Ni, Pt, повышенная t и повышенное давление Н 2: С 6 Н 6 + 3 Н 2 → С 6 Н 12 (t=100 -200˚, 100 атм) Хлорирование: УФ-облучение: С 6 Н 6 Cl 6 (гексахлоран) Озонолиз: С 6 Н 6 +3 О 2 → С 6 Н 6 О 6 (триозонид) + 3 Н 2 О → 3 С 2 О 2 Н 2 (глиоксаль) + 3 Н 2 О 2
Реакции присоединения бензола l l l Не обесцвечивает раствор брома Не присоединяет галогеноводороды Гидрирование: кат – Ni, Pt, повышенная t и повышенное давление Н 2: С 6 Н 6 + 3 Н 2 → С 6 Н 12 (t=100 -200˚, 100 атм) Хлорирование: УФ-облучение: С 6 Н 6 Cl 6 (гексахлоран) Озонолиз: С 6 Н 6 +3 О 2 → С 6 Н 6 О 6 (триозонид) + 3 Н 2 О → 3 С 2 О 2 Н 2 (глиоксаль) + 3 Н 2 О 2
 Реакции окисления бензола l l l В обычных условиях – устойчив к действию сильных окислителей (КMn. O 4, K 2 Cr 2 O 7+H 2 SO 4, разбавленный раствор HNO 3) В промышленности – окисление кислородом воздуха при сильном нагревании, кат – V 2 O 5 → малеиновый ангидрид → малеиновая кислота Горение бензола – коптящее пламя
Реакции окисления бензола l l l В обычных условиях – устойчив к действию сильных окислителей (КMn. O 4, K 2 Cr 2 O 7+H 2 SO 4, разбавленный раствор HNO 3) В промышленности – окисление кислородом воздуха при сильном нагревании, кат – V 2 O 5 → малеиновый ангидрид → малеиновая кислота Горение бензола – коптящее пламя
 Окисление гомологов бензола l l Окисление алкилбензолов сильными окислителями (окисляются алкильные заместители, связанные с бензольным кольцом) → бензойная кислота Окисление диалкилбензолов → дикарбоновые кислоты
Окисление гомологов бензола l l Окисление алкилбензолов сильными окислителями (окисляются алкильные заместители, связанные с бензольным кольцом) → бензойная кислота Окисление диалкилбензолов → дикарбоновые кислоты
 Реакции электрофильного замещения (SE) l l l Легко протекают Механизм – ионный (атака электрофильного реагента) Нитрование: небольшое нагревание, смесь концентрированных азотной и серной кислот (нитрующая смесь) → нитробензол Галогенирование: (Cl 2, Br 2), кат – галогениды алюминия или железа (III) → хлор- или бромбензол Сульфирование: олеум, комн. T, → бензолсульфокислота, обратимо, т. е. при действии горячего водяного пара → бензол + серная кислота Алкилирование: бензол + галогенопроизводные алканов → алкилбензол, кат – галогениды алюминия
Реакции электрофильного замещения (SE) l l l Легко протекают Механизм – ионный (атака электрофильного реагента) Нитрование: небольшое нагревание, смесь концентрированных азотной и серной кислот (нитрующая смесь) → нитробензол Галогенирование: (Cl 2, Br 2), кат – галогениды алюминия или железа (III) → хлор- или бромбензол Сульфирование: олеум, комн. T, → бензолсульфокислота, обратимо, т. е. при действии горячего водяного пара → бензол + серная кислота Алкилирование: бензол + галогенопроизводные алканов → алкилбензол, кат – галогениды алюминия
 Механизм SE для ароматических соединений l l l Стадия 1 – образование пи-комплекса (не требует больших затрат энергии, протекает быстро) Стадия 2 – образование σ-комплекса (электрофильная частица отнимает у кольца пару электронов и образует σ-связь с одним из атомов С кольца; стадия протекает медленно и требует больших затрат энергии – лимитирующая стадия) Стадия 3 – распад σ-комплекса и образование продуктов реакции, восстановление ароматического кольца, отщепляющийся протон взаимодействует с нуклеофилом)
Механизм SE для ароматических соединений l l l Стадия 1 – образование пи-комплекса (не требует больших затрат энергии, протекает быстро) Стадия 2 – образование σ-комплекса (электрофильная частица отнимает у кольца пару электронов и образует σ-связь с одним из атомов С кольца; стадия протекает медленно и требует больших затрат энергии – лимитирующая стадия) Стадия 3 – распад σ-комплекса и образование продуктов реакции, восстановление ароматического кольца, отщепляющийся протон взаимодействует с нуклеофилом)
 Нитрование бензола l l l l l Электрофил – NO 2+, нуклеофил – HSO 4 Катализатор – серная кислота Протонирование азотной кислоты серной кислотой: H 2 SO 4 + HO-NO 2 → Распад протонированной азотной кислоты на воду и NO 2+ (нитроний-катион) Нитроний – катион – сильный электрофил Атака молекулы бензола нитроний-катионом Образование пи-комплекса Образование σ-комплекса Отщепление протона, образование нитробензола. Восстановление катализатора (серной кислоты)
Нитрование бензола l l l l l Электрофил – NO 2+, нуклеофил – HSO 4 Катализатор – серная кислота Протонирование азотной кислоты серной кислотой: H 2 SO 4 + HO-NO 2 → Распад протонированной азотной кислоты на воду и NO 2+ (нитроний-катион) Нитроний – катион – сильный электрофил Атака молекулы бензола нитроний-катионом Образование пи-комплекса Образование σ-комплекса Отщепление протона, образование нитробензола. Восстановление катализатора (серной кислоты)
 Галогенирование бензола l l l l Электрофилы- X+, нуклеофил – Al. X 4 -, где Х – Cl, Br Катализаторы – галогениды алюминия Al. X 3 + X: X → Al. X 4 - + X+ Атака бензольного кольца электрофилом – образование пи-комплекса Образование σ-комплекса Отщепление протона, образование продукта Н+ + Al. X 4 - → HX + Al. X 3
Галогенирование бензола l l l l Электрофилы- X+, нуклеофил – Al. X 4 -, где Х – Cl, Br Катализаторы – галогениды алюминия Al. X 3 + X: X → Al. X 4 - + X+ Атака бензольного кольца электрофилом – образование пи-комплекса Образование σ-комплекса Отщепление протона, образование продукта Н+ + Al. X 4 - → HX + Al. X 3
 Алкилирование бензола l l l Электрофил – R+, нуклеофил – Al. X 4 Al. X 3 + R: X → Al. X 4 - + R+ Атака элетрофила и образование пикомплекса Образование σ-комплекса Отщепление протона, образование продуктов Восстановление катализатора
Алкилирование бензола l l l Электрофил – R+, нуклеофил – Al. X 4 Al. X 3 + R: X → Al. X 4 - + R+ Атака элетрофила и образование пикомплекса Образование σ-комплекса Отщепление протона, образование продуктов Восстановление катализатора
 Сульфирование бензола l l l l Электрофил – SO 3, Нуклеофил – HSO 4 Очень концентрированные растворы серной кислоты (С близка к 100%) Протонирование молекул воды серной кислотой H 2 SO 4 + H 2 O → H 3 O+ +HSO 4 Разложение серной кислоты H 2 SO 4 → SO 3 + H 2 O Суммарно: 2 H 2 SO 4 → H 3 O+ + HSO 4 - + SO 3 Чем выше концентрация раствора H 2 SO 4, тем больше смещено равновесие в сторону образования SO 3, … В молекуле SO 3 все 3 связи SO поляризованы: электроны смещены от атома S к О. Положительный заряд на атоме серы делает SO 3 сильным электрофилом, способным присоединиться к бензольному кольцу с образованием связи СS
Сульфирование бензола l l l l Электрофил – SO 3, Нуклеофил – HSO 4 Очень концентрированные растворы серной кислоты (С близка к 100%) Протонирование молекул воды серной кислотой H 2 SO 4 + H 2 O → H 3 O+ +HSO 4 Разложение серной кислоты H 2 SO 4 → SO 3 + H 2 O Суммарно: 2 H 2 SO 4 → H 3 O+ + HSO 4 - + SO 3 Чем выше концентрация раствора H 2 SO 4, тем больше смещено равновесие в сторону образования SO 3, … В молекуле SO 3 все 3 связи SO поляризованы: электроны смещены от атома S к О. Положительный заряд на атоме серы делает SO 3 сильным электрофилом, способным присоединиться к бензольному кольцу с образованием связи СS
 Стадии сульфирования l l l Атака бензольного кольца молекулой SO 3 Образование пи- комплекса Образование σ-комплекса Взаимодействие σ-комплекса с HSO 4 - → образование аниона сульфокислоты и молекулы H 2 SO 4 Взаимодействие аниона сульфокислоты с H 3 O+ → бензолсульфокислота (очень сильная, поэтому равновесие сильно смещено влево) + Н 2 О
Стадии сульфирования l l l Атака бензольного кольца молекулой SO 3 Образование пи- комплекса Образование σ-комплекса Взаимодействие σ-комплекса с HSO 4 - → образование аниона сульфокислоты и молекулы H 2 SO 4 Взаимодействие аниона сульфокислоты с H 3 O+ → бензолсульфокислота (очень сильная, поэтому равновесие сильно смещено влево) + Н 2 О
 Сравнение SE и АЕ l l l l Сходство: атака электрофильного реагента, направленная на пи-элетронное облако образование пи- комплекса образование σ-комплекса Отличие: АЕ- последующее присоединение нуклеофила SE – последующее отщепление протона и взаимодействие его с нуклеофилом (выгодно восстановление ароматичности, т. к. дает выигрыш в энергии)
Сравнение SE и АЕ l l l l Сходство: атака электрофильного реагента, направленная на пи-элетронное облако образование пи- комплекса образование σ-комплекса Отличие: АЕ- последующее присоединение нуклеофила SE – последующее отщепление протона и взаимодействие его с нуклеофилом (выгодно восстановление ароматичности, т. к. дает выигрыш в энергии)
 Влияние заместителей в бензольном кольце на электрофильное замещение l l Монозамещенные производные бензола С 6 Н 5 Х (где Х = NO 2, , Cl, CH 3, OH, и др. ) могут подвергаться дальнейшему замещению Экспериментальные данные реакций замещения: нитрование толуола ( 58% онитротолуола, 4% м-нитротолуола, 38% пнитротолуола); нитрование нитробензола (6, 4% о-динитробензола, 93, 3% мдинитробензола, 0, 7% п-динитробензола)
Влияние заместителей в бензольном кольце на электрофильное замещение l l Монозамещенные производные бензола С 6 Н 5 Х (где Х = NO 2, , Cl, CH 3, OH, и др. ) могут подвергаться дальнейшему замещению Экспериментальные данные реакций замещения: нитрование толуола ( 58% онитротолуола, 4% м-нитротолуола, 38% пнитротолуола); нитрование нитробензола (6, 4% о-динитробензола, 93, 3% мдинитробензола, 0, 7% п-динитробензола)
 l l l Скорость и ориентация замещения определяется заместителем, уже имеющимся в кольце Активирующие заместители – повышают реакционную способность бензольного кольца по отношению к SЕ (кольцо становится более активным) Дезактивирующие заместители – делают кольцо менее активным, чем кольцо бензола О- и п- ориентанты – связанные с бензольным кольцом заместители, направляющие вновь поступающую группу в о- и п- положения кольца М- ориентанты - связанные с бензольным кольцом заместители, направляющие вновь поступающую группу в м- положение кольца
l l l Скорость и ориентация замещения определяется заместителем, уже имеющимся в кольце Активирующие заместители – повышают реакционную способность бензольного кольца по отношению к SЕ (кольцо становится более активным) Дезактивирующие заместители – делают кольцо менее активным, чем кольцо бензола О- и п- ориентанты – связанные с бензольным кольцом заместители, направляющие вновь поступающую группу в о- и п- положения кольца М- ориентанты - связанные с бензольным кольцом заместители, направляющие вновь поступающую группу в м- положение кольца
 Классификация заместителей l l l l l Активирующие о-, п. ориентанты: -СН 3 и др. алкилы (+I) -OH, -OR, -NH 2, -NHR, NR 2 (+M>> -I) Дезактивирующие м-ориетанты: -CF 3, -CCl 3 (-I) -COH, -COR, -COOH, -COOR (-M) -NO 2, -SO 3 H, -CN (-M, -I) Дезактивирующие о-, п-ориентанты: -Cl, Br, -I (+M=-I)
Классификация заместителей l l l l l Активирующие о-, п. ориентанты: -СН 3 и др. алкилы (+I) -OH, -OR, -NH 2, -NHR, NR 2 (+M>> -I) Дезактивирующие м-ориетанты: -CF 3, -CCl 3 (-I) -COH, -COR, -COOH, -COOR (-M) -NO 2, -SO 3 H, -CN (-M, -I) Дезактивирующие о-, п-ориентанты: -Cl, Br, -I (+M=-I)
 Электронные эффекты заместителей l l Электронный эффект заместителя – воздействие, которое оказывает заместитель на распределение электронной плотности в молекуле I – эффект – способность заместителя вызывать смещение электронных пар 2 -хцентровых связей в молекуле (электроны смещаются от менее к более ЭО атому) -I – оттягивание электронной плотности от С к более ЭО атому +I – отталкивание электронной плотности от менее ЭО атома к атому С
Электронные эффекты заместителей l l Электронный эффект заместителя – воздействие, которое оказывает заместитель на распределение электронной плотности в молекуле I – эффект – способность заместителя вызывать смещение электронных пар 2 -хцентровых связей в молекуле (электроны смещаются от менее к более ЭО атому) -I – оттягивание электронной плотности от С к более ЭО атому +I – отталкивание электронной плотности от менее ЭО атома к атому С
 Электронные эффекты заместителей l l l М – эффект заместителя – смещение пиэлектронов многоцентровой связи, происходящее под действием заместителя. Проявляется, когда р-орбитали одного или нескольких атомов заместителя принимают участие в сопряжении. +М – заместители отдают свои электроны в общую сопряженную пи-систему -М – заместители вытягивают электронную плотность из пи-системы
Электронные эффекты заместителей l l l М – эффект заместителя – смещение пиэлектронов многоцентровой связи, происходящее под действием заместителя. Проявляется, когда р-орбитали одного или нескольких атомов заместителя принимают участие в сопряжении. +М – заместители отдают свои электроны в общую сопряженную пи-систему -М – заместители вытягивают электронную плотность из пи-системы
 Различия между М и I l l l I – эффекты характерны для соединений любых типов, а М – эффекты проявляются только в соединениях с многоцентровыми пи- связями (где есть сопряжение) I – эффект заместителя намного слабее, чем М – эффект того же заместителя I – эффекты передаются только на сравнительно небольшие расстояния, Мэффекты могут сильно сказываться на удаленных от заместителя атомах С
Различия между М и I l l l I – эффекты характерны для соединений любых типов, а М – эффекты проявляются только в соединениях с многоцентровыми пи- связями (где есть сопряжение) I – эффект заместителя намного слабее, чем М – эффект того же заместителя I – эффекты передаются только на сравнительно небольшие расстояния, Мэффекты могут сильно сказываться на удаленных от заместителя атомах С
 Типы заместителей l l l Электронодонорные заместители – суммарное электронное влияние - повышение электронной плотности на др. атомах (группах атомов) в молекуле Электроноакцепторные заместители - суммарное электронное влияние – уменьшение электронной плотности на др. атомах (группах атомов) в молекуле Электронодонорные заместители – алкильные группы (+I), группы: -ОН, OR, -NH 2, -NHR, -NR 2 (+M) Электроноакцепторные заместители - -CF 3, -CCl 3 (-I), -COH, COR, -COOH, -COOR (-M), -NO 2, -SO 3 H, -CN (-M, -I) Электроноакцепторное влияние может иметь место всегда, когда атом, при помощи которого заместитель непосредственно соединен с кольцом, связан кратной связью с еще более электроотрицательным атомом
Типы заместителей l l l Электронодонорные заместители – суммарное электронное влияние - повышение электронной плотности на др. атомах (группах атомов) в молекуле Электроноакцепторные заместители - суммарное электронное влияние – уменьшение электронной плотности на др. атомах (группах атомов) в молекуле Электронодонорные заместители – алкильные группы (+I), группы: -ОН, OR, -NH 2, -NHR, -NR 2 (+M) Электроноакцепторные заместители - -CF 3, -CCl 3 (-I), -COH, COR, -COOH, -COOR (-M), -NO 2, -SO 3 H, -CN (-M, -I) Электроноакцепторное влияние может иметь место всегда, когда атом, при помощи которого заместитель непосредственно соединен с кольцом, связан кратной связью с еще более электроотрицательным атомом
 l l l Промежуточное положение между электронодонорными и электроноакцепторными заместителями – заместители – галогены (-Cl, -Br, -I) -I – эффект р-орбиталь атома Г, содержащая неподеленную пару электронов, перекрывается с пи- системой (+М) +М-эффект Г намного слабее, чем у группы –ОН и др. +М и –I компенсируют друга, суммарное электронное влияние Г не является ни электронодонорным, ни электроноакцепторным
l l l Промежуточное положение между электронодонорными и электроноакцепторными заместителями – заместители – галогены (-Cl, -Br, -I) -I – эффект р-орбиталь атома Г, содержащая неподеленную пару электронов, перекрывается с пи- системой (+М) +М-эффект Г намного слабее, чем у группы –ОН и др. +М и –I компенсируют друга, суммарное электронное влияние Г не является ни электронодонорным, ни электроноакцепторным
 l l Электронодонорные заместители повышают устойчивость промежуточных карбркатионов, образующихся при взаимодействии замещенных производных бензола с электрофилом, скорость реакции производных больше, чем у самого бензола Донорное влияние заместителей особенно сильно проявляется тогда, когда электрофил вступает в о- или п- положение, поэтому о- и п- изомеры образуются быстрее и в больших количествах, чем мизомеры.
l l Электронодонорные заместители повышают устойчивость промежуточных карбркатионов, образующихся при взаимодействии замещенных производных бензола с электрофилом, скорость реакции производных больше, чем у самого бензола Донорное влияние заместителей особенно сильно проявляется тогда, когда электрофил вступает в о- или п- положение, поэтому о- и п- изомеры образуются быстрее и в больших количествах, чем мизомеры.
 l l l Электроноакцепторные заместители уменьшают устойчивость карбокатионов, поэтому такие производные бензола реагируют медленнее, чем бензол. Акцепторное влияние заместителя особенно сильно проявляется тогда, когда электрофил вступает в о- или п- положение, поэтому эти изомеры образуются медленнее и в меньших количествах, чем мизомер Заместители-галогены: делают кольцо менее активным (-I), способствуют образованию о- и п- изомеров (+М)
l l l Электроноакцепторные заместители уменьшают устойчивость карбокатионов, поэтому такие производные бензола реагируют медленнее, чем бензол. Акцепторное влияние заместителя особенно сильно проявляется тогда, когда электрофил вступает в о- или п- положение, поэтому эти изомеры образуются медленнее и в меньших количествах, чем мизомер Заместители-галогены: делают кольцо менее активным (-I), способствуют образованию о- и п- изомеров (+М)
 Природные источники бензола и его гомологов l l l Природные источники – уголь и нефть При нагревании угля до 1000ºС →каменноугольная смола При перегонке каменноугольной смолы – ароматические соединения (бензол, толуол, фенол, нафталин и т. д. )
Природные источники бензола и его гомологов l l l Природные источники – уголь и нефть При нагревании угля до 1000ºС →каменноугольная смола При перегонке каменноугольной смолы – ароматические соединения (бензол, толуол, фенол, нафталин и т. д. )
 Способы синтеза бензола и его гомологов l l l Дегидрирование циклогексана и его гомологов Циклогексан (Pt, Pd, 300ºC)→бензол +3 Н 2 (Зелинский, 1912) Дегидроциклизация алканов Алканы с >6 атомами С (Pt, 300ºC) → бензол или его гомологи + Н 2 Каталитический риформинг нефти
Способы синтеза бензола и его гомологов l l l Дегидрирование циклогексана и его гомологов Циклогексан (Pt, Pd, 300ºC)→бензол +3 Н 2 (Зелинский, 1912) Дегидроциклизация алканов Алканы с >6 атомами С (Pt, 300ºC) → бензол или его гомологи + Н 2 Каталитический риформинг нефти
 Способы синтеза бензола и его гомологов l l l l Диспропорционирование циклоалкенов и циклоалкадиенов 3 циклогексен (Pt, комн. t) → бензол + 2 циклогексан 3 циклогексадиен – 1, 3 (Pt) → 2 бензол + циклогексан Циклотримеризация ацетилена 3 С 2 Н 2 (Сакт, 450ºС) → С 6 Н 6 Алкилирование бензола С 6 Н 6 + RCl → C 6 H 5 Cl + HCl
Способы синтеза бензола и его гомологов l l l l Диспропорционирование циклоалкенов и циклоалкадиенов 3 циклогексен (Pt, комн. t) → бензол + 2 циклогексан 3 циклогексадиен – 1, 3 (Pt) → 2 бензол + циклогексан Циклотримеризация ацетилена 3 С 2 Н 2 (Сакт, 450ºС) → С 6 Н 6 Алкилирование бензола С 6 Н 6 + RCl → C 6 H 5 Cl + HCl


