Некроз_и_апоптоз.ppt
- Количество слайдов: 34
 Апоптоз и некроз
Апоптоз и некроз
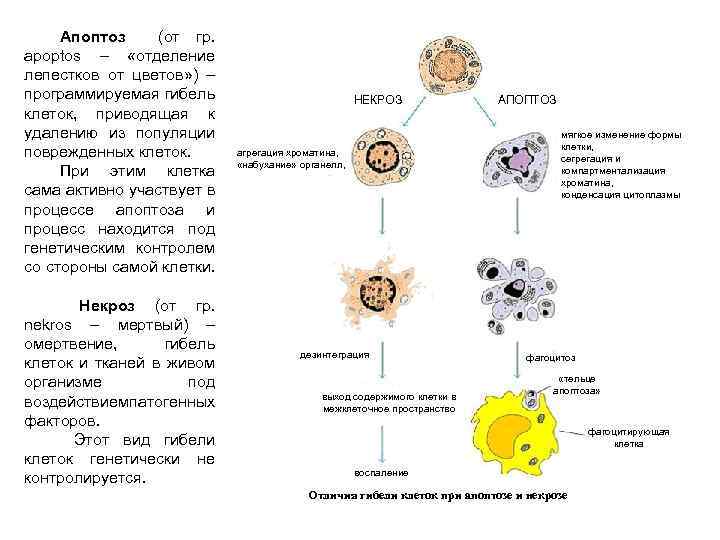 Апоптоз (от гр. apoptos – «отделение лепестков от цветов» ) – программируемая гибель клеток, приводящая к удалению из популяции поврежденных клеток. При этим клетка сама активно участвует в процессе апоптоза и процесс находится под генетическим контролем со стороны самой клетки. Некроз (от гр. nekros – мертвый) – омертвение, гибель клеток и тканей в живом организме под воздействием атогенных п факторов. Этот вид гибели клеток генетически не контролируется. НЕКРОЗ АПОПТОЗ мягкое изменение формы клетки, сегрегация и компартментализация хроматина, конденсация цитоплазмы агрегация хроматина, «набухание» органелл, дезинтеграция выход содержимого клетки в межклеточное пространство фагоцитоз «тельце апоптоза» фагоцитирующая клетка воспаление Отличия гибели клеток при апоптозе и некрозе
Апоптоз (от гр. apoptos – «отделение лепестков от цветов» ) – программируемая гибель клеток, приводящая к удалению из популяции поврежденных клеток. При этим клетка сама активно участвует в процессе апоптоза и процесс находится под генетическим контролем со стороны самой клетки. Некроз (от гр. nekros – мертвый) – омертвение, гибель клеток и тканей в живом организме под воздействием атогенных п факторов. Этот вид гибели клеток генетически не контролируется. НЕКРОЗ АПОПТОЗ мягкое изменение формы клетки, сегрегация и компартментализация хроматина, конденсация цитоплазмы агрегация хроматина, «набухание» органелл, дезинтеграция выход содержимого клетки в межклеточное пространство фагоцитоз «тельце апоптоза» фагоцитирующая клетка воспаление Отличия гибели клеток при апоптозе и некрозе
 Некроз (непрограммируемая форма гибели клетки) характеризуется ее набуханием и разрывом клеточных мембран, что приводит к разрушению органелл, высвобождению ферментов лизосом, выравниванию клеточных градиентов и выходу внутриклеточного содержимого наружу. Некроз является результатом внешнего повреждения клетки, приводящего к остановке метаболизма с утратой способности поддерживать ионный гомеостаз. Дезентиграция клетки и выход клеточного содержимого в наружную среду вызывает ответ со стороны иммунной системы и приводит к развитию воспалительной реакции Некротическая форма гибели при облучении клеток наиболее характерна для сильных воздействий, например для облучения клеток и организма в высоких, летальных дозах. В основе некротической гибели при этом лежит нарушение оксилительно-восстановительного равновесия в клетке, достигающее уровня патологии.
Некроз (непрограммируемая форма гибели клетки) характеризуется ее набуханием и разрывом клеточных мембран, что приводит к разрушению органелл, высвобождению ферментов лизосом, выравниванию клеточных градиентов и выходу внутриклеточного содержимого наружу. Некроз является результатом внешнего повреждения клетки, приводящего к остановке метаболизма с утратой способности поддерживать ионный гомеостаз. Дезентиграция клетки и выход клеточного содержимого в наружную среду вызывает ответ со стороны иммунной системы и приводит к развитию воспалительной реакции Некротическая форма гибели при облучении клеток наиболее характерна для сильных воздействий, например для облучения клеток и организма в высоких, летальных дозах. В основе некротической гибели при этом лежит нарушение оксилительно-восстановительного равновесия в клетке, достигающее уровня патологии.
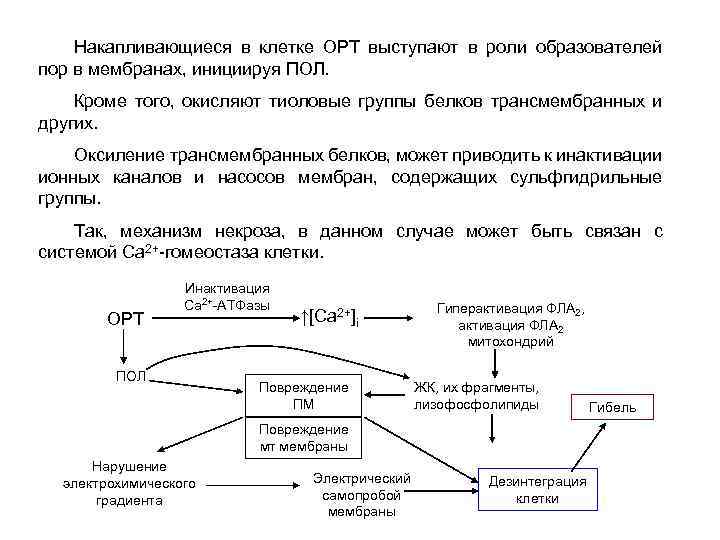 Накапливающиеся в клетке ОРТ выступают в роли образователей пор в мембранах, инициируя ПОЛ. Кроме того, окисляют тиоловые группы белков трансмембранных и других. Оксиление трансмембранных белков, может приводить к инактивации ионных каналов и насосов мембран, содержащих сульфгидрильные группы. Так, механизм некроза, в данном случае может быть связан с системой Са 2+-гомеостаза клетки. ОРТ Инактивация Са 2+-АТФазы ПОЛ ↑[Ca 2+]i Повреждение ПМ Гиперактивация ФЛА 2, активация ФЛА 2 митохондрий ЖК, их фрагменты, лизофосфолипиды Гибель Повреждение мт мембраны Нарушение электрохимического градиента Электрический самопробой мембраны Дезинтеграция клетки
Накапливающиеся в клетке ОРТ выступают в роли образователей пор в мембранах, инициируя ПОЛ. Кроме того, окисляют тиоловые группы белков трансмембранных и других. Оксиление трансмембранных белков, может приводить к инактивации ионных каналов и насосов мембран, содержащих сульфгидрильные группы. Так, механизм некроза, в данном случае может быть связан с системой Са 2+-гомеостаза клетки. ОРТ Инактивация Са 2+-АТФазы ПОЛ ↑[Ca 2+]i Повреждение ПМ Гиперактивация ФЛА 2, активация ФЛА 2 митохондрий ЖК, их фрагменты, лизофосфолипиды Гибель Повреждение мт мембраны Нарушение электрохимического градиента Электрический самопробой мембраны Дезинтеграция клетки
 Апоптоз Явление программируемой клеточной смерти, сопровождаемой набором характерных морфологических признаков (маркеров апоптоза) и молекулярных процессов, имеющих различия у одноклеточных и многоклеточных организмов (т. е. изменений в строении и функционировании клетки, характерных для апоптоза). Отличие апоптоза заключается в том, что это программируемая клеточная гибель, то есть существуют определенные механизмы, в результате реализации которых клетка сама завершает свое существование. Термин"апоптоз", предложенный в 1972 г. английскими учеными J. F. R. Кеrr, А. Н. Wyllie и A. R. Currie, состоит из двух греческих слов и означает в буквальном смысле "отделение лепестков от цветов", а применимо к клетке - особый тип смерти путем разделения ее на части ("апоптозные тельца"), которые впоследствии фагоцитируются соседними клетками разного типа. Основное биологическое назначение апоптоза состоит в том, чтобы в процессе эмбрионального морфонегеза создавать органы и ткани с эволюционно закрепленными конфигурациями и размерами и затем поддерживать эти параметры с допустимыми допусками в течение жизни. Важнейшим проявлением этой функции апоптоза после окончания развития человека и других млекопитающих является его участие в процессе физиологической регенерации (обновления) клеток разных тканей и органов и поддержании клеточного гомеостаза. Другой важнейшей функцией апоптоза является контроль за внутренней средой клетки, в том числе клеточного ядра с его содержимым. При возникновении в клетке нарушений, превышающие допустимые пределы, клетка подвергается самоуничтожению. Апоптоз возникает при действии различных повреждающих факторов, которые способны вызвать некроз, но действующих в небольших дозах, например, при действии высокой температуры, ионизирующего излучения, противоопухолевых препаратов.
Апоптоз Явление программируемой клеточной смерти, сопровождаемой набором характерных морфологических признаков (маркеров апоптоза) и молекулярных процессов, имеющих различия у одноклеточных и многоклеточных организмов (т. е. изменений в строении и функционировании клетки, характерных для апоптоза). Отличие апоптоза заключается в том, что это программируемая клеточная гибель, то есть существуют определенные механизмы, в результате реализации которых клетка сама завершает свое существование. Термин"апоптоз", предложенный в 1972 г. английскими учеными J. F. R. Кеrr, А. Н. Wyllie и A. R. Currie, состоит из двух греческих слов и означает в буквальном смысле "отделение лепестков от цветов", а применимо к клетке - особый тип смерти путем разделения ее на части ("апоптозные тельца"), которые впоследствии фагоцитируются соседними клетками разного типа. Основное биологическое назначение апоптоза состоит в том, чтобы в процессе эмбрионального морфонегеза создавать органы и ткани с эволюционно закрепленными конфигурациями и размерами и затем поддерживать эти параметры с допустимыми допусками в течение жизни. Важнейшим проявлением этой функции апоптоза после окончания развития человека и других млекопитающих является его участие в процессе физиологической регенерации (обновления) клеток разных тканей и органов и поддержании клеточного гомеостаза. Другой важнейшей функцией апоптоза является контроль за внутренней средой клетки, в том числе клеточного ядра с его содержимым. При возникновении в клетке нарушений, превышающие допустимые пределы, клетка подвергается самоуничтожению. Апоптоз возникает при действии различных повреждающих факторов, которые способны вызвать некроз, но действующих в небольших дозах, например, при действии высокой температуры, ионизирующего излучения, противоопухолевых препаратов.
 В процессе апоптоза в клетке задействованы сложные молекулярные каскады, в результате реализации которых происходит сморщивание цитоплазматической мембраны, уменьшение объёма клетки, разрывы нитей ядерной ДНК, конденсация хроматина по периферии ядра, последующий распад ядра на части, фрагментация клеток на везикулы (пузырьки) с внутриклеточным содержимым — апоптотические тельца или «тельца апоптоза» , которые захватываются соседними клетками, а также фагоцитами. Выброса клеточного содержимого не происходит, в связи с чем воспаления, сопровождающего, как правило, некроз, не возникает. Фазы апоптоза 1. Сигнальная фаза (индукция и проведения сигнала); 2. Эффекторная фаза (различные инициирующие пути конвертируются в один общий путь апоптоза); 3. Деградационная фаза
В процессе апоптоза в клетке задействованы сложные молекулярные каскады, в результате реализации которых происходит сморщивание цитоплазматической мембраны, уменьшение объёма клетки, разрывы нитей ядерной ДНК, конденсация хроматина по периферии ядра, последующий распад ядра на части, фрагментация клеток на везикулы (пузырьки) с внутриклеточным содержимым — апоптотические тельца или «тельца апоптоза» , которые захватываются соседними клетками, а также фагоцитами. Выброса клеточного содержимого не происходит, в связи с чем воспаления, сопровождающего, как правило, некроз, не возникает. Фазы апоптоза 1. Сигнальная фаза (индукция и проведения сигнала); 2. Эффекторная фаза (различные инициирующие пути конвертируются в один общий путь апоптоза); 3. Деградационная фаза
 Сигнальная фаза апоптоза Основных пути индукции сигнала апоптоза: рецептор-зависимый сигнальный путь с участием рецепторов гибели клетки (рецепторы смерти) (Death receptors - DR) и митохондриальный путь. Оба пути приводят к активации каспаз и запуску каскада реакций приводящих к гибели клетки.
Сигнальная фаза апоптоза Основных пути индукции сигнала апоптоза: рецептор-зависимый сигнальный путь с участием рецепторов гибели клетки (рецепторы смерти) (Death receptors - DR) и митохондриальный путь. Оба пути приводят к активации каспаз и запуску каскада реакций приводящих к гибели клетки.
 Рецептор-зависимый путь Рецептор-зависимый сигнальный путь индукции апоптоза начинается с взаимодействия специфических внеклеточных лигандов с рецепторами клеточной гибели, экспрессированными на поверхности клеточной мембраны. Наиболее изученными рецепторами смерти, для которых описана и определена роль в апоптозе, являются CD 95 (Apo 1, Fas) и TNFR 1 (tumor necrosis factor receptor 1). К дополнительным относятся DR 3 (Apo 3, Wsl 1), DR 4 и DR 5. . Все рецепторы смерти содержат общую последовательность из 80 аминокислотных остатков в цитоплазматическом участке, получившую название «death domain» - домен смерти - DD.
Рецептор-зависимый путь Рецептор-зависимый сигнальный путь индукции апоптоза начинается с взаимодействия специфических внеклеточных лигандов с рецепторами клеточной гибели, экспрессированными на поверхности клеточной мембраны. Наиболее изученными рецепторами смерти, для которых описана и определена роль в апоптозе, являются CD 95 (Apo 1, Fas) и TNFR 1 (tumor necrosis factor receptor 1). К дополнительным относятся DR 3 (Apo 3, Wsl 1), DR 4 и DR 5. . Все рецепторы смерти содержат общую последовательность из 80 аминокислотных остатков в цитоплазматическом участке, получившую название «death domain» - домен смерти - DD.
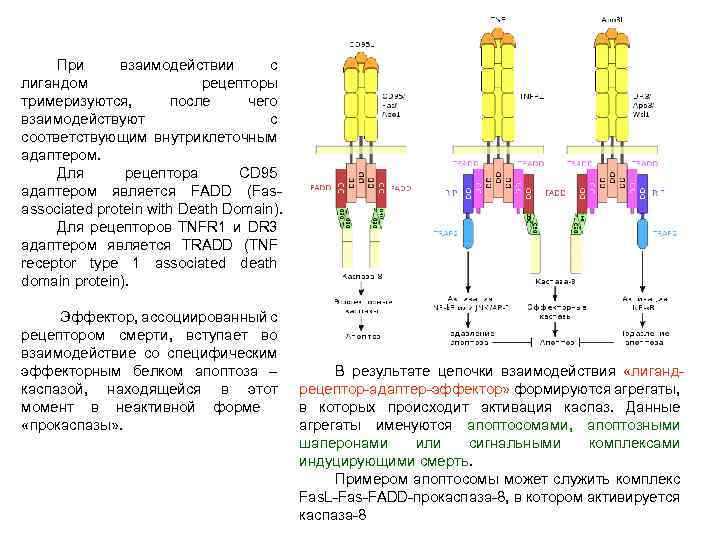 При взаимодействии с лигандом рецепторы тримеризуются, после чего взаимодействуют с соответствующим внутриклеточным адаптером. Для рецептора CD 95 адаптером является FADD (Fasassociated protein with Death Domain). Для рецепторов TNFR 1 и DR 3 адаптером является TRADD (TNF receptor type 1 associated death domain protein). Эффектор, ассоциированный с рецептором смерти, вступает во взаимодействие со специфическим эффекторным белком апоптоза – каспазой, находящейся в этот момент в неактивной форме «прокаспазы» . В результате цепочки взаимодействия «лигандрецептор-адаптер-эффектор» формируются агрегаты, в которых происходит активация каспаз. Данные агрегаты именуются апоптосомами, апоптозными шаперонами или сигнальными комплексами индуцирующими смерть. Примером апоптосомы может служить комплекс Fas. L-Fas-FADD-прокаспаза-8, в котором активируется каспаза-8
При взаимодействии с лигандом рецепторы тримеризуются, после чего взаимодействуют с соответствующим внутриклеточным адаптером. Для рецептора CD 95 адаптером является FADD (Fasassociated protein with Death Domain). Для рецепторов TNFR 1 и DR 3 адаптером является TRADD (TNF receptor type 1 associated death domain protein). Эффектор, ассоциированный с рецептором смерти, вступает во взаимодействие со специфическим эффекторным белком апоптоза – каспазой, находящейся в этот момент в неактивной форме «прокаспазы» . В результате цепочки взаимодействия «лигандрецептор-адаптер-эффектор» формируются агрегаты, в которых происходит активация каспаз. Данные агрегаты именуются апоптосомами, апоптозными шаперонами или сигнальными комплексами индуцирующими смерть. Примером апоптосомы может служить комплекс Fas. L-Fas-FADD-прокаспаза-8, в котором активируется каспаза-8
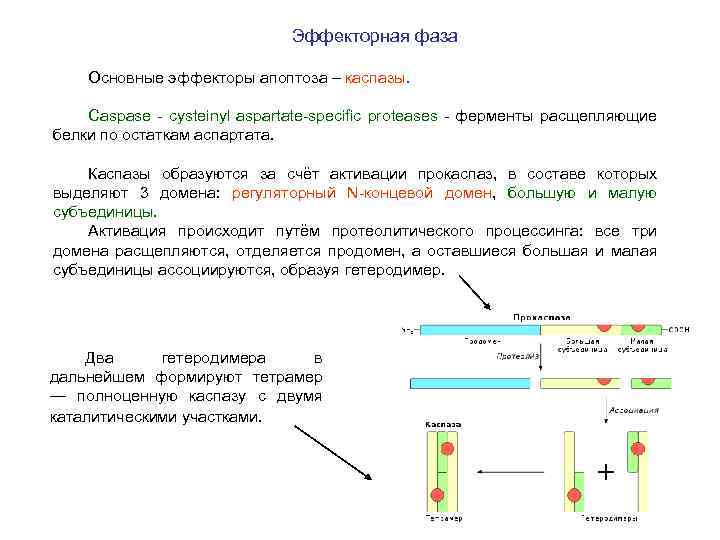 Эффекторная фаза Основные эффекторы апоптоза – каспазы. Caspase - cysteinyl aspartate-specific proteases - ферменты расщепляющие белки по остаткам аспартата. Каспазы образуются за счёт активации прокаспаз, в составе которых выделяют 3 домена: регуляторный N-концевой домен, большую и малую субъединицы. Активация происходит путём протеолитического процессинга: все три домена расщепляются, отделяется продомен, а оставшиеся большая и малая субъединицы ассоциируются, образуя гетеродимер. Два гетеродимера в дальнейшем формируют тетрамер — полноценную каспазу с двумя каталитическими участками.
Эффекторная фаза Основные эффекторы апоптоза – каспазы. Caspase - cysteinyl aspartate-specific proteases - ферменты расщепляющие белки по остаткам аспартата. Каспазы образуются за счёт активации прокаспаз, в составе которых выделяют 3 домена: регуляторный N-концевой домен, большую и малую субъединицы. Активация происходит путём протеолитического процессинга: все три домена расщепляются, отделяется продомен, а оставшиеся большая и малая субъединицы ассоциируются, образуя гетеродимер. Два гетеродимера в дальнейшем формируют тетрамер — полноценную каспазу с двумя каталитическими участками.
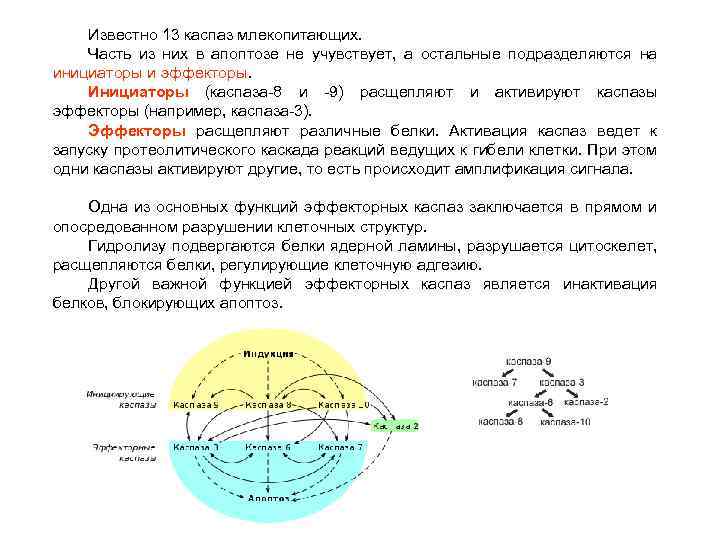 Известно 13 каспаз млекопитающих. Часть из них в апоптозе не учувствует, а остальные подразделяются на инициаторы и эффекторы. Инициаторы (каспаза-8 и -9) расщепляют и активируют каспазы эффекторы (например, каспаза-3). Эффекторы расщепляют различные белки. Активация каспаз ведет к запуску протеолитического каскада реакций ведущих к гибели клетки. При этом одни каспазы активируют другие, то есть происходит амплификация сигнала. Одна из основных функций эффекторных каспаз заключается в прямом и опосредованном разрушении клеточных структур. Гидролизу подвергаются белки ядерной ламины, разрушается цитоскелет, расщепляются белки, регулирующие клеточную адгезию. Другой важной функцией эффекторных каспаз является инактивация белков, блокирующих апоптоз.
Известно 13 каспаз млекопитающих. Часть из них в апоптозе не учувствует, а остальные подразделяются на инициаторы и эффекторы. Инициаторы (каспаза-8 и -9) расщепляют и активируют каспазы эффекторы (например, каспаза-3). Эффекторы расщепляют различные белки. Активация каспаз ведет к запуску протеолитического каскада реакций ведущих к гибели клетки. При этом одни каспазы активируют другие, то есть происходит амплификация сигнала. Одна из основных функций эффекторных каспаз заключается в прямом и опосредованном разрушении клеточных структур. Гидролизу подвергаются белки ядерной ламины, разрушается цитоскелет, расщепляются белки, регулирующие клеточную адгезию. Другой важной функцией эффекторных каспаз является инактивация белков, блокирующих апоптоз.
 Помимо каспаз существуют и другие эффекторы апоптоза. Например, флавопротеин AIF, высвобождающийся из межмембранного пространства митохондрий, действует по независимому от каспаз пути. Попадая в клеточное ядро, AIF вызывает конденсацию хроматина и активирует эндонуклеазы, которые участвуют в фрагментации ДНК. На уровне генетического материала в ходе апоптоза происходит фрагментация ДНК с участием ферментов нуклеаз, расщепляющих ДНК. Изначально образуются крупные фрагменты с 30 000— 700 000 пар оснований, которые в дальнейшем расщепляются в межнуклеосомной области на отрезки по 180— 190 пар оснований или кратные этим величинам.
Помимо каспаз существуют и другие эффекторы апоптоза. Например, флавопротеин AIF, высвобождающийся из межмембранного пространства митохондрий, действует по независимому от каспаз пути. Попадая в клеточное ядро, AIF вызывает конденсацию хроматина и активирует эндонуклеазы, которые участвуют в фрагментации ДНК. На уровне генетического материала в ходе апоптоза происходит фрагментация ДНК с участием ферментов нуклеаз, расщепляющих ДНК. Изначально образуются крупные фрагменты с 30 000— 700 000 пар оснований, которые в дальнейшем расщепляются в межнуклеосомной области на отрезки по 180— 190 пар оснований или кратные этим величинам.
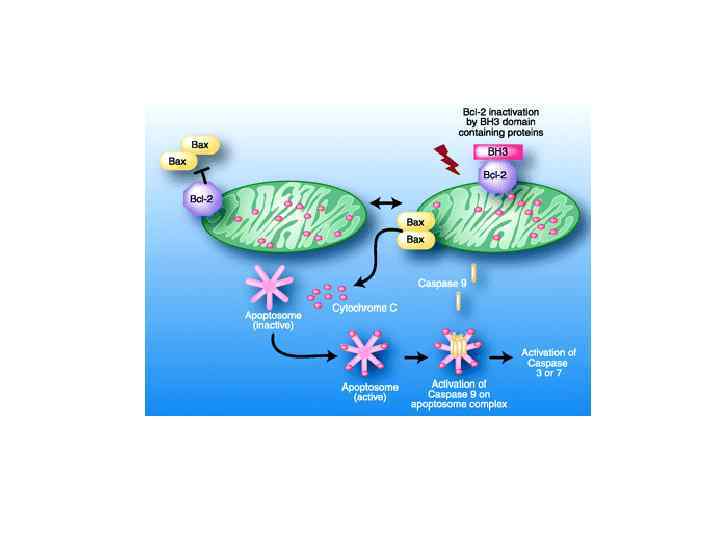
 Митохондриальный путь Митохондриальный сигнальный путь индукции апоптоза реализуется в результате выхода апоптогенных белков из межмембранного пространства митохондрий в цитоплазму клетки. Высвобождение апоптогенных белков, предположительно, может осуществляться двумя путями: за счёт разрыва митохондриальной мембраны или же путём открытия высокопроницаемых каналов на внешней мембране митохондрий. В цитоплазму высвобождаются: цитохром c — белок с молекулярной массой 15 к. Да; прокаспазы − 2, − 3 и − 9; AIF (Apoptosis Inducing Factor) — флавопротеин с молекулярной массой 57 к. Да. SMAC
Митохондриальный путь Митохондриальный сигнальный путь индукции апоптоза реализуется в результате выхода апоптогенных белков из межмембранного пространства митохондрий в цитоплазму клетки. Высвобождение апоптогенных белков, предположительно, может осуществляться двумя путями: за счёт разрыва митохондриальной мембраны или же путём открытия высокопроницаемых каналов на внешней мембране митохондрий. В цитоплазму высвобождаются: цитохром c — белок с молекулярной массой 15 к. Да; прокаспазы − 2, − 3 и − 9; AIF (Apoptosis Inducing Factor) — флавопротеин с молекулярной массой 57 к. Да. SMAC
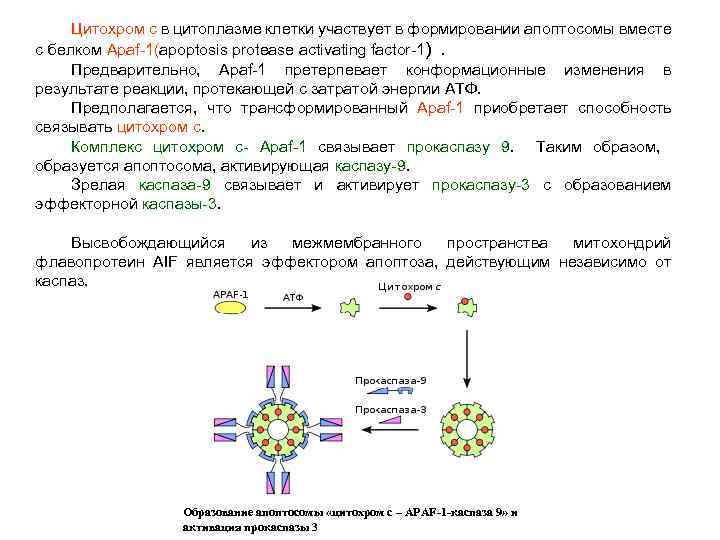 Цитохром c в цитоплазме клетки участвует в формировании апоптосомы вместе с белком Apaf-1(apoptosis protease activating factor-1) . Предварительно, Apaf-1 претерпевает конформационные изменения в результате реакции, протекающей с затратой энергии АТФ. Предполагается, что трансформированный Apaf-1 приобретает способность связывать цитохром c. Комплекс цитохром с- Apaf-1 связывает прокаспазу 9. Таким образом, образуется апоптосома, активирующая каспазу-9. Зрелая каспаза-9 связывает и активирует прокаспазу-3 с образованием эффекторной каспазы-3. Высвобождающийся из межмембранного пространства митохондрий флавопротеин AIF является эффектором апоптоза, действующим независимо от каспаз. Образование апоптосомы «цитохром с – APAF-1 -каспаза 9» и активация прокаспазы 3
Цитохром c в цитоплазме клетки участвует в формировании апоптосомы вместе с белком Apaf-1(apoptosis protease activating factor-1) . Предварительно, Apaf-1 претерпевает конформационные изменения в результате реакции, протекающей с затратой энергии АТФ. Предполагается, что трансформированный Apaf-1 приобретает способность связывать цитохром c. Комплекс цитохром с- Apaf-1 связывает прокаспазу 9. Таким образом, образуется апоптосома, активирующая каспазу-9. Зрелая каспаза-9 связывает и активирует прокаспазу-3 с образованием эффекторной каспазы-3. Высвобождающийся из межмембранного пространства митохондрий флавопротеин AIF является эффектором апоптоза, действующим независимо от каспаз. Образование апоптосомы «цитохром с – APAF-1 -каспаза 9» и активация прокаспазы 3
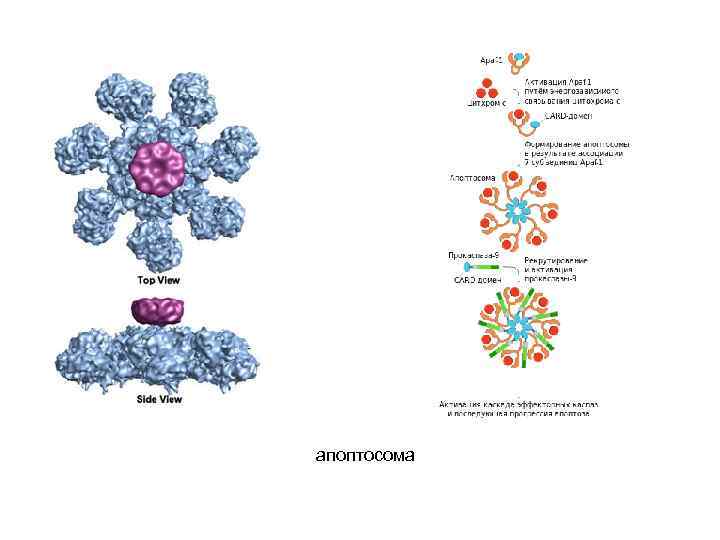 апоптосома
апоптосома
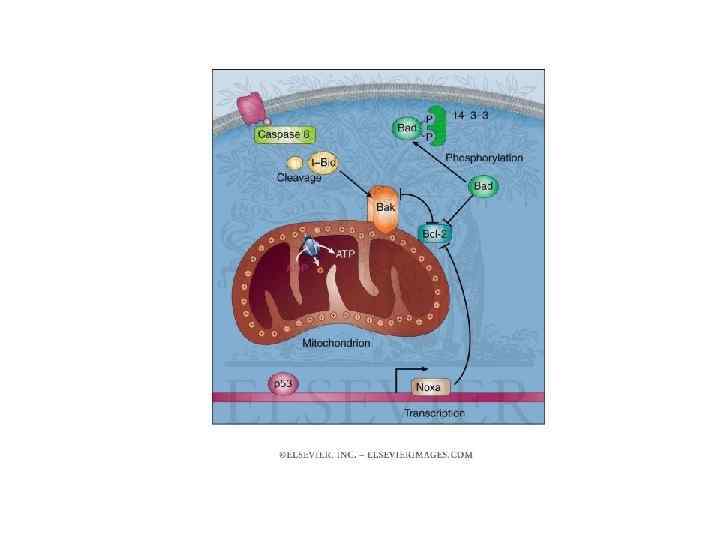
 Механизмы регуляции апоптоза Основными регуляторами апоптоза в клетках являются белки семейства Bcl-2 (B-cell lymphoma 2). В семействе Bcl-2 различают проапоптозные и антиапоптозные белки. К группе ингибиторов апоптоза принадлежат: Bcl-2, Bcl-x. L, Bcl-w, Md-1, A-1, Boo и др. К противоположной группе промоторов апоптоза относят белки подсемейства Bax и BH 3: Вах, Bad, Bok, Bcl-x. S, Bak, Bid, Bik, Bim, Krk, Mtd и др. Предполагается, что для регуляции ответа клетки на сигналы смерти, имеет значение соотношение про- и антиапоптозных белков. При этом регуляция апоптоза белками семейства Bcl-2 осуществляется преимущественно на отрезке митохондриального сигнального пути, так как сигналы от рецепторов смерти в основном обходят контроль со стороны Bcl-2.
Механизмы регуляции апоптоза Основными регуляторами апоптоза в клетках являются белки семейства Bcl-2 (B-cell lymphoma 2). В семействе Bcl-2 различают проапоптозные и антиапоптозные белки. К группе ингибиторов апоптоза принадлежат: Bcl-2, Bcl-x. L, Bcl-w, Md-1, A-1, Boo и др. К противоположной группе промоторов апоптоза относят белки подсемейства Bax и BH 3: Вах, Bad, Bok, Bcl-x. S, Bak, Bid, Bik, Bim, Krk, Mtd и др. Предполагается, что для регуляции ответа клетки на сигналы смерти, имеет значение соотношение про- и антиапоптозных белков. При этом регуляция апоптоза белками семейства Bcl-2 осуществляется преимущественно на отрезке митохондриального сигнального пути, так как сигналы от рецепторов смерти в основном обходят контроль со стороны Bcl-2.
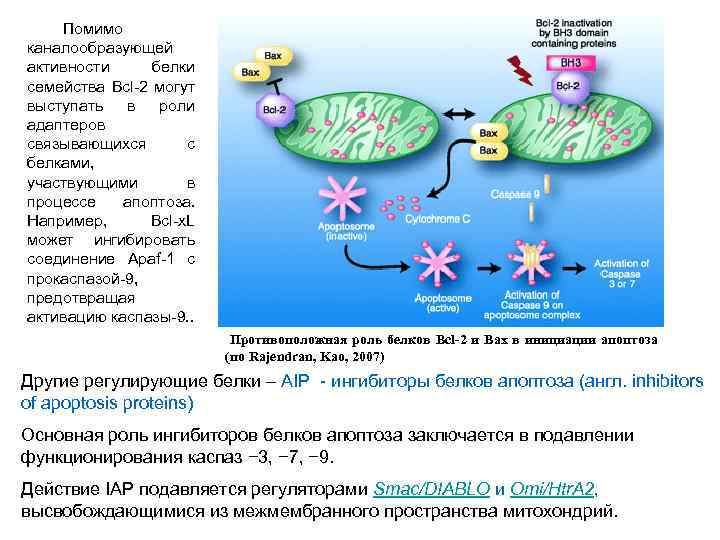 Помимо каналообразующей активности белки семейства Bcl-2 могут выступать в роли адаптеров связывающихся с белками, участвующими в процессе апоптоза. Например, Bcl-x. L может ингибировать соединение Apaf-1 с прокаспазой-9, предотвращая активацию каспазы-9. . Противоположная роль белков Bcl-2 и Bax в инициации апоптоза (по Rajendran, Kao, 2007) Другие регулирующие белки – AIP - ингибиторы белков апоптоза (англ. inhibitors of apoptosis proteins) Основная роль ингибиторов белков апоптоза заключается в подавлении функционирования каспаз − 3, − 7, − 9. Действие IAP подавляется регуляторами Smac/DIABLO и Omi/Htr. A 2, высвобождающимися из межмембранного пространства митохондрий.
Помимо каналообразующей активности белки семейства Bcl-2 могут выступать в роли адаптеров связывающихся с белками, участвующими в процессе апоптоза. Например, Bcl-x. L может ингибировать соединение Apaf-1 с прокаспазой-9, предотвращая активацию каспазы-9. . Противоположная роль белков Bcl-2 и Bax в инициации апоптоза (по Rajendran, Kao, 2007) Другие регулирующие белки – AIP - ингибиторы белков апоптоза (англ. inhibitors of apoptosis proteins) Основная роль ингибиторов белков апоптоза заключается в подавлении функционирования каспаз − 3, − 7, − 9. Действие IAP подавляется регуляторами Smac/DIABLO и Omi/Htr. A 2, высвобождающимися из межмембранного пространства митохондрий.
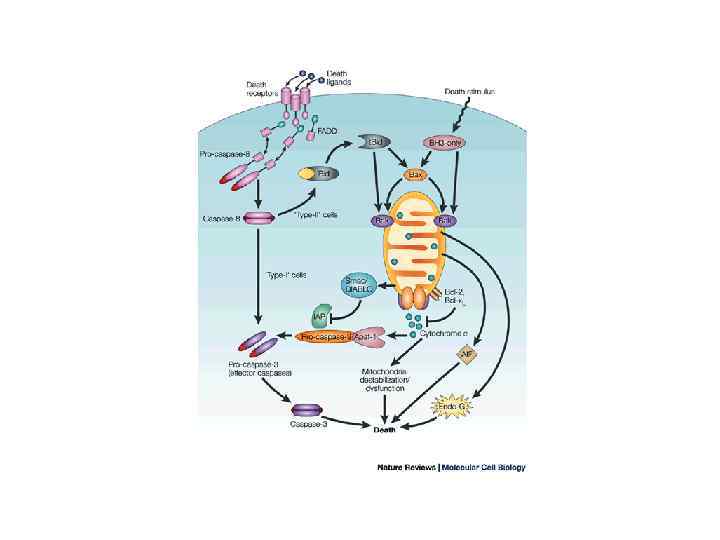
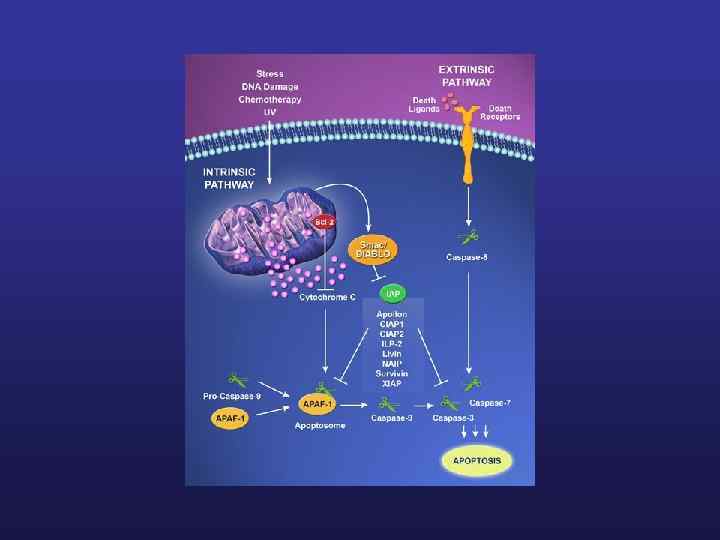
 Другие пути индукции апоптоза В качестве ещё одного фактора индукции апоптоза рассматривается атака инфицированных клеток цитотоксическими Т-лимфоцитами, которые, помимо активации Fas-рецептора, способны секретировать перфорин вблизи мембраны заражённой клетки. Перфорин, полимеризуясь, образует трансмембранные каналы, через которые внутрь клетки поступают гранзимы. Далее гранзим B активирует каспазу-3 и запускается каспазный каскад. Возможна инициация клеточной смерти при высвобождении лизосомальных протеаз — катепсинов. К примеру, каспаза-8 вызывает выход из лизосом активного катепсина B, который затем расщепляет регуляторный белок Bid. В результате образуется активный белок t-Bid, активирующий в свою очередь проапоптозный белок Bax. -Еще одним фактором, способным запускать апоптоз, является церамид, высвобождаемый из мембраны клеток ферментом сфингомиелиназой. Не смотря на то, что сигнальные пути, запускаемые церамидом до конца не изучены, показано, что потенциальными мишенями церамида, являются серин-треотиновые фосфатазы (ceramid-activated serine/threonine phosphatases – CAPP), так называемые PP 2 A и PP 1. Активированные фосфатазы действию на различные белки клетки, в том числе такой проапоптозный фактор, как Bcl 2, что может приводить к апоптозу.
Другие пути индукции апоптоза В качестве ещё одного фактора индукции апоптоза рассматривается атака инфицированных клеток цитотоксическими Т-лимфоцитами, которые, помимо активации Fas-рецептора, способны секретировать перфорин вблизи мембраны заражённой клетки. Перфорин, полимеризуясь, образует трансмембранные каналы, через которые внутрь клетки поступают гранзимы. Далее гранзим B активирует каспазу-3 и запускается каспазный каскад. Возможна инициация клеточной смерти при высвобождении лизосомальных протеаз — катепсинов. К примеру, каспаза-8 вызывает выход из лизосом активного катепсина B, который затем расщепляет регуляторный белок Bid. В результате образуется активный белок t-Bid, активирующий в свою очередь проапоптозный белок Bax. -Еще одним фактором, способным запускать апоптоз, является церамид, высвобождаемый из мембраны клеток ферментом сфингомиелиназой. Не смотря на то, что сигнальные пути, запускаемые церамидом до конца не изучены, показано, что потенциальными мишенями церамида, являются серин-треотиновые фосфатазы (ceramid-activated serine/threonine phosphatases – CAPP), так называемые PP 2 A и PP 1. Активированные фосфатазы действию на различные белки клетки, в том числе такой проапоптозный фактор, как Bcl 2, что может приводить к апоптозу.
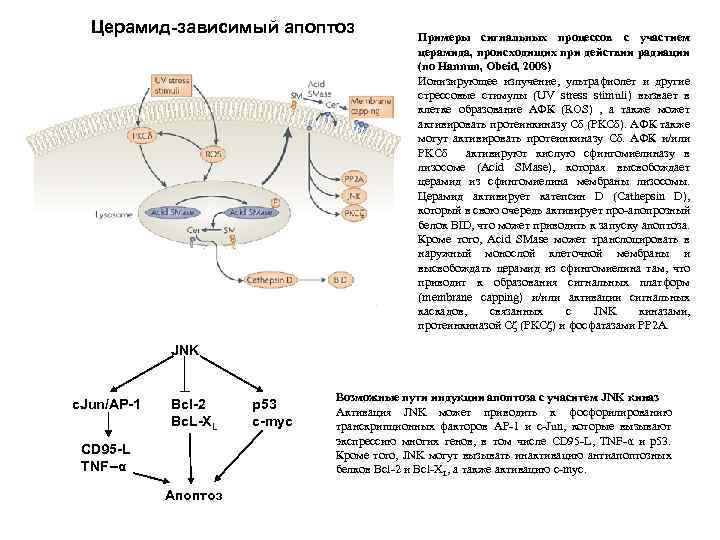 Церамид-зависимый апоптоз Примеры сигнальных процессов с участием церамида, происходищих при действии радиации (по Hannun, Obeid, 2008) Ионизирующее излучение, ультрафиолет и другие стрессовые стимулы (UV stress stimuli) вызвает в клетке образование АФК (ROS) , а также может активировать протеинкиназу Сδ (PKCδ). АФК также могут активировать протеинкиназу Сδ. АФК и/или PKCδ активируют кислую сфингомиелиназу в лизосоме (Acid SMase), которая высвобождает церамид из сфингомиелина мембраны лизосомы. Церамид активирует катепсин D (Cathepsin D), который в свою очередь активирует про-апопрозный белок BID, что может приводить к запуску апоптоза. Кроме того, Acid SMase может транслоцировать в наружный монослой клеточной мембраны и высвобождать церамид из сфингомиелина там, что приводит к образования сигнальных платформ (membrane capping) и/или активации сигнальных каскадов, связанных с JNK киназами, протеинкиназой Сζ (PKCζ) и фосфатазами РР 2 А. JNK c. Jun/AP-1 Bcl-2 Bc. L-XL CD 95 -L TNF--α Апоптоз p 53 c-myc Возможные пути индукции апоптоза с учаситем JNK киназ Активация JNK может приводить к фосфорилированию транскрипционных факторов AP-1 и с-Jun, которые вызывают экспрессию многих генов, в том числе CD 95 -L, TNF-α и p 53. Кроме того, JNK могут вызывать инактивацию антиапоптозных белков Bcl-2 и Bcl-XL, а также активацию c-myc.
Церамид-зависимый апоптоз Примеры сигнальных процессов с участием церамида, происходищих при действии радиации (по Hannun, Obeid, 2008) Ионизирующее излучение, ультрафиолет и другие стрессовые стимулы (UV stress stimuli) вызвает в клетке образование АФК (ROS) , а также может активировать протеинкиназу Сδ (PKCδ). АФК также могут активировать протеинкиназу Сδ. АФК и/или PKCδ активируют кислую сфингомиелиназу в лизосоме (Acid SMase), которая высвобождает церамид из сфингомиелина мембраны лизосомы. Церамид активирует катепсин D (Cathepsin D), который в свою очередь активирует про-апопрозный белок BID, что может приводить к запуску апоптоза. Кроме того, Acid SMase может транслоцировать в наружный монослой клеточной мембраны и высвобождать церамид из сфингомиелина там, что приводит к образования сигнальных платформ (membrane capping) и/или активации сигнальных каскадов, связанных с JNK киназами, протеинкиназой Сζ (PKCζ) и фосфатазами РР 2 А. JNK c. Jun/AP-1 Bcl-2 Bc. L-XL CD 95 -L TNF--α Апоптоз p 53 c-myc Возможные пути индукции апоптоза с учаситем JNK киназ Активация JNK может приводить к фосфорилированию транскрипционных факторов AP-1 и с-Jun, которые вызывают экспрессию многих генов, в том числе CD 95 -L, TNF-α и p 53. Кроме того, JNK могут вызывать инактивацию антиапоптозных белков Bcl-2 и Bcl-XL, а также активацию c-myc.
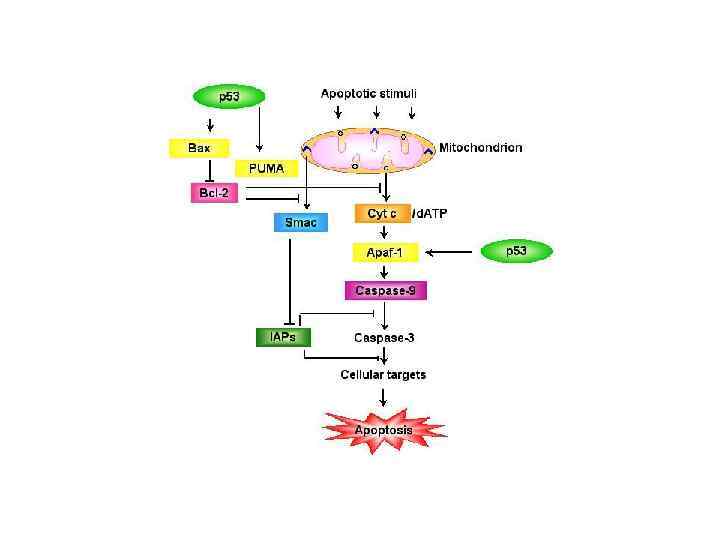
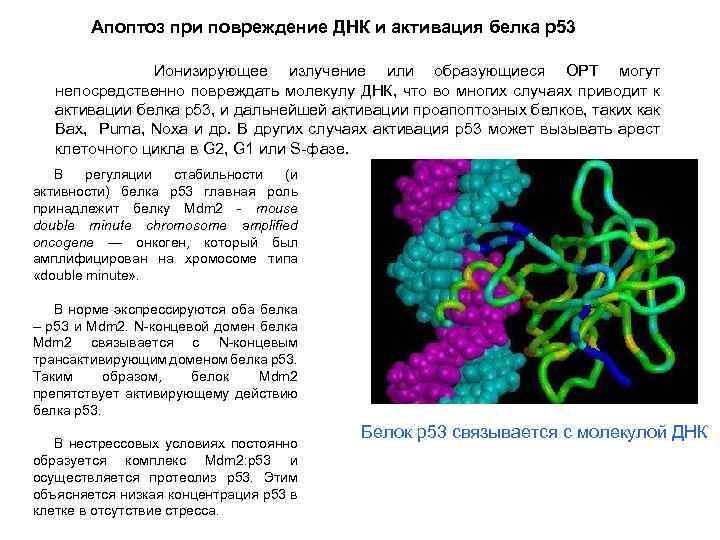 Апоптоз при повреждение ДНК и активация белка р53 Ионизирующее излучение или образующиеся ОРТ могут непосредственно повреждать молекулу ДНК, что во многих случаях приводит к активации белка р53, и дальнейшей активации проапоптозных белков, таких как Bax, Puma, Noxa и др. В других случаях активация р53 может вызывать арест клеточного цикла в G 2, G 1 или S-фазе. В регуляции стабильности (и активности) белка р53 главная роль принадлежит белку Mdm 2 - mouse double minute chromosome amplified oncogene — онкоген, который был амплифицирован на хромосоме типа «double minute» . В норме экспрессируются оба белка – p 53 и Mdm 2. N-концевой домен белка Mdm 2 связывается с N-концевым трансактивирующим доменом белка р53. Таким образом, белок Mdm 2 препятствует активирующему действию белка р53. В нестрессовых условиях постоянно образуется комплекс Mdm 2: р53 и осуществляется протеолиз р53. Этим объясняется низкая концентрация р53 в клетке в отсутствие стресса. Белок p 53 связывается с молекулой ДНК
Апоптоз при повреждение ДНК и активация белка р53 Ионизирующее излучение или образующиеся ОРТ могут непосредственно повреждать молекулу ДНК, что во многих случаях приводит к активации белка р53, и дальнейшей активации проапоптозных белков, таких как Bax, Puma, Noxa и др. В других случаях активация р53 может вызывать арест клеточного цикла в G 2, G 1 или S-фазе. В регуляции стабильности (и активности) белка р53 главная роль принадлежит белку Mdm 2 - mouse double minute chromosome amplified oncogene — онкоген, который был амплифицирован на хромосоме типа «double minute» . В норме экспрессируются оба белка – p 53 и Mdm 2. N-концевой домен белка Mdm 2 связывается с N-концевым трансактивирующим доменом белка р53. Таким образом, белок Mdm 2 препятствует активирующему действию белка р53. В нестрессовых условиях постоянно образуется комплекс Mdm 2: р53 и осуществляется протеолиз р53. Этим объясняется низкая концентрация р53 в клетке в отсутствие стресса. Белок p 53 связывается с молекулой ДНК
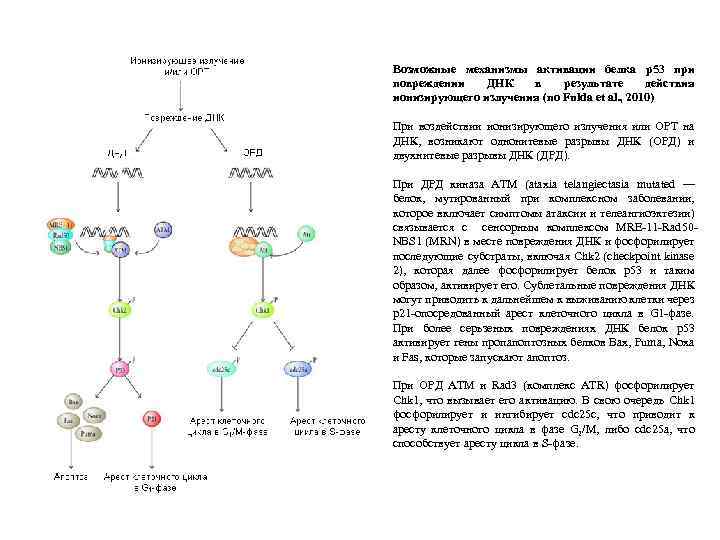 Возможные механизмы активации белка р53 при повреждении ДНК в результате действия ионизирующего излучения (по Fulda et al. , 2010) При воздействии ионизирующего излучения или ОРТ на ДНК, возникают однонитевые разрывы ДНК (ОРД) и двухнитевые разрывы ДНК (ДРД). При ДРД киназа АТМ (ataxia telangiectasia mutated — белок, мутированный при комплексном заболевании, которое включает симптомы атаксии и телеангиоэктезии) связывается с сенсорным комплексом MRE-11 -Rad 50 NBS 1 (MRN) в месте повреждения ДНК и фосфорилирует последующие субстраты, включая Chk 2 (checkpoint kinase 2), которая далее фосфорилирует белок р53 и таким образом, активирует его. Сублетальные повреждения ДНК могут приводить к дальнейшем к выживанию клетки через р21 -опосредованный арест клеточного цикла в G 1 -фазе. При более серьзеных повреждениях ДНК белок р53 активирует гены пропапоптозных белков Bax, Puma, Noxa и Fas, которые запускают апоптоз. При ОРД ATM и Rad 3 (комплекс ATR) фосфорилирует Chk 1, что вызывает его активацию. В свою очередь Chk 1 фосфорилирует и ингибирует cdc 25 c, что приводит к аресту клеточного цикла в фазе G 2/M, либо cdc 25 a, что способствует аресту цикла в S-фазе.
Возможные механизмы активации белка р53 при повреждении ДНК в результате действия ионизирующего излучения (по Fulda et al. , 2010) При воздействии ионизирующего излучения или ОРТ на ДНК, возникают однонитевые разрывы ДНК (ОРД) и двухнитевые разрывы ДНК (ДРД). При ДРД киназа АТМ (ataxia telangiectasia mutated — белок, мутированный при комплексном заболевании, которое включает симптомы атаксии и телеангиоэктезии) связывается с сенсорным комплексом MRE-11 -Rad 50 NBS 1 (MRN) в месте повреждения ДНК и фосфорилирует последующие субстраты, включая Chk 2 (checkpoint kinase 2), которая далее фосфорилирует белок р53 и таким образом, активирует его. Сублетальные повреждения ДНК могут приводить к дальнейшем к выживанию клетки через р21 -опосредованный арест клеточного цикла в G 1 -фазе. При более серьзеных повреждениях ДНК белок р53 активирует гены пропапоптозных белков Bax, Puma, Noxa и Fas, которые запускают апоптоз. При ОРД ATM и Rad 3 (комплекс ATR) фосфорилирует Chk 1, что вызывает его активацию. В свою очередь Chk 1 фосфорилирует и ингибирует cdc 25 c, что приводит к аресту клеточного цикла в фазе G 2/M, либо cdc 25 a, что способствует аресту цикла в S-фазе.
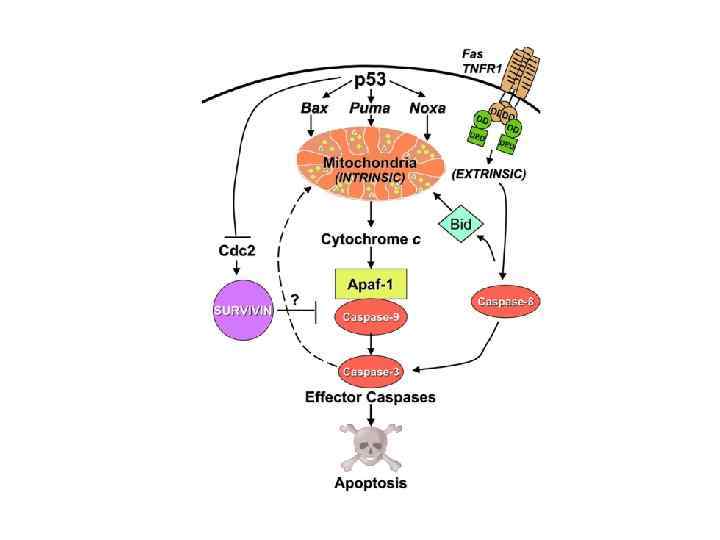
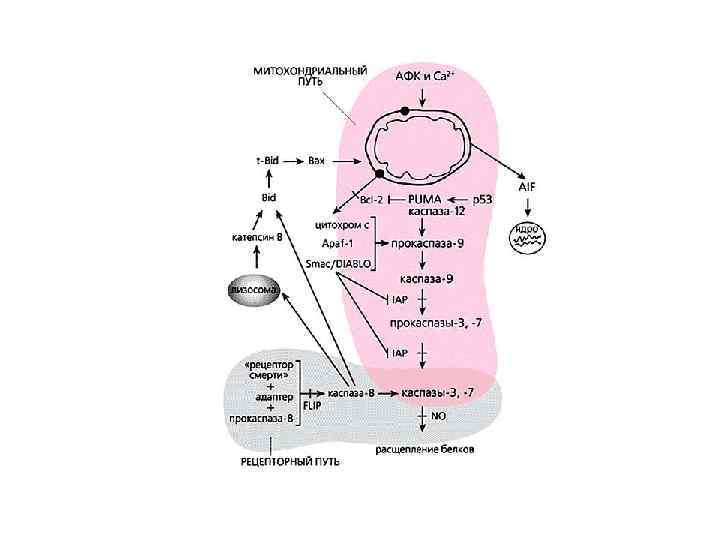
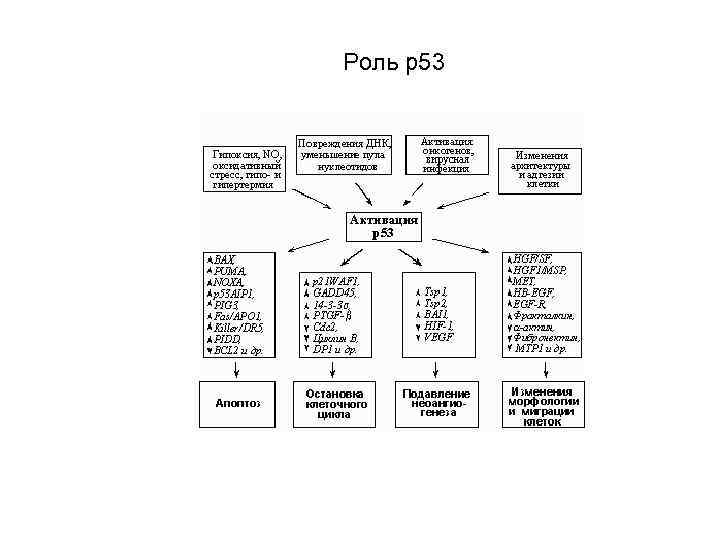 Роль р53
Роль р53
 Деградационная фаза Деградацию погибающей клетки можно условно разделить на три последовательных фазы: высвобождения, блеббинга и конденсации. Фаза высвобождения начинается с высвобождения клеточных контактов посредством внеклеточного матрикса и реорганизации фокальной адгезии. Внутри погибающей клетки деполимеризуются микротрубочки цитоскелета. Внутриклеточные актиновые микрофиламенты реорганизуются в связанные с мембраной периферийные кольцевые пучки. В итоге клетка приобретает округлую форму. Следующая стадия - блеббинга, характеризуется сокращением периферийных актиновых колец. В результате сокращений клеточная мембрана образует вздутия, клетка как бы «кипит» . Процесс блеббинга энергозависим и требует большого количества АТФ. Фаза блеббинга в нормальных условиях завершается примерно через час. В итоге клетка вступает в фазу конденсации - фрагментируется на маленькие апоптотические тела, либо целиком конденсируется, округляясь и уменьшаясь в размерах.
Деградационная фаза Деградацию погибающей клетки можно условно разделить на три последовательных фазы: высвобождения, блеббинга и конденсации. Фаза высвобождения начинается с высвобождения клеточных контактов посредством внеклеточного матрикса и реорганизации фокальной адгезии. Внутри погибающей клетки деполимеризуются микротрубочки цитоскелета. Внутриклеточные актиновые микрофиламенты реорганизуются в связанные с мембраной периферийные кольцевые пучки. В итоге клетка приобретает округлую форму. Следующая стадия - блеббинга, характеризуется сокращением периферийных актиновых колец. В результате сокращений клеточная мембрана образует вздутия, клетка как бы «кипит» . Процесс блеббинга энергозависим и требует большого количества АТФ. Фаза блеббинга в нормальных условиях завершается примерно через час. В итоге клетка вступает в фазу конденсации - фрагментируется на маленькие апоптотические тела, либо целиком конденсируется, округляясь и уменьшаясь в размерах.
 Механизмы апоптоза облученных клеток Поскольку, механизм апоптоза является универсальным для разных типов стрессирующих воздействий на клетку, особое значения при апоптозе, индуцированном облучением, является то, каким образом апоптоз в данном случае инициируется. Ключевым фактором запуска апоптоза при облучении, также как и в случае радиационно-обусловленного некроза, является образование в клетке избытка ОРТ. Однако, в отличие от некроза, уже незначительные нарушения окислительно-восстановительного гомеостаза клетки, могут послужить инициирующим фактором для реализации апоптоза. При этом к запуску апоптоза в облученной клетке, то есть к удалению поврежденной клетки из популяции, могут быть причастны другие клетки.
Механизмы апоптоза облученных клеток Поскольку, механизм апоптоза является универсальным для разных типов стрессирующих воздействий на клетку, особое значения при апоптозе, индуцированном облучением, является то, каким образом апоптоз в данном случае инициируется. Ключевым фактором запуска апоптоза при облучении, также как и в случае радиационно-обусловленного некроза, является образование в клетке избытка ОРТ. Однако, в отличие от некроза, уже незначительные нарушения окислительно-восстановительного гомеостаза клетки, могут послужить инициирующим фактором для реализации апоптоза. При этом к запуску апоптоза в облученной клетке, то есть к удалению поврежденной клетки из популяции, могут быть причастны другие клетки.
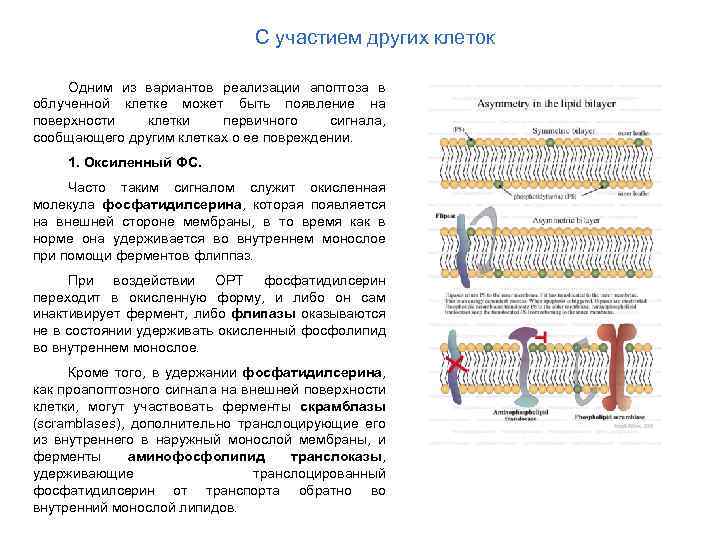 С участием других клеток Одним из вариантов реализации апоптоза в облученной клетке может быть появление на поверхности клетки первичного сигнала, сообщающего другим клетках о ее повреждении. 1. Оксиленный ФС. Часто таким сигналом служит окисленная молекула фосфатидилсерина, которая появляется на внешней стороне мембраны, в то время как в норме она удерживается во внутреннем монослое при помощи ферментов флиппаз. При воздействии ОРТ фосфатидилсерин переходит в окисленную форму, и либо он сам инактивирует фермент, либо флипазы оказываются не в состоянии удерживать окисленный фосфолипид во внутреннем монослое. Кроме того, в удержании фосфатидилсерина, как проапоптозного сигнала на внешней поверхности клетки, могут участвовать ферменты скрамблазы (scramblases), дополнительно транслоцирующие его из внутреннего в наружный монослой мембраны, и ферменты аминофосфолипид транслоказы, удерживающие транслоцированный фосфатидилсерин от транспорта обратно во внутренний монослой липидов.
С участием других клеток Одним из вариантов реализации апоптоза в облученной клетке может быть появление на поверхности клетки первичного сигнала, сообщающего другим клетках о ее повреждении. 1. Оксиленный ФС. Часто таким сигналом служит окисленная молекула фосфатидилсерина, которая появляется на внешней стороне мембраны, в то время как в норме она удерживается во внутреннем монослое при помощи ферментов флиппаз. При воздействии ОРТ фосфатидилсерин переходит в окисленную форму, и либо он сам инактивирует фермент, либо флипазы оказываются не в состоянии удерживать окисленный фосфолипид во внутреннем монослое. Кроме того, в удержании фосфатидилсерина, как проапоптозного сигнала на внешней поверхности клетки, могут участвовать ферменты скрамблазы (scramblases), дополнительно транслоцирующие его из внутреннего в наружный монослой мембраны, и ферменты аминофосфолипид транслоказы, удерживающие транслоцированный фосфатидилсерин от транспорта обратно во внутренний монослой липидов.
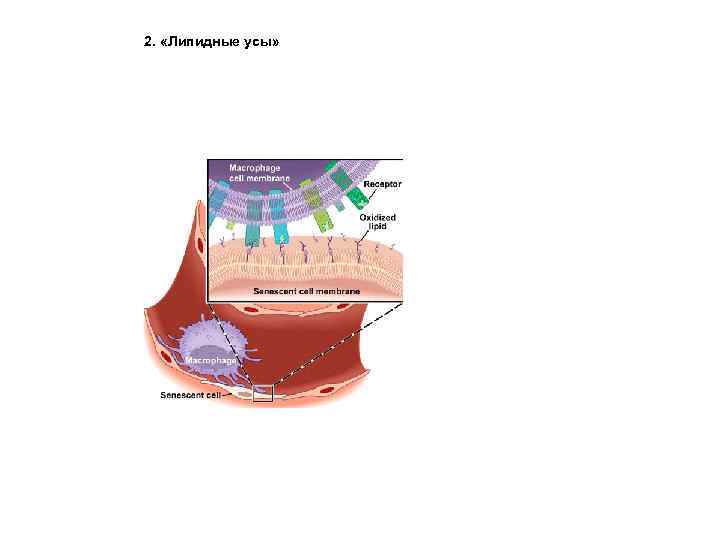 2. «Липидные усы»
2. «Липидные усы»
 Эндогенные пути 1. Митохондриальный путь с участием Са 2+ и ФЛА 2. Внутренние мембраны митохондрий содержат фосфолипазу А 2, активируемую ионами Са 2+. В норме, ионы Са 2+ находятся только в области наружной мембраны митохондрий, поэтому фосфолипаза А 2 остается неактивной. 3. При действии ионизирующего излучения происходит накопление ОРТ и в мембранах появляются поры, в результате чего ионы Са 2+ проникаются внутрь и активируют фосфолипазу А 2. 4. Продукты окисления липидов фосфолипазой А 2 – ЛРТ и лизофосфолипиды вызывают дальнейшее повреждение мембраны митохондрии. 5. В результате мембрана митохондрий перфорируется, происходит набухание матрикса внутри митохондрий, разрыв внешней митохондриальной мембраны и освобождение в цитозоль цитохрома с и т. д. .
Эндогенные пути 1. Митохондриальный путь с участием Са 2+ и ФЛА 2. Внутренние мембраны митохондрий содержат фосфолипазу А 2, активируемую ионами Са 2+. В норме, ионы Са 2+ находятся только в области наружной мембраны митохондрий, поэтому фосфолипаза А 2 остается неактивной. 3. При действии ионизирующего излучения происходит накопление ОРТ и в мембранах появляются поры, в результате чего ионы Са 2+ проникаются внутрь и активируют фосфолипазу А 2. 4. Продукты окисления липидов фосфолипазой А 2 – ЛРТ и лизофосфолипиды вызывают дальнейшее повреждение мембраны митохондрии. 5. В результате мембрана митохондрий перфорируется, происходит набухание матрикса внутри митохондрий, разрыв внешней митохондриальной мембраны и освобождение в цитозоль цитохрома с и т. д. .


