Апластическая анемия.pptx
- Количество слайдов: 31

Апластическая анемия Ассистент кафедры лабораторной диагностики ИПО БГМУ, к. м. н. Билалов Фаниль Салимович

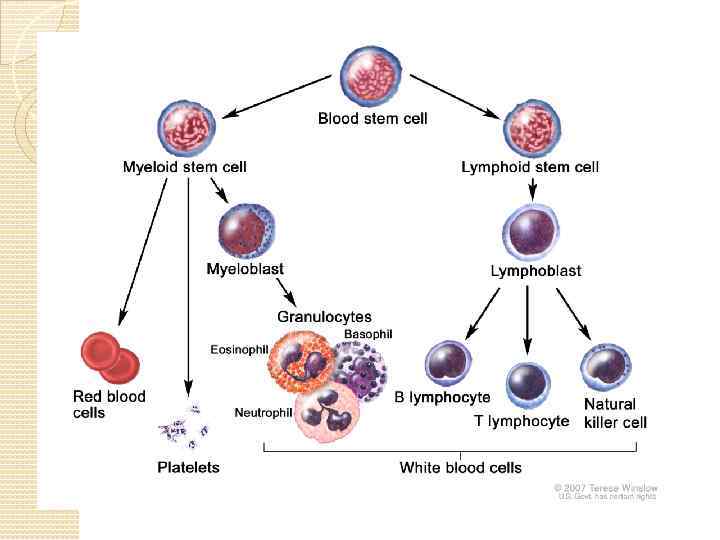
Анемия апластическая — заболевание кроветворной системы, характеризующееся депрессией кроветворения (сокращением всех трех кроветворных ростков костного мозга), развитием панцитопении.

История Впервые это заболевание было описано Паулем Эрлихом в 1888 году у 21 летней женщины. Термин «апластическая анемия» был предложен Чауфордом в 1904 году. Апластическая анемия — одно из самых тяжелых растройств гемопоэза с летальностью превышающей 80 %. Длительный период времени апластическая (гипопластическая) анемия рассматривалась как синдром, объединяющий патологические состояния костного мозга протекающие с выраженной гипоплазией кроветворения.

История В настоящее время заболевание с названием «апластическая анемия» выделяют как самостоятельную нозологическую единицу — и четко разграничивают его от синдрома гипоплазии кроветворения, являющегося проявлением ряда известных самостоятельных заболеваний костного мозга.

Классификация МКБ Aplastic anemia МКБ-10 D 60. -D 61.
Апластическая анемия (АА) Врожденная АА (анемия Фанкони) Приобретенная АА

Анемия Фанкони Анеми я Фанко ни — редкое наследственное заболевание. Встречается с частотой 1 на 350 000 новорождённых. Чаще выявляется среди евреев-ашкеназов и у народов Южной Африки.

Этиология Анемия Фанкони в большинстве случаев имеет аутосомно-рецессивный тип наследования. В редких случаях анемия Фанкони имеет Х-сцепленный рецессивный тип наследования. При этом только мать является носителем мутации, а вероятность заболевания у сыновей составляет 50 %.

В настоящее время известно 15 генов, связанных с анемией Фанкони. Только один из них — FANCB — находится на Х-хромосоме. Остальные гены расположены на аутосомах. Каждый из этих генов отвечает за синтез определённого фермента.

Анемия Фанкони возникает при наличии дефекта в кластере белков, отвечающих за репарацию ДНК. Характерна повышенная ломкость хромосом. В результате этого в среднем к 40 годам у больных развивается неопластический процесс (чаще всего острая миелоидная лейкемия) и апластическая анемия.

У 60— 75 % больных также встречаются врожденные дефекты, такие как низкорослость, ненормальная пигментация, маленькая голова, аномалии скелета (отсутствие или укорочение большого пальца рук, недоразвитие лучевой кости, врождённый вывих бедра, шейное ребро, косолапость).

Кроме этого, определяется ряд неврологических расстройств (косоглазие, недоразвитие одного или обоих глаз, опущение века, глазное дрожание, глухота, умственная отсталость), поражения половых органов (недоразвитие половых органов, отсутствие одного или обоих яичек, гипоспадия), почечные аномалии (недоразвитие почек, удвоение лоханки или мочеточника, подковообразная почка, множественные кисты в тканях почек), врождённые пороки сердца. Средняя продолжительность жизни у больных анемией Фанкони составляет около 30 лет.

Этиология приобретенной АА 1. 2. 3. 4. 5. Химические вещества (мышьяк, соли тяжёлых металлов). Ионизирующее излучение Лекарственные препараты (НПВС, цитостатики, мерказолил, анальгин). Инфекционные агенты (вирусы, м/о). Аутоимунные процессы (СКВ, Синдром Шегрена).
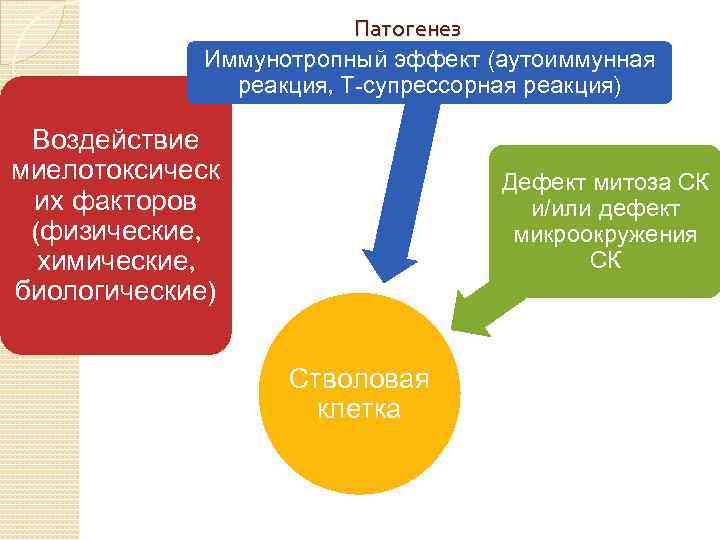
Патогенез Иммунотропный эффект (аутоиммунная реакция, Т-супрессорная реакция) Воздействие миелотоксическ их факторов (физические, химические, биологические) Дефект митоза СК и/или дефект микроокружения СК Стволовая клетка

Клиника Анемический синдром (головокружение, снижение работоспособности, утомляемость, бледность кожных покровов и слизистых, сердцебиение, непереносимость длительных физических нагрузок и т. д. ) 2. Геморагический синдром (вследствие снижения количества тромбоцитов: кровоточивость, склонность к диапедезам, геморрагии) 3. Инфекционные осложнения (последствия уменьшения количества гранулоцитов). 1.

Лабораторная диагностика 1. клинический анализ крови 2. трепанобиопсия (гистологические исследования)

Лабораторные показатели крови 1. - Анемия. 2. - Ретикулоцитопения. 3. - Лейкопения. 4. - Тромбоцитопения. Характерным для АА является выраженная лейкопения с абсолютной нейтропенией и относительным лимфоцитозом. В случае присоединения инфекции и может наблюдаться сдвиг влево до миелоцитов.

Картина периферической крови Hb - может достигать критического уровня 20 — 30 г/л. ЦП – 1, 0 или более 1, 0 , но в ряде случаев может быть гиперхромия и макроцитоз эритроцитов. Ret - резко снижено. Gran - Характерна выраженная лейкопения (агранулоцитоз). Lym - Абсолютное содержание лимфоцитов не изменено или снижено. Plt - Количество тромбоцитов всегда снижено, в некоторых случаях не удается обнаружить их вообще. СОЭ - до 40 — 60 мм/час

Отправной точкой диагностического поиска является клиническое исследование крови с подсчетом количества ретикулоцитов и тромбоцитов. Выявление би- или трицитопении при исследовании периферической крови служит основанием для выполнения морфологического исследования костного мозга.

Диагноз АА устанавливают на основании типичной гистологической картины костного мозга, получаемого методом трепанобиопсии гребня подвздошной кости.

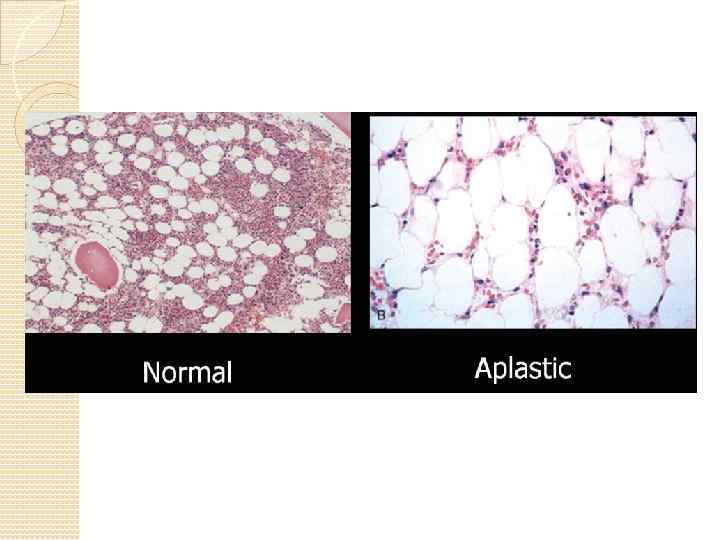
При гистологическом исследовании костного мозга обнаруживается большое количество жировой ткани, содержание которой может достигать 90 %. Среди доминирующей жировой ткани встречаются стромальные и лимфоидные элементы. Гематогенные клетки представлены крайне скудно: в небольшом количестве встречаются эритроидные и гранулоцитарные предшественники. Мегакариоциты отсутствуют.

Лечение Основным и единственным патогенетическим методом лечения апластической анемии, позволяющим рассчитывать на спасение жизни больного, является трансплантация костного мозга от совместимого донора.
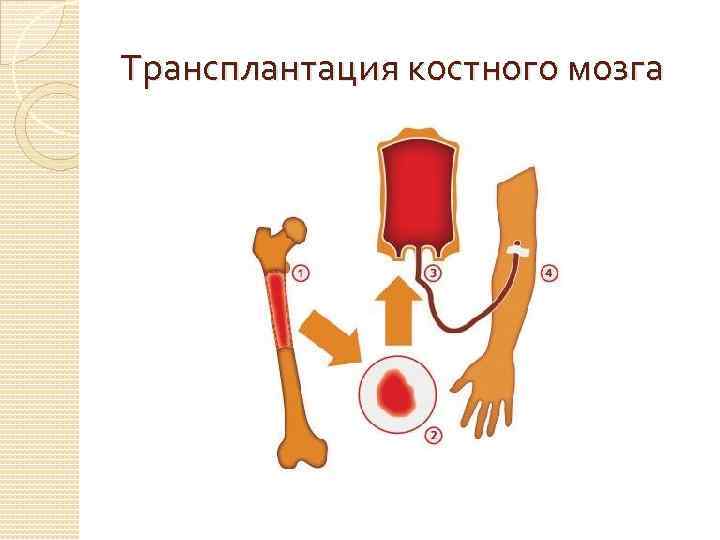
Трансплантация костного мозга

В качестве базисного препарата используется иммунодепрессант циклоспорин А. У больных нетяжелой апластической анемией использование данного препарата позволяет рассчитывать в ряде случаев на успех. Кроме того использование циклоспорина А целесообразно и с тех позиций, что глюкокортикоиды, андрогены и антилимфоцитарный глобулин способны улучшить состояние гемопоэза у больных нетяжелой апластической анемией, но, однако, при этом следует принимать во внимание повышенный риск развития в последующем клональных заболеваний костного мозга. Применение циклоспорина А сводит такой риск к минимуму.

Следует также отметить, что у части больных нетяжелой апластической анемией, преодолевших 6 -месячный порог выживаемости, может наступить спонтанное улучшение даже если им не проводилось никакой иммуносупрессивной терапии. Эффект от иммуносупрессивной терапии у больных тяжелой и крайне тяжелой апластической анемией сомнителен.

Все больные апластической анемией нуждаются в заместительной трансфузионной терапии эритроцитарной и/или тромбоцитарной массой. Объём трансфузионной терапии определяется показателями периферической крови и клиническими проявлениями заболевания. Кроме того проводится антибактериальная и микостатическая терапия с целью профилактики или лечения инфекционных осложнений.

Ремиссию удается получить примерно у половины больных. Прогноз несколько лучше у детей, чем у взрослых. Наличие большого количества жира в костном мозге не говорит о необратимости процесса. Бывают случаи, когда и у таких больных наступает полная ремиссия и полная репарация костномозгового кроветворения.

Прогноз лучше, когда увеличено содержание ретикулоцитов, когда в костном мозге имеется более полиморфная картина, когда имеется небольшое увеличение размеров селезенки и хотя бы небольшой, но четкий эффект от кортикостероидных гормонов. В этих случаях спленэктомия оказывает чаще хороший эффект вплоть до полного выздоровления. У части больных апластический синдром является началом острого лейкоза. Иногда признаки гемобластоза выявляются лишь через несколько лет от начала болезни.

Спасибо за внимание !
Апластическая анемия.pptx