f5408065f3e3b0c04072010ed45d5c70.ppt
- Количество слайдов: 35

Apixaban: Farmakologický profil M. Táborský XX. Výroční sjezd ČKS Brno, 16. 5. 2012

APIXABAN o Antikoagulans ze skupiny xabanů Phe 174 Cys 220 Cys 191 Gly 216 Arg 143 S 4 Trp 215 Gln 192 S 1 Tyr 99 X-ray Crystalová struktura

Apixaban Mechanismus účinku o perorální o přímý (působení bez nutnosti konverze na aktivní metabolit) o vysoce selektivní inhibitor aktivovaného faktoru Xa koagulační kaskády n Váže se přímo na aktivní místo faktoru Xa a spouští antikoagulační a antitrombotický efekt poklesem přeměny protrombinu na thrombin, a tím omezuje aktivitu trombinu 1, 2 n Na rozdíl od nepřímých inhibitorů Xa, apixaban nevyžaduje ke své aktivitě přítomnost antitrombinu 3 1. Eriksson BI, Quinlan DJ, Weitz Jl. Comparative pharmacodynamics and pharmacokinetics of oral direct thrombin and factor Xa inhibitors in development. Clin Pharmacokinet. 2009; 48: 1 -22. 2. Turpie AGG. Arterioscler Thromb Vasc Biol. 2007; 27: 1238 -1247. 3. Ansell J. J Thromb Haemost. 2007; 5(suppl 1): 60 -64.
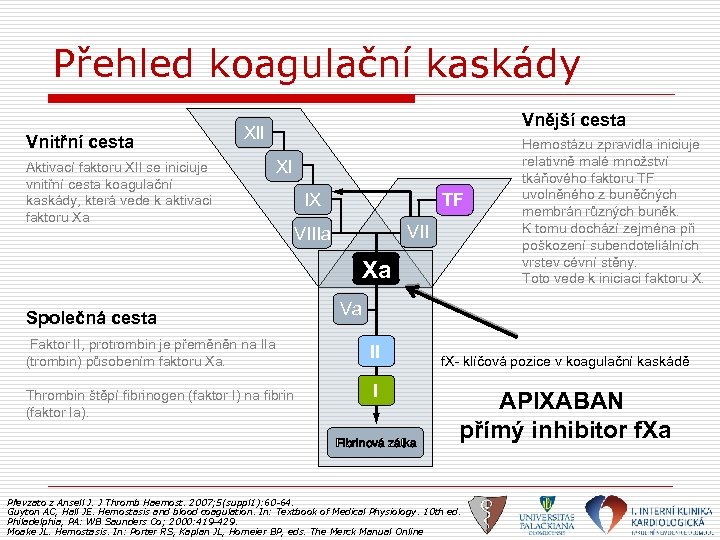
Přehled koagulační kaskády Vnitřní cesta Aktivací faktoru XII se iniciuje vnitřní cesta koagulační kaskády, která vede k aktivaci faktoru Xa Vnější cesta Xll Xl l. X TF VIIIa Xa Společná cesta Hemostázu zpravidla iniciuje relativně malé množství tkáňového faktoru TF uvolněného z buněčných membrán různých buněk. K tomu dochází zejména při poškození subendoteliálních vrstev cévní stěny. Toto vede k iniciaci faktoru X. Va Faktor II, protrombin je přeměněn na IIa (trombin) působením faktoru Xa. II Thrombin štěpí fibrinogen (faktor I) na fibrin (faktor Ia). I Fibrinová zátka f. X- klíčová pozice v koagulační kaskádě APIXABAN přímý inhibitor f. Xa Převzato z Ansell J. J Thromb Haemost. 2007; 5(suppl 1): 60 -64. Guyton AC, Hall JE. Hemostasis and blood coagulation. In: Textbook of Medical Physiology. 10 th ed. Philadelphia, PA: WB Saunders Co; 2000: 419 -429. Moake JL. Hemostasis. In: Porter RS, Kaplan JL, Homeier BP, eds. The Merck Manual Online

Indikace o Prevence žilních tromboembolických příhod u dospělých pacientů, kteří podstoupili elektivní náhradu kyčelního nebo kolenního kloubu. Eliquis SPC 2011
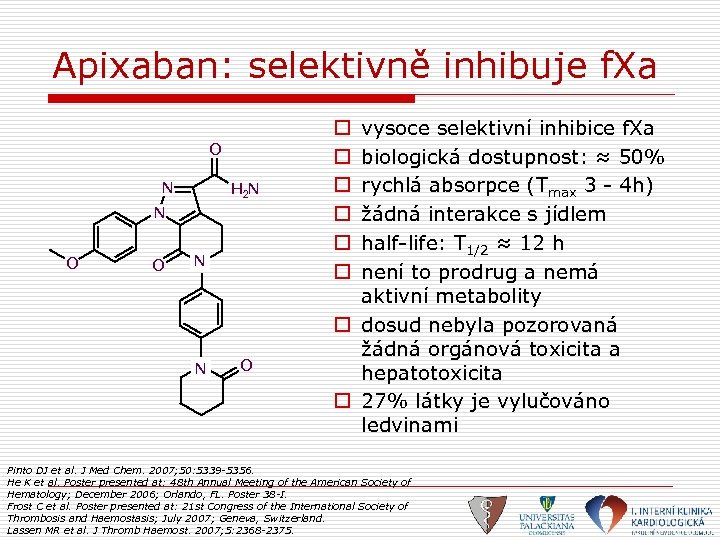
Apixaban: selektivně inhibuje f. Xa O N H 2 N N O O N N O vysoce selektivní inhibice f. Xa biologická dostupnost: ≈ 50% rychlá absorpce (Tmax 3 - 4 h) žádná interakce s jídlem half-life: T 1/2 ≈ 12 h není to prodrug a nemá aktivní metabolity o dosud nebyla pozorovaná žádná orgánová toxicita a hepatotoxicita o 27% látky je vylučováno ledvinami o o o Pinto DJ et al. J Med Chem. 2007; 50: 5339 -5356. He K et al. Poster presented at: 48 th Annual Meeting of the American Society of Hematology; December 2006; Orlando, FL. Poster 38 -I. Frost C et al. Poster presented at: 21 st Congress of the International Society of Thrombosis and Haemostasis; July 2007; Geneva, Switzerland. Lassen MR et al. J Thromb Haemost. 2007; 5: 2368 -2375.
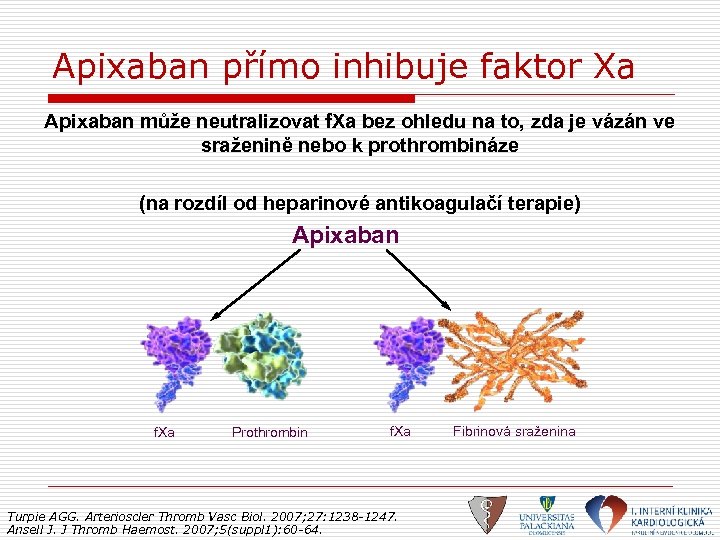
Apixaban přímo inhibuje faktor Xa Apixaban může neutralizovat f. Xa bez ohledu na to, zda je vázán ve sraženině nebo k prothrombináze (na rozdíl od heparinové antikoagulačí terapie) Apixaban f. Xa Prothrombin f. Xa Turpie AGG. Arterioscler Thromb Vasc Biol. 2007; 27: 1238 -1247. Ansell J. J Thromb Haemost. 2007; 5(suppl 1): 60 -64. Fibrinová sraženina
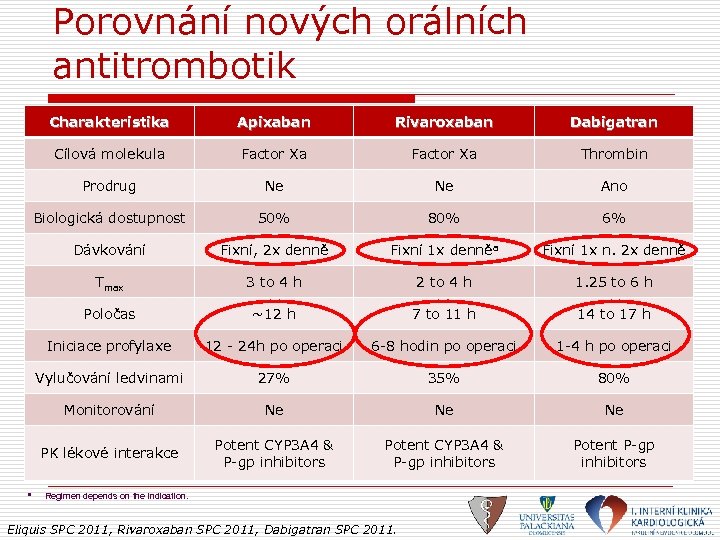
Porovnání nových orálních antitrombotik Charakteristika Rivaroxaban Dabigatran Cílová molekula Factor Xa Thrombin Prodrug Ne Ne Ano Biologická dostupnost 50% 80% 6% Dávkování Fixní, 2 x denně Fixní 1 x denněa Fixní 1 x n. 2 x denně Tmax 3 to 4 h 2 to 4 h 1. 25 to 6 h Poločas ~12 h 7 to 11 h 14 to 17 h Iniciace profylaxe 12 - 24 h po operaci 6 -8 hodin po operaci 1 -4 h po operaci Vylučování ledvinami 27% 35% 80% Monitorování Ne Ne Ne PK lékové interakce a Apixaban Potent CYP 3 A 4 & P-gp inhibitors Potent P-gp inhibitors Regimen depends on the indication. Eliquis SPC 2011, Rivaroxaban SPC 2011, Dabigatran SPC 2011.

Pouze 27% apixabanu je vylučováno ledvinami Eliminace žlučí Metabolizováno játry (cca 25%) Vylučování ledvinami Střevní exkrece Eliquis SPC 2011
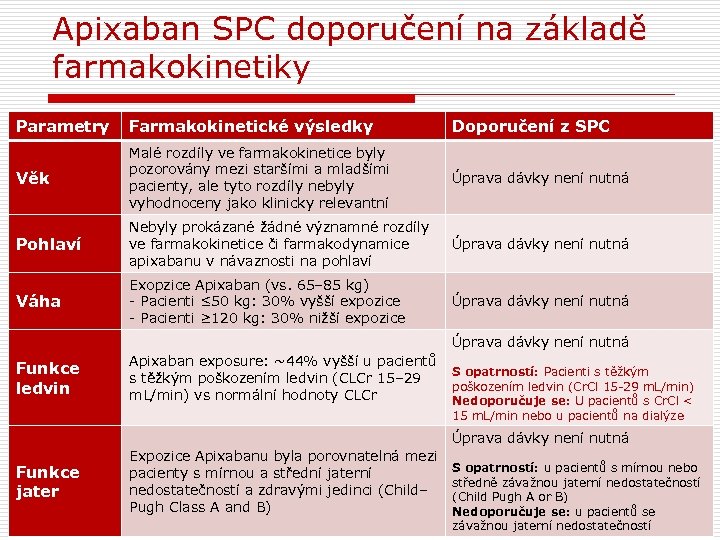
Apixaban SPC doporučení na základě farmakokinetiky Parametry Farmakokinetické výsledky Doporučení z SPC Věk Malé rozdíly ve farmakokinetice byly pozorovány mezi staršími a mladšími pacienty, ale tyto rozdíly nebyly vyhodnoceny jako klinicky relevantní Úprava dávky není nutná Pohlaví Nebyly prokázané žádné významné rozdíly ve farmakokinetice či farmakodynamice apixabanu v návaznosti na pohlaví Úprava dávky není nutná Váha Exopzice Apixaban (vs. 65– 85 kg) - Pacienti ≤ 50 kg: 30% vyšší expozice - Pacienti ≥ 120 kg: 30% nižší expozice Úprava dávky není nutná Funkce ledvin Apixaban exposure: ~44% vyšší u pacientů S opatrností: Pacienti s těžkým poškozením ledvin (CLCr 15– 29 poškozením ledvin (Cr. Cl 15 -29 m. L/min) vs normální hodnoty CLCr Nedoporučuje se: U pacientů s Cr. Cl < 15 m. L/min nebo u pacientů na dialýze Úprava dávky není nutná Funkce jater Expozice Apixabanu byla porovnatelná mezi pacienty s mírnou a střední jaterní nedostatečností a zdravými jedinci (Child– Pugh Class A and B) S opatrností: u pacientů s mírnou nebo středně závažnou jaterní nedostatečností (Child Pugh A or B) Nedoporučuje se: u pacientů se závažnou jaterní nedostatečností

Lékové interakce vybraných antikoagulancií Apixaban 1 Rivaroxaban 2 Dabigatran 3 Používat s opatrností: §se silnými induktory CYP 3 A 4 a P-gp §u starších pacientů současně užívajících aspirin §u pacientů se závažnou renální nedostatečností (Cr. Cl 15 -29 m. L/min) v monoterapii nebo současně na aspirinu §u pacientů, kteří jsou současně léčeni nesteroidními protizánětlivými léky (kyselina acetylsalicilová a jiné) Používat s opatrností: §se silnými induktory CYP 3 A 4 a P-gp §u pacientů se závažnou renální nedostatečností (Cr. Cl 15 -29 m. L/min) §u pacientů léčených přípravky ovlivňující hemostázu aspirin, protidestičková léčba Doporučuje pacienty sledovat: §NSAIDs (aspirin) §Clarithromycin §m <50 kg a >100 kg Přípravek se nedoporučuje: §U pacientů, kteří jsou současně léčeni - celkově podávanými silnými inhibitory CYP 3 A 4 and P‑gp §Jinými inhibitory agregace destiček nebo jinými antitrombotickými látkami (LMWH, hepariny, fondaparinux, klopidogrel, warfarin) a perorální antikoagulancia 1. Eliquis. TM SPC 2011. Přípravek se nedoporučuje: §U pacientů, kteří jsou současně léčeni - celkově podávanými silnými inhibitory CYP 3 A 4 and P‑gp §Jinými inhibitory agregace destiček nebo jinými antitrombotickými látkami 2. Rivaroxaban SPC 2011. Používat s opatrností: §se silnými induktory P-gp §se silnými inhibitory P-gp §u pacientů s poruchou funkce ledvin (Cr. CL 30 -50 ml/min) §pacienti starší 75 let Léková interakce s: §Amiodarone §Verapamil §Quinidine Přípravek je kontraindikován: §u pacientů se závažnou renální nedostatečností (Cr. Cl < 30 m. L/min] 3. Dabigatran SPC 2011.
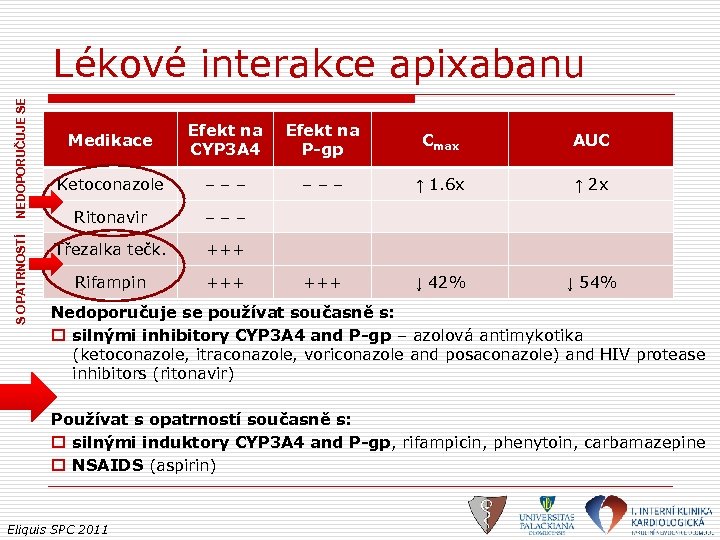
S OPATRNOSTÍ NEDOPORUČUJE SE Lékové interakce apixabanu Medikace Efekt na CYP 3 A 4 Efekt na P-gp Cmax AUC Ketoconazole – – – ↑ 1. 6 x ↑ 2 x Ritonavir – – – Třezalka tečk. +++ Rifampin +++ ↓ 42% ↓ 54% Nedoporučuje se používat současně s: o silnými inhibitory CYP 3 A 4 and P-gp – azolová antimykotika (ketoconazole, itraconazole, voriconazole and posaconazole) and HIV protease inhibitors (ritonavir) Používat s opatrností současně s: o silnými induktory CYP 3 A 4 and P-gp, rifampicin, phenytoin, carbamazepine o NSAIDS (aspirin) Eliquis SPC 2011

Dávkování: 2 x denně 2, 5 mg PROČ?
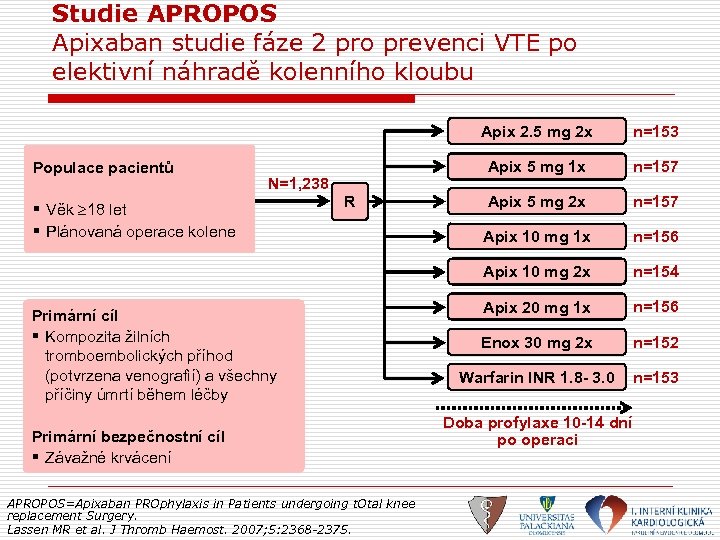
Studie APROPOS Apixaban studie fáze 2 pro prevenci VTE po elektivní náhradě kolenního kloubu Apix 2. 5 mg 2 x Apix 5 mg 1 x N=1, 238 § Věk 18 let § Plánovaná operace kolene R Primární cíl § Kompozita žilních tromboembolických příhod (potvrzena venografií) a všechny příčiny úmrtí během léčby Primární bezpečnostní cíl § Závažné krvácení APROPOS=Apixaban PROphylaxis in Patients undergoing t. Otal knee replacement Surgery. Lassen MR et al. J Thromb Haemost. 2007; 5: 2368 -2375. n=157 Apix 5 mg 2 x n=157 Apix 10 mg 1 x n=156 Apix 10 mg 2 x Populace pacientů n=153 n=154 Apix 20 mg 1 x n=156 Enox 30 mg 2 x n=152 Warfarin INR 1. 8 - 3. 0 n=153 Doba profylaxe 10 -14 dní po operaci
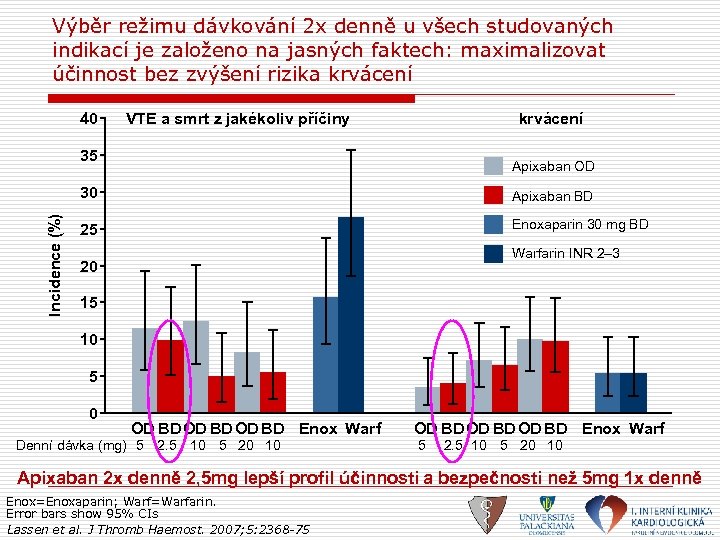
Výběr režimu dávkování 2 x denně u všech studovaných indikací je založeno na jasných faktech: maximalizovat účinnost bez zvýšení rizika krvácení 40 VTE a smrt z jakékoliv příčiny krvácení 35 Apixaban OD Incidence (%) 30 Apixaban BD 25 Enoxaparin 30 mg BD Warfarin INR 2– 3 20 15 10 5 0 OD BD Enox Warf Denní dávka (mg) 5 2. 5 10 5 20 10 OD BD Enox Warf 5 2. 5 10 5 20 10 Apixaban 2 x denně 2, 5 mg lepší profil účinnosti a bezpečnosti než 5 mg 1 x denně Enox=Enoxaparin; Warf=Warfarin. Error bars show 95% CIs Lassen et al. J Thromb Haemost. 2007; 5: 2368 -75
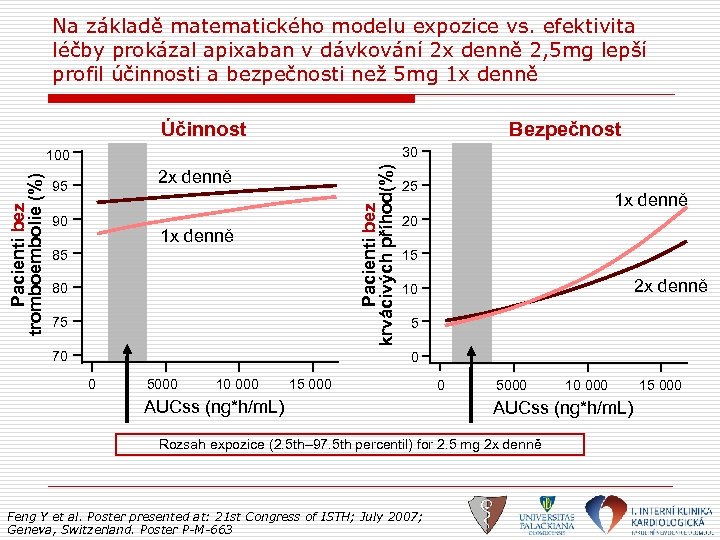
Na základě matematického modelu expozice vs. efektivita léčby prokázal apixaban v dávkování 2 x denně 2, 5 mg lepší profil účinnosti a bezpečnosti než 5 mg 1 x denně Bezpečnost Účinnost 30 Pacienti bez krvácivých příhod(%) Pacienti bez tromboembolie (%) 100 2 x denně 95 90 1 x denně 85 80 75 70 25 1 x denně 20 15 2 x denně 10 5 0 0 5000 10 000 15 000 AUCss (ng*h/m. L) 0 5000 AUCss (ng*h/m. L) Rozsah expozice (2. 5 th– 97. 5 th percentil) for 2. 5 mg 2 x denně Feng Y et al. Poster presented at: 21 st Congress of ISTH; July 2007; Geneva, Switzerland. Poster P-M-663 10 000 15 000
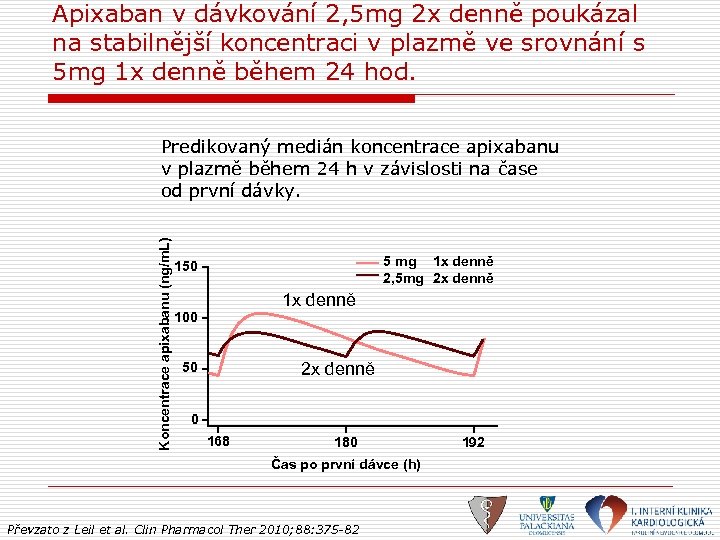
Apixaban v dávkování 2, 5 mg 2 x denně poukázal na stabilnější koncentraci v plazmě ve srovnání s 5 mg 1 x denně během 24 hod. Koncentrace apixabanu (ng/m. L) Predikovaný medián koncentrace apixabanu v plazmě během 24 h v závislosti na čase od první dávky. 5 mg 1 x denně 2, 5 mg 2 x denně 150 1 x denně 100 2 x denně 50 0 168 180 Čas po první dávce (h) Převzato z Leil et al. Clin Pharmacol Ther 2010; 88: 375 -82 192

Monitorování
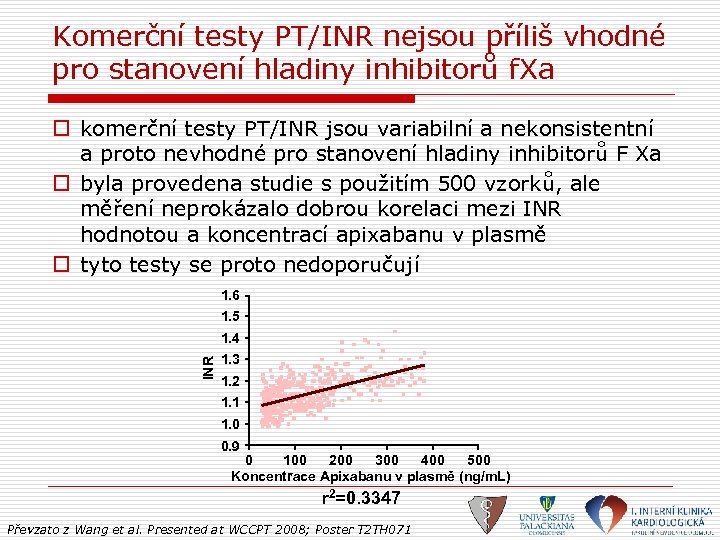
Komerční testy PT/INR nejsou příliš vhodné pro stanovení hladiny inhibitorů f. Xa o komerční testy PT/INR jsou variabilní a nekonsistentní a proto nevhodné pro stanovení hladiny inhibitorů F Xa o byla provedena studie s použitím 500 vzorků, ale měření neprokázalo dobrou korelaci mezi INR hodnotou a koncentrací apixabanu v plasmě o tyto testy se proto nedoporučují 1. 6 1. 5 INR 1. 4 1. 3 1. 2 1. 1 1. 0 0. 9 0 100 200 300 400 500 Koncentrace Apixabanu v plasmě (ng/m. L) r 2=0. 3347 Převzato z Wang et al. Presented at WCCPT 2008; Poster T 2 TH 071
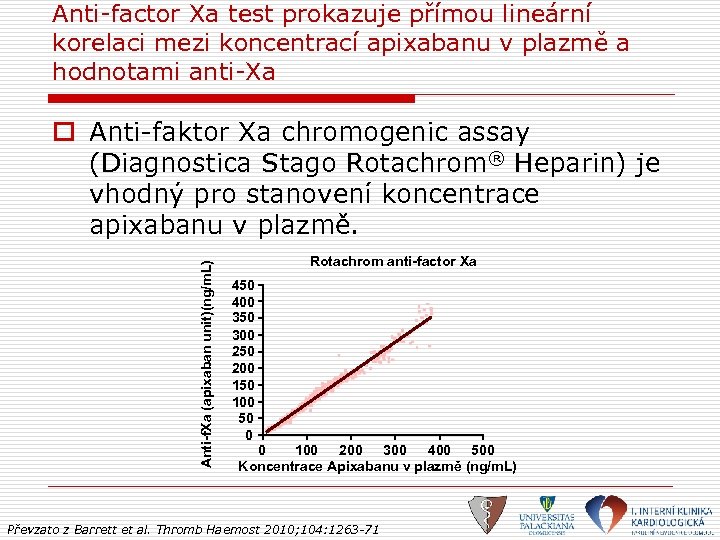
Anti-factor Xa test prokazuje přímou lineární korelaci mezi koncentrací apixabanu v plazmě a hodnotami anti-Xa Anti-f. Xa (apixaban unit)(ng/m. L) o Anti-faktor Xa chromogenic assay (Diagnostica Stago Rotachrom® Heparin) je vhodný pro stanovení koncentrace apixabanu v plazmě. Rotachrom anti-factor Xa 450 400 350 300 250 200 150 100 50 0 0 100 200 300 400 500 Koncentrace Apixabanu v plazmě (ng/m. L) Převzato z Barrett et al. Thromb Haemost 2010; 104: 1263 -71

Jak zvládnout pacienty s krvácením ?

o neexistuje žádné antidotum o předávkování apixabanem může mít za následek zvýšené riziko krvácení o je možno zvážit podání aktivního uhlí až do 3 hodin po užití apixabanu o v kontrolovaných klinických studiích, perorální podávaní apixabanu zdravým dobrovolníkům v dávkách až 10 krát vyšších než denní doporučená dávka nemělo klinicky významné nežádoucí účinky o Doporučení v případě krvácivých komplikací: n n n Přerušit léčbu Vyšetřit zdroj krvácení Chirurgická zástava krvácení Transfuze čerstvé mražené plazmy Podání rekombinantního faktoru VIIa (Novoseven)

APIXABAN a epidurální anestezie
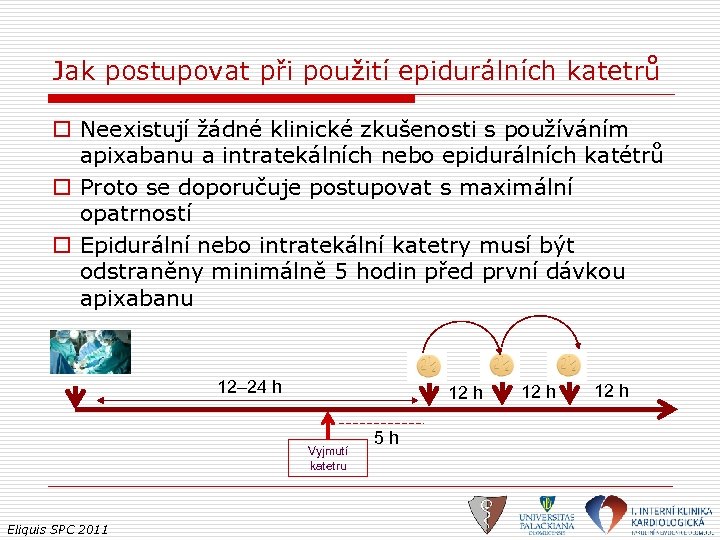
Jak postupovat při použití epidurálních katetrů o Neexistují žádné klinické zkušenosti s používáním apixabanu a intratekálních nebo epidurálních katétrů o Proto se doporučuje postupovat s maximální opatrností o Epidurální nebo intratekální katetry musí být odstraněny minimálně 5 hodin před první dávkou apixabanu 12– 24 h 12 h Vyjmutí katetru Eliquis SPC 2011 5 h 12 h

Jaká jsou doporučení u permanentních intratekální nebo epidurální katetrů u pacientů léčených apixaban? o Neexistují žádné klinické zkušenosti s používáním apixabanu současně s permanentními intratekálními nebo epidurálními katétry o Proto se doporučuje postupovat s opatrností o Doporučení jsou založena na farmakokinetice přípravku o Doporučuje se vyhradit časový prostor 20 -30 h (tj. 2 x poločas) mezi poslední dávkou apixabanu a vyjmutím katétru o Další dávka apixabanu může být podána minimálně 5 hodin po odstranění katétru 20– 30 h 12 -24 h 12 h X 12 h Vyjmutí katetru Eliquis SPC 2011 X 12 h 5 h 12 h
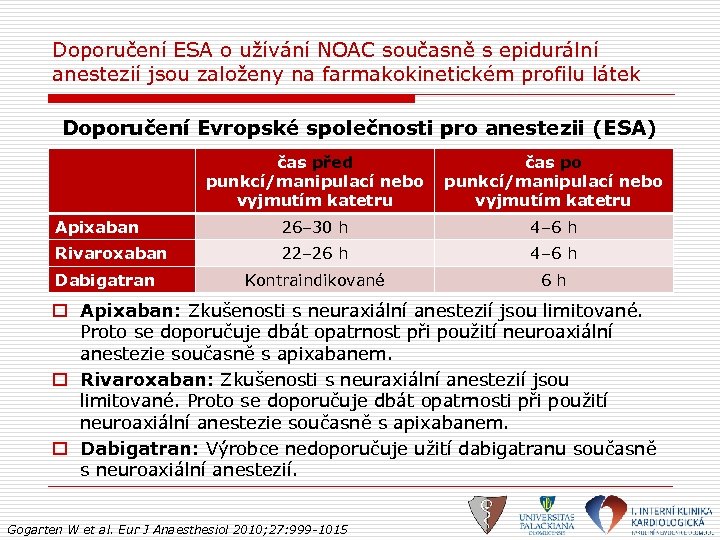
Doporučení ESA o užívání NOAC současně s epidurální anestezií jsou založeny na farmakokinetickém profilu látek Doporučení Evropské společnosti pro anestezii (ESA) čas před punkcí/manipulací nebo vyjmutím katetru čas po punkcí/manipulací nebo vyjmutím katetru Apixaban 26– 30 h 4– 6 h Rivaroxaban 22– 26 h 4– 6 h Kontraindikované 6 h Dabigatran o Apixaban: Zkušenosti s neuraxiální anestezií jsou limitované. Proto se doporučuje dbát opatrnost při použití neuroaxiální anestezie současně s apixabanem. o Rivaroxaban: Zkušenosti s neuraxiální anestezií jsou limitované. Proto se doporučuje dbát opatrnosti při použití neuroaxiální anestezie současně s apixabanem. o Dabigatran: Výrobce nedoporučuje užití dabigatranu současně s neuroaxiální anestezií. Gogarten W et al. Eur J Anaesthesiol 2010; 27: 999 -1015

ZÁVĚR o Apixaban je představitel nových antitrombotik ze skupiny xabanů o přímý a selektivní inhibitor f. Xa (f. Xa - centrální úloha v koagulační kaskádě) o vysoká biologická dostupnost o dlouhý plazmatický poločas o duální vylučování (játra, ledviny) o jednotné dávkování (úprava dávky není nutná)
BMS/Pfizer confidential. For internal use only. Not for further distribution. 28

ZKRÁCENÁ INFORMACE O PŘÍPRAVKU Název: ELIQUIS 2, 5 mg potahované tablety. Kvalitativní a kvantitativní složení: Jedna potahovaná tableta obsahuje apixabanum 2, 5 mg. Terapeutické indikace: Prevence žilních tromboembolických příhod (VTE) u dospělých pacientů, kteří podstoupili elektivní náhradu kyčelního nebo kolenního kloubu. Dávkování a způsob podání: Doporučená dávka je 2, 5 mg perorálně 2 x denně. Počáteční dávka by měla být užita 12 až 24 hodin po operaci. Doporučená délka léčby je: u hospitalizovaných pacientů po elektivní náhradě kyčelního kloubu 32 až 38 dní, u hospitalizovaných pacientů po elektivní náhradě kolenního kloubu 10 až 14 dní. Dávka se neupravuje s ohledem na věk, pohlaví a hmotnost. Kontraindikace: Hypersenzitivita na léčivou látku nebo na kteroukoli pomocnou látku, klinicky významné aktivní krvácení, jaterní onemocnění spojené s koagulopatií a klinicky relevantním rizikem krvácení. Zvláštní upozornění: Doporučuje se, aby byl přípravek používán s opatrností v podmínkách vyššího rizika krvácení, jako jsou například: vrozené nebo získané krvácivé poruchy; aktivní vředová gastrointestinální choroba; bakteriální endokarditida; trombocytopenie; poruchy destiček; anamnéza hemoragické cévní mozkové příhody; závažná nekontrolovaná hypertenze; a nedávná mozková, míšní nebo oční operace. Permanentní epidurální nebo intrathekální katetry musí být odstraněny nejpozději 5 hodin před podáním první dávky přípravku Eliquis. Podávání přípravku ELIQUIS by se mělo přerušit, jestliže se vyskytne závažné krvácení. Renální nedostatečnost: u pacientů s clearance kreatininu < 15 ml/min nebo u hemodialyzovaných pacientů se apixaban nedoporučuje. U pacientů s mírnou nebo středně závažnou renální nedostatečností není nutná úprava dávkování. Jaterní nedostatečnost: apixaban se nedoporučuje u pacientů se závažnou jaterní nedostatečností a doporučuje se používat s opatrností u pacientů s mírnou nebo středně závažnou jaterní nedostatečností. Interakce s jinými léčivými přípravky a jiné formy interakce: Užívání se nedoporučuje u pacientů, kteří současně užívají systémově silné inhibitory CYP 3 A 4 a P-gp, jakými jsou azolová antimykotika a inhibitory HIV proteázy. Při současném podávání se slabšími inhibitory CYP 3 A 4 a/nebo P-gp není nutná úprava dávky apixabanu. Při současném podávání apixabanu se silnými induktory CYP 3 A 4 a P-gp není nutná žádná úprava dávky apixabanu, avšak silné induktory CYP 3 A 4 a P-gp by se měly současně podávat s opatrností. V důsledku vyššího rizika krvácení se musí přípravek používat se zvýšenou opatrností, jestliže jsou pacienti současně léčeni kterýmikoli jinými antikoagulancii. Přípravek ELIQUIS je nutné užívat s opatrností při současné léčbě s NSAID (včetně kyseliny acetylsalicylové). Přípravky spojené se závažným krvácením nejsou doporučeny k současnému podání s přípravkem ELIQUIS. Těhotenství a kojení: Užívání apixabanu v průběhu těhotenství se nedoporučuje. Účinky na schopnost řídit a obsluhovat stroje: Apixaban nemá žádný nebo má zanedbatelný vliv na schopnost řídit nebo obsluhovat stroje. Nežádoucí účinky: Časté: anémie, krvácení, nevolnost, kontuze. Méně časté: trombocytopenie, hypotenze, gastrointestinální krvácení, hematochezie, zvýšení transamináz, vyšší AST, vyšší gammaglutamyltransferáza, abnormální jaterní testy, vyšší krevní alkalická fosfatáza, vyšší krevní bilirubin, hematurie, krvácení po zákroku. Předávkování: Neexistuje antidotum přípravku ELIQUIS. Předávkování apixabanem může způsobit vyšší riziko krvácení. Zvláštní opatření pro uchování: Nevyžaduje žádné zvláštní podmínky uchovávání. Druh obalu a velikost balení: Blistry s 10 potahovanými tabletami. Krabičky obsahují 10, 20 a 60, 100 tablet. Držitel rozhodnutí o registraci: Bristol-Myers Squibb/Pfizer EEIG, Bristol-Myers-Squibb House, Uxbridge Business Park, Sanderson Road, Uxbridge, Middlesex UB 8 1 DH, Velká Británie Registrační číslo: EU/1/11/691/001 -5. Datum první registrace: 18. 05. 2011. Datum poslední revize textu: 18. 05. 2011. Výdej léčivého přípravku je vázán na lékařský předpis. Přípravek je hrazen z veřejného zdravotního pojištění. Dříve než předepíšete tento lék, přečtěte si prosím úplné znění Souhrnu údajů o přípravku. Podrobné informace o tomto přípravku jsou dostupné na adresách zástupců držitele rozhodnutí o registraci v ČR: Bristol-Myers Squibb spol. s r. o. , Olivova 4/2096, 110 00 Praha 1, Pfizer, spol. s r. o. , Stroupežnického 17, 150 00 Praha 5. Reference: Příslušné reference naleznete na jednotlivých diapozitivech a na vyžádání na Pfizer Medical Info – medical. Info. cz@pfizer. com ELQ- 2012. 01. 026 432 CZ 12 PM 016
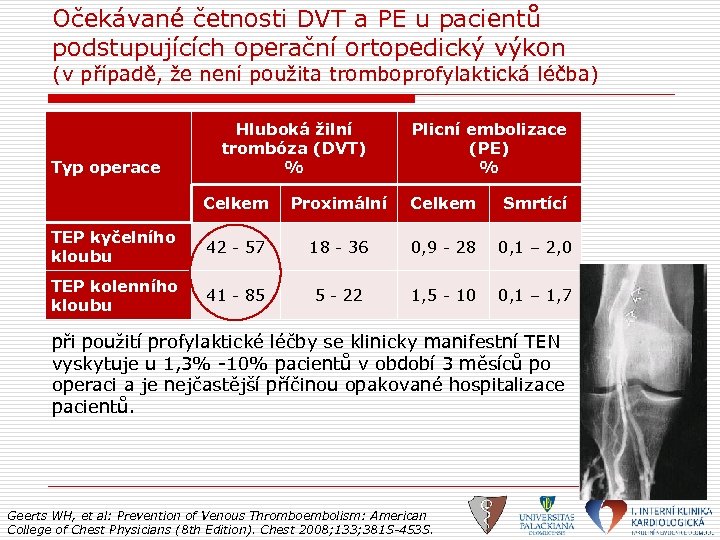
Očekávané četnosti DVT a PE u pacientů podstupujících operační ortopedický výkon (v případě, že není použita tromboprofylaktická léčba) Typ operace Hluboká žilní trombóza (DVT) % Plicní embolizace (PE) % Celkem Proximální Celkem Smrtící TEP kyčelního kloubu 42 - 57 18 - 36 0, 9 - 28 0, 1 – 2, 0 TEP kolenního kloubu 41 - 85 5 - 22 1, 5 - 10 0, 1 – 1, 7 při použití profylaktické léčby se klinicky manifestní TEN vyskytuje u 1, 3% -10% pacientů v období 3 měsíců po operaci a je nejčastější příčinou opakované hospitalizace pacientů. Geerts WH, et al: Prevention of Venous Thromboembolism: American College of Chest Physicians (8 th Edition). Chest 2008; 133; 381 S-453 S.

ORTOPEDICKÝ VÝKON o Při ortopedickém výkonu jsou přítomny prakticky všechny faktory pro hemokoagulaci Virchowova trias: 1. poškození cévní stěny (opich, ligatura, elektrokoagulace) 2. stáza krve (sádrová fixace, turniket) 3. aktivace hemokoagulačních faktorů při mechanickém poškození tkáně (traumatizace měkkých tkání, poškození kostní dřeně – vyplavení tkáňového faktoru, zvýšení koncentrace trombinu a fibrinopeptidu A, prokoagulační působení cementové hmoty) Chlumský J. a kolektiv: Antikoagulační léčba, 1. vydání. Praha. Grada Publishing, 2005
Hemostatická rovnováha prokoagulační faktory antikoagulační faktory
Hemostatická rovnováha narušena antikoagulační faktory prokoagulační faktory
Trombembolická nemoc o Přítomnost trombů v žilním řečišti, kde působí částečnou či úplnou obstrukci žilního toku. o Stav se může následně komplikovat uvolněním trombu a jeho embolizací do plic Klener P. et al. : Vnitřní lékařství. 4. přepracované a doplněné vydání. Praha, Galén, 2011

Rizikové faktory TEN o vrozené koagulační poruchy – trombofilní stavy (Leiden. mutace) o získané koagulační poruchy – VĚK pacienta! o nad 75 let postihuje TEN asi 1% populace o do 40 let 0, 01% populace o náhrady kloubů hlavně u starších nemocných Poul H. : Trombofilní stavy významné v patogenezi žilní tromboembolické nemoci Doporučení pro klinickou praxi 2006
f5408065f3e3b0c04072010ed45d5c70.ppt