Апикальное тельце и цитоскелет 3 2011.ppt
- Количество слайдов: 67

Апикальное тельце (Spitzenkorper)

Морфогенез у мицелиальных грибов и почкующихся дрожжей (Momany, 2002) Мицелиальные грибы Изотропный рост Поляризованный рост Дрожжи
• Вегетативное тело большинства грибов представлено мицелием, состоящим из сильно разветвленных гиф, растущих в определенном направлении (поляризованно) за счет роста апикального района гифы. • Рост клеток мицелия происходит за счет активных процессов синтеза клеточной стенки, протекающих в апикальной клетке мицелия за счет деятельности апикального тельца.
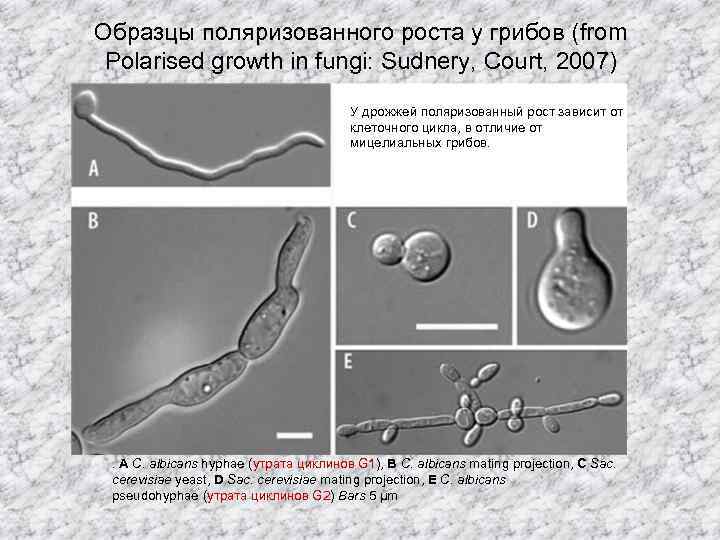
Образцы поляризованного роста у грибов (from Polarised growth in fungi: Sudnery, Court, 2007) У дрожжей поляризованный рост зависит от клеточного цикла, в отличие от мицелиальных грибов. . A C. albicans hyphae (утрата циклинов G 1), B C. albicans mating projection, C Sac. cerevisiae yeast, D Sac. cerevisiae mating projection, E C. albicans pseudohyphae (утрата циклинов G 2) Bars 5 μm
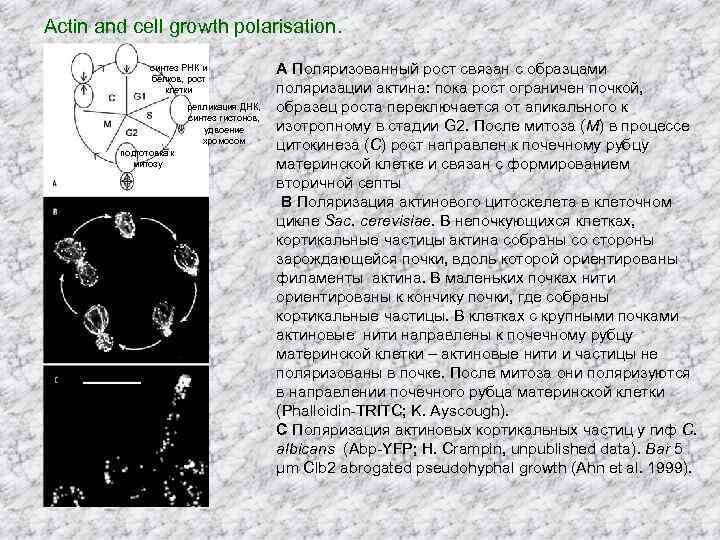
Actin and cell growth polarisation. синтез РНК и белков, рост клетки репликация ДНК, синтез гистонов, удвоение хромосом подготовка к митозу A Поляризованный рост связан с образцами поляризации актина: пока рост ограничен почкой, образец роста переключается от апикального к изотропному в стадии G 2. После митоза (M) в процессе цитокинеза (C) рост направлен к почечному рубцу материнской клетке и связан с формированием вторичной септы B Поляризация актинового цитоскелета в клеточном цикле Sac. cerevisiae. В непочкующихся клетках, кортикальные частицы актина собраны со стороны зарождающейся почки, вдоль которой ориентированы филаменты актина. В маленьких почках нити ориентированы к кончику почки, где собраны кортикальные частицы. В клетках с крупными почками актиновые нити направлены к почечному рубцу материнской клетки – актиновые нити и частицы не поляризованы в почке. После митоза они поляризуются в направлении почечного рубца материнской клетки (Phalloidin-TRITC; K. Ayscough). C Поляризация актиновых кортикальных частиц у гиф C. albicans (Abp-YFP; H. Crampin, unpublished data). Bar 5 μm Clb 2 abrogated pseudohyphal growth (Ahn et al. 1999).

Механизмы поляризованного роста у дрожжей и мицелиальных грибов имеют определенное сходство, но есть и различия. • У дрожжей поляризованный рост обеспечивается участием кортикальных маркеров, белковых структур (полярисома, экзоциста и др. ), везикул и элементов цитоскелета, которые обеспечивают невысокий градиент синтеза клеточной стенки. Скорость роста гифы Neurospora crassa – 16 мкм в минуту, дрожжей Saccharomyces cerevisiae – 0, 16 мкм в минуту У мицелиальных грибов поляризованный рост происходит также при участии всех компонентов, перечисленных выше и апикального тельца (подробно см. ниже).
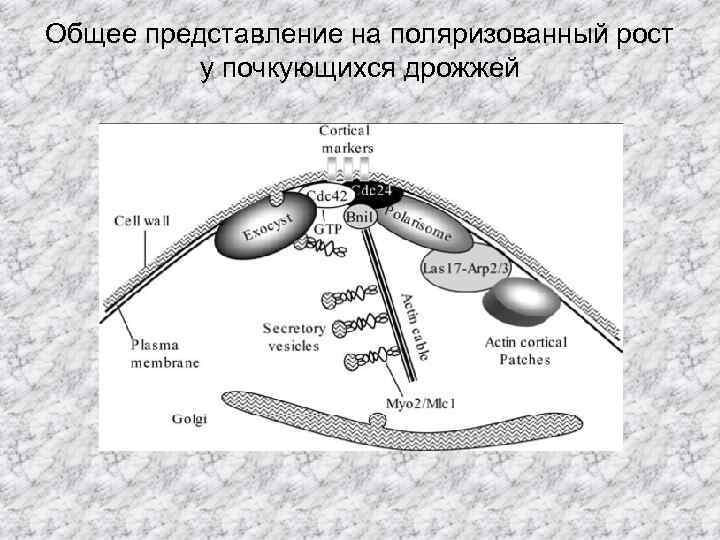
Общее представление на поляризованный рост у почкующихся дрожжей
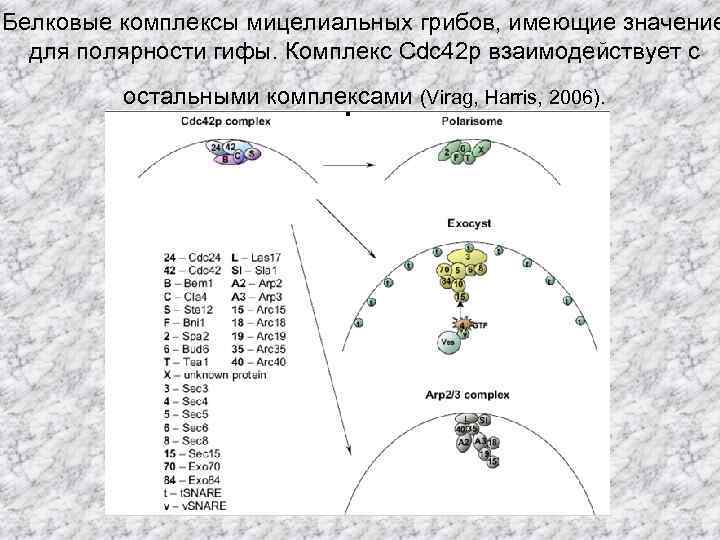
Белковые комплексы мицелиальных грибов, имеющие значение для полярности гифы. Комплекс Cdc 42 p взаимодействует с остальными комплексами (Virag, Harris, 2006).

Полярисома • Полярисома дрожжей состоит из белков Bni 1, Spa 2, Bud 6 и Pea 1, локализованных в виде полумесяца у места зарождающейся почки, и направляет микрофиламенты и другие клеточные компоненты к сайтам поляризованного роста • Полярисома мицелиальных грибов состоит из Bni 1, Spa 2 и Bud 6

Экзоциста • Экзоциста - второй белковый комплекс, который вовлечен в стыковку везикул и с плазматической мембраной • Экзоциста мицелиальных грибов содержит восемь белков: Sec 3, Sec 5, Sec 6, Sec 8, Sec 10, Sec 15, Exo 70, и Exo 84, и взаимодействует с Rho-GTPазой Cdc 42, Rho 1, Rho 3, а также с Sec 4, Rab GTPаза присутствующей на поверхности мембраны везикул
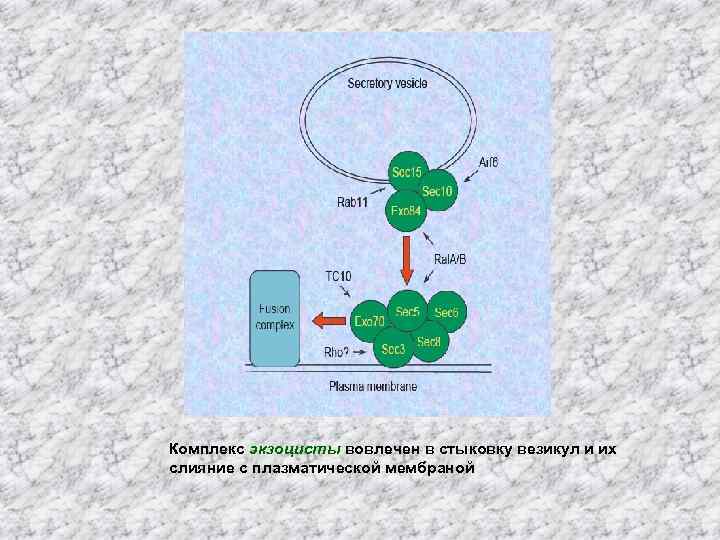
Комплекс экзоцисты вовлечен в стыковку везикул и их слияние с плазматической мембраной

Комплекс Arp 2/3 • Комплекс Arp 2/3 – другая серия белков мицелиальных грибов важных для поддержания полярности и включает Arp 2, Arp 3, Arc 40, Arc 35, Arc 18, Arc 19, и Arc 15. Комплекс Arp 2/3 отвечает за инициацию ветвления актиновых филаментов, образующих кортикальную актиновую сеть, и эндоцитоз. Он локализован около актиновых пятен, примыкающих к плазматической мембране в апикальном районе растягивающегося кончика гифы.

Впервые апикальное тельце было описано у фиксированных и окрашенных клеток двух видов рода Coprinus Brunswik (1924) c помощью световой микроскопии. Пионерской работой положившей начало в исследовании биологии Spitzenkörper (апикальное тельце) считается работа Girbardt (1957), проделанная c использованием фазово-контрастной микроскопии. Girbardt приводит первое описание Spitzenkörper для живой растущей гифы высших грибов, как темная в фазово изображении структура, локализованная в грибе Polystictus versicolor. Его тщательное исследование растущей гифы показало, - оно присутствует только в кончике растущей вегетативной гифы, - образуется на месте прорастания споры и боковых ответвлений, - локализовано в том месте гифы, которое коррелирует с направлением роста гифы. Таким образом, функции апикального тельца – обеспечение апикального роста гифы и направленного синтеза клеточной стенки. Далее были проведены детальные исследования ультраструктуры апикального тельца у разных групп грибов в 6 -70 -ые годы (Grove, Braсker), которые показали, что это мультикомпонентный комплекс, в котором доминируют везикулы.

Исследование структуры апикального тельца на уровне электронного микроскопа


Pythium aphanidermatum (Oomycetes)
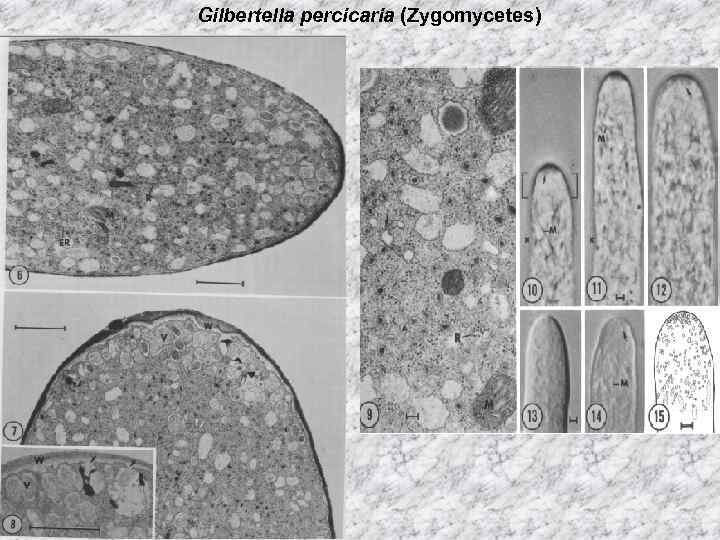
Gilbertella percicaria (Zygomycetes)
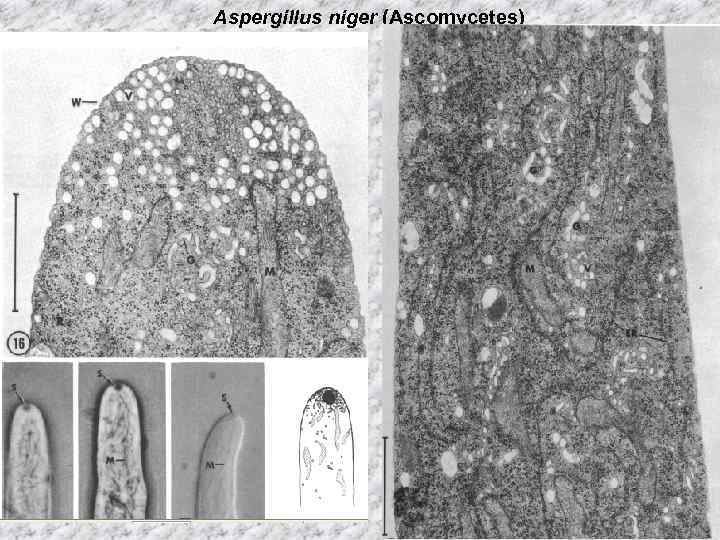
Aspergillus niger (Ascomycetes)
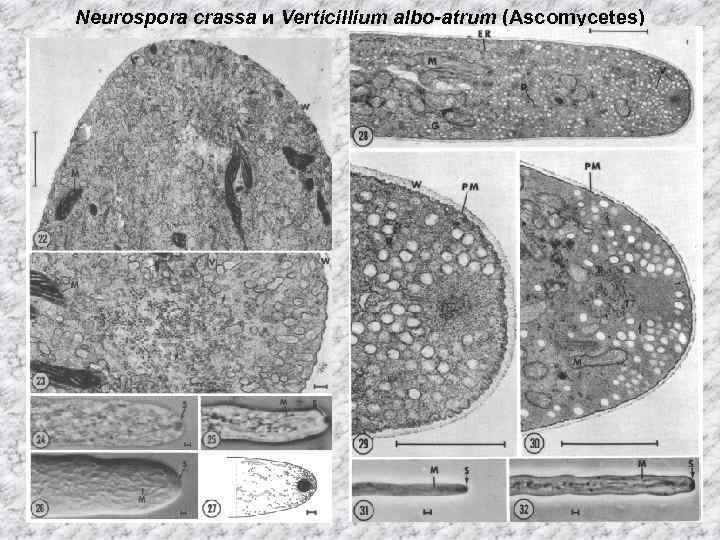
Neurospora crassa и Verticillium albo-atrum (Ascomycetes)
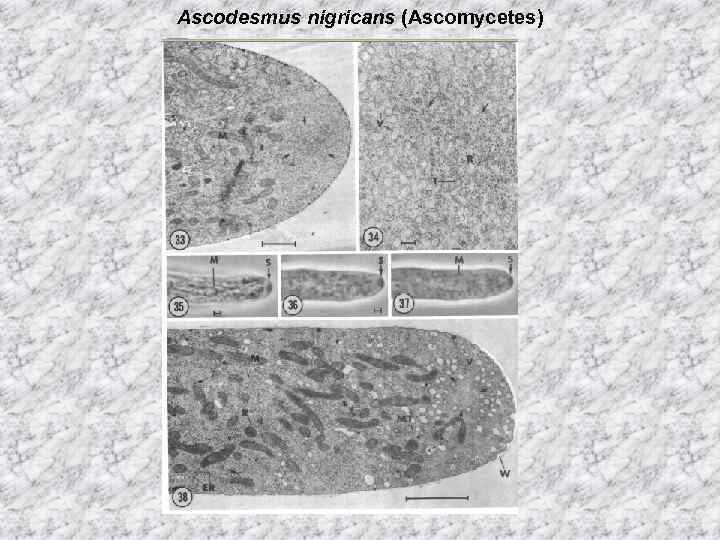
Ascodesmus nigricans (Ascomycetes)
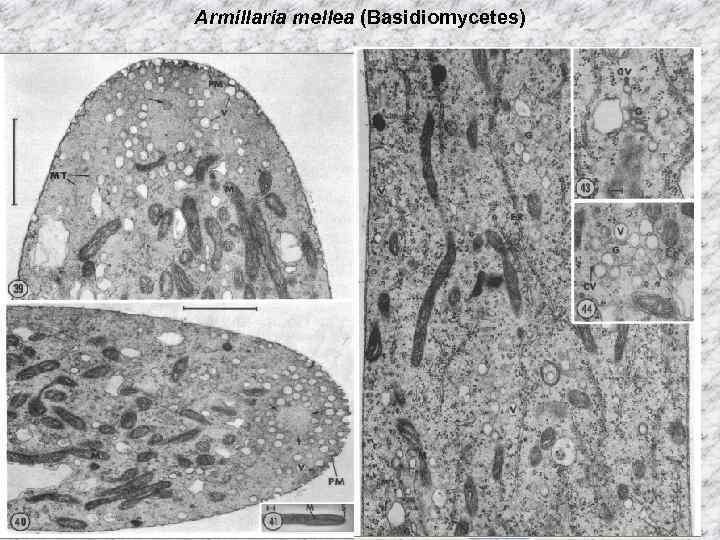
Armillaria mellea (Basidiomycetes)
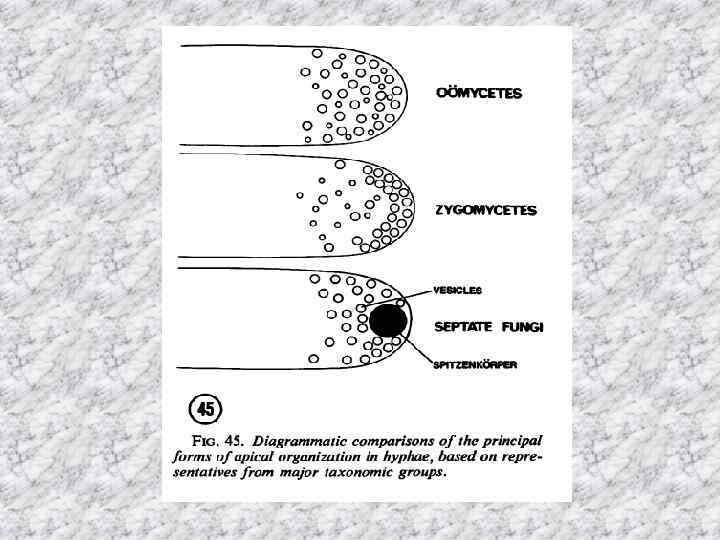

Исследования апикального центра на уровне светового и электронного микроскопа показало, что апикальное тельце присутствует у септированных грибов и его атрибутами являются (Grove, Bracker, 1970): • Один сферический комплекс. • Он выглядит темным в фазово-контрастном изображении. • У него отсутствует дискретная граница. • Локализовано в апикальном своде апикально растущей гифы. • Требуется для роста гифы. • Состоит из апикальных везикул, микровезикул, микрофиламентов и иногда рибосом. • Имеет полярность и билатеральную симметрию по форме и организации. • Является, по-видимому, источником везикул в процессе экзоцитоза и роста гифы.

Trichoderma viride Эта структура присутствует у активно растущих кончиков и исчезает во время остановки роста. Изменение положения апикального тельца влияет на направление роста гифы


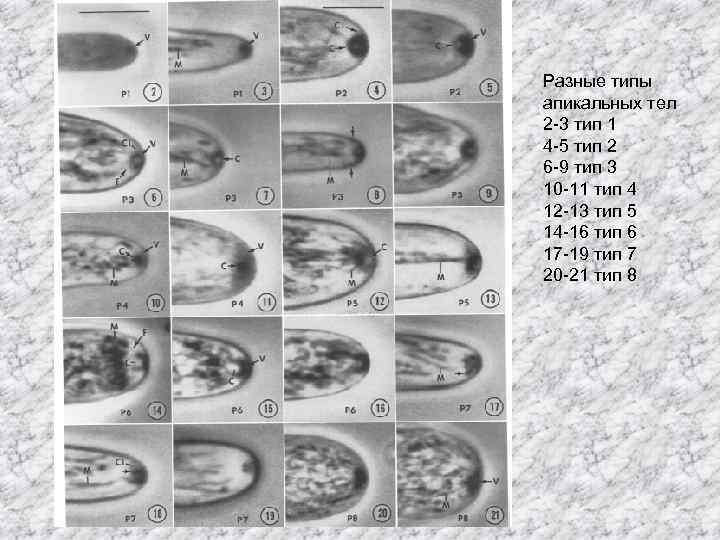
Разные типы апикальных тел 2 -3 тип 1 4 -5 тип 2 6 -9 тип 3 10 -11 тип 4 12 -13 тип 5 14 -16 тип 6 17 -19 тип 7 20 -21 тип 8
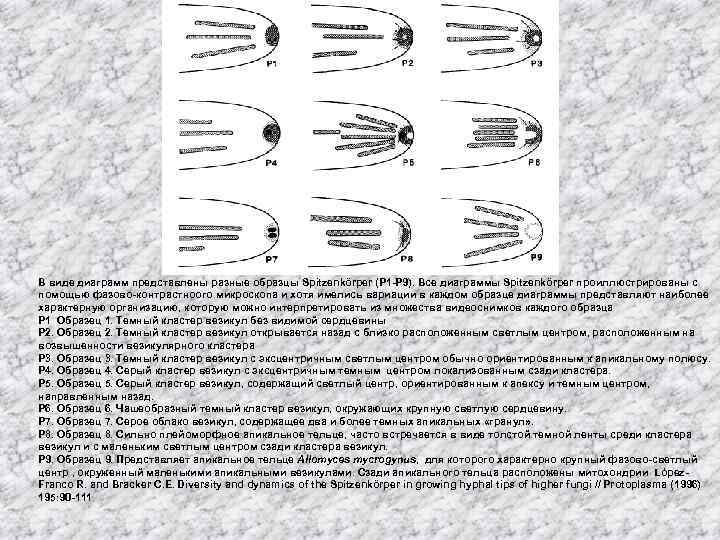
В виде диаграмм представлены разные образцы Spitzenkörper (Р 1 -Р 9). Все диаграммы Spitzenkörper проиллюстрированы с помощью фазово-контрастноого микроскопа и хотя имелись вариации в каждом образце диаграммы представляют наиболее характерную организацию, которую можно интерпретировать из множества видеоснимков каждого образца Р 1 Образец 1. Темный кластер везикул без видимой сердцевины Р 2. Образец 2. Темный кластер везикул открывается назад с близко расположенным светлым центром, расположенным на возвышенности везикулярного кластера Р 3. Образец 3. Темный кластер везикул с эксцентричным светлым центром обычно ориентированным к апикальному полюсу. Р 4. Образец 4. Серый кластер везикул с эксцентричным темным центром локализованным сзади кластера. Р 5. Образец 5. Серый кластер везикул, содержащий светлый центр, ориентированным к апексу и темным центром, направленным назад. Р 6. Образец 6. Чашеобразный темный кластер везикул, окружающих крупную светлую сердцевину. Р 7. Образец 7. Серое облако везикул, содержащее два и более темных апикальных «гранул» . Р 8. Образец 8. Сильно плейоморфное апикальное тельце, часто встречается в виде толстой темной ленты среди кластера везикул и с маленьким светлым центром сзади кластера везикул. Р 9. Образец 9. Представляет апикальное тельце Allomyces mycrogynus, для которого характерно крупный фазово-светлый центр , окруженный маленькими апикальными везикулами. Сзади апикального тельца расположены митохондрии López. Franco R. and Bracker C. E. Diversity and dynamics of the Spitzenkörper in growing hyphal tips of higher fungi // Protoplasma (1996) 195: 90 -111

• Клеточные компоненты, связанные с апикальным тельцем: митохондрии и микрофиламенты. • Показаны изменения размера, формы и положения апикального тельца. • Морфология апикального тельца родоспецифична. • Несептированные грибы из рода Allomyces имеют тип 9 апикального центра, состоящего из кольца мелких везикул. • Действие стрессовых факторов (световой, температурный, электрический) приводит к миграции апикального центра в субапикальную зону или к его исчезновению. В обеих случаях изменяется форма гифы и прекращается рост.

Спутник Spitzenkörper • Спутник Spitzenkörper представляет собой маленькую группы везикул, которые появляются на расстоянии нескольких микрометров позади апикального полюса, быстро мигрируют к апексу гифы и поглощаются основным Spitzenkörper, таким образом, внося вклад в рост гифы. Этот способ поглощения Spitzenkörper спутника было предложено считать принадлежностью пульсирующего роста кончика гифы

Гипотетическая модель организации путей перемещения везикул в растущей гифе построенная на распределении флуоресцентного красителя FM 64. Внутриклеточный транспорт показан голубыми стрелками, экзоцитоз – зелеными, эндоцитоз – красными стрелками (мод. Fischer-Parton et al. , 2000).

. Модель устойчивого состояния роста гифы (Wessels, 1993) Согласно этой модели: Литические ферменты не вовлечены в апикальный рост; Вновь образующаяся стенка на самом кончике гифы – ВЯЗКОЭЛАСТИЧНАЯ; Новые компоненты стенки встраиваются на апексе; Отступя от апекса клеточная стенка затвердевает за счет формирования химических связей.
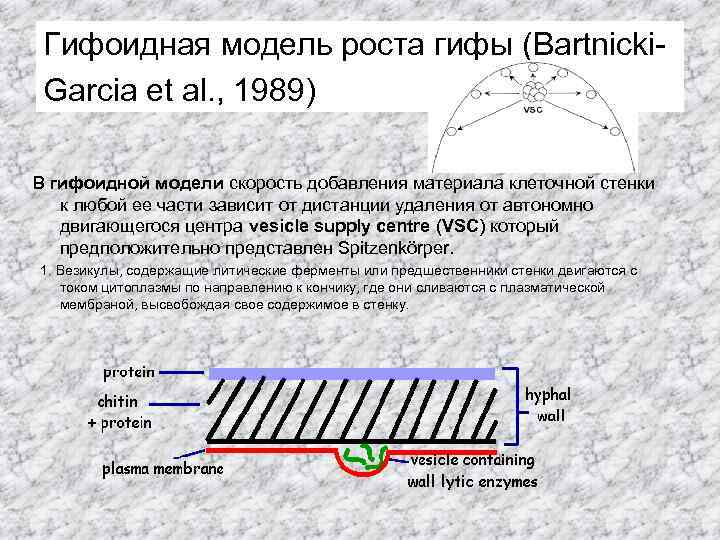
Гифоидная модель роста гифы (Bartnicki. Garcia et al. , 1989) В гифоидной модели скорость добавления материала клеточной стенки к любой ее части зависит от дистанции удаления от автономно двигающегося центра vesicle supply centre (VSC) который предположительно представлен Spitzenkörper. 1. Везикулы, содержащие литические ферменты или предшественники стенки двигаются с током цитоплазмы по направлению к кончику, где они сливаются с плазматической мембраной, высвобождая свое содержимое в стенку.
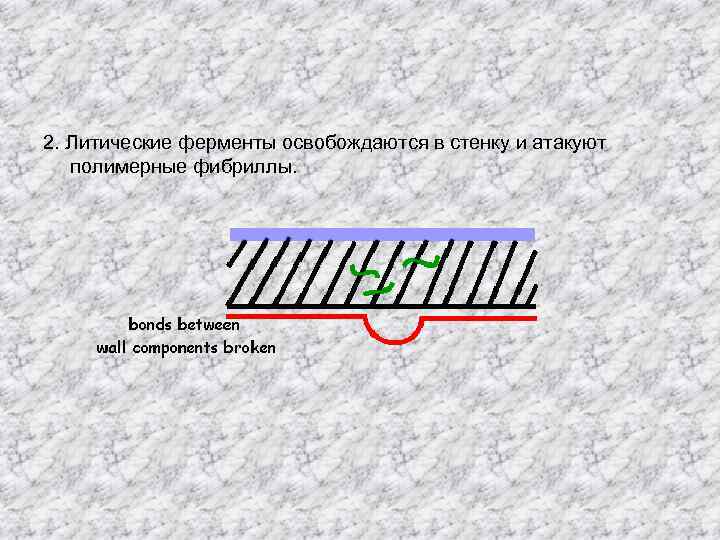
2. Литические ферменты освобождаются в стенку и атакуют полимерные фибриллы.
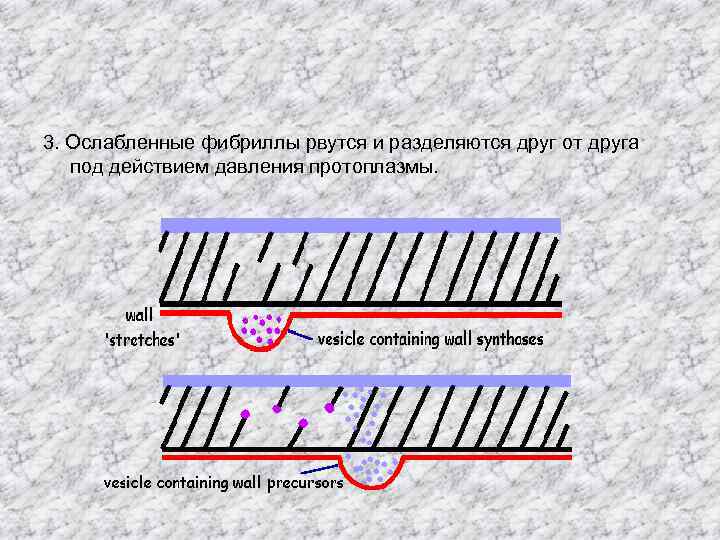
3. Ослабленные фибриллы рвутся и разделяются друг от друга под действием давления протоплазмы.

4. Синтазные ферменты стенки строят новые фибриллы и дополнятся аморфными компонентами стенки. В результате поверхность стенки гифы увеличивается. Слияние везикул с плазматической мембраной вносит вклад в увеличение площади поверхности.
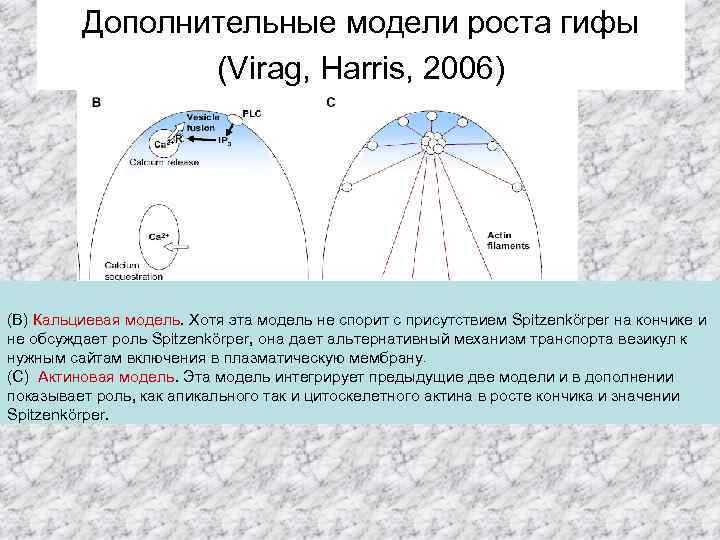
Дополнительные модели роста гифы (Virag, Harris, 2006) (В) Кальциевая модель. Хотя эта модель не спорит с присутствием Spitzenkörper на кончике и не обсуждает роль Spitzenkörper, она дает альтернативный механизм транспорта везикул к нужным сайтам включения в плазматическую мембрану. (С) Актиновая модель. Эта модель интегрирует предыдущие две модели и в дополнении показывает роль, как апикального так и цитоскелетного актина в росте кончика и значении Spitzenkörper.
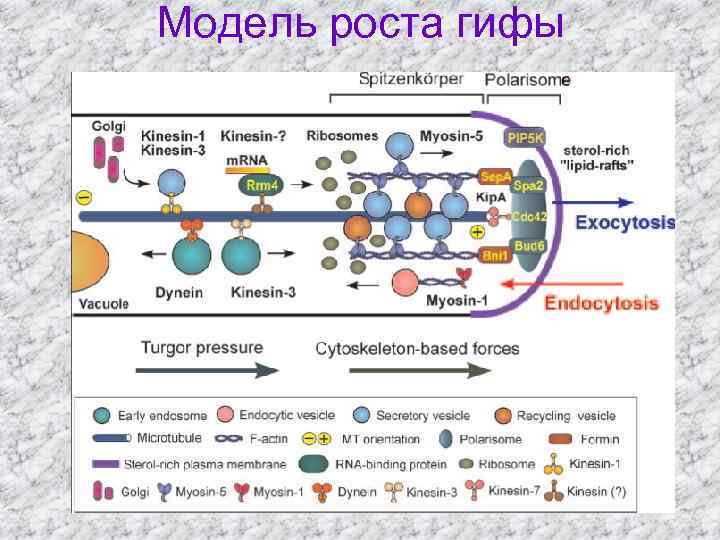
Модель роста гифы

• 38 000 везикул сливаются с апикальной мембраной каждую минуту для поддержания роста у Neurospora crassa когда гифа растет с максимальной скоростью !

Онтогенез апикального тельца • По-видимому, формирование de novo • Наблюдения дихотомического ветвления у Aspergillus niger мутанта ‘ramosa’ показали, что Spitzenkörper исчезает перед формированием новых дихотомических веточек. Два новых Spitzenkörper образуются после того, как становятся заметными инициали двух новых веточек, по одному у вершины новой веточки (Reynaga-Peña, Bartnicki-García, 1997)

Цитоскелет грибной клетки

• Функции цитоскелета - обеспечение внутриклеточного транспорта везикул и органелл, сегрегации хромосом в процессе ядерного деления, а также секреции и поляризованном росте у клеток грибов.

Состав цитоскелета Имеется три главных компонента составляющих цитоскелет эукариот: филаменты актина или микрофиламенты, промежуточные филаменты и микротрубочки: • филаменты актина или микрофиламенты твердые палочки около 7 nm в диаметре, состоящие из двух цепей глобулярного белка названного актином (один из самых распростарненных белков в природе). Эти филаменты сократимы и вносят вклад в изменение формы, связи клетка-с -клетой или клетка-со-стенкой, сигнальную трансдукию, цитокинез и течение цитоплазмы. • Промежуточные филаменты это очень обширный класс фиброзных белков формирующих структурные фибриллы в диапазоне от 8 до 12 nm в диаметре. Они также принимают участие в межклеточных связях и контактах с окружающей средой, но в большинстве своем функционируют как элементы-выдерживающие напряжение для поддержания формы и жесткости клетки животных, и структуры мембранных структур подобных ядерной оболочки. Первый ген промежуточных фибрилл у грибов был охарактеризован у мицелиальног гриба A. nidulans mbm. B продукт гена, колокализован с митохондриями, и делеция mdm. B влияет на морфологию и распределение митохондрий; • микротрубочки это прямые, полые цилиндры около 25 nm в диаметре, обычно состоящие из 13 профиламентов, которые являются полимером α- и β-тубулина. Они имеют очень динамичное поведение и выполняют азные функции от транспорта до структурной поддержки.

Актин у дрожжей Важность актина у почкующихся дрожжей очевидна из фенотипических изменений в результате мутации гена, который кодирует актин, они включают: • крупные морфологические дефекты, • аномальное отложение хитина, • дефектный выбор сайта почкования, • аномальная сегрегация ядер, • аномальный цитокинез, • аномальное распределение внутриклеточных органелл, • аномальная секреция и захват/uptake, • изменена чувствительность к окружающим факторам (температуре, концентрации осмотика и ионов).

Функции микрофиламентов • Микрофиламенты актина требуются у грибов для движения органелл, • Поляризованного роста • Септирования (цитокинеза). • Он необходим для секреции везикул и растяжении клеточной стенки. • И, возможно, вместе с микротрубочками цитоскелета - для локализации маркерных белков на кончике клетки, которые контролируют непосредственно направление роста.

Структура актина • Белок актин имеет молекулярный вес порядка 42 k. Da (375 аминокислот), который существует как мономер (глобулярный или G-actin) или как линейный полимер, состоящий из мономера известен как филаменты или F-актин. Эти филаменты, которые так важны в морфогенезе, движении органелл и цитокинезе; микрофиламенты чрезвычайно динамичные структуры, которые могут быть быстро модифицированы при взаимодействии с набором актин связанных белков actin binding proteins (ABPs) (Sutherland & Witke, 1999; Walker & Garrill, 2006).
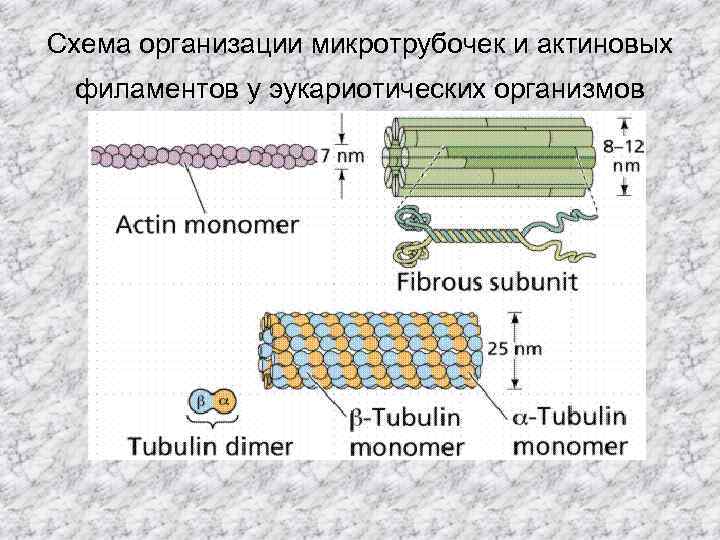
Схема организации микротрубочек и актиновых филаментов у эукариотических организмов

Образование микрофиламентов • Формины - факторы зарождения актина у эукариотических клеток. У дрожжей было обнаружено, что формины требуются для сборки и поддержания неветвящихся актиновых нитей независимо от комплекса Arp 2/3 (рис. 12). Комплекс Arp 2/3 принимает участие в инициации образования ветвящейся сети актина. • Интересно, что у Saccharomyces cerevisiae присутствует два разных формина, у Schizosaccharomyces pombe кодируется три формина, а A. nidulans и N. crassa кодирует один формин. Формин A. nidulans, SEPA, локализован в обеих сайтах: септирования и кончике гифы, что указывает на использование мицелиальными грибами сайт-специфических регуляторных механизмов для контроля опосредованной формином полимеризации актина.

Актин мицелиальных грибов • Актиновый цитоскелет мицелиальных грибов требуется для создания и поддержания полярности кончика гифы и для формирования сократительного кольца в месте септирования. Родственые актину белки известные как формины, идентифицированы как независимые затравки полимеризации актина. Мицелиальные грибы содержат единственный формин, который локализован как в кончике гифы, так и в местах септирования (Xiang & Plamann, 2003).

Микротрубочки • Микротрубочки состоят из димера α- and βтубулина который собран в цилиндрическую трубки с диаметром около 25 nm но сильно варьируют по длине. • Динамика полимеризации микротрубочек является центральной для биологических функций. • Даже in vitro, очищенные тубулиновые димеры беспрерывно самособираются и разбираются; полимеризация микротрубочек и удлинение происходит до случайного переключения на деполимеризацию.
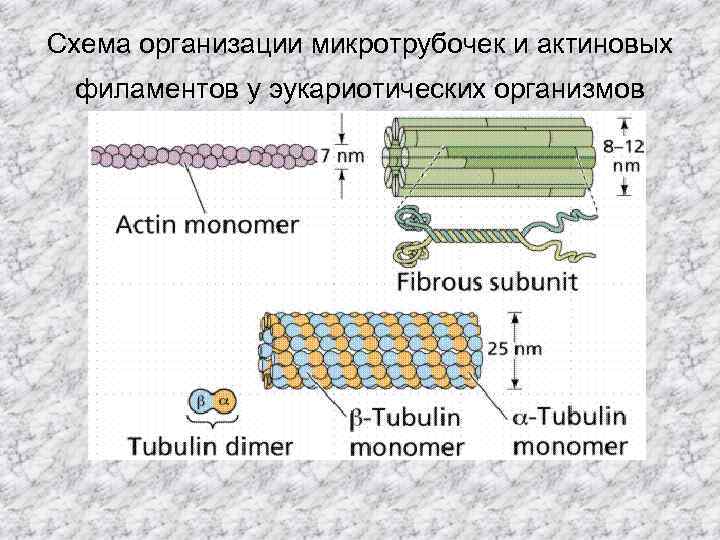
Схема организации микротрубочек и актиновых филаментов у эукариотических организмов

Функции микротрубочек • Микротрубочки и ассоциированные с ними белки вовлечены в широкий круг внутриклеточных функций, как и актиновые микрофиламенты (действительно, они работают вместе в большинстве случаев), частично транспорт и положение органелл, везикул и ядер. • Имеется видоспецифическая вариация в механизмах транспорта органелл, таких как митохондрии, они транспортируются по актиновым путям у почкующихся дрожжей и некоторых мицелиальных грибов, но у N. crassa, их движение зависит от микротрубочек.

• Деполимеризация приводит к быстрому укорочению микротрубочек, приводящее либо к полному исчезновению, либо к обратному переключению на удлинение (которое называют термином. • Эта динамичная нестабильность является особым свойством микротрубочек, так как это дает возможность им выполнять механическую работу. • Удлинение микротрубочек поляризовано, быстро растущий plus конец, и медленно или не-растущий minus конец (в клетках, минус конец обычно якорная точка).

Происхождение микротрубочек • MTs не могут эффективно собираться de novo в эукариотической клетке, но требуют точки инициации. Эту функцию у эукариот и грибов в том числе выполняет центр организации микротрубочек (MTOCs), который является протеиновым комплексом, характерным компонентом которого является γ-тубулин Известно, что γ-тубулин высших эукариот формирует 2. 2 -MDa комплексное кольцо, состоящее из 12 или 13 (разное число по литературным данным) γ-тубулиновых субъединиц связанных с другими белками, так называемый γtubulin ring complex (γ-Tu. RC; Aldaz et al. 2005). γ-Tu. RC действует как инициаторный комплекс, откуда и исходит 13 тубулиновых протофиламентов.

MTOCs у грибов могут быть локализованы в разных компартментах клетки. -У дрожжей и мицелиальных грибов главным/единственным центром организации микротрубочек является встроенное в мембрану ядра полярное тело веретена, ПТВ -дисперсные MTOCs, локализованные в цитоплазме -полярные MTOCs
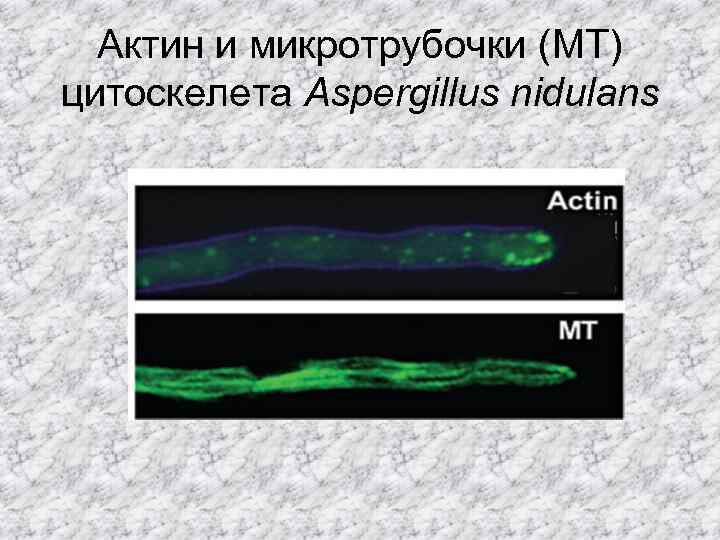
Актин и микротрубочки (MT) цитоскелета Aspergillus nidulans
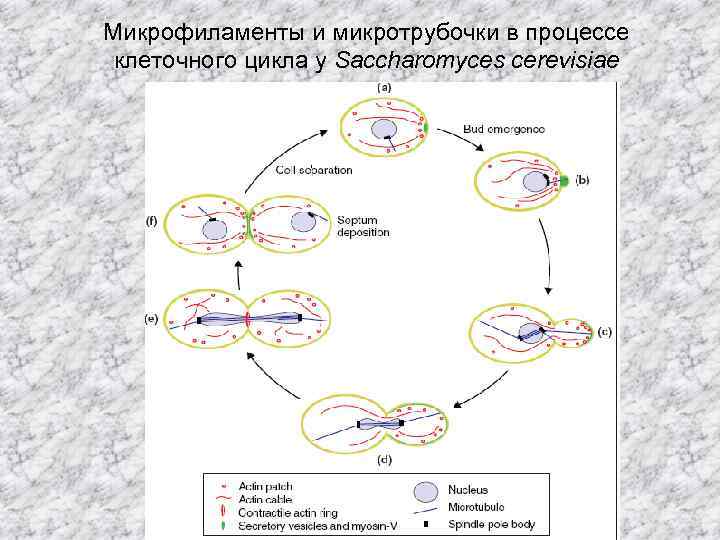
Микрофиламенты и микротрубочки в процессе клеточного цикла у Saccharomyces cerevisiae
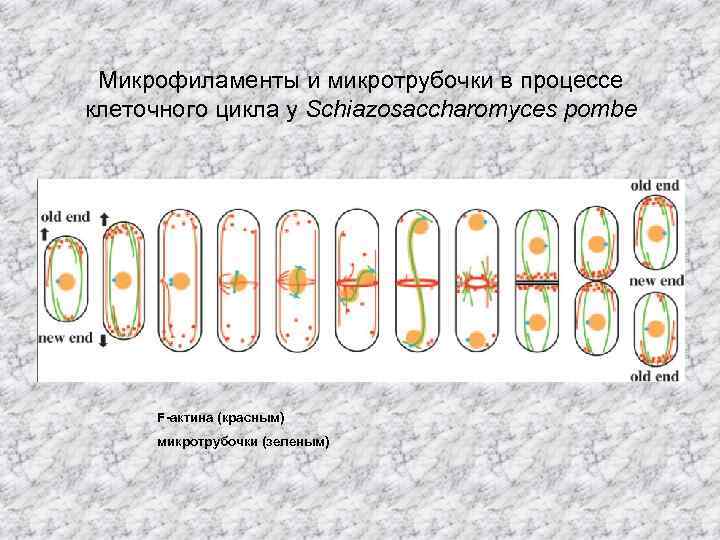
Микрофиламенты и микротрубочки в процессе клеточного цикла у Schiazosaccharomyces pombe F-актина (красным) микротрубочки (зеленым)
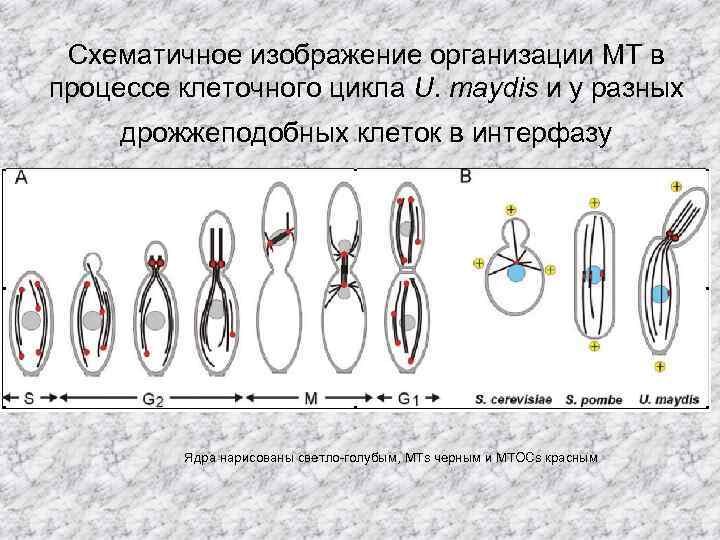
Схематичное изображение организации MT в процессе клеточного цикла U. maydis и у разных дрожжеподобных клеток в интерфазу Ядра нарисованы светло-голубым, MTs черным и MTOCs красным
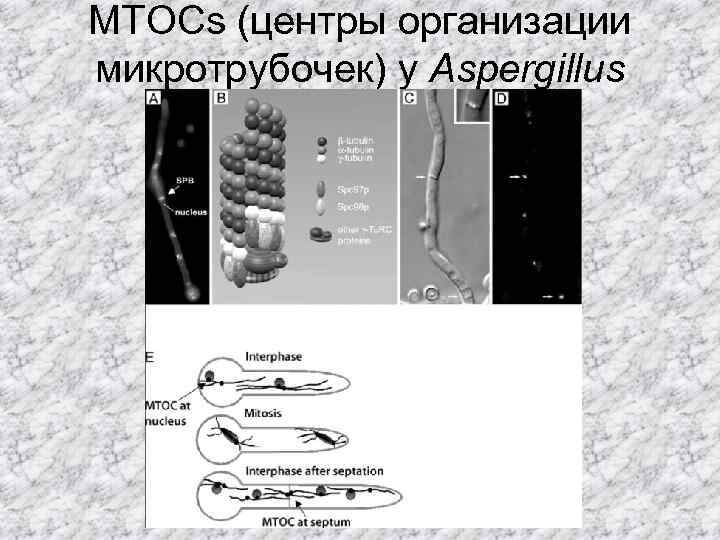
MTOCs (центры организации микротрубочек) у Aspergillus nidulans.
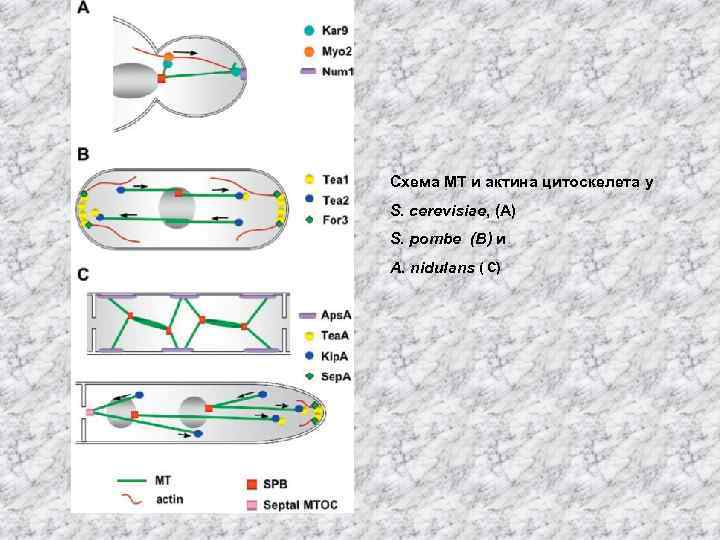
Схема MT и актина цитоскелета у S. cerevisiae, (A) S. pombe (B) и A. nidulans ( C)

MT-зависимые моторные белки MTs и их динамика в принципе достаточны для создания силы и транспорта грузов (приуроченных к растущему концу) в клетке. Однако, два класса моторных белков вовлечено для гарантированного быстрого MT-зависимого движения в клетке, минус направленный конец - динеин и плюс направленный конец кинезины
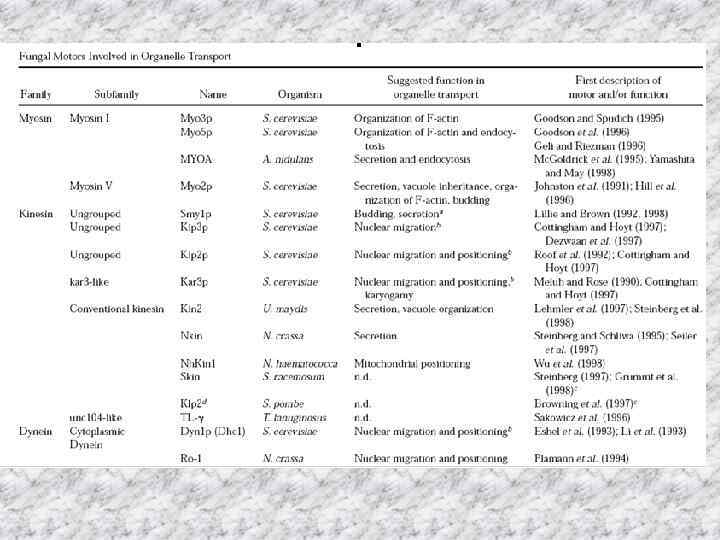
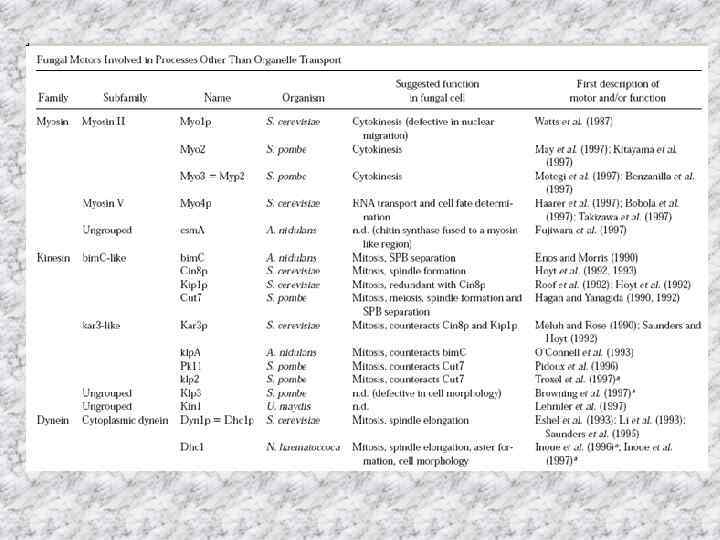

Актин-зависимые моторные белки (таблица 1, 2) • Функции актинового цитоскелета зависят от активности моторных белков, миозинов. Миозины используются для разных клеточных функций и группируются в 18 разных классов. У Asp. nidulans миозины класса I были идентифицированы и показана их востребованность для секреции белка и поляризованного роста и с особой ролью для жизнеспособности. Они локализованы у растущего кончика гифы. Данность, что миозиновые моторы вовлечены в транспорт везикул к кортексу клетки и слияние везикул с клеточной мембраной, очень интересно, что Asp. nidulans использует миозиновый моторный домен для транспортировки хитин синтаз класса V и VI, где моторный домен непосредственно сливается с ферментом. Миозиновые моторные белки других классов описаны напр у Sac. cerevisiae, где класс V миозин моторов вовлечен в наследование пероксисом и др органелл. Класс V myosin необходим для транспортировки RNA. • Делеция миозинового гена, myo. A, летальна.
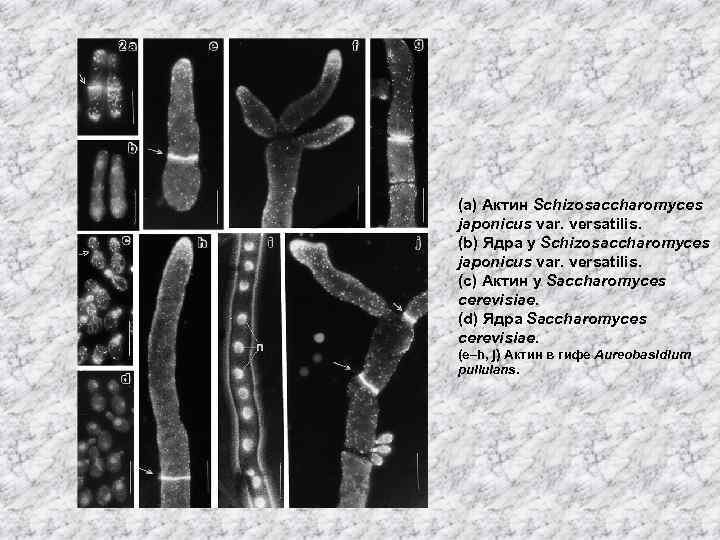
(a) Актин Schizosaccharomyces japonicus var. versatilis. (b) Ядра у Schizosaccharomyces japonicus var. versatilis. (c) Актин у Saccharomyces cerevisiae. (d) Ядра Saccharomyces cerevisiae. (e–h, j) Актин в гифе Aureobasidium pullulans.

Направленный в почку транспорт органелл у клеток S. cerevisiae
Апикальное тельце и цитоскелет 3 2011.ppt