ЛТ при РМЖ.pptx
- Количество слайдов: 31
 АО «Медицинский университет Астана» Кафедра онкологии Препараты, применяемые при лекарственной терапии рака молочной железы. Проверил: Жакипбаев К. А. Подготовила: Качулина А. , 143 Аи. Г Астана, 2016 г.
АО «Медицинский университет Астана» Кафедра онкологии Препараты, применяемые при лекарственной терапии рака молочной железы. Проверил: Жакипбаев К. А. Подготовила: Качулина А. , 143 Аи. Г Астана, 2016 г.
 План: 1. 2. 3. 4. 5. 6. 7. Цели при лечении пациенток с РМЖ. Лекарственные средства, используемые для лечения РМЖ. Рекомендации по применению адъювантной систоемной терапии РМЖ. Гормонотерапия РМЖ. Химиотерапия РМЖ. Таргетная терапия РМЖ. Список литературы.
План: 1. 2. 3. 4. 5. 6. 7. Цели при лечении пациенток с РМЖ. Лекарственные средства, используемые для лечения РМЖ. Рекомендации по применению адъювантной систоемной терапии РМЖ. Гормонотерапия РМЖ. Химиотерапия РМЖ. Таргетная терапия РМЖ. Список литературы.
 Конечными целями при лечении пациентов с РМЖ являются: Увеличение продолжительности жизни; Улучшение качества жизни этих больных; Увеличение безрецидивного периода.
Конечными целями при лечении пациентов с РМЖ являются: Увеличение продолжительности жизни; Улучшение качества жизни этих больных; Увеличение безрецидивного периода.
 На данный момент лекарственные методы лечения РМЖ подразделяются на: Эндокринотерапию (гормонотерапию) Цитотоксическую терапию (химиотерапию) Таргетную терапию. Единого стандарта лечения РМЖ не существует. Выбор варианта лекарственной терапии осуществляется с учетом биологических маркеров (РЭ и РП, HER-2, Ki 67), факторов риска и клинико-анамнестических особенностей больного. Лечение метастатической болезни обычно включает химио- и / или гормонотерапию, которые должны дополняться таргетной терапией по показаниям.
На данный момент лекарственные методы лечения РМЖ подразделяются на: Эндокринотерапию (гормонотерапию) Цитотоксическую терапию (химиотерапию) Таргетную терапию. Единого стандарта лечения РМЖ не существует. Выбор варианта лекарственной терапии осуществляется с учетом биологических маркеров (РЭ и РП, HER-2, Ki 67), факторов риска и клинико-анамнестических особенностей больного. Лечение метастатической болезни обычно включает химио- и / или гормонотерапию, которые должны дополняться таргетной терапией по показаниям.
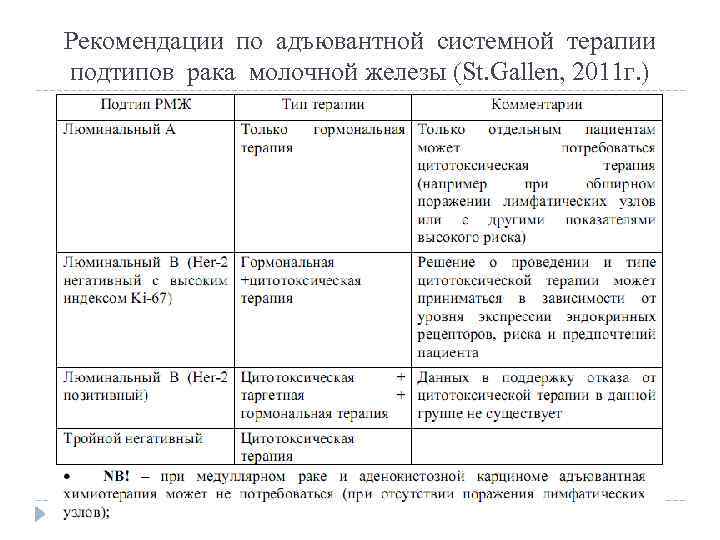 Рекомендации по адъювантной системной терапии подтипов рака молочной железы (St. Gallen, 2011 г. )
Рекомендации по адъювантной системной терапии подтипов рака молочной железы (St. Gallen, 2011 г. )
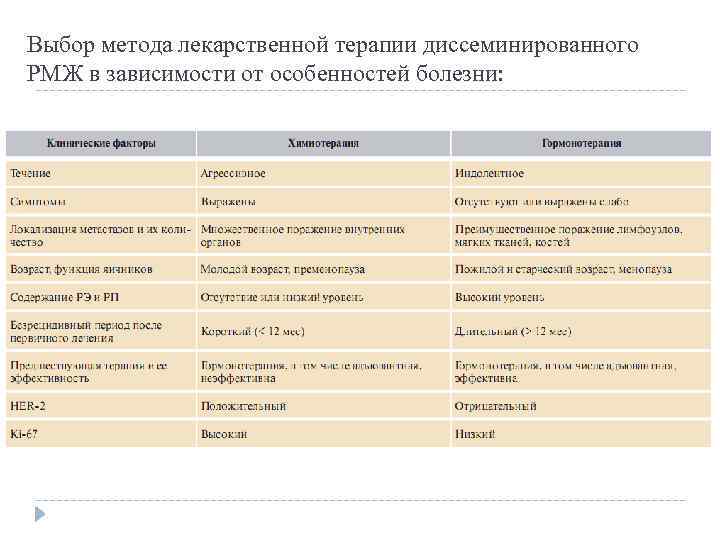 Выбор метода лекарственной терапии диссеминированного РМЖ в зависимости от особенностей болезни:
Выбор метода лекарственной терапии диссеминированного РМЖ в зависимости от особенностей болезни:
 Основной целью эндокринной терапии РМЖ является устранение или ослабление продукции гормонов, поддерживающих опухолевый рост, а так же нейтрализация их активности. При этом, если имеются и РЭ и РП, то эффективность составляет 50 -70%, если имеются рецепторы только одного вида, то эффективность соответственно сниажается до 33%. В случае рецептор-отрицательных опухолей в небольшом проценте случаев (около 11%) гормонотерапия может быть успешной.
Основной целью эндокринной терапии РМЖ является устранение или ослабление продукции гормонов, поддерживающих опухолевый рост, а так же нейтрализация их активности. При этом, если имеются и РЭ и РП, то эффективность составляет 50 -70%, если имеются рецепторы только одного вида, то эффективность соответственно сниажается до 33%. В случае рецептор-отрицательных опухолей в небольшом проценте случаев (около 11%) гормонотерапия может быть успешной.
 Гормонотерапия РМЖ разделяется на 4 класса: 1 -й класс. Это агенты и методы, снижающие уровень эстрогенов, связывающихся с ЭР. Сюда относят: овариэктомия, агонисты лютеинизирующего гормона рилизинг-гормона (ЛГРГ), подавляющие овариальную функцию, ингибиторы ароматазы (ИА), снижающие синтез периферических эстрогенов, старые хирургические методы снижения продукции эстрогенов – гипофизэктомия и адреналэктомия. 2 -й класс. Это селективные модуляторы эстрогеновых рецепторов (SERM), такие как тамоксифен и торемифен. Эти препараты связываются с ЭР и препятствуют связыванию ними эстрогенов. 3 -й класс. «Чистые» антиэстрогены, имеющие минимальную активность или не имеющие эстрогенной активности. «Чистые» антиэстрогены (фульвестрант) связываются с ЭР и блокируют их, вызывая деградацию. 4 -й класс включает фармакологические дозы эстрогенов, андрогенов и прогестинов. С учетом того, что все эти классы гормонотерапии работают по различному механизму, они не обладают перекрестной резсистентностью. Из этого следует, что при развитии резистентности к одному из классов гормонотерапии, возможно их последовательное применение.
Гормонотерапия РМЖ разделяется на 4 класса: 1 -й класс. Это агенты и методы, снижающие уровень эстрогенов, связывающихся с ЭР. Сюда относят: овариэктомия, агонисты лютеинизирующего гормона рилизинг-гормона (ЛГРГ), подавляющие овариальную функцию, ингибиторы ароматазы (ИА), снижающие синтез периферических эстрогенов, старые хирургические методы снижения продукции эстрогенов – гипофизэктомия и адреналэктомия. 2 -й класс. Это селективные модуляторы эстрогеновых рецепторов (SERM), такие как тамоксифен и торемифен. Эти препараты связываются с ЭР и препятствуют связыванию ними эстрогенов. 3 -й класс. «Чистые» антиэстрогены, имеющие минимальную активность или не имеющие эстрогенной активности. «Чистые» антиэстрогены (фульвестрант) связываются с ЭР и блокируют их, вызывая деградацию. 4 -й класс включает фармакологические дозы эстрогенов, андрогенов и прогестинов. С учетом того, что все эти классы гормонотерапии работают по различному механизму, они не обладают перекрестной резсистентностью. Из этого следует, что при развитии резистентности к одному из классов гормонотерапии, возможно их последовательное применение.
 Ингибиторы ароматазы Наиболее известные ингибиторы ароматазы – аминоглютетемид (ориметен, мамомит), ингибитор ароматазы первого поколения, стероидный инактиватор ароматазы – экземестан (аромазин) и препараты третьего поколения – летрозол (фемара), анастрозол (аримидекс). Экземестан, летрозол и анастрозол менее токсичны и не требуют заместительной кортикостероидной терапии. Они эффективны и у больных, принимавших ранее аминоглютетемид: если лечение аминоглютетемидом было эффективным, частота ответа составляет 25– 33%, если неэффективным – 6– 12%. У пременопаузальных больных ингибиторы ароматазы назначаются только после выключения функции яичников, чтобы избежать активизации синтеза эстрогенов в функционирующих яичниках по принципу «обратной связи» .
Ингибиторы ароматазы Наиболее известные ингибиторы ароматазы – аминоглютетемид (ориметен, мамомит), ингибитор ароматазы первого поколения, стероидный инактиватор ароматазы – экземестан (аромазин) и препараты третьего поколения – летрозол (фемара), анастрозол (аримидекс). Экземестан, летрозол и анастрозол менее токсичны и не требуют заместительной кортикостероидной терапии. Они эффективны и у больных, принимавших ранее аминоглютетемид: если лечение аминоглютетемидом было эффективным, частота ответа составляет 25– 33%, если неэффективным – 6– 12%. У пременопаузальных больных ингибиторы ароматазы назначаются только после выключения функции яичников, чтобы избежать активизации синтеза эстрогенов в функционирующих яичниках по принципу «обратной связи» .
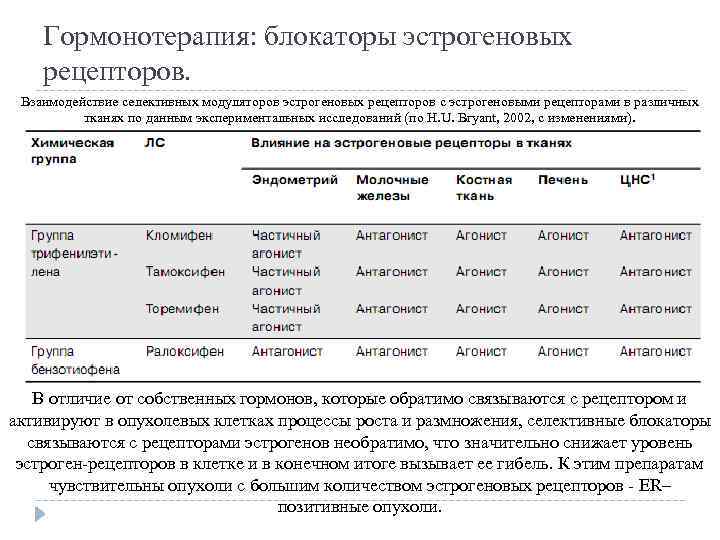 Гормонотерапия: блокаторы эстрогеновых рецепторов. Взаимодействие селективных модуляторов эстрогеновых рецепторов с эстрогеновыми рецепторами в различных тканях по данным экспериментальных исследований (по H. U. Bryant, 2002, с изменениями). В отличие от собственных гормонов, которые обратимо связываются с рецептором и активируют в опухолевых клетках процессы роста и размножения, селективные блокаторы связываются с рецепторами эстрогенов необратимо, что значительно снижает уровень эстроген-рецепторов в клетке и в конечном итоге вызывает ее гибель. К этим препаратам чувствительны опухоли с большим количеством эстрогеновых рецепторов - ER– позитивные опухоли.
Гормонотерапия: блокаторы эстрогеновых рецепторов. Взаимодействие селективных модуляторов эстрогеновых рецепторов с эстрогеновыми рецепторами в различных тканях по данным экспериментальных исследований (по H. U. Bryant, 2002, с изменениями). В отличие от собственных гормонов, которые обратимо связываются с рецептором и активируют в опухолевых клетках процессы роста и размножения, селективные блокаторы связываются с рецепторами эстрогенов необратимо, что значительно снижает уровень эстроген-рецепторов в клетке и в конечном итоге вызывает ее гибель. К этим препаратам чувствительны опухоли с большим количеством эстрогеновых рецепторов - ER– позитивные опухоли.
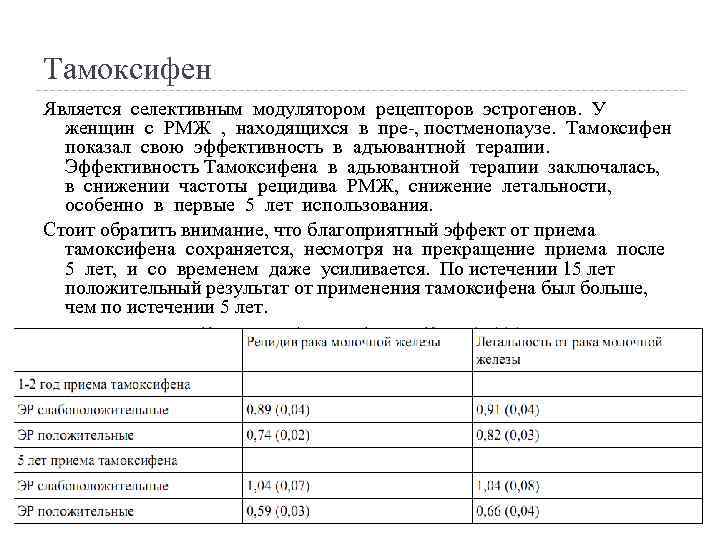 Тамоксифен Является селективным модулятором рецепторов эстрогенов. У женщин с РМЖ , находящихся в пре-, постменопаузе. Тамоксифен показал свою эффективность в адъювантной терапии. Эффективность Тамоксифена в адьювантной терапии заключалась, в снижении частоты рецидива РМЖ, снижение летальности, особенно в первые 5 лет использования. Стоит обратить внимание, что благоприятный эффект от приема тамоксифена сохраняется, несмотря на прекращение приема после 5 лет, и со временем даже усиливается. По истечении 15 лет положительный результат от применения тамоксифена был больше, чем по истечении 5 лет.
Тамоксифен Является селективным модулятором рецепторов эстрогенов. У женщин с РМЖ , находящихся в пре-, постменопаузе. Тамоксифен показал свою эффективность в адъювантной терапии. Эффективность Тамоксифена в адьювантной терапии заключалась, в снижении частоты рецидива РМЖ, снижение летальности, особенно в первые 5 лет использования. Стоит обратить внимание, что благоприятный эффект от приема тамоксифена сохраняется, несмотря на прекращение приема после 5 лет, и со временем даже усиливается. По истечении 15 лет положительный результат от применения тамоксифена был больше, чем по истечении 5 лет.
 Тамоксифен Стандартная доза тамоксифена – 20 мгсут (или 10 мг 2 раза в сутки). Повышение дозировки не приводит к увеличению эффективности. Доказано, что эффективность от приема тамоксифена в течении 5 лет намного выше, чем ограниченного 1 -2 годами. Прием тамоксифена может сопровождаться побочными эффектами, не связанным с его влиянием на рак молочной железы. Побочные эффекты Тамоксифена (наиболее часто встречающиеся): головная боль, головокружение, утомляемость, диспепсические явления, потеря аппетита, нарушение стула, увеличение уровня печеночных ферментов, кровотечение или выделения из влагалища, аменорея или нерегулярность наступления менструаций у пациенток в предклимактерическом периоде, кожная сыпь, боль в области очага поражения и/или в костях, увеличение размера мягкотканных образований, гиперкальциемия; при длительном применении – случаи изменения эндометрия, включающие гиперплазию, полипы, внутриматочную фиброму и в единичных случаях– рак эндометрия. Учитывая риск гиперплазии эндометрия, пациенткам должно назначаться ультрозвуковое исследование органов малого таза (прицельно толщина эндометрия матки) 1 раз в 3(6) месяца.
Тамоксифен Стандартная доза тамоксифена – 20 мгсут (или 10 мг 2 раза в сутки). Повышение дозировки не приводит к увеличению эффективности. Доказано, что эффективность от приема тамоксифена в течении 5 лет намного выше, чем ограниченного 1 -2 годами. Прием тамоксифена может сопровождаться побочными эффектами, не связанным с его влиянием на рак молочной железы. Побочные эффекты Тамоксифена (наиболее часто встречающиеся): головная боль, головокружение, утомляемость, диспепсические явления, потеря аппетита, нарушение стула, увеличение уровня печеночных ферментов, кровотечение или выделения из влагалища, аменорея или нерегулярность наступления менструаций у пациенток в предклимактерическом периоде, кожная сыпь, боль в области очага поражения и/или в костях, увеличение размера мягкотканных образований, гиперкальциемия; при длительном применении – случаи изменения эндометрия, включающие гиперплазию, полипы, внутриматочную фиброму и в единичных случаях– рак эндометрия. Учитывая риск гиперплазии эндометрия, пациенткам должно назначаться ультрозвуковое исследование органов малого таза (прицельно толщина эндометрия матки) 1 раз в 3(6) месяца.
 Фазлодекс Единственный препарат, механизм действия которого заключается в том, что он разрушает имеющиеся на поверхности клеток эстрогеновые рецепторы. Стероидный антиэстроген Фазлодекс (фулвестрант) продемонстрировал в доклинических исследованиях полное отсутствие эстрогенной активности, большую в сравнении с тамоксифеном эффективность на моделях рака молочной железы (РМЖ) и вызвал подавление роста тамоксифенрезистентных штаммов РМЖ. В сравнительных клинических исследованиях Фазлодекс обнаружил равную анастрозолу эффективность в гормонотерапии 2 -й линии у больных распространенным РМЖ, исчерпавших возможности тамоксифена. При проведении гормонотерапии 1 -й линии метастатического РМЖ не выявлено преимуществ Фазлодекса перед тамоксифеном. В настоящее время Фазлодекс рекомендован к применению у больных метастатическим РМЖ в менопаузе с позитивным рецепторным статусом при прогрессировании на предшествующей терапии антиэстрогенами. Обсуждаются роль и место Фазлодекса в гормональном лечении распространенного РМЖ.
Фазлодекс Единственный препарат, механизм действия которого заключается в том, что он разрушает имеющиеся на поверхности клеток эстрогеновые рецепторы. Стероидный антиэстроген Фазлодекс (фулвестрант) продемонстрировал в доклинических исследованиях полное отсутствие эстрогенной активности, большую в сравнении с тамоксифеном эффективность на моделях рака молочной железы (РМЖ) и вызвал подавление роста тамоксифенрезистентных штаммов РМЖ. В сравнительных клинических исследованиях Фазлодекс обнаружил равную анастрозолу эффективность в гормонотерапии 2 -й линии у больных распространенным РМЖ, исчерпавших возможности тамоксифена. При проведении гормонотерапии 1 -й линии метастатического РМЖ не выявлено преимуществ Фазлодекса перед тамоксифеном. В настоящее время Фазлодекс рекомендован к применению у больных метастатическим РМЖ в менопаузе с позитивным рецепторным статусом при прогрессировании на предшествующей терапии антиэстрогенами. Обсуждаются роль и место Фазлодекса в гормональном лечении распространенного РМЖ.
 Оценка эффективности гормонотерапии: Эффективность гормонотерапии нужно оценивать через 6 -8 нед от момента лечения, и только при наличии достоверных признаков прогрессирования болезни гормонотерапию следует отменить. Но при этом надо учитывать, что в течение первого месяца приема тамоксифена, прогестинов, андрогенов (но не ингибиторов ароматаз) симптомы, связанные с опухолевым ростом, могут усилиться (так называемый эффект «flare» ). Так же отмечено, что при отмене гормонотерапии, в связи с прогрессированием, наоборот, может произойти стабилизация процесса или уменьшение проявлений болезни (так называемый симптом отмены).
Оценка эффективности гормонотерапии: Эффективность гормонотерапии нужно оценивать через 6 -8 нед от момента лечения, и только при наличии достоверных признаков прогрессирования болезни гормонотерапию следует отменить. Но при этом надо учитывать, что в течение первого месяца приема тамоксифена, прогестинов, андрогенов (но не ингибиторов ароматаз) симптомы, связанные с опухолевым ростом, могут усилиться (так называемый эффект «flare» ). Так же отмечено, что при отмене гормонотерапии, в связи с прогрессированием, наоборот, может произойти стабилизация процесса или уменьшение проявлений болезни (так называемый симптом отмены).
![Гормонотерапия при диссеминированном раке молочной железы: эффективность различных методов [цит. по C. Henderson, 1991] Гормонотерапия при диссеминированном раке молочной железы: эффективность различных методов [цит. по C. Henderson, 1991]](https://present5.com/presentation/37100379_439590746/image-15.jpg) Гормонотерапия при диссеминированном раке молочной железы: эффективность различных методов [цит. по C. Henderson, 1991] *Преимущественно постменопаузальные больные. ** Исключительно больные репродуктивного возраста или в менопаузе менее 1 года (4)
Гормонотерапия при диссеминированном раке молочной железы: эффективность различных методов [цит. по C. Henderson, 1991] *Преимущественно постменопаузальные больные. ** Исключительно больные репродуктивного возраста или в менопаузе менее 1 года (4)
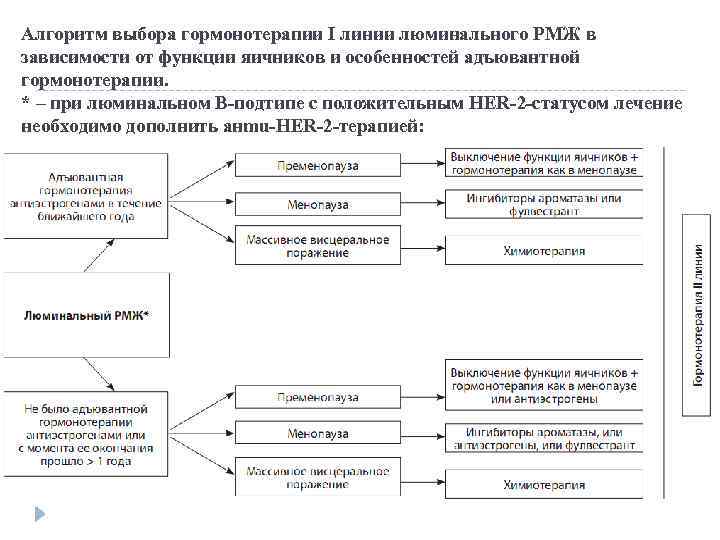 Алгоритм выбора гормонотерапии I линии люминального РМЖ в зависимости от функции яичников и особенностей адъювантной гормонотерапии. * – при люминальном В-подтипе с положительным HER-2 -статусом лечение необходимо дополнить aнmu-HER-2 -терапией:
Алгоритм выбора гормонотерапии I линии люминального РМЖ в зависимости от функции яичников и особенностей адъювантной гормонотерапии. * – при люминальном В-подтипе с положительным HER-2 -статусом лечение необходимо дополнить aнmu-HER-2 -терапией:
 Больные с сохранной функцией яичников: Если адъювантной терапии тамоксифеном не проводилось или после ее отмены прошло > 1 года: • тамоксифен 20 мг / сут ± выключение функции яичников; • выключение функции яичников + гормонотерапия по аналогии с больными в менопаузе (ингибиторы ароматазы (летрозол 2, 5 мг / сут, или анастрозол 1 мг / сут, или эксеместан 25 мг / сут в сочетании с препаратами Са 2+ и витамином D) или фулвестрант 500 мг 1 раз в месяц). Если адъювантная терапия тамоксифеном проводилась в течение ближайшего года: • выключение функции яичников + гормонотерапия по аналогии с больными в менопаузе (ингибиторы ароматазы (летрозол 2, 5 мг / сут, или анастрозол 1 мг / сут, или эксеместан 25 мг / сут в сочетании с препаратами Са 2+ и витамином D) или фулвестрант 500 мг 1 раз в месяц). Дальнейшие линии гормонотерапии после выключения функции яичников не отличаются от таковых у больных в менопаузе.
Больные с сохранной функцией яичников: Если адъювантной терапии тамоксифеном не проводилось или после ее отмены прошло > 1 года: • тамоксифен 20 мг / сут ± выключение функции яичников; • выключение функции яичников + гормонотерапия по аналогии с больными в менопаузе (ингибиторы ароматазы (летрозол 2, 5 мг / сут, или анастрозол 1 мг / сут, или эксеместан 25 мг / сут в сочетании с препаратами Са 2+ и витамином D) или фулвестрант 500 мг 1 раз в месяц). Если адъювантная терапия тамоксифеном проводилась в течение ближайшего года: • выключение функции яичников + гормонотерапия по аналогии с больными в менопаузе (ингибиторы ароматазы (летрозол 2, 5 мг / сут, или анастрозол 1 мг / сут, или эксеместан 25 мг / сут в сочетании с препаратами Са 2+ и витамином D) или фулвестрант 500 мг 1 раз в месяц). Дальнейшие линии гормонотерапии после выключения функции яичников не отличаются от таковых у больных в менопаузе.
 Больные в менопаузе: Если адъювантная терапия тамоксифеном или ингибиторами ароматазы не проводилась или после ее отмены прошло > 1 года: • ингибиторы ароматазы (летрозол 2, 5 мг / сут, или анастрозол 1 мг / сут, или эксеместан 25 мг / сут в сочетании с препаратами Са 2+ и витамином D); • фулвестрант 500 мг 1 раз в месяц; • тамоксифен 20 мг / сут. Если адъювантная терапия тамоксифеном проводилась в течение ближайшего года: • ингибиторы ароматазы (летрозол 2, 5 мг / сут, или анастрозол 1 мг / сут, или эксеместан 25 мг / сут в сочетании с препаратами Са 2+ и витамином D); • фулвестрант 500 мг 1 раз в месяц. Если адъювантная терапия ингибиторами ароматазы проводилась в течение ближайшего года: • тамоксифен 20 мг / сут; • фулвестрант 500 мг 1 раз в месяц; • ингибиторы ароматазы со сменой нестероидного препарата (летрозол, анастрозол) на стероидный (эксеместан) и наоборот.
Больные в менопаузе: Если адъювантная терапия тамоксифеном или ингибиторами ароматазы не проводилась или после ее отмены прошло > 1 года: • ингибиторы ароматазы (летрозол 2, 5 мг / сут, или анастрозол 1 мг / сут, или эксеместан 25 мг / сут в сочетании с препаратами Са 2+ и витамином D); • фулвестрант 500 мг 1 раз в месяц; • тамоксифен 20 мг / сут. Если адъювантная терапия тамоксифеном проводилась в течение ближайшего года: • ингибиторы ароматазы (летрозол 2, 5 мг / сут, или анастрозол 1 мг / сут, или эксеместан 25 мг / сут в сочетании с препаратами Са 2+ и витамином D); • фулвестрант 500 мг 1 раз в месяц. Если адъювантная терапия ингибиторами ароматазы проводилась в течение ближайшего года: • тамоксифен 20 мг / сут; • фулвестрант 500 мг 1 раз в месяц; • ингибиторы ароматазы со сменой нестероидного препарата (летрозол, анастрозол) на стероидный (эксеместан) и наоборот.
 Больные в менопаузе: Больные, получающие тамоксифен, должны быть проинформированы о недопустимости одновременного приема модуляторов активности CYP 2 D 6. Вторая линия гормонотерапии больных в менопаузе может включать тамоксифен, препараты третьего поколения ингибиторов ароматазы (если они не использовались ранее), фулвестрант, прогестины в зависимости от того, что использовалось ранее. У больных HER-2 отрицательным РМЖ в удовлетворительном общем состоянии, с нормальной функцией внутренних органов, в том числе при нормальном уровне глюкозы в крови, гормонотерапия второй линии ингибиторами ароматазы может быть дополнена ингибитором m-TOR – эверолимусом (10 мг / сут внутрь ежедневно).
Больные в менопаузе: Больные, получающие тамоксифен, должны быть проинформированы о недопустимости одновременного приема модуляторов активности CYP 2 D 6. Вторая линия гормонотерапии больных в менопаузе может включать тамоксифен, препараты третьего поколения ингибиторов ароматазы (если они не использовались ранее), фулвестрант, прогестины в зависимости от того, что использовалось ранее. У больных HER-2 отрицательным РМЖ в удовлетворительном общем состоянии, с нормальной функцией внутренних органов, в том числе при нормальном уровне глюкозы в крови, гормонотерапия второй линии ингибиторами ароматазы может быть дополнена ингибитором m-TOR – эверолимусом (10 мг / сут внутрь ежедневно).
 Химиотерапия Существует несколько видов химиотерапии, которые отличаются по цели назначения: неоадъювантная химиотерапия опухолей назначается до операции, с целью уменьшения неоперабельной опухоли для проведения операции, а так же для выявления чувствительности раковых клеток к препаратам для дальнейшего назначения после операции. адъювантная химиотерапия назначается после хирургического лечения для предотвращения метастазирования и снижения риска рецидивов. лечебная химиотерапия назначается для уменьшения метастатических раковых опухолей. В зависимости от локализации и вида опухоли химиотерапия назначается по разным схемам и имеет свои особенности.
Химиотерапия Существует несколько видов химиотерапии, которые отличаются по цели назначения: неоадъювантная химиотерапия опухолей назначается до операции, с целью уменьшения неоперабельной опухоли для проведения операции, а так же для выявления чувствительности раковых клеток к препаратам для дальнейшего назначения после операции. адъювантная химиотерапия назначается после хирургического лечения для предотвращения метастазирования и снижения риска рецидивов. лечебная химиотерапия назначается для уменьшения метастатических раковых опухолей. В зависимости от локализации и вида опухоли химиотерапия назначается по разным схемам и имеет свои особенности.
 Химиотерапия показана следующим категориям больных РМЖ: отказа пациента от операции; улучшение отдаленных результатов лечения при неблагоприятных фенотипах опухоли (тройной негативный, Her 2 -негативный рак). цитологически и гистологически верифицированные РМЖ; при лечении местно- распространенных опухолей; метастазы в регионарных лимфатических узлах/ отдаленные органы – легкие, печень, головной мозг, костная структура; рецидив опухоли; удовлетворительная картина крови у пациента: нормальные показатели гемоглобина и гемокрита, абсолютное число гранулоцитов – более 200, тромбоцитов – более 100000; сохраненная функция печени, почек, дыхательной системы и ССС; возможность перевода неоперабельного опухолевого процесса в операбельный; Лекарственная терапия (ХТ, ГТ) ЛТ с паллиативной целью (при мтс поражении костей скелета)
Химиотерапия показана следующим категориям больных РМЖ: отказа пациента от операции; улучшение отдаленных результатов лечения при неблагоприятных фенотипах опухоли (тройной негативный, Her 2 -негативный рак). цитологически и гистологически верифицированные РМЖ; при лечении местно- распространенных опухолей; метастазы в регионарных лимфатических узлах/ отдаленные органы – легкие, печень, головной мозг, костная структура; рецидив опухоли; удовлетворительная картина крови у пациента: нормальные показатели гемоглобина и гемокрита, абсолютное число гранулоцитов – более 200, тромбоцитов – более 100000; сохраненная функция печени, почек, дыхательной системы и ССС; возможность перевода неоперабельного опухолевого процесса в операбельный; Лекарственная терапия (ХТ, ГТ) ЛТ с паллиативной целью (при мтс поражении костей скелета)
 Противопоказания к химиотерапии: Абсолютные противопоказания: гипертермия >38 градусов; заболевание в стадии декомпенсации (сердечно-сосудистой системы, дыхательной системы печени, почек); наличие острых инфекционных заболеваний; психические заболевания; неэффективность данного вида лечения, подтвержденная одним или несколькими специалистами; распад опухоли (угроза кровотечения); тяжелое состояние больного по шкале Карновского 50% и меньше. Относительные противопоказания: беременность; интоксикация организма; активный туберкулез легких; стойкие патологические изменения состава крови (анемия, лейкопения, тромбоцитопения); кахексия.
Противопоказания к химиотерапии: Абсолютные противопоказания: гипертермия >38 градусов; заболевание в стадии декомпенсации (сердечно-сосудистой системы, дыхательной системы печени, почек); наличие острых инфекционных заболеваний; психические заболевания; неэффективность данного вида лечения, подтвержденная одним или несколькими специалистами; распад опухоли (угроза кровотечения); тяжелое состояние больного по шкале Карновского 50% и меньше. Относительные противопоказания: беременность; интоксикация организма; активный туберкулез легких; стойкие патологические изменения состава крови (анемия, лейкопения, тромбоцитопения); кахексия.
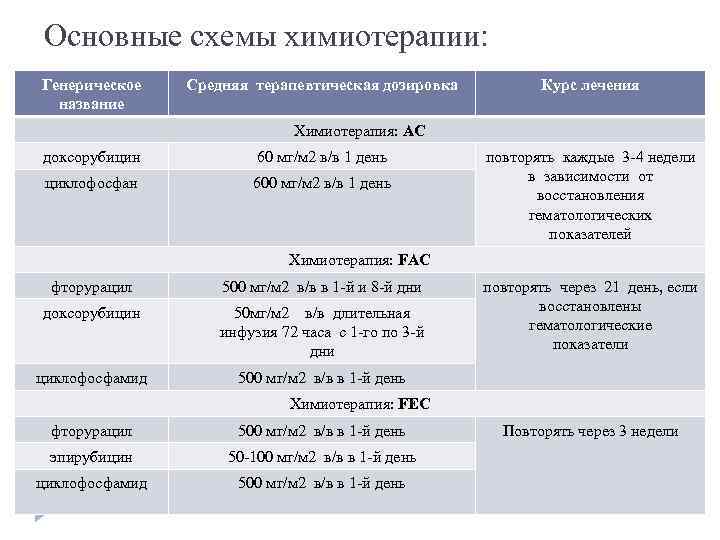 Основные схемы химиотерапии: Генерическое название Средняя терапевтическая дозировка Курс лечения Химиотерапия: АС доксорубицин 60 мг/м 2 в/в 1 день циклофосфан 600 мг/м 2 в/в 1 день повторять каждые 3 -4 недели в зависимости от восстановления гематологических показателей Химиотерапия: FАС фторурацил 500 мг/м 2 в/в в 1 -й и 8 -й дни доксорубицин 50 мг/м 2 в/в длительная инфузия 72 часа с 1 -го по 3 -й дни циклофосфамид повторять через 21 день, если восстановлены гематологические показатели 500 мг/м 2 в/в в 1 -й день Химиотерапия: FЕС фторурацил 500 мг/м 2 в/в в 1 -й день эпирубицин 50 -100 мг/м 2 в/в в 1 -й день циклофосфамид 500 мг/м 2 в/в в 1 -й день Повторять через 3 недели
Основные схемы химиотерапии: Генерическое название Средняя терапевтическая дозировка Курс лечения Химиотерапия: АС доксорубицин 60 мг/м 2 в/в 1 день циклофосфан 600 мг/м 2 в/в 1 день повторять каждые 3 -4 недели в зависимости от восстановления гематологических показателей Химиотерапия: FАС фторурацил 500 мг/м 2 в/в в 1 -й и 8 -й дни доксорубицин 50 мг/м 2 в/в длительная инфузия 72 часа с 1 -го по 3 -й дни циклофосфамид повторять через 21 день, если восстановлены гематологические показатели 500 мг/м 2 в/в в 1 -й день Химиотерапия: FЕС фторурацил 500 мг/м 2 в/в в 1 -й день эпирубицин 50 -100 мг/м 2 в/в в 1 -й день циклофосфамид 500 мг/м 2 в/в в 1 -й день Повторять через 3 недели
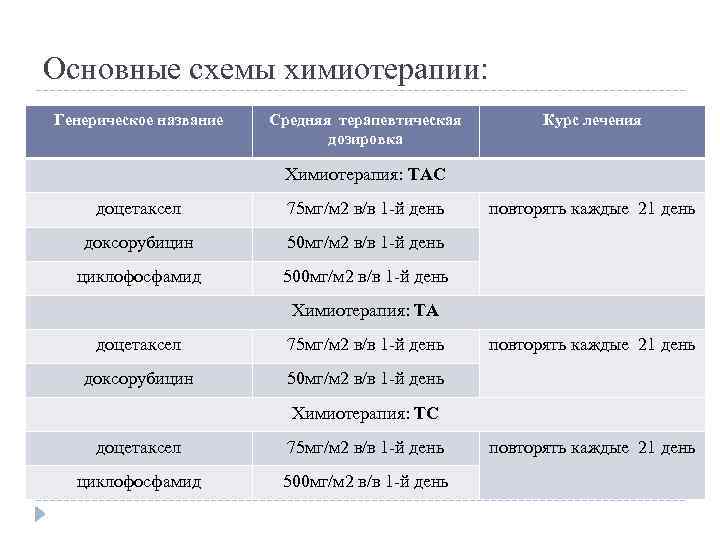 Основные схемы химиотерапии: Генерическое название Средняя терапевтическая дозировка Курс лечения Химиотерапия: ТАС доцетаксел 75 мг/м 2 в/в 1 -й день доксорубицин 50 мг/м 2 в/в 1 -й день циклофосфамид повторять каждые 21 день 500 мг/м 2 в/в 1 -й день Химиотерапия: ТА доцетаксел 75 мг/м 2 в/в 1 -й день доксорубицин повторять каждые 21 день 50 мг/м 2 в/в 1 -й день Химиотерапия: ТС доцетаксел 75 мг/м 2 в/в 1 -й день циклофосфамид 500 мг/м 2 в/в 1 -й день повторять каждые 21 день
Основные схемы химиотерапии: Генерическое название Средняя терапевтическая дозировка Курс лечения Химиотерапия: ТАС доцетаксел 75 мг/м 2 в/в 1 -й день доксорубицин 50 мг/м 2 в/в 1 -й день циклофосфамид повторять каждые 21 день 500 мг/м 2 в/в 1 -й день Химиотерапия: ТА доцетаксел 75 мг/м 2 в/в 1 -й день доксорубицин повторять каждые 21 день 50 мг/м 2 в/в 1 -й день Химиотерапия: ТС доцетаксел 75 мг/м 2 в/в 1 -й день циклофосфамид 500 мг/м 2 в/в 1 -й день повторять каждые 21 день
 Таргетная терапия при РМЖ: Последние два десятилетия привели к прорыву в области лечения рака молочной железы – в клиническую практику вошли препараты точечного воздействия на измененные раковые клетки. Они получили название «таргетных» - или препаратов цели (англ. target). Как синоним используется термины “молекулярная таргетная терапия” и „иммунная таргет-терапия“. Таргетная терапия вызывает только гибель опухолевых клеток, практически не оказывая неблагоприятного воздействия на остальные ткани организма, и, как следствие, практически не вызывает побочных эффектов.
Таргетная терапия при РМЖ: Последние два десятилетия привели к прорыву в области лечения рака молочной железы – в клиническую практику вошли препараты точечного воздействия на измененные раковые клетки. Они получили название «таргетных» - или препаратов цели (англ. target). Как синоним используется термины “молекулярная таргетная терапия” и „иммунная таргет-терапия“. Таргетная терапия вызывает только гибель опухолевых клеток, практически не оказывая неблагоприятного воздействия на остальные ткани организма, и, как следствие, практически не вызывает побочных эффектов.
 Aнти-HER-2 -терапия: Больные HER-2 -положительным РМЖ должны получать анти-HER-2 -терапию в сочетании с химио- или гормонотерапией (при люминальных опухолях). В качестве первой линии рекомендуется трастузумаб (если он не назначался с адъювантной целью) в сочетании с химиотерапией или гормонотерапией (при люминальном В -варианте РМЖ). Необходима оценка сократительной способности миокарда в процессе терапии трастузумабом и до нее. При первом эпизоде прогрессирования на фоне лечения трастузумабом возможно продолжение лечения этим же препаратом со сменой химиотерапевтического режима или переход на лапатиниб.
Aнти-HER-2 -терапия: Больные HER-2 -положительным РМЖ должны получать анти-HER-2 -терапию в сочетании с химио- или гормонотерапией (при люминальных опухолях). В качестве первой линии рекомендуется трастузумаб (если он не назначался с адъювантной целью) в сочетании с химиотерапией или гормонотерапией (при люминальном В -варианте РМЖ). Необходима оценка сократительной способности миокарда в процессе терапии трастузумабом и до нее. При первом эпизоде прогрессирования на фоне лечения трастузумабом возможно продолжение лечения этим же препаратом со сменой химиотерапевтического режима или переход на лапатиниб.
 Трастузумаб Мишенью для трастузумаба (герцептина) является рецептор человеческого эпидермального фактора роста (англ. human epidermal growth factor receptor, сокращенно - Her-2). Уникальной особенностью Her-2 опосредование большинства сигналов активаторов роста, передающихся к опухолевым клеткам. По сравнению с другими таргетными препаратами трастузумаб имеет существенно большую эффективность в отношении подавления (супрессии) опухолевых клеток. Кроме того, трастузумаб стимулирует иммунную систему к атаке на клетки, имеющие высокую концентрацию Her-2. Как экспериментальные, так и клинические исследования показали, что HER 2–статус (сверхэкспрессия протеина/генная амплификация) является главным предсказывающим фактором ответа на лечение трастузумабом. Поэтому определение HER 2 экспрессии/амплификации представляет существенный шаг для отбора больных для лечения таким агентом. Последние in vitro эксперименты свидетельствуют о возможных молекулярных механизмах резистентности к трастузумабу, включая потерю PTEN, увеличение активности рецептора инсулин–подобного фактора роста, нарушение регуляции р27 и VEFG–опосредованного ангиогенеза.
Трастузумаб Мишенью для трастузумаба (герцептина) является рецептор человеческого эпидермального фактора роста (англ. human epidermal growth factor receptor, сокращенно - Her-2). Уникальной особенностью Her-2 опосредование большинства сигналов активаторов роста, передающихся к опухолевым клеткам. По сравнению с другими таргетными препаратами трастузумаб имеет существенно большую эффективность в отношении подавления (супрессии) опухолевых клеток. Кроме того, трастузумаб стимулирует иммунную систему к атаке на клетки, имеющие высокую концентрацию Her-2. Как экспериментальные, так и клинические исследования показали, что HER 2–статус (сверхэкспрессия протеина/генная амплификация) является главным предсказывающим фактором ответа на лечение трастузумабом. Поэтому определение HER 2 экспрессии/амплификации представляет существенный шаг для отбора больных для лечения таким агентом. Последние in vitro эксперименты свидетельствуют о возможных молекулярных механизмах резистентности к трастузумабу, включая потерю PTEN, увеличение активности рецептора инсулин–подобного фактора роста, нарушение регуляции р27 и VEFG–опосредованного ангиогенеза.
 Лапатиниб (Tykerb в США, Tyverb/Тайверб в Европе) – представляет собой малые молекулы, активные при пероральном приеме, ингибирующие и тирозинкиназу Erb. B 2 (HER 2), и, рецептор эпидермального фактора роста (EGFR) I–го типа. Таким образом, лапатиниб – это первый двойной ингибитор тирозинкиназы. Важно и то, что в преклинических исследованиях лапатиниб не показал перекрестной резистентности с трастузумабом. Лапатиниб – ингибитор тирозин–киназы, блокирующий сигнальные пути Erb. B 2 (HER 2) и EGFR через ингибицию аутофосфорилизирующих сайтов рецепторов, клинически активен даже при трастузумаб–резистентном или рефрактерном Erb. B 2 (HER 2) позитивном РМЖ, то есть у «сильно предлеченных» пациенток.
Лапатиниб (Tykerb в США, Tyverb/Тайверб в Европе) – представляет собой малые молекулы, активные при пероральном приеме, ингибирующие и тирозинкиназу Erb. B 2 (HER 2), и, рецептор эпидермального фактора роста (EGFR) I–го типа. Таким образом, лапатиниб – это первый двойной ингибитор тирозинкиназы. Важно и то, что в преклинических исследованиях лапатиниб не показал перекрестной резистентности с трастузумабом. Лапатиниб – ингибитор тирозин–киназы, блокирующий сигнальные пути Erb. B 2 (HER 2) и EGFR через ингибицию аутофосфорилизирующих сайтов рецепторов, клинически активен даже при трастузумаб–резистентном или рефрактерном Erb. B 2 (HER 2) позитивном РМЖ, то есть у «сильно предлеченных» пациенток.
 Ингибиторы ангиогенеза: Бевацизумаб и Пазопаниб Еще одной мишенью для биологически направленной терапии является ангиогенез. Ангиогенез играет существенную роль в развитии РМЖ, инвазии и метастазировании. VEGF – наиболее мощный регулирующий ангиогенный фактор. Биологические эффекты VEGF опосредуются специфическими рецепторами эндотелия: VЕGF–R 1, VEGF–R 2 и VEGF–R 3. Ряд антиангиогенных агентов исследованы в I, II и III фазах, в том числе, анти–VEGF–A моноклональное антитело бевацизумаб, показавший в исследовании III фазы, в комбинации с паклитакселом, большую эффективность, по сравнению с паклитакселом в монотерапии. Наиболее часто встречаемыми побочными эффектами при этом были гипертензия, протеинурия и нейропатия. Антиангиогенные агенты исследуются и в неоадъювантных режимах. Кроме того, в настоящее время проводятся клинические исследования нового мощного ингибитора киназы рецептора VEGF (VEGFR) пазопаниба при Erb. B 2 (HER 2) позитивном РМЖ, показавшего весьма привлекательное соотношение эффективности и безопасности в более ранних исследованиях, в том числе в комбинации с лапатинибом. Так, анализ безопасности пазопаниба в дозе 200– 500 мг в сутки per os, в сочетании с лапатинибом в дозе 750– 1500 мг в день per os, проводившийся в рамках одного из клинических исследований, показал, что большинство побочных явлений на фоне комбинированной терапии были не более чем 2 степени, и что, в целом, переносимость комбинации не отличалась от переносимости каждого из препаратов при их назначении в режиме монотерапии.
Ингибиторы ангиогенеза: Бевацизумаб и Пазопаниб Еще одной мишенью для биологически направленной терапии является ангиогенез. Ангиогенез играет существенную роль в развитии РМЖ, инвазии и метастазировании. VEGF – наиболее мощный регулирующий ангиогенный фактор. Биологические эффекты VEGF опосредуются специфическими рецепторами эндотелия: VЕGF–R 1, VEGF–R 2 и VEGF–R 3. Ряд антиангиогенных агентов исследованы в I, II и III фазах, в том числе, анти–VEGF–A моноклональное антитело бевацизумаб, показавший в исследовании III фазы, в комбинации с паклитакселом, большую эффективность, по сравнению с паклитакселом в монотерапии. Наиболее часто встречаемыми побочными эффектами при этом были гипертензия, протеинурия и нейропатия. Антиангиогенные агенты исследуются и в неоадъювантных режимах. Кроме того, в настоящее время проводятся клинические исследования нового мощного ингибитора киназы рецептора VEGF (VEGFR) пазопаниба при Erb. B 2 (HER 2) позитивном РМЖ, показавшего весьма привлекательное соотношение эффективности и безопасности в более ранних исследованиях, в том числе в комбинации с лапатинибом. Так, анализ безопасности пазопаниба в дозе 200– 500 мг в сутки per os, в сочетании с лапатинибом в дозе 750– 1500 мг в день per os, проводившийся в рамках одного из клинических исследований, показал, что большинство побочных явлений на фоне комбинированной терапии были не более чем 2 степени, и что, в целом, переносимость комбинации не отличалась от переносимости каждого из препаратов при их назначении в режиме монотерапии.
 Блокаторы PARP–белка Перспективными препаратами таргетной терапии являются ингибиторы (блокаторы) PARP–белка, которые принимают участие в восстановления поврежденной ДНК, которая очень активная в опухолевых клетках. Блокада PARP–белка включает программу “клеточной смерти” (апоптоз). Основными препаратами данной группы являются Олапариб, Инипариб, Велипариб. Блокаторы PARP–белка применяются в тех случаях, когда клетки опухоли не имеют основных рецепторов – эпидермального фактора роста Her-2, эстроген-рецептора ЕR, прогестеронового рецептора PR - “три-негативные опухоли”.
Блокаторы PARP–белка Перспективными препаратами таргетной терапии являются ингибиторы (блокаторы) PARP–белка, которые принимают участие в восстановления поврежденной ДНК, которая очень активная в опухолевых клетках. Блокада PARP–белка включает программу “клеточной смерти” (апоптоз). Основными препаратами данной группы являются Олапариб, Инипариб, Велипариб. Блокаторы PARP–белка применяются в тех случаях, когда клетки опухоли не имеют основных рецепторов – эпидермального фактора роста Her-2, эстроген-рецептора ЕR, прогестеронового рецептора PR - “три-негативные опухоли”.
 Список литературы: КЛИНИЧЕСКИЙ ПРОТОКОЛ ДИАГНОСТИКИ ЛЕЧЕНИЯ: РАК МОЛОЧНОЙ ЖЕЛЕЗЫ. Рекомендовано Экспертным советом РГП на ПХВ «Республиканский центр развития здравоохранения» . Министерства здравоохранения и социального развития Республики Казахстан от « 27» ноября 2015 года. Протокол № 17. Семиглазов В. Ф. , Иванов В. Г. , Семиглазов В. В. , Криворотько П. В. , Малодушева А. А. , Коларькова В. В. , Шамина Е. А. , Кочетова И. А. Биологически направленная (таргетная) терапия рака молочной железы // РМЖ. 2007. № 25. Таргетная терапия рака молочной железы (новые направления). Семиглазов В. Ф. , Дашян Г. А. , Семиглазов В. В. , Палтуев P. M. , Манихас А. Г. , Бессонов А. А. , Ермаченкова А. М. , Щедрин Д. Е. , Табагуа Т. Т. , Гречухина И. А. , Криворотько П. В. , Донских Р. В. , Семиглазова Т. Ю. , Коларькова В. В. 2011 г. АДЪЮВАНТНАЯ ТЕРАПИЯ АНТИЭСТРОГЕНАМИ ДИССЕМЕНИРОВАННОГО РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ. Опубликовано в 2015, Выпуск Ноябрь 2015, Парсаданян А. М. , Чернопятова И. А.
Список литературы: КЛИНИЧЕСКИЙ ПРОТОКОЛ ДИАГНОСТИКИ ЛЕЧЕНИЯ: РАК МОЛОЧНОЙ ЖЕЛЕЗЫ. Рекомендовано Экспертным советом РГП на ПХВ «Республиканский центр развития здравоохранения» . Министерства здравоохранения и социального развития Республики Казахстан от « 27» ноября 2015 года. Протокол № 17. Семиглазов В. Ф. , Иванов В. Г. , Семиглазов В. В. , Криворотько П. В. , Малодушева А. А. , Коларькова В. В. , Шамина Е. А. , Кочетова И. А. Биологически направленная (таргетная) терапия рака молочной железы // РМЖ. 2007. № 25. Таргетная терапия рака молочной железы (новые направления). Семиглазов В. Ф. , Дашян Г. А. , Семиглазов В. В. , Палтуев P. M. , Манихас А. Г. , Бессонов А. А. , Ермаченкова А. М. , Щедрин Д. Е. , Табагуа Т. Т. , Гречухина И. А. , Криворотько П. В. , Донских Р. В. , Семиглазова Т. Ю. , Коларькова В. В. 2011 г. АДЪЮВАНТНАЯ ТЕРАПИЯ АНТИЭСТРОГЕНАМИ ДИССЕМЕНИРОВАННОГО РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ. Опубликовано в 2015, Выпуск Ноябрь 2015, Парсаданян А. М. , Чернопятова И. А.


