оксиды кислоты серы гаманькова.ppt
- Количество слайдов: 26
 Антон Чехович Кислородсодержащие соединения серы Оксиды серы
Антон Чехович Кислородсодержащие соединения серы Оксиды серы
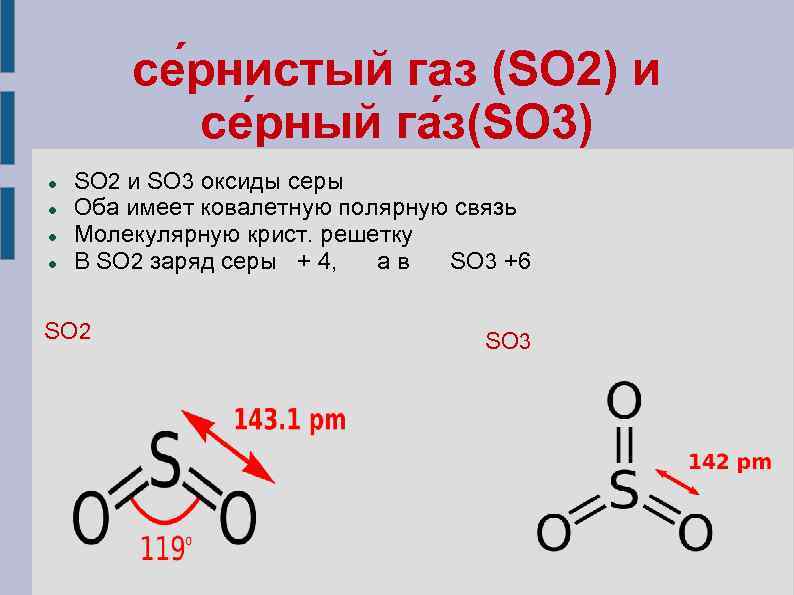 се рнистый газ (SO 2) и се рный га з(SO 3) SO 2 и SO 3 оксиды серы Оба имеет ковалетную полярную связь Молекулярную крист. решетку В SO 2 заряд серы + 4, а в SO 3 +6 SO 2 SO 3
се рнистый газ (SO 2) и се рный га з(SO 3) SO 2 и SO 3 оксиды серы Оба имеет ковалетную полярную связь Молекулярную крист. решетку В SO 2 заряд серы + 4, а в SO 3 +6 SO 2 SO 3
 SO 2 физические свойства Оксид серы IV, диоксид серы, сернистый ангидрид Бесцветный газ с характерным резким запахом (запах загорающейся спички) Растворяется в воде с образованием нестойкой се рнистой кислоты(H 2 SO 3) Температура кипения − 10, 01 °C SO 2 очень токсичен Сернистый газ – не природный продукт, он появляется в результате активной промышленной деятельности человека
SO 2 физические свойства Оксид серы IV, диоксид серы, сернистый ангидрид Бесцветный газ с характерным резким запахом (запах загорающейся спички) Растворяется в воде с образованием нестойкой се рнистой кислоты(H 2 SO 3) Температура кипения − 10, 01 °C SO 2 очень токсичен Сернистый газ – не природный продукт, он появляется в результате активной промышленной деятельности человека
 SO 3 физические свойства Оксид серы VI, триоксид серы, серный ангидрид Легколетучая бесцветная масленистая жидкость с удушающим запахом При температурах ниже 16, 9 °C застывает и образует смеси различных кристаллических модификаций Температура кипения 45 °C В природе не встречается Ядовит Мало растворим в воде проявляет свойствами сильного окислителя
SO 3 физические свойства Оксид серы VI, триоксид серы, серный ангидрид Легколетучая бесцветная масленистая жидкость с удушающим запахом При температурах ниже 16, 9 °C застывает и образует смеси различных кристаллических модификаций Температура кипения 45 °C В природе не встречается Ядовит Мало растворим в воде проявляет свойствами сильного окислителя
 SO 2 получения Промышленный способ получения — сжигание серы или обжиг сульфидов, в основном — пирита: 4 Fe. S 2+11 O 2→ 2 Fe 2 O 3+8 SO 2 В лабораторных условиях SO 2 получают воздействием сильных кислот на сульфиты и гидросульфиты. Образующаяся сернистая кислота H 2 SO 3 сразу разлагается на SO 2 и H 2 O: Na 2 SO 3+H 2 SO 4→Na 2 SO 4+H 2 SO 3→H 2 O+SO 2 Также диоксид серы можно получить действием концентрированной серной кислоты на малоактивные металлы при нагревании: Cu+2 H 2 SO 4→Cu. SO 4+SO 2+2 H 2 O
SO 2 получения Промышленный способ получения — сжигание серы или обжиг сульфидов, в основном — пирита: 4 Fe. S 2+11 O 2→ 2 Fe 2 O 3+8 SO 2 В лабораторных условиях SO 2 получают воздействием сильных кислот на сульфиты и гидросульфиты. Образующаяся сернистая кислота H 2 SO 3 сразу разлагается на SO 2 и H 2 O: Na 2 SO 3+H 2 SO 4→Na 2 SO 4+H 2 SO 3→H 2 O+SO 2 Также диоксид серы можно получить действием концентрированной серной кислоты на малоактивные металлы при нагревании: Cu+2 H 2 SO 4→Cu. SO 4+SO 2+2 H 2 O
 SO 3 получения Получают, окисляя оксид серы (IV) кислородом воздуха при нагревании, в присутствии катализатора V 2 O 5 2 SO 2+O 2 → 2 SO 3 t, kat Можно получить термическим разложением сульфатов: Fe 2(SO 4)3 → Fe 2 O 3+2 SO 3 t или взаимодействием SO 2 с озоном: SO 2+O 3 → SO 3+O 2 Для окисления SO 2 используют также NO 2: SO 2+NO 2 → SO 3+NO Эта реакция лежит в основе исторически первого, нитрозного способа получения серной кислоты.
SO 3 получения Получают, окисляя оксид серы (IV) кислородом воздуха при нагревании, в присутствии катализатора V 2 O 5 2 SO 2+O 2 → 2 SO 3 t, kat Можно получить термическим разложением сульфатов: Fe 2(SO 4)3 → Fe 2 O 3+2 SO 3 t или взаимодействием SO 2 с озоном: SO 2+O 3 → SO 3+O 2 Для окисления SO 2 используют также NO 2: SO 2+NO 2 → SO 3+NO Эта реакция лежит в основе исторически первого, нитрозного способа получения серной кислоты.
 SO 2 химические свойства SO 2 реагирует с: • Водой SO 2+H 2 O=H 2 SO 3 • Основными оксидами SO 2+Na 2 O=Na 2 SO 3 • Амфотерными оксидами SO 2 + Fe 2 O 3=Fe. SO 3 • Co Щелочами SO 2+Na. OH=Na 2 SO 3+H 2 O SO 2+Na. OH=Na. HSO 3+H 2 O SO 2+Pb(NO 3)2+H 2 O=Pb. SO 3+HNO 3 • С растворами солей • с сульфитами образуя кислые соли Na 2 SO 3 +SO 2+H 2 O → 2 Na. HSO 3
SO 2 химические свойства SO 2 реагирует с: • Водой SO 2+H 2 O=H 2 SO 3 • Основными оксидами SO 2+Na 2 O=Na 2 SO 3 • Амфотерными оксидами SO 2 + Fe 2 O 3=Fe. SO 3 • Co Щелочами SO 2+Na. OH=Na 2 SO 3+H 2 O SO 2+Na. OH=Na. HSO 3+H 2 O SO 2+Pb(NO 3)2+H 2 O=Pb. SO 3+HNO 3 • С растворами солей • с сульфитами образуя кислые соли Na 2 SO 3 +SO 2+H 2 O → 2 Na. HSO 3
 Химическая активность SO 2 весьма велика. Наиболее ярко выражены восстановительные свойства SO 2+Br 2+2 H 2 O → H 2 SO 4+HBr SO 2+I 2+2 H 2 O = H 2 SO 4+2 HI 2 SO 2+O 2→ 2 SO 3 t 450 5 SO 2+2 KMn. O 4+H 2 O→ 2 H 2 SO 4+2 Mn. SO 4+K 2 SO 4 качественная реакция на сульфит ион и на. SO 2 (обесцвечивание фиолетового раствора). В присутствии сильных восстановителей SO 2 способен проявлять окислительные свойства SO 2+2 CO→ 2 CO 2+S Или для получения фосфорноватистой кислоты: PH 3+SO 2→H 3 PO 2+S Реакция контрдиспропорционирования с сероводородом 4 SO 2 + 2 H 2 S + 6 Na. OH → 3 Na 2 S 2 O 3 + 5 H 2 O
Химическая активность SO 2 весьма велика. Наиболее ярко выражены восстановительные свойства SO 2+Br 2+2 H 2 O → H 2 SO 4+HBr SO 2+I 2+2 H 2 O = H 2 SO 4+2 HI 2 SO 2+O 2→ 2 SO 3 t 450 5 SO 2+2 KMn. O 4+H 2 O→ 2 H 2 SO 4+2 Mn. SO 4+K 2 SO 4 качественная реакция на сульфит ион и на. SO 2 (обесцвечивание фиолетового раствора). В присутствии сильных восстановителей SO 2 способен проявлять окислительные свойства SO 2+2 CO→ 2 CO 2+S Или для получения фосфорноватистой кислоты: PH 3+SO 2→H 3 PO 2+S Реакция контрдиспропорционирования с сероводородом 4 SO 2 + 2 H 2 S + 6 Na. OH → 3 Na 2 S 2 O 3 + 5 H 2 O
 SO 3 химические свойства Основными оксидами SO 3+Na 2 O = Na 2 SO 4 Амфотерными оксидами Zn. O+SO 3 = Zn. SO 4 Водой SO 2+H 2 O=H 2 SO 4 Основаниями 2 KOH+SO 3→K 2 SO 4+H 2 O KOH+SO 3(изб)→KHSO 4 Взаимодействует с сульфатами образуя Na 2 SO 4 +SO 3+H 2 O → 2 Na. HSO 4 кислые соли SO 3 растворяется в 98% ой H 2 SO 4+SO 3→H 2 S 2 O 7 (олеум) серной кислоте, образуя олеум:
SO 3 химические свойства Основными оксидами SO 3+Na 2 O = Na 2 SO 4 Амфотерными оксидами Zn. O+SO 3 = Zn. SO 4 Водой SO 2+H 2 O=H 2 SO 4 Основаниями 2 KOH+SO 3→K 2 SO 4+H 2 O KOH+SO 3(изб)→KHSO 4 Взаимодействует с сульфатами образуя Na 2 SO 4 +SO 3+H 2 O → 2 Na. HSO 4 кислые соли SO 3 растворяется в 98% ой H 2 SO 4+SO 3→H 2 S 2 O 7 (олеум) серной кислоте, образуя олеум:
 Окислительновосстановительные: SO 3 характеризуется сильными окислительными свойствами, восстанавливается, обычно, до сернистого ангидрида: 5 SO 3+2 P → P 2 O 5+5 SO 2 3 SO 3+H 2 S → 4 SO 2+H 2 O 2 SO 3+2 KI → SO 2+I 2+K 2 SO 4
Окислительновосстановительные: SO 3 характеризуется сильными окислительными свойствами, восстанавливается, обычно, до сернистого ангидрида: 5 SO 3+2 P → P 2 O 5+5 SO 2 3 SO 3+H 2 S → 4 SO 2+H 2 O 2 SO 3+2 KI → SO 2+I 2+K 2 SO 4
 SO 2 применения Для производства серной кислоты В качестве консерванта (пищевая добавка E 220) в вине Так как этот газ убивает микроорганизмы, им окуривают овощехранилища и склады. Для отбеливания соломы, шелка и шерсти(когда невозможно использлвать хлор) В качестве растворителя в лабораториях
SO 2 применения Для производства серной кислоты В качестве консерванта (пищевая добавка E 220) в вине Так как этот газ убивает микроорганизмы, им окуривают овощехранилища и склады. Для отбеливания соломы, шелка и шерсти(когда невозможно использлвать хлор) В качестве растворителя в лабораториях
 SO 3 применения Для получения серной кислоты
SO 3 применения Для получения серной кислоты
 Кислородсодержащие кислоты и соли серы H 2 S 2 O 3 серноватистая (тиосерная) кислота не существует в свободном виде, сильная кислота, по силе похожа на серную H 2 S 2 O 3 = H 2 O+ SO 2+ S разлагается при комнатной температуре H 2 S 2 O 7 олеум, пиросерная кислота, купаросное масло H 2 S 2 O 5 пиросернистая кислота, дисерная кислота соли бисульфит натрия, натрий пиросульфит H 2 SO 3 сернистая неустойчивая кислота H 2 SO 4 серная кислота Cu. SO 4*5 H 2 O медный купорос Fe. SO 4*7 H 2 O железный купорос Сa. SO 4*2 H 2 O гипс
Кислородсодержащие кислоты и соли серы H 2 S 2 O 3 серноватистая (тиосерная) кислота не существует в свободном виде, сильная кислота, по силе похожа на серную H 2 S 2 O 3 = H 2 O+ SO 2+ S разлагается при комнатной температуре H 2 S 2 O 7 олеум, пиросерная кислота, купаросное масло H 2 S 2 O 5 пиросернистая кислота, дисерная кислота соли бисульфит натрия, натрий пиросульфит H 2 SO 3 сернистая неустойчивая кислота H 2 SO 4 серная кислота Cu. SO 4*5 H 2 O медный купорос Fe. SO 4*7 H 2 O железный купорос Сa. SO 4*2 H 2 O гипс
 Сернистая кислота — неустойчивая двухосновная неорганическая кислота средней силы. Химическая формула H 2 SO 3. Раствор сернистой кислоты H 2 SO 3 обладает восстановительными свойствами.
Сернистая кислота — неустойчивая двухосновная неорганическая кислота средней силы. Химическая формула H 2 SO 3. Раствор сернистой кислоты H 2 SO 3 обладает восстановительными свойствами.
 Физические свойства
Физические свойства
 Химические свойства со щелочами образует два ряда солей: кислые — гидросульфиты (в недостатке щёлочи): H 2 SO 3 изб. + КОН ® KHSO 3 + H 2 O и средние — сульфиты (в избытке щёлочи): H 2 SO 3 + 2 Na. OH ® Na 2 SO 3 + 2 H 2 O сернистая кислота и её соли являются сильными восстановителями: H 2 SO 3 + Br 2 + H 2 O ® H 2 SO 3 + 2 HBr при взаимодействии с ещё более сильными восстановителями может играть роль окислителя: H 2 SO 3 +2 H 2 S ® 3 S + 3 H 2 O
Химические свойства со щелочами образует два ряда солей: кислые — гидросульфиты (в недостатке щёлочи): H 2 SO 3 изб. + КОН ® KHSO 3 + H 2 O и средние — сульфиты (в избытке щёлочи): H 2 SO 3 + 2 Na. OH ® Na 2 SO 3 + 2 H 2 O сернистая кислота и её соли являются сильными восстановителями: H 2 SO 3 + Br 2 + H 2 O ® H 2 SO 3 + 2 HBr при взаимодействии с ещё более сильными восстановителями может играть роль окислителя: H 2 SO 3 +2 H 2 S ® 3 S + 3 H 2 O
 сильная двухосновная кислота, отвечающая высшей степени окисления серы (+6).
сильная двухосновная кислота, отвечающая высшей степени окисления серы (+6).
 Физические свойства Тяжелая маслянистая жидкость ("купоросное масло"); хорошо растворима в воде – с сильным нагревом до 98 ; обладает водоотнимающими свойствами (обугливание бумаги, дерева, сахара). концентрированная 98% H 2 SO 4 – сильный окислитель
Физические свойства Тяжелая маслянистая жидкость ("купоросное масло"); хорошо растворима в воде – с сильным нагревом до 98 ; обладает водоотнимающими свойствами (обугливание бумаги, дерева, сахара). концентрированная 98% H 2 SO 4 – сильный окислитель
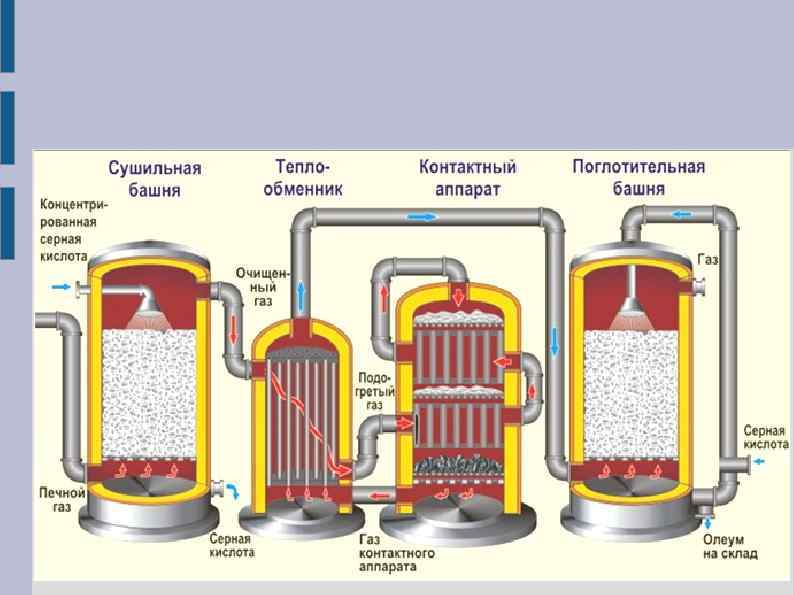
 Получение 1 -я стадия. Обжиг пирита (серного колчедана) 4 Fe. S 2 + 11 O 2 = 2 Fe 2 O 3 + 8 SO 2 + Q Процесс гетерогенный: 800 о. С 1) измельчение железного колчедана (пирита) 2) метод "кипящего слоя" 2 -я стадия. Окисление сернистого газа. После очистки, осушки и теплообмена сернистый газ поступает в контактный аппарат, где окисляется в серный ангидрид (450°С – 500°С; катализатор V 2 O 5): 2 SO 2 + O 2 ⇄ 2 SO 3 + Q 3 -я стадия. Поглощение серного ангидрида. Поглотительная башня: n. SO 3 + H 2 SO 4(конц) = (H 2 SO 4 • n. SO 3)(олеум) Воду использовать нельзя из за образования тумана.
Получение 1 -я стадия. Обжиг пирита (серного колчедана) 4 Fe. S 2 + 11 O 2 = 2 Fe 2 O 3 + 8 SO 2 + Q Процесс гетерогенный: 800 о. С 1) измельчение железного колчедана (пирита) 2) метод "кипящего слоя" 2 -я стадия. Окисление сернистого газа. После очистки, осушки и теплообмена сернистый газ поступает в контактный аппарат, где окисляется в серный ангидрид (450°С – 500°С; катализатор V 2 O 5): 2 SO 2 + O 2 ⇄ 2 SO 3 + Q 3 -я стадия. Поглощение серного ангидрида. Поглотительная башня: n. SO 3 + H 2 SO 4(конц) = (H 2 SO 4 • n. SO 3)(олеум) Воду использовать нельзя из за образования тумана.
 Химические свойства • Индикатор лакмус(красный) метилоранж(красный) фенолфтал. (б/ц) • 1) Диссоциация ступенчатая H 2 SO 4→ H+ + HSO 4 (α =1) HSO 4 ⇄ H+ + SO 42 (α<1) • С основными и амфотерными оксидами Cu. O + H 2 SO 4 = Cu. SO 4 + H 2 O Al 2 O 3 +3 H 2 SO 4 = Al 2(SO 4)3 +3 Н 2 О • С основаниями H 2 SO 4 + 2 Na. OH = Na 2 SO 4 + 2 H 2 O H 2 SO 4 изб. + КОН = KHSO 4 + H 2 O • С солями, если образуется осадок, газ или вода. Са. СО 3 + H 2 SO 4 = Са. SO 4 + CO 2 + H 2 O Ba. Cl 2 + H 2 SO 4 = Ba. SO 4 + 2 HCl качественная реакция на серную кислоту. Образуется белый осадок Ba. SO 4
Химические свойства • Индикатор лакмус(красный) метилоранж(красный) фенолфтал. (б/ц) • 1) Диссоциация ступенчатая H 2 SO 4→ H+ + HSO 4 (α =1) HSO 4 ⇄ H+ + SO 42 (α<1) • С основными и амфотерными оксидами Cu. O + H 2 SO 4 = Cu. SO 4 + H 2 O Al 2 O 3 +3 H 2 SO 4 = Al 2(SO 4)3 +3 Н 2 О • С основаниями H 2 SO 4 + 2 Na. OH = Na 2 SO 4 + 2 H 2 O H 2 SO 4 изб. + КОН = KHSO 4 + H 2 O • С солями, если образуется осадок, газ или вода. Са. СО 3 + H 2 SO 4 = Са. SO 4 + CO 2 + H 2 O Ba. Cl 2 + H 2 SO 4 = Ba. SO 4 + 2 HCl качественная реакция на серную кислоту. Образуется белый осадок Ba. SO 4
 • Взаимодействие с металлами • С щелочными и щелочноземельными металлами 8 Na +5 H 2 SO 4(конц) → 4 Na 2 SO 4 + H 2 S + 4 H 2 O Na + H 2 SO 4(разб) → Na 2 SO 4 + H 2 • С металлами до водорода Zn + H 2 SO 4(разб) → Zn. SO 4 + H 2 O Al + H 2 SO 4(конц) = SO 2 + H 2 O + Al 2(SO 4)3 –t° Al, Fe, Cr + конц. → без нагревания пассивируют, т. е. не идут. • С металлами после водорода Разбавленная серная кислота не реагирует с металлами после водорода. Pt и Au не реагируют с H 2 SO 4(конц). Cu + H 2 SO 4(конц) → Cu. SO 4 + SO 2 + H 2 O
• Взаимодействие с металлами • С щелочными и щелочноземельными металлами 8 Na +5 H 2 SO 4(конц) → 4 Na 2 SO 4 + H 2 S + 4 H 2 O Na + H 2 SO 4(разб) → Na 2 SO 4 + H 2 • С металлами до водорода Zn + H 2 SO 4(разб) → Zn. SO 4 + H 2 O Al + H 2 SO 4(конц) = SO 2 + H 2 O + Al 2(SO 4)3 –t° Al, Fe, Cr + конц. → без нагревания пассивируют, т. е. не идут. • С металлами после водорода Разбавленная серная кислота не реагирует с металлами после водорода. Pt и Au не реагируют с H 2 SO 4(конц). Cu + H 2 SO 4(конц) → Cu. SO 4 + SO 2 + H 2 O
 • С неметаллами P+H 2 SO 4(конц) + H 2 O → SO 2 + H 3 PO 4 С + 2 H 2 SO 4(конц) → CO 2 + 2 SO 2 + 2 H 2 O S + 2 H 2 SO 4(конц) → 3 SO 2 + 2 H 2 O • С солями 8 Na. I + 9 H 2 S 04 (конц) = H 2 S + 4 I 2 + 8 Na. HS 04 + 4 H 20
• С неметаллами P+H 2 SO 4(конц) + H 2 O → SO 2 + H 3 PO 4 С + 2 H 2 SO 4(конц) → CO 2 + 2 SO 2 + 2 H 2 O S + 2 H 2 SO 4(конц) → 3 SO 2 + 2 H 2 O • С солями 8 Na. I + 9 H 2 S 04 (конц) = H 2 S + 4 I 2 + 8 Na. HS 04 + 4 H 20
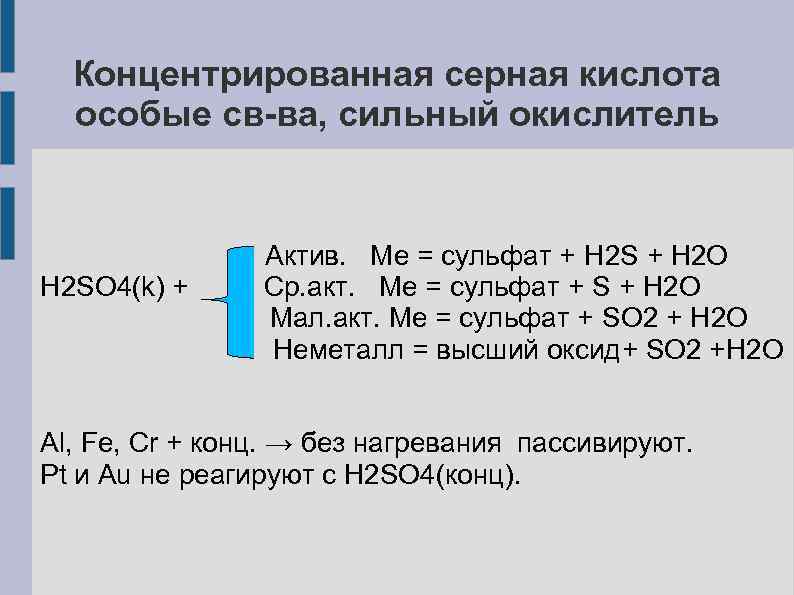 Концентрированная серная кислота особые св-ва, сильный окислитель Актив. Ме = сульфат + H 2 S + H 2 O H 2 SO 4(k) + Ср. акт. Ме = сульфат + S + H 2 O Мал. акт. Ме = сульфат + SO 2 + H 2 O Неметалл = высший оксид+ SO 2 +H 2 O Al, Fe, Cr + конц. → без нагревания пассивируют. Pt и Au не реагируют с H 2 SO 4(конц).
Концентрированная серная кислота особые св-ва, сильный окислитель Актив. Ме = сульфат + H 2 S + H 2 O H 2 SO 4(k) + Ср. акт. Ме = сульфат + S + H 2 O Мал. акт. Ме = сульфат + SO 2 + H 2 O Неметалл = высший оксид+ SO 2 +H 2 O Al, Fe, Cr + конц. → без нагревания пассивируют. Pt и Au не реагируют с H 2 SO 4(конц).
 Применение в производстве минеральных удобрений; как электролит в свинцовых аккумуляторах
Применение в производстве минеральных удобрений; как электролит в свинцовых аккумуляторах
 Оксид серы (I) S 2 O. Оксид серы (I) S 2 O это желтый газ, который может несколько часов сохраняться при комнатной температуре (в чистом и сухом сосуде) лишь под давлением не выше 40 мм. рт. ст. Молекула SO 2 полярна. Сильное охлаждение переводит закись серы в оранжево красное твердое вещество. Молекулярным кислородом при обычной температуре не окисляется, а водой легко разлагается. Более или менее легко реагирует с большинством металлов. Получают при взаимодействии SO 2 с серой.
Оксид серы (I) S 2 O. Оксид серы (I) S 2 O это желтый газ, который может несколько часов сохраняться при комнатной температуре (в чистом и сухом сосуде) лишь под давлением не выше 40 мм. рт. ст. Молекула SO 2 полярна. Сильное охлаждение переводит закись серы в оранжево красное твердое вещество. Молекулярным кислородом при обычной температуре не окисляется, а водой легко разлагается. Более или менее легко реагирует с большинством металлов. Получают при взаимодействии SO 2 с серой.


