804b112dfb3769547a17737d66fec019.ppt
- Количество слайдов: 56
 ANTIVIRAIS DE AÇÃO DIRETA PARA HEPATITE C DAAS Cláudia Ivantes, MD, Ph. D COA – Prefeitura Municipal de Curitiba Serviço de Gastroenterologia, Hepatologia e Transplante Hepáico do HNSG
ANTIVIRAIS DE AÇÃO DIRETA PARA HEPATITE C DAAS Cláudia Ivantes, MD, Ph. D COA – Prefeitura Municipal de Curitiba Serviço de Gastroenterologia, Hepatologia e Transplante Hepáico do HNSG
 AGENDA: Evolução do tratamento Alvos virais específicos Telaprevir e Boceprevir Simeprevir Sofosbuvir Daclatasvir 3 D PCDT
AGENDA: Evolução do tratamento Alvos virais específicos Telaprevir e Boceprevir Simeprevir Sofosbuvir Daclatasvir 3 D PCDT
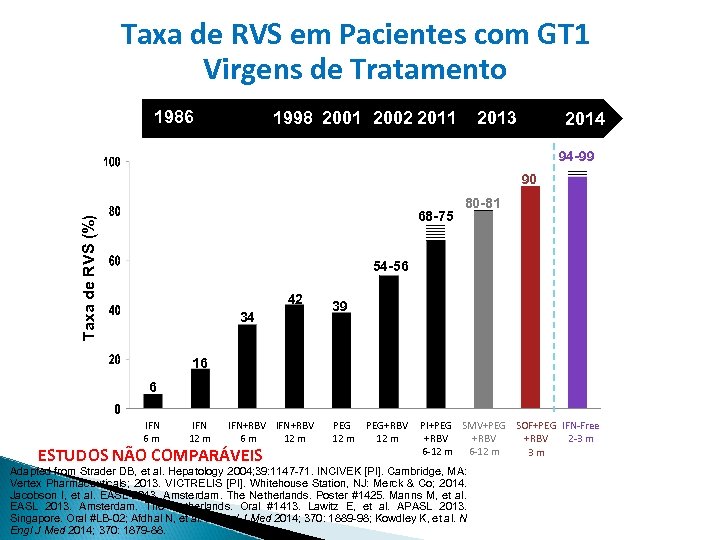 Taxa de RVS em Pacientes com GT 1 Virgens de Tratamento 1986 1998 2001 2002 2011 2013 2014 94 -99 90 Taxa de RVS (%) 68 -75 80 -81 54 -56 42 34 39 16 6 IFN 6 m IFN 12 m IFN+RBV 6 m 12 m ESTUDOS NÃO COMPARÁVEIS PEG 12 m PEG+RBV 12 m PI+PEG SMV+PEG SOF+PEG IFN-Free +RBV 2 -3 m +RBV 6 -12 m 3 m Adapted from Strader DB, et al. Hepatology 2004; 39: 1147 -71. INCIVEK [PI]. Cambridge, MA: Vertex Pharmaceuticals; 2013. VICTRELIS [PI]. Whitehouse Station, NJ: Merck & Co; 2014. Jacobson I, et al. EASL 2013. Amsterdam. The Netherlands. Poster #1425. Manns M, et al. EASL 2013. Amsterdam. The Netherlands. Oral #1413. Lawitz E, et al. APASL 2013. Singapore. Oral #LB-02; Afdhal N, et al. N Engl J Med 2014; 370: 1889 -98; Kowdley K, et al. N Engl J Med 2014; 370: 1879 -88.
Taxa de RVS em Pacientes com GT 1 Virgens de Tratamento 1986 1998 2001 2002 2011 2013 2014 94 -99 90 Taxa de RVS (%) 68 -75 80 -81 54 -56 42 34 39 16 6 IFN 6 m IFN 12 m IFN+RBV 6 m 12 m ESTUDOS NÃO COMPARÁVEIS PEG 12 m PEG+RBV 12 m PI+PEG SMV+PEG SOF+PEG IFN-Free +RBV 2 -3 m +RBV 6 -12 m 3 m Adapted from Strader DB, et al. Hepatology 2004; 39: 1147 -71. INCIVEK [PI]. Cambridge, MA: Vertex Pharmaceuticals; 2013. VICTRELIS [PI]. Whitehouse Station, NJ: Merck & Co; 2014. Jacobson I, et al. EASL 2013. Amsterdam. The Netherlands. Poster #1425. Manns M, et al. EASL 2013. Amsterdam. The Netherlands. Oral #1413. Lawitz E, et al. APASL 2013. Singapore. Oral #LB-02; Afdhal N, et al. N Engl J Med 2014; 370: 1889 -98; Kowdley K, et al. N Engl J Med 2014; 370: 1879 -88.
 Visão global do tratamento do HCV 1 a onda: Boceprevir + PEG/RBV Telaprevir + PEG/RBV Três ondas 2 a onda: Sofosbuvir + PEG/RBV Simeprevir + PEG/RBV --------------Sofosbuvir + Simeprevir Sofosbuvir + Daclatasvir 3 a onda: 3 D Com PEG RVS: 66 a 75% Com PEG RVS: 80 a 89% Sem PEG RVS: 85 a 95% Sem PEG RVS: 95 a 100%
Visão global do tratamento do HCV 1 a onda: Boceprevir + PEG/RBV Telaprevir + PEG/RBV Três ondas 2 a onda: Sofosbuvir + PEG/RBV Simeprevir + PEG/RBV --------------Sofosbuvir + Simeprevir Sofosbuvir + Daclatasvir 3 a onda: 3 D Com PEG RVS: 66 a 75% Com PEG RVS: 80 a 89% Sem PEG RVS: 85 a 95% Sem PEG RVS: 95 a 100%
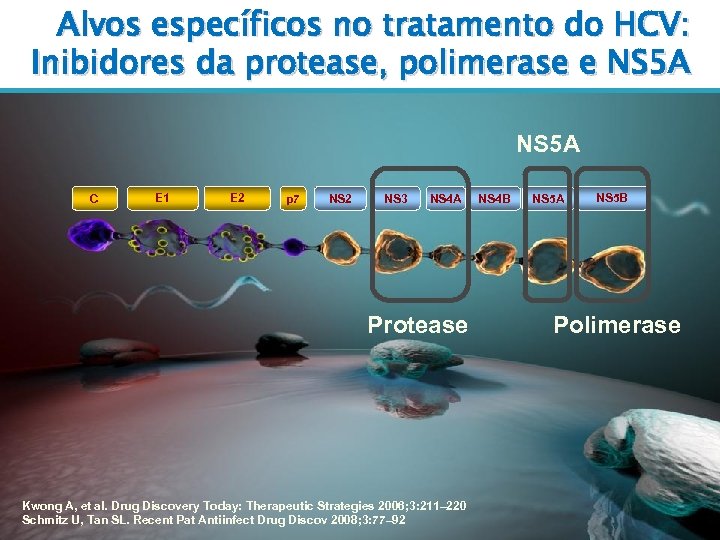 Alvos específicos no tratamento do HCV: Inibidores da protease, polimerase e NS 5 A C E 1 E 2 p 7 NS 2 NS 3 NS 4 A Protease Kwong A, et al. Drug Discovery Today: Therapeutic Strategies 2006; 3: 211– 220 Schmitz U, Tan SL. Recent Pat Antiinfect Drug Discov 2008; 3: 77– 92 NS 4 B NS 5 A NS 5 B Polimerase
Alvos específicos no tratamento do HCV: Inibidores da protease, polimerase e NS 5 A C E 1 E 2 p 7 NS 2 NS 3 NS 4 A Protease Kwong A, et al. Drug Discovery Today: Therapeutic Strategies 2006; 3: 211– 220 Schmitz U, Tan SL. Recent Pat Antiinfect Drug Discov 2008; 3: 77– 92 NS 4 B NS 5 A NS 5 B Polimerase
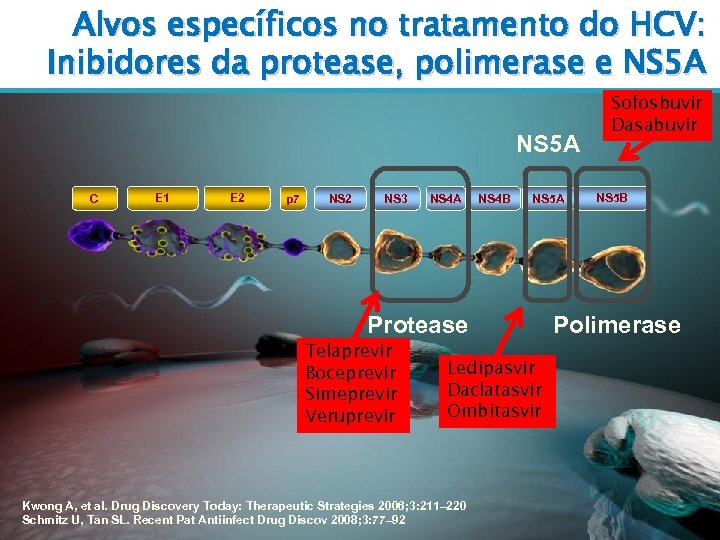 Alvos específicos no tratamento do HCV: Inibidores da protease, polimerase e NS 5 A C E 1 E 2 p 7 NS 2 NS 3 NS 4 A NS 4 B NS 5 A Protease Telaprevir Boceprevir Simeprevir Veruprevir Ledipasvir Daclatasvir Ombitasvir Kwong A, et al. Drug Discovery Today: Therapeutic Strategies 2006; 3: 211– 220 Schmitz U, Tan SL. Recent Pat Antiinfect Drug Discov 2008; 3: 77– 92 Sofosbuvir Dasabuvir NS 5 B Polimerase
Alvos específicos no tratamento do HCV: Inibidores da protease, polimerase e NS 5 A C E 1 E 2 p 7 NS 2 NS 3 NS 4 A NS 4 B NS 5 A Protease Telaprevir Boceprevir Simeprevir Veruprevir Ledipasvir Daclatasvir Ombitasvir Kwong A, et al. Drug Discovery Today: Therapeutic Strategies 2006; 3: 211– 220 Schmitz U, Tan SL. Recent Pat Antiinfect Drug Discov 2008; 3: 77– 92 Sofosbuvir Dasabuvir NS 5 B Polimerase
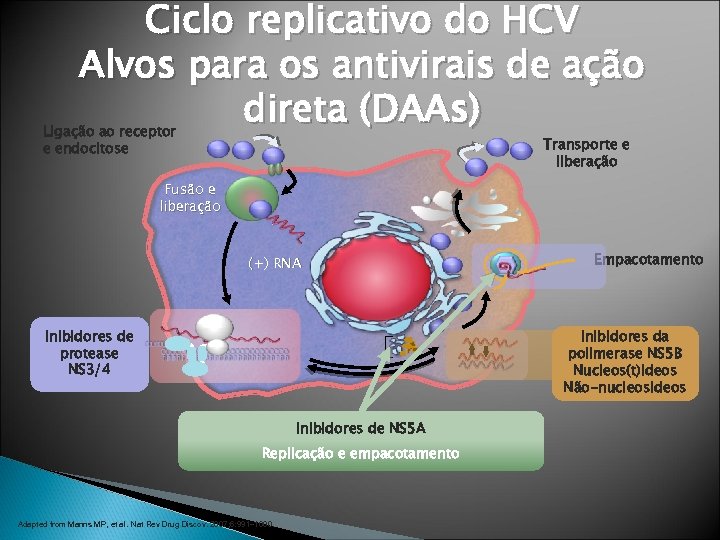 Ciclo replicativo do HCV Alvos para os antivirais de ação direta (DAAs) Ligação ao receptor e endocitose Transporte e liberação Fusão e liberação (+) RNA Tradução e Inibidores de processamento protease da poliproteína NS 3/4 Empacotamento Inibidores da Replicação do polimerase NS 5 B RNA Nucleos(t)ideos Não-nucleosideos Inibidores de NS 5 A Replicação e empacotamento Adapted from Manns MP, et al. Nat Rev Drug Discov. 2007; 6: 991– 1000.
Ciclo replicativo do HCV Alvos para os antivirais de ação direta (DAAs) Ligação ao receptor e endocitose Transporte e liberação Fusão e liberação (+) RNA Tradução e Inibidores de processamento protease da poliproteína NS 3/4 Empacotamento Inibidores da Replicação do polimerase NS 5 B RNA Nucleos(t)ideos Não-nucleosideos Inibidores de NS 5 A Replicação e empacotamento Adapted from Manns MP, et al. Nat Rev Drug Discov. 2007; 6: 991– 1000.
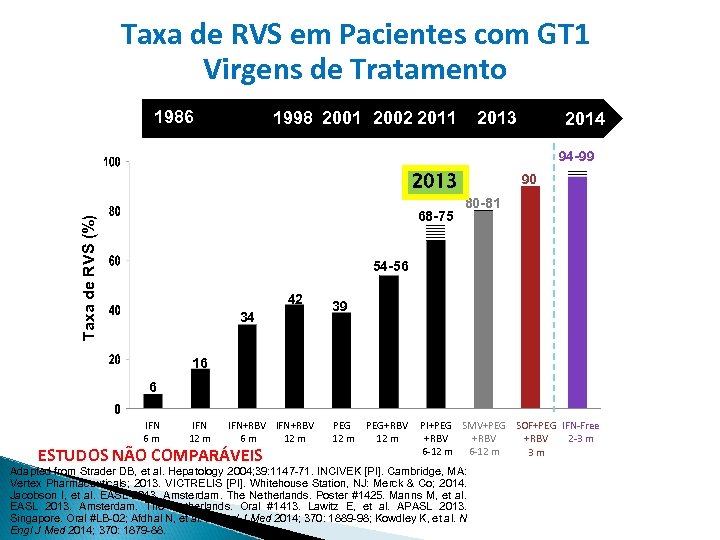 Taxa de RVS em Pacientes com GT 1 Virgens de Tratamento 1986 1998 2001 2002 2011 2013 2014 94 -99 2013 Taxa de RVS (%) 68 -75 90 80 -81 54 -56 42 34 39 16 6 IFN 6 m IFN 12 m IFN+RBV 6 m 12 m ESTUDOS NÃO COMPARÁVEIS PEG 12 m PEG+RBV 12 m PI+PEG SMV+PEG SOF+PEG IFN-Free +RBV 2 -3 m +RBV 6 -12 m 3 m Adapted from Strader DB, et al. Hepatology 2004; 39: 1147 -71. INCIVEK [PI]. Cambridge, MA: Vertex Pharmaceuticals; 2013. VICTRELIS [PI]. Whitehouse Station, NJ: Merck & Co; 2014. Jacobson I, et al. EASL 2013. Amsterdam. The Netherlands. Poster #1425. Manns M, et al. EASL 2013. Amsterdam. The Netherlands. Oral #1413. Lawitz E, et al. APASL 2013. Singapore. Oral #LB-02; Afdhal N, et al. N Engl J Med 2014; 370: 1889 -98; Kowdley K, et al. N Engl J Med 2014; 370: 1879 -88.
Taxa de RVS em Pacientes com GT 1 Virgens de Tratamento 1986 1998 2001 2002 2011 2013 2014 94 -99 2013 Taxa de RVS (%) 68 -75 90 80 -81 54 -56 42 34 39 16 6 IFN 6 m IFN 12 m IFN+RBV 6 m 12 m ESTUDOS NÃO COMPARÁVEIS PEG 12 m PEG+RBV 12 m PI+PEG SMV+PEG SOF+PEG IFN-Free +RBV 2 -3 m +RBV 6 -12 m 3 m Adapted from Strader DB, et al. Hepatology 2004; 39: 1147 -71. INCIVEK [PI]. Cambridge, MA: Vertex Pharmaceuticals; 2013. VICTRELIS [PI]. Whitehouse Station, NJ: Merck & Co; 2014. Jacobson I, et al. EASL 2013. Amsterdam. The Netherlands. Poster #1425. Manns M, et al. EASL 2013. Amsterdam. The Netherlands. Oral #1413. Lawitz E, et al. APASL 2013. Singapore. Oral #LB-02; Afdhal N, et al. N Engl J Med 2014; 370: 1889 -98; Kowdley K, et al. N Engl J Med 2014; 370: 1879 -88.
 Resultado da terapia tripla em Curitiba: COA N=80 (resultados 63) ◦ Serviço público→ 36 ◦ Serviço privado → 44 17 médicos prescritores 80, 95% TVR 19, 04% BOC 36% resposta nula anterior 44, 44% genotipo 1 a RVS ◦ ITT 46, 03% ◦ PP 50, 00% Causas de interrupção: ◦ Virológica em 13 indivíduos ◦ Evento adverso 16 pacientes
Resultado da terapia tripla em Curitiba: COA N=80 (resultados 63) ◦ Serviço público→ 36 ◦ Serviço privado → 44 17 médicos prescritores 80, 95% TVR 19, 04% BOC 36% resposta nula anterior 44, 44% genotipo 1 a RVS ◦ ITT 46, 03% ◦ PP 50, 00% Causas de interrupção: ◦ Virológica em 13 indivíduos ◦ Evento adverso 16 pacientes
 Visão global do tratamento do HCV 1 a onda: Boceprevir + PEG/RBV Telaprevir + PEG/RBV Três ondas 2 a onda: Sofosbuvir + PEG/RBV Simeprevir + PEG/RBV --------------Sofosbuvir + Simeprevir Sofosbuvir + Daclatasvir 3 a onda: 3 D Com PEG RVS: 66 a 75% Com PEG RVS: 80 a 89% Sem PEG RVS: 85 a 95% Sem PEG RVS: 95 a 100%
Visão global do tratamento do HCV 1 a onda: Boceprevir + PEG/RBV Telaprevir + PEG/RBV Três ondas 2 a onda: Sofosbuvir + PEG/RBV Simeprevir + PEG/RBV --------------Sofosbuvir + Simeprevir Sofosbuvir + Daclatasvir 3 a onda: 3 D Com PEG RVS: 66 a 75% Com PEG RVS: 80 a 89% Sem PEG RVS: 85 a 95% Sem PEG RVS: 95 a 100%
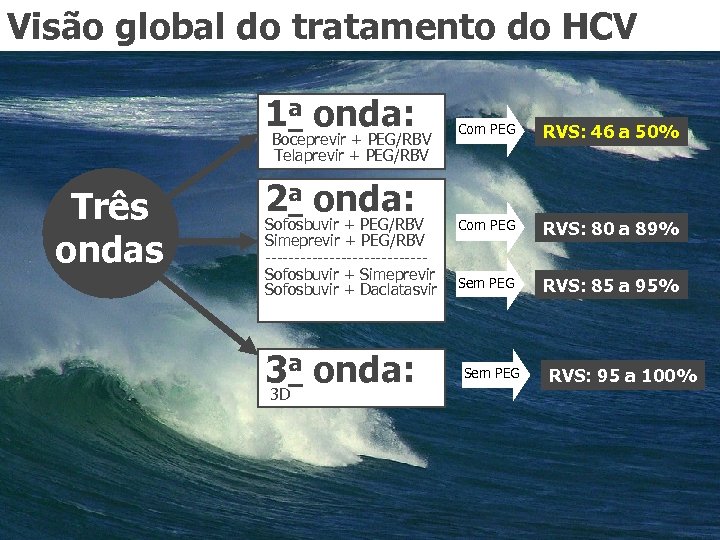 Visão global do tratamento do HCV 1 a onda: Boceprevir + PEG/RBV Telaprevir + PEG/RBV Três ondas 2 a onda: Sofosbuvir + PEG/RBV Simeprevir + PEG/RBV --------------Sofosbuvir + Simeprevir Sofosbuvir + Daclatasvir 3 a onda: 3 D Com PEG RVS: 46 a 50% Com PEG RVS: 80 a 89% Sem PEG RVS: 85 a 95% Sem PEG RVS: 95 a 100%
Visão global do tratamento do HCV 1 a onda: Boceprevir + PEG/RBV Telaprevir + PEG/RBV Três ondas 2 a onda: Sofosbuvir + PEG/RBV Simeprevir + PEG/RBV --------------Sofosbuvir + Simeprevir Sofosbuvir + Daclatasvir 3 a onda: 3 D Com PEG RVS: 46 a 50% Com PEG RVS: 80 a 89% Sem PEG RVS: 85 a 95% Sem PEG RVS: 95 a 100%
 Visão global do tratamento do HCV 1 a onda: Boceprevir + PEG/RBV Telaprevir + PEG/RBV Três ondas 2 a onda: Sofosbuvir + PEG/RBV Simeprevir + PEG/RBV --------------Sofosbuvir + Simeprevir Sofosbuvir + Daclatasvir 3 a onda: 3 D Com PEG RVS: 46 a 50% Com PEG RVS: 80 a 89% Sem PEG RVS: 85 a 95% Sem PEG RVS: 95 a 100%
Visão global do tratamento do HCV 1 a onda: Boceprevir + PEG/RBV Telaprevir + PEG/RBV Três ondas 2 a onda: Sofosbuvir + PEG/RBV Simeprevir + PEG/RBV --------------Sofosbuvir + Simeprevir Sofosbuvir + Daclatasvir 3 a onda: 3 D Com PEG RVS: 46 a 50% Com PEG RVS: 80 a 89% Sem PEG RVS: 85 a 95% Sem PEG RVS: 95 a 100%
 Visão global do tratamento do HCV 1 a onda: Boceprevir + PEG/RBV Telaprevir + PEG/RBV Três ondas 2 a onda: Sofosbuvir + PEG/RBV Simeprevir + PEG/RBV --------------Sofosbuvir + Simeprevir Sofosbuvir + Daclatasvir 3 a onda: 3 D Com PEG RVS: 46 a 50% Com PEG RVS: 80 a 89% Sem PEG RVS: 85 a 95% Sem PEG RVS: 95 a 100%
Visão global do tratamento do HCV 1 a onda: Boceprevir + PEG/RBV Telaprevir + PEG/RBV Três ondas 2 a onda: Sofosbuvir + PEG/RBV Simeprevir + PEG/RBV --------------Sofosbuvir + Simeprevir Sofosbuvir + Daclatasvir 3 a onda: 3 D Com PEG RVS: 46 a 50% Com PEG RVS: 80 a 89% Sem PEG RVS: 85 a 95% Sem PEG RVS: 95 a 100%
 Alvos específicos no tratamento do HCV: Inibidores da protease, polimerase e NS 5 A C E 1 E 2 p 7 NS 2 NS 3 NS 4 A NS 4 B NS 5 A Protease Telaprevir Boceprevir Simeprevir Veruprevir Ledipasvir Daclatasvir Ombitasvir Kwong A, et al. Drug Discovery Today: Therapeutic Strategies 2006; 3: 211– 220 Schmitz U, Tan SL. Recent Pat Antiinfect Drug Discov 2008; 3: 77– 92 Sofosbuvir Dasabuvir NS 5 B Polimerase
Alvos específicos no tratamento do HCV: Inibidores da protease, polimerase e NS 5 A C E 1 E 2 p 7 NS 2 NS 3 NS 4 A NS 4 B NS 5 A Protease Telaprevir Boceprevir Simeprevir Veruprevir Ledipasvir Daclatasvir Ombitasvir Kwong A, et al. Drug Discovery Today: Therapeutic Strategies 2006; 3: 211– 220 Schmitz U, Tan SL. Recent Pat Antiinfect Drug Discov 2008; 3: 77– 92 Sofosbuvir Dasabuvir NS 5 B Polimerase
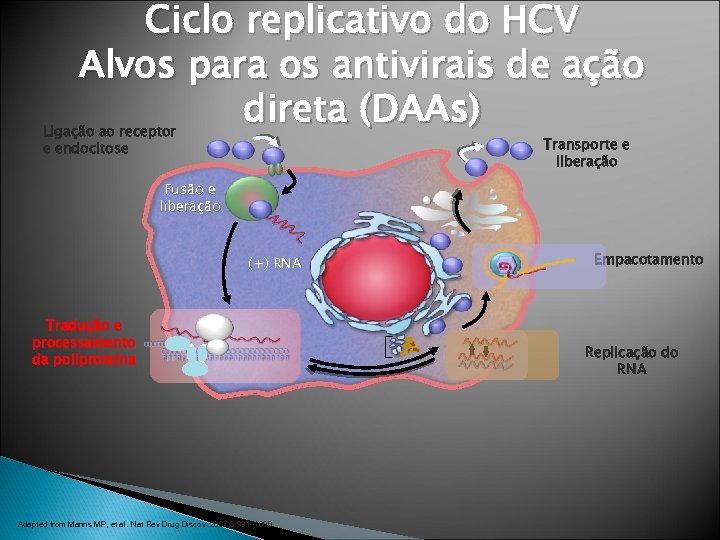 Ciclo replicativo do HCV Alvos para os antivirais de ação direta (DAAs) Ligação ao receptor e endocitose Transporte e liberação Fusão e liberação (+) RNA Tradução e processamento da poliproteína Adapted from Manns MP, et al. Nat Rev Drug Discov. 2007; 6: 991– 1000. Empacotamento Replicação do RNA
Ciclo replicativo do HCV Alvos para os antivirais de ação direta (DAAs) Ligação ao receptor e endocitose Transporte e liberação Fusão e liberação (+) RNA Tradução e processamento da poliproteína Adapted from Manns MP, et al. Nat Rev Drug Discov. 2007; 6: 991– 1000. Empacotamento Replicação do RNA
 SIMEPREVIR Olysio™ Janssen Cápsulas de 150 mg Frascos com 28 cápsulas Genótipos 1 a e 1 b Orientações aos pacientes ◦ Sensibilidade à luz solar ◦ Uso de métodos contraceptivos eficazes durante o tratamento ◦ Armazenar em temperatura ambiente protegido da luz ◦ Ingerir com algum alimento
SIMEPREVIR Olysio™ Janssen Cápsulas de 150 mg Frascos com 28 cápsulas Genótipos 1 a e 1 b Orientações aos pacientes ◦ Sensibilidade à luz solar ◦ Uso de métodos contraceptivos eficazes durante o tratamento ◦ Armazenar em temperatura ambiente protegido da luz ◦ Ingerir com algum alimento
 Interações medicamentosas: Digoxina Amiodarona Claritromicina, eritromicina Varfarina Carbamazepina, fenobarbital, fenitoína, oxcarbazepina Itraconazol, fluconazol, cetoconazol Rifampicina Anlodipina, nifedipina, verapamil Dexametasona Atorvastatina, rosuvastatina, sinvastatina Midazolan Sildenafil
Interações medicamentosas: Digoxina Amiodarona Claritromicina, eritromicina Varfarina Carbamazepina, fenobarbital, fenitoína, oxcarbazepina Itraconazol, fluconazol, cetoconazol Rifampicina Anlodipina, nifedipina, verapamil Dexametasona Atorvastatina, rosuvastatina, sinvastatina Midazolan Sildenafil
 Interações medicamentosas: Tratamento da infecção pelo HIV: ◦ atazanavir, darunavir, delavirdina, efavirenz, etravirina, fosamprenavir, indinavir, lopinavir, nelfinavir, nevirapina, ritonavir, saquinavir ou tipranavir Imunossupressores: ◦ Sirolimus, tacrolimus e ciclosporina
Interações medicamentosas: Tratamento da infecção pelo HIV: ◦ atazanavir, darunavir, delavirdina, efavirenz, etravirina, fosamprenavir, indinavir, lopinavir, nelfinavir, nevirapina, ritonavir, saquinavir ou tipranavir Imunossupressores: ◦ Sirolimus, tacrolimus e ciclosporina
 Falha na tomada: Se tiver passado de 12 horas do horário da tomada, não tome a dose esquecida e tome no horário habitual programado Se não tiver passado de 12 horas, tome imediatamente com alimento e continue a tomar no horário habitual programado
Falha na tomada: Se tiver passado de 12 horas do horário da tomada, não tome a dose esquecida e tome no horário habitual programado Se não tiver passado de 12 horas, tome imediatamente com alimento e continue a tomar no horário habitual programado
 Eventos adversos Reação muito comum (ocorre em mais de 10% dos pacientes que utilizam este medicamento): ◦ prurido ◦ erupção na pele Reação comum (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento): ◦ aumento dos níveis de bilirrubina ◦ fotossensibilidade ◦ constipação
Eventos adversos Reação muito comum (ocorre em mais de 10% dos pacientes que utilizam este medicamento): ◦ prurido ◦ erupção na pele Reação comum (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento): ◦ aumento dos níveis de bilirrubina ◦ fotossensibilidade ◦ constipação
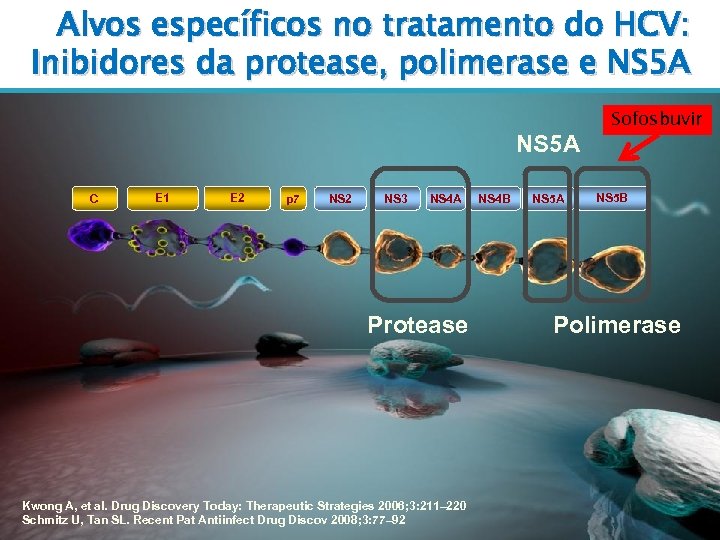 Alvos específicos no tratamento do HCV: Inibidores da protease, polimerase e NS 5 A C E 1 E 2 p 7 NS 2 NS 3 NS 4 A Protease Kwong A, et al. Drug Discovery Today: Therapeutic Strategies 2006; 3: 211– 220 Schmitz U, Tan SL. Recent Pat Antiinfect Drug Discov 2008; 3: 77– 92 NS 4 B NS 5 A Sofosbuvir NS 5 B Polimerase
Alvos específicos no tratamento do HCV: Inibidores da protease, polimerase e NS 5 A C E 1 E 2 p 7 NS 2 NS 3 NS 4 A Protease Kwong A, et al. Drug Discovery Today: Therapeutic Strategies 2006; 3: 211– 220 Schmitz U, Tan SL. Recent Pat Antiinfect Drug Discov 2008; 3: 77– 92 NS 4 B NS 5 A Sofosbuvir NS 5 B Polimerase
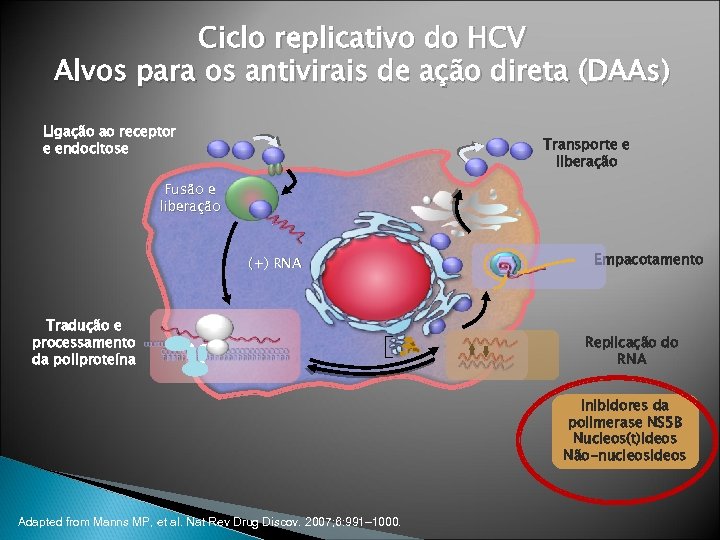 Ciclo replicativo do HCV Alvos para os antivirais de ação direta (DAAs) Ligação ao receptor e endocitose Transporte e liberação Fusão e liberação (+) RNA Tradução e processamento da poliproteína Empacotamento Replicação do RNA Inibidores da polimerase NS 5 B Nucleos(t)ideos Não-nucleosideos Adapted from Manns MP, et al. Nat Rev Drug Discov. 2007; 6: 991– 1000.
Ciclo replicativo do HCV Alvos para os antivirais de ação direta (DAAs) Ligação ao receptor e endocitose Transporte e liberação Fusão e liberação (+) RNA Tradução e processamento da poliproteína Empacotamento Replicação do RNA Inibidores da polimerase NS 5 B Nucleos(t)ideos Não-nucleosideos Adapted from Manns MP, et al. Nat Rev Drug Discov. 2007; 6: 991– 1000.
 SOFOSBUVIR Sovaldi™ Gilead Comprimidos de 400 mg Frascos com 28 comprimidos Pangenotípico Alta barreira genética Orientações aos pacientes ◦ Armazenar em temperatura ambiente ◦ Ingerir com ou sem alimento
SOFOSBUVIR Sovaldi™ Gilead Comprimidos de 400 mg Frascos com 28 comprimidos Pangenotípico Alta barreira genética Orientações aos pacientes ◦ Armazenar em temperatura ambiente ◦ Ingerir com ou sem alimento
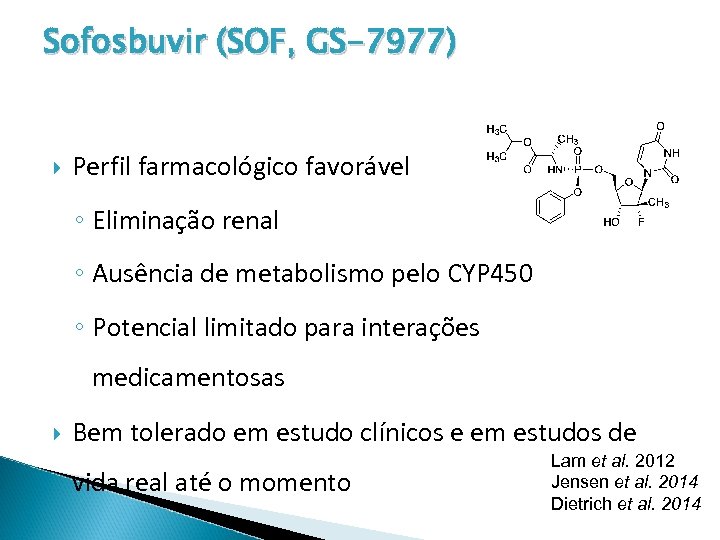 Sofosbuvir (SOF, GS-7977) Perfil farmacológico favorável ◦ Eliminação renal ◦ Ausência de metabolismo pelo CYP 450 ◦ Potencial limitado para interações medicamentosas Bem tolerado em estudo clínicos e em estudos de vida real até o momento Lam et al. 2012 Jensen et al. 2014 Dietrich et al. 2014
Sofosbuvir (SOF, GS-7977) Perfil farmacológico favorável ◦ Eliminação renal ◦ Ausência de metabolismo pelo CYP 450 ◦ Potencial limitado para interações medicamentosas Bem tolerado em estudo clínicos e em estudos de vida real até o momento Lam et al. 2012 Jensen et al. 2014 Dietrich et al. 2014
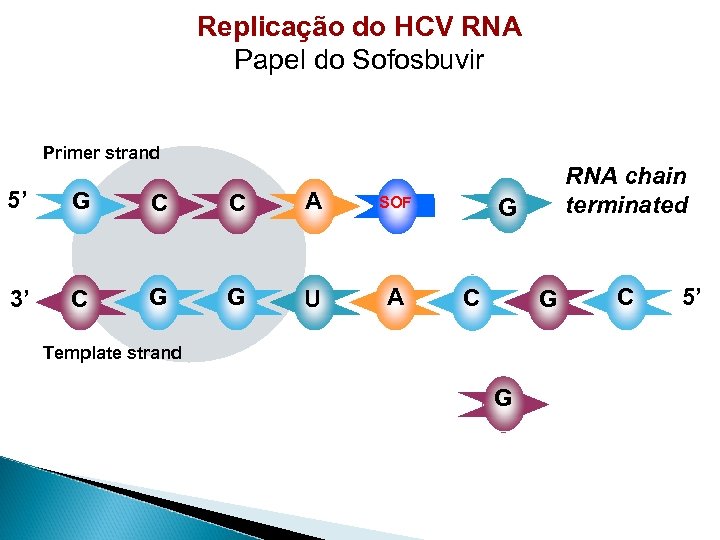 Replicação do HCV RNA Papel do Sofosbuvir Primer strand 5’ G C C A SOF 3’ C G G U A RNA chain terminated G C G Template strand G C 5’
Replicação do HCV RNA Papel do Sofosbuvir Primer strand 5’ G C C A SOF 3’ C G G U A RNA chain terminated G C G Template strand G C 5’
 Interações medicamentosas: Amiodarona Carbamazepina, fenobarbital, fenitoína, oxcarbazepina Rifampicina, rifabutina, rifapentina Erva-de-São João
Interações medicamentosas: Amiodarona Carbamazepina, fenobarbital, fenitoína, oxcarbazepina Rifampicina, rifabutina, rifapentina Erva-de-São João
 Interações medicamentosas: Tratamento da infecção pelo HIV: ◦ Tipranavir/ritonavir Imunossupressores: ◦ NÃO é necessário fazer ajuste de doses com tacrolimos e ciclosporina
Interações medicamentosas: Tratamento da infecção pelo HIV: ◦ Tipranavir/ritonavir Imunossupressores: ◦ NÃO é necessário fazer ajuste de doses com tacrolimos e ciclosporina
 Falha na tomada: Se tiver passado de 12 horas do horário da tomada, não tome a dose esquecida e tome no horário habitual programado Se não tiver passado de 12 horas, tome imediatamente e continue a tomar no horário habitual programado
Falha na tomada: Se tiver passado de 12 horas do horário da tomada, não tome a dose esquecida e tome no horário habitual programado Se não tiver passado de 12 horas, tome imediatamente e continue a tomar no horário habitual programado
 Eventos adversos: Reação muito comum (ocorre em mais de 10% dos pacientes que utilizam este medicamento): ◦ ◦ ◦ fadiga cefaléia náusea insônia prurido Reação comum (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento): ◦ ◦ ◦ Anemia Astenia Erupção cutânea Redução do apetite Diarréia
Eventos adversos: Reação muito comum (ocorre em mais de 10% dos pacientes que utilizam este medicamento): ◦ ◦ ◦ fadiga cefaléia náusea insônia prurido Reação comum (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento): ◦ ◦ ◦ Anemia Astenia Erupção cutânea Redução do apetite Diarréia
 Alvos específicos no tratamento do HCV: Inibidores da protease, polimerase e NS 5 A C E 1 E 2 p 7 NS 2 NS 3 NS 4 A NS 4 B NS 5 A Protease Telaprevir Boceprevir Simeprevir Veruprevir Ledipasvir Daclatasvir Ombitasvir Kwong A, et al. Drug Discovery Today: Therapeutic Strategies 2006; 3: 211– 220 Schmitz U, Tan SL. Recent Pat Antiinfect Drug Discov 2008; 3: 77– 92 Sofosbuvir Dasabuvir NS 5 B Polimerase
Alvos específicos no tratamento do HCV: Inibidores da protease, polimerase e NS 5 A C E 1 E 2 p 7 NS 2 NS 3 NS 4 A NS 4 B NS 5 A Protease Telaprevir Boceprevir Simeprevir Veruprevir Ledipasvir Daclatasvir Ombitasvir Kwong A, et al. Drug Discovery Today: Therapeutic Strategies 2006; 3: 211– 220 Schmitz U, Tan SL. Recent Pat Antiinfect Drug Discov 2008; 3: 77– 92 Sofosbuvir Dasabuvir NS 5 B Polimerase
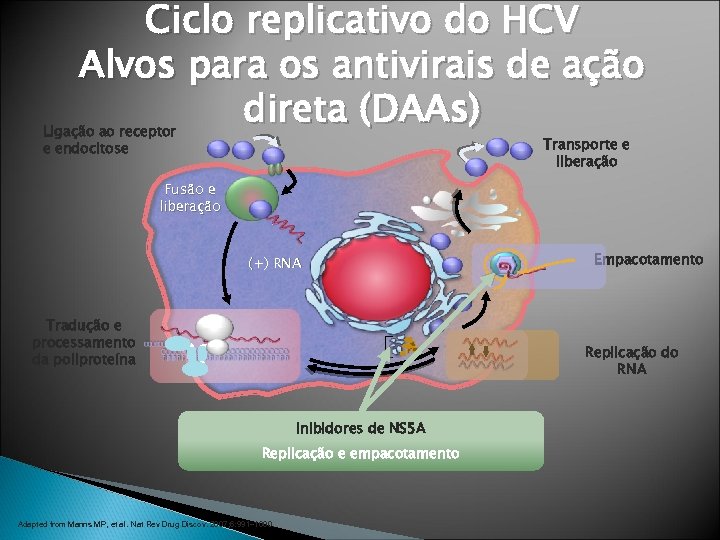 Ciclo replicativo do HCV Alvos para os antivirais de ação direta (DAAs) Ligação ao receptor e endocitose Transporte e liberação Fusão e liberação (+) RNA Tradução e processamento da poliproteína Empacotamento Replicação do RNA Inibidores de NS 5 A Replicação e empacotamento Adapted from Manns MP, et al. Nat Rev Drug Discov. 2007; 6: 991– 1000.
Ciclo replicativo do HCV Alvos para os antivirais de ação direta (DAAs) Ligação ao receptor e endocitose Transporte e liberação Fusão e liberação (+) RNA Tradução e processamento da poliproteína Empacotamento Replicação do RNA Inibidores de NS 5 A Replicação e empacotamento Adapted from Manns MP, et al. Nat Rev Drug Discov. 2007; 6: 991– 1000.
 DACLATASVIR Daklinza™ Bristol Comprimidos de 60 mg Caixas com 28 comprimidos Pangenotípico Orientações aos pacientes ◦ Uso de métodos contraceptivos eficazes durante o tratamento ◦ Armazenar em temperatura ambiente ◦ Ingerir com ou sem alimento
DACLATASVIR Daklinza™ Bristol Comprimidos de 60 mg Caixas com 28 comprimidos Pangenotípico Orientações aos pacientes ◦ Uso de métodos contraceptivos eficazes durante o tratamento ◦ Armazenar em temperatura ambiente ◦ Ingerir com ou sem alimento
 Interações medicamentosas: Carbamazepina, fenobarbital, fenitoína, oxcarbazepina Rifampicina, rifabutina, rifapentina Dexametasona sistêmica Erva-de-São João
Interações medicamentosas: Carbamazepina, fenobarbital, fenitoína, oxcarbazepina Rifampicina, rifabutina, rifapentina Dexametasona sistêmica Erva-de-São João
 Interações medicamentosas: Potencial interação no tratamento da infecção pelo HIV: ◦ Lopinavir, indinavir, fosamprenavir, saquinavir, tipranavir, etravirine, darunavir, delavirdine, nevirapine Interação no tratamento da infecção pelo HIV: ◦ Atazanavir (↓ DAC para 30 mg/dia) ◦ Efavirenz (↑ DAC para 90 mg/dia)
Interações medicamentosas: Potencial interação no tratamento da infecção pelo HIV: ◦ Lopinavir, indinavir, fosamprenavir, saquinavir, tipranavir, etravirine, darunavir, delavirdine, nevirapine Interação no tratamento da infecção pelo HIV: ◦ Atazanavir (↓ DAC para 30 mg/dia) ◦ Efavirenz (↑ DAC para 90 mg/dia)
 Falha na tomada: Se tiver passado de 20 horas do horário da tomada, não tome a dose esquecida e tome no horário habitual programado Se não tiver passado de 20 horas, tome imediatamente e continue a tomar no horário habitual programado
Falha na tomada: Se tiver passado de 20 horas do horário da tomada, não tome a dose esquecida e tome no horário habitual programado Se não tiver passado de 20 horas, tome imediatamente e continue a tomar no horário habitual programado
 Eventos adversos: Reação muito comum (ocorre em mais de 10% dos pacientes que utilizam este medicamento): ◦ fadiga ◦ cefaléia ◦ náusea Reação comum (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento): ◦ ◦ ◦ ◦ ◦ Anemia Redução do apetite Rubor quente Depressão, ansiedade, insônia Tontura, enxaqueca Tosse, dispneia, congestão nasal Diarréia, dor abdominal, boca seca, vômitos Prurido Artralgia, mialgia Irritabilidade
Eventos adversos: Reação muito comum (ocorre em mais de 10% dos pacientes que utilizam este medicamento): ◦ fadiga ◦ cefaléia ◦ náusea Reação comum (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento): ◦ ◦ ◦ ◦ ◦ Anemia Redução do apetite Rubor quente Depressão, ansiedade, insônia Tontura, enxaqueca Tosse, dispneia, congestão nasal Diarréia, dor abdominal, boca seca, vômitos Prurido Artralgia, mialgia Irritabilidade
 Visão global do tratamento do HCV 1 a onda: Boceprevir + PEG/RBV Telaprevir + PEG/RBV Três ondas 2 a onda: Sofosbuvir + PEG/RBV Simeprevir + PEG/RBV --------------Sofosbuvir + Simeprevir Sofosbuvir + Daclatasvir 3 a onda: 3 D Com PEG RVS: 46 a 50% Com PEG RVS: 80 a 89% Sem PEG RVS: 85 a 95% Sem PEG RVS: 95 a 100%
Visão global do tratamento do HCV 1 a onda: Boceprevir + PEG/RBV Telaprevir + PEG/RBV Três ondas 2 a onda: Sofosbuvir + PEG/RBV Simeprevir + PEG/RBV --------------Sofosbuvir + Simeprevir Sofosbuvir + Daclatasvir 3 a onda: 3 D Com PEG RVS: 46 a 50% Com PEG RVS: 80 a 89% Sem PEG RVS: 85 a 95% Sem PEG RVS: 95 a 100%
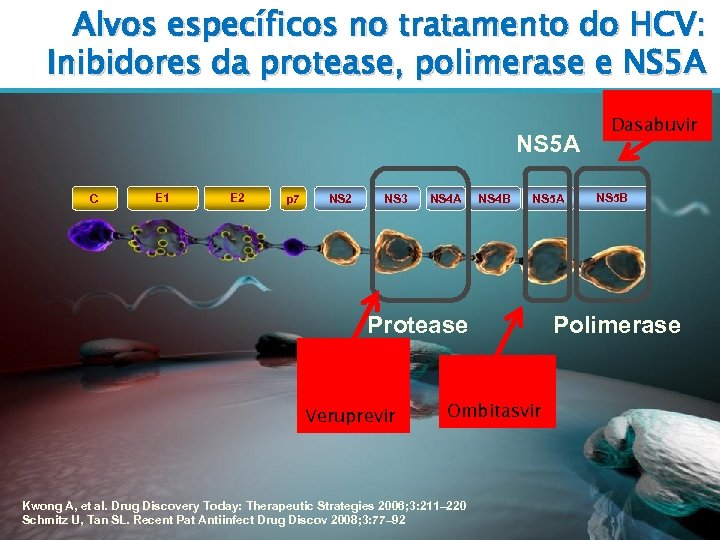 Alvos específicos no tratamento do HCV: Inibidores da protease, polimerase e NS 5 A C E 1 E 2 p 7 NS 2 NS 3 NS 4 A NS 4 B NS 5 A Protease Telaprevir Boceprevir Simeprevir Veruprevir Ledipasvir Daclatasvir Ombitasvir Kwong A, et al. Drug Discovery Today: Therapeutic Strategies 2006; 3: 211– 220 Schmitz U, Tan SL. Recent Pat Antiinfect Drug Discov 2008; 3: 77– 92 Sofosbuvir Dasabuvir NS 5 B Polimerase
Alvos específicos no tratamento do HCV: Inibidores da protease, polimerase e NS 5 A C E 1 E 2 p 7 NS 2 NS 3 NS 4 A NS 4 B NS 5 A Protease Telaprevir Boceprevir Simeprevir Veruprevir Ledipasvir Daclatasvir Ombitasvir Kwong A, et al. Drug Discovery Today: Therapeutic Strategies 2006; 3: 211– 220 Schmitz U, Tan SL. Recent Pat Antiinfect Drug Discov 2008; 3: 77– 92 Sofosbuvir Dasabuvir NS 5 B Polimerase
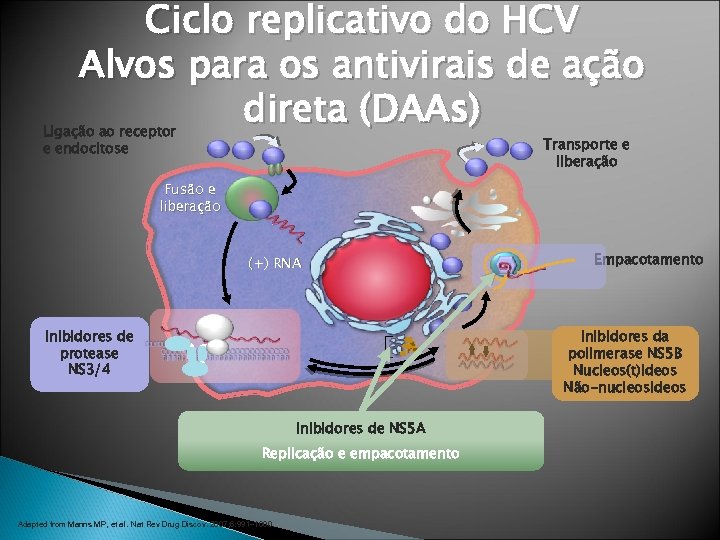 Ciclo replicativo do HCV Alvos para os antivirais de ação direta (DAAs) Ligação ao receptor e endocitose Transporte e liberação Fusão e liberação (+) RNA Tradução e Inibidores de processamento protease da poliproteína NS 3/4 Empacotamento Inibidores da Replicação do polimerase NS 5 B RNA Nucleos(t)ideos Não-nucleosideos Inibidores de NS 5 A Replicação e empacotamento Adapted from Manns MP, et al. Nat Rev Drug Discov. 2007; 6: 991– 1000.
Ciclo replicativo do HCV Alvos para os antivirais de ação direta (DAAs) Ligação ao receptor e endocitose Transporte e liberação Fusão e liberação (+) RNA Tradução e Inibidores de processamento protease da poliproteína NS 3/4 Empacotamento Inibidores da Replicação do polimerase NS 5 B RNA Nucleos(t)ideos Não-nucleosideos Inibidores de NS 5 A Replicação e empacotamento Adapted from Manns MP, et al. Nat Rev Drug Discov. 2007; 6: 991– 1000.
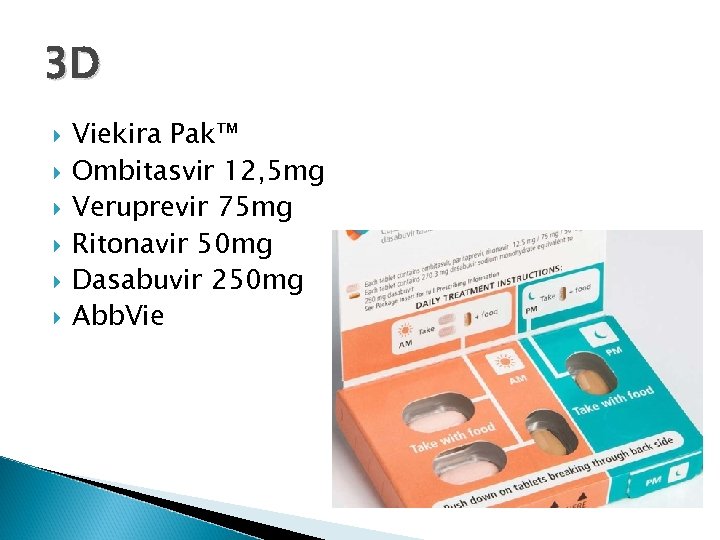 3 D Viekira Pak™ Ombitasvir 12, 5 mg Veruprevir 75 mg Ritonavir 50 mg Dasabuvir 250 mg Abb. Vie
3 D Viekira Pak™ Ombitasvir 12, 5 mg Veruprevir 75 mg Ritonavir 50 mg Dasabuvir 250 mg Abb. Vie
 Informação ao paciente: ◦ Tomar durante a refeição sem importar o conteúdo de gordura ou calórico ◦ Armazenamento a uma temperatura de 30⁰C ou menos • • • Apresentação: Caixa com 28 dias de tratamento Cada caixa inclui 4 caixas semanais Cada caixa semanal inclui 7 pacotes de doses diárias
Informação ao paciente: ◦ Tomar durante a refeição sem importar o conteúdo de gordura ou calórico ◦ Armazenamento a uma temperatura de 30⁰C ou menos • • • Apresentação: Caixa com 28 dias de tratamento Cada caixa inclui 4 caixas semanais Cada caixa semanal inclui 7 pacotes de doses diárias

 Eventos adversos: ◦ ◦ ◦ ◦ Muito comuns: Fadiga Náusea Comuns: Prurido Reações cutâneas Insônia Astenia
Eventos adversos: ◦ ◦ ◦ ◦ Muito comuns: Fadiga Náusea Comuns: Prurido Reações cutâneas Insônia Astenia
 Anomalias de laboratório: • • • Transaminases: • Elevações de ALT superiores a 5 X LSN - 1% • Geralmente nas primeiras 4 semanas de tratamento. • A maioria teve resolução com o prosseguimento da terapia • A presença de cirrose não foi um fator de risco para aumento de ALT Bilirrubinas: • Mais comum (15%) em indivíduos que receberam RBV associada • Predominantemente BI mediante hemólise induzida por veruprevir e ribavirina • Pico na semana 1 • Resolvidas com o avanço do tratamento • Não associadas a elevações de ALT Anemia: • Mudança média de hemoglobina de -0, 5 g/d. L • Nas primeiras 3 semanas • <1% dos pacientes com VIEKIRA PAK e RBV apresentaram Hb < 8 g/d. L • 7% necessitaram de redução na dose de RBV • Nenhum paciente tratado sem RBV apresentou hemoglobina < 10 g/d. L
Anomalias de laboratório: • • • Transaminases: • Elevações de ALT superiores a 5 X LSN - 1% • Geralmente nas primeiras 4 semanas de tratamento. • A maioria teve resolução com o prosseguimento da terapia • A presença de cirrose não foi um fator de risco para aumento de ALT Bilirrubinas: • Mais comum (15%) em indivíduos que receberam RBV associada • Predominantemente BI mediante hemólise induzida por veruprevir e ribavirina • Pico na semana 1 • Resolvidas com o avanço do tratamento • Não associadas a elevações de ALT Anemia: • Mudança média de hemoglobina de -0, 5 g/d. L • Nas primeiras 3 semanas • <1% dos pacientes com VIEKIRA PAK e RBV apresentaram Hb < 8 g/d. L • 7% necessitaram de redução na dose de RBV • Nenhum paciente tratado sem RBV apresentou hemoglobina < 10 g/d. L
 Interações medicamentosas: • • Monitoramento: digoxina, varfarina Diminuição da dose: amiodarona, biperidil, lidocaína, quinidina, disopiramida, propafenona, cetoconazol, anlodipina, furosemida, rosuvastatina, pravastatina Atazanavir: o comprimido contendo ritonavir vai potencializar o atazanavir Darunavir: não deverá ser administrado com ritonavir adicional Ciclosporina: 1/5 da dose diária, uma vez ao dia Tacrolimo: 0, 5 mg uma vez por semana Omeprazol: Utilizar doses maiores, se clinicamente indicado
Interações medicamentosas: • • Monitoramento: digoxina, varfarina Diminuição da dose: amiodarona, biperidil, lidocaína, quinidina, disopiramida, propafenona, cetoconazol, anlodipina, furosemida, rosuvastatina, pravastatina Atazanavir: o comprimido contendo ritonavir vai potencializar o atazanavir Darunavir: não deverá ser administrado com ritonavir adicional Ciclosporina: 1/5 da dose diária, uma vez ao dia Tacrolimo: 0, 5 mg uma vez por semana Omeprazol: Utilizar doses maiores, se clinicamente indicado
 Falha na tomada: • • Em caso de omitir uma dose de ombitasvir, veruprevir, ritonavir: • a dose prescrita pode ser administrada dentro de 12 horas • se tiver transcorrido mais de 12 horas, a dose omitida NÃO deve ser administrada Em caso de omitir uma dose de dasabuvir: • a dose prescrita pode ser administrada dentro de 6 horas • se tiver transcorrido mais de 6 horas, a dose omitida NÃO deve ser administrada
Falha na tomada: • • Em caso de omitir uma dose de ombitasvir, veruprevir, ritonavir: • a dose prescrita pode ser administrada dentro de 12 horas • se tiver transcorrido mais de 12 horas, a dose omitida NÃO deve ser administrada Em caso de omitir uma dose de dasabuvir: • a dose prescrita pode ser administrada dentro de 6 horas • se tiver transcorrido mais de 6 horas, a dose omitida NÃO deve ser administrada
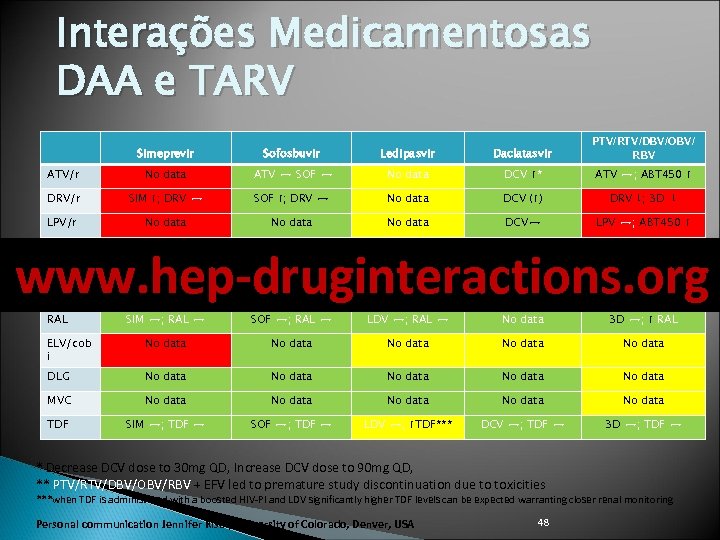 Interações Medicamentosas DAA e TARV Simeprevir Sofosbuvir Ledipasvir Daclatasvir PTV/RTV/DBV/OBV/ RBV ATV/r No data ATV ↔ SOF ↔ No data DCV ↑* ATV ↔; ABT 450 ↑ DRV/r SIM ↑; DRV ↔ SOF ↑; DRV ↔ No data DCV (↑) DRV ↓; 3 D ↓ LPV/r No data DCV↔ LPV ↔; ABT 450 ↑ EFV SIM ↓; EFV ↔ SOF ↔; EFV ↔ LDV ↓; EFV ↓ DCV ↓* No PK data** RPV SIM ↔; RPV ↔ SOF ↔; RPV ↔ LDV ↔; RPV ↔ No data ABT 450 ↑; RPV ↑ ETV No data No data RAL SIM ↔; RAL ↔ SOF ↔; RAL ↔ LDV ↔; RAL ↔ No data 3 D ↔; ↑ RAL ELV/cob i No data No data DLG No data No data MVC No data No data TDF SIM ↔; TDF ↔ SOF ↔; TDF ↔ LDV ↔; ↑TDF*** DCV ↔; TDF ↔ 3 D ↔; TDF ↔ www. hep-druginteractions. org * Decrease DCV dose to 30 mg QD, Increase DCV dose to 90 mg QD, ** PTV/RTV/DBV/OBV/RBV + EFV led to premature study discontinuation due to toxicities ***when TDF is administered with a boosted HIV-PI and LDV significantly higher TDF levels can be expected warranting closer renal monitoring Personal communication Jennifer Kiser, University of Colorado, Denver, USA 48
Interações Medicamentosas DAA e TARV Simeprevir Sofosbuvir Ledipasvir Daclatasvir PTV/RTV/DBV/OBV/ RBV ATV/r No data ATV ↔ SOF ↔ No data DCV ↑* ATV ↔; ABT 450 ↑ DRV/r SIM ↑; DRV ↔ SOF ↑; DRV ↔ No data DCV (↑) DRV ↓; 3 D ↓ LPV/r No data DCV↔ LPV ↔; ABT 450 ↑ EFV SIM ↓; EFV ↔ SOF ↔; EFV ↔ LDV ↓; EFV ↓ DCV ↓* No PK data** RPV SIM ↔; RPV ↔ SOF ↔; RPV ↔ LDV ↔; RPV ↔ No data ABT 450 ↑; RPV ↑ ETV No data No data RAL SIM ↔; RAL ↔ SOF ↔; RAL ↔ LDV ↔; RAL ↔ No data 3 D ↔; ↑ RAL ELV/cob i No data No data DLG No data No data MVC No data No data TDF SIM ↔; TDF ↔ SOF ↔; TDF ↔ LDV ↔; ↑TDF*** DCV ↔; TDF ↔ 3 D ↔; TDF ↔ www. hep-druginteractions. org * Decrease DCV dose to 30 mg QD, Increase DCV dose to 90 mg QD, ** PTV/RTV/DBV/OBV/RBV + EFV led to premature study discontinuation due to toxicities ***when TDF is administered with a boosted HIV-PI and LDV significantly higher TDF levels can be expected warranting closer renal monitoring Personal communication Jennifer Kiser, University of Colorado, Denver, USA 48
 Histórico Consulta pública 1 – abril de 2015 Consulta pública 2 – 19 de junho de 2015 –
Histórico Consulta pública 1 – abril de 2015 Consulta pública 2 – 19 de junho de 2015 –
 Indicações de Tratamento Imediato Coinfecção com o HIV Manifestações extra-hepáticas: ◦ porfiria cutânea, ◦ líquen plano grave com envolvimento de mucosa, ◦ Crioglobulinemia com manifestação em órgão-alvo (olhos, pulmão, sistema nervoso periférico e central), Glomerulonefrite, Vasculites e Poliarterite Nodosa. ◦ Púrpura Trombocitopênica Idiopática (PTI) Sinais clínicos ou evidências ecográficas sugestivas de cirrose hepática (varizes de esôfago, ascite) Insuficiência hepática e ausência de carcinoma hepatocelular, independente da necessidade de transplante hepático Insuficiência renal crônica Pós-transplante de fígado Fibrose hepática avançada (METAVIR F 3 ou F 4) Biópsia hepática com resultado METAVIR F 2 há mais de 3 anos
Indicações de Tratamento Imediato Coinfecção com o HIV Manifestações extra-hepáticas: ◦ porfiria cutânea, ◦ líquen plano grave com envolvimento de mucosa, ◦ Crioglobulinemia com manifestação em órgão-alvo (olhos, pulmão, sistema nervoso periférico e central), Glomerulonefrite, Vasculites e Poliarterite Nodosa. ◦ Púrpura Trombocitopênica Idiopática (PTI) Sinais clínicos ou evidências ecográficas sugestivas de cirrose hepática (varizes de esôfago, ascite) Insuficiência hepática e ausência de carcinoma hepatocelular, independente da necessidade de transplante hepático Insuficiência renal crônica Pós-transplante de fígado Fibrose hepática avançada (METAVIR F 3 ou F 4) Biópsia hepática com resultado METAVIR F 2 há mais de 3 anos
 Recomendação de tratamento O tratamento está indicado para todos os pacientes com biópsia hepática METAVIR ≥ F 3. O tratamento também está indicado para pacientes com resultado de biópsia hepática METAVIR F 2 há mais de 3 (três) anos. Recomenda –se o tratamento para pacientes com resultado de elastografia de onda transitória ≥ 9, 5 k. Pa. Este valor de corte corresponde ao estágio F 3 de fibrose hepática. O tratamento está indicado para pacientes monoinfectados pelo HCV com APRI > 1, 5 ou FIB 4 > 3, 25, caracterizando METAVIR ≥ F 3.
Recomendação de tratamento O tratamento está indicado para todos os pacientes com biópsia hepática METAVIR ≥ F 3. O tratamento também está indicado para pacientes com resultado de biópsia hepática METAVIR F 2 há mais de 3 (três) anos. Recomenda –se o tratamento para pacientes com resultado de elastografia de onda transitória ≥ 9, 5 k. Pa. Este valor de corte corresponde ao estágio F 3 de fibrose hepática. O tratamento está indicado para pacientes monoinfectados pelo HCV com APRI > 1, 5 ou FIB 4 > 3, 25, caracterizando METAVIR ≥ F 3.
 GT 1 O acréscimo da ribavirina aos regimes sofosbuvir + simeprevir e sofosbuvir + daclatasvir poderá ser realizado em pacientes portadores de cirrose hepática. EASL:
GT 1 O acréscimo da ribavirina aos regimes sofosbuvir + simeprevir e sofosbuvir + daclatasvir poderá ser realizado em pacientes portadores de cirrose hepática. EASL:
 GT 2 EASL:
GT 2 EASL:
 GT 3 (RVS 82 -92%) EASL:
GT 3 (RVS 82 -92%) EASL:
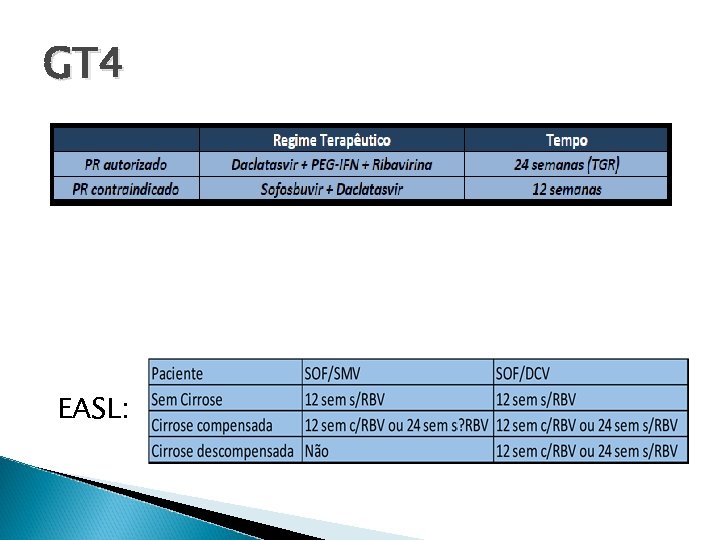 GT 4 EASL:
GT 4 EASL:
 56
56



