Антитела магомедова 4 гр. 2 к. стом фак.pptx
- Количество слайдов: 23
 Антитела Выполнила Магомедова Ж. З. 2 к. 4 гр. ст. ф.
Антитела Выполнила Магомедова Ж. З. 2 к. 4 гр. ст. ф.
 Антитела (иммуноглобулины, ИГ, Ig) — это особый класс гликопротеинов, присутствующих на поверхности В-клеток в виде мембраносвязанных рецепторов и в сыворотке крови и тканевой жидкости в виде растворимых молекул. Они являются важнейшим фактором специфического гуморального иммунитета. Антитела используются иммунной системой для идентификации и нейтрализации чужеродных объектов — например, бактерий и вирусов. Антитела выполняют две функции: антиген связывающую и эффекторную (вызывают тот или иной иммунный ответ, например, запускают классическую схему активации комплемента).
Антитела (иммуноглобулины, ИГ, Ig) — это особый класс гликопротеинов, присутствующих на поверхности В-клеток в виде мембраносвязанных рецепторов и в сыворотке крови и тканевой жидкости в виде растворимых молекул. Они являются важнейшим фактором специфического гуморального иммунитета. Антитела используются иммунной системой для идентификации и нейтрализации чужеродных объектов — например, бактерий и вирусов. Антитела выполняют две функции: антиген связывающую и эффекторную (вызывают тот или иной иммунный ответ, например, запускают классическую схему активации комплемента).
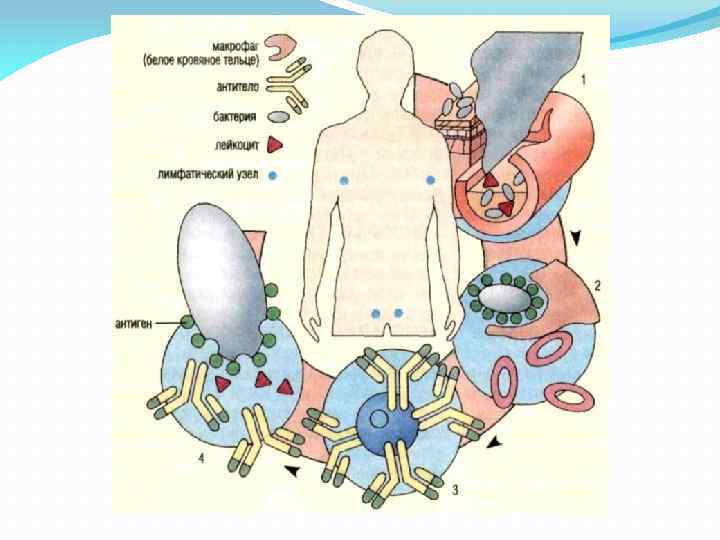
 Антитела синтезируются плазматическими клетками , которыми становятся В-лимфоциты в ответ на присутствие антигенов. Для каждого антигена формируются соответствующие ему специализировавшиеся плазматические клетки, вырабатывающие специфичные для этого антигена антитела. Антитела распознают антигены, связываясь с определённым эпитопом — характерным фрагментом поверхности или линейной аминокислотной цепи антигена.
Антитела синтезируются плазматическими клетками , которыми становятся В-лимфоциты в ответ на присутствие антигенов. Для каждого антигена формируются соответствующие ему специализировавшиеся плазматические клетки, вырабатывающие специфичные для этого антигена антитела. Антитела распознают антигены, связываясь с определённым эпитопом — характерным фрагментом поверхности или линейной аминокислотной цепи антигена.
 Функции антител Иммуноглобулины всех изотипов бифункциональны. Это означает, что иммуноглобулин любого типа распознает и связывает антиген, а затем усиливает киллинг и/или удаление иммунных комплексов, сформированных в результате активации эффекторных механизмов. Одна область молекулы антител (Fab) определяет ее антигенную специфичность, а другая (Fc) осуществляет эффекторные функции: связывание с рецепторами, которые экспрессированы на клетках организма (например, фагоцитах); связывание с первым компонентом (C 1 q) системы комплемента для инициации классического пути каскада комплемента.
Функции антител Иммуноглобулины всех изотипов бифункциональны. Это означает, что иммуноглобулин любого типа распознает и связывает антиген, а затем усиливает киллинг и/или удаление иммунных комплексов, сформированных в результате активации эффекторных механизмов. Одна область молекулы антител (Fab) определяет ее антигенную специфичность, а другая (Fc) осуществляет эффекторные функции: связывание с рецепторами, которые экспрессированы на клетках организма (например, фагоцитах); связывание с первым компонентом (C 1 q) системы комплемента для инициации классического пути каскада комплемента.
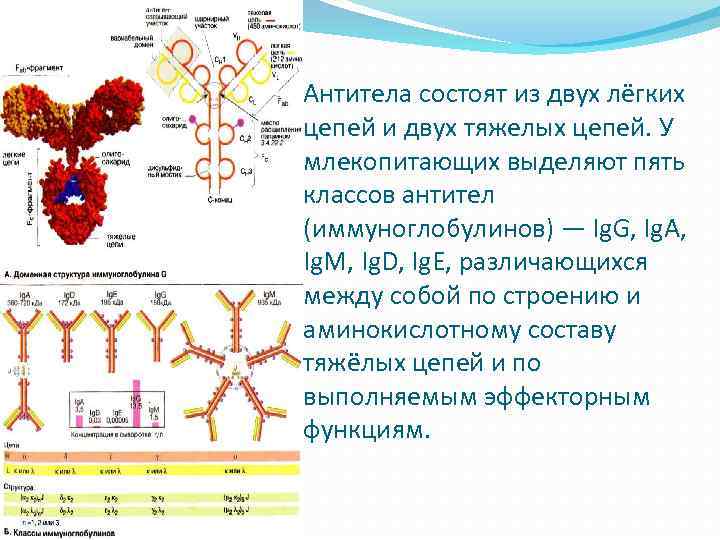 Антитела состоят из двух лёгких цепей и двух тяжелых цепей. У млекопитающих выделяют пять классов антител (иммуноглобулинов) — Ig. G, Ig. A, Ig. M, Ig. D, Ig. E, различающихся между собой по строению и аминокислотному составу тяжёлых цепей и по выполняемым эффекторным функциям.
Антитела состоят из двух лёгких цепей и двух тяжелых цепей. У млекопитающих выделяют пять классов антител (иммуноглобулинов) — Ig. G, Ig. A, Ig. M, Ig. D, Ig. E, различающихся между собой по строению и аминокислотному составу тяжёлых цепей и по выполняемым эффекторным функциям.
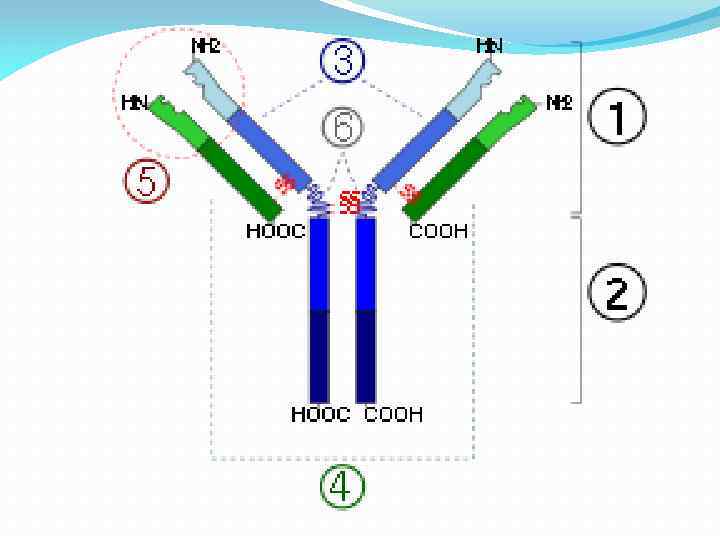
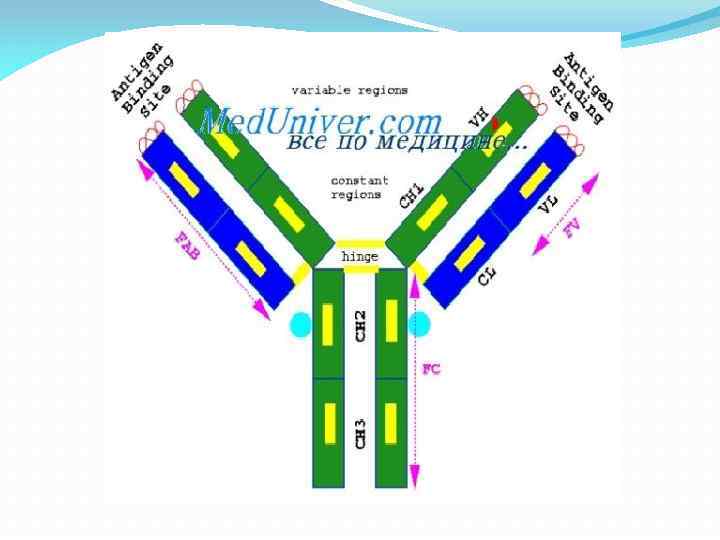
 Антитела являются относительно крупными (~150 к. Да— Ig. G) , гликопротеинами имеющими сложное строение. Состоят из двух идентичных тяжелых цепей (H-цепи, в свою очередь состоящие из VH, CH 1, шарнира, CH 2 и CH 3 доменов) и из двух идентичных (L-цепей, состоящих из VL и CL доменов). К тяжелым цепям ковалентно присоединены олигосахариды. При помощи протеазы папаина антитела можно расщепить на два Fab (англ. fragment antigen binding — антигенсвязывающий фрагмент) и один Fc (англ. fragment crystallizable — фрагмент, способный к кристаллизации).
Антитела являются относительно крупными (~150 к. Да— Ig. G) , гликопротеинами имеющими сложное строение. Состоят из двух идентичных тяжелых цепей (H-цепи, в свою очередь состоящие из VH, CH 1, шарнира, CH 2 и CH 3 доменов) и из двух идентичных (L-цепей, состоящих из VL и CL доменов). К тяжелым цепям ковалентно присоединены олигосахариды. При помощи протеазы папаина антитела можно расщепить на два Fab (англ. fragment antigen binding — антигенсвязывающий фрагмент) и один Fc (англ. fragment crystallizable — фрагмент, способный к кристаллизации).
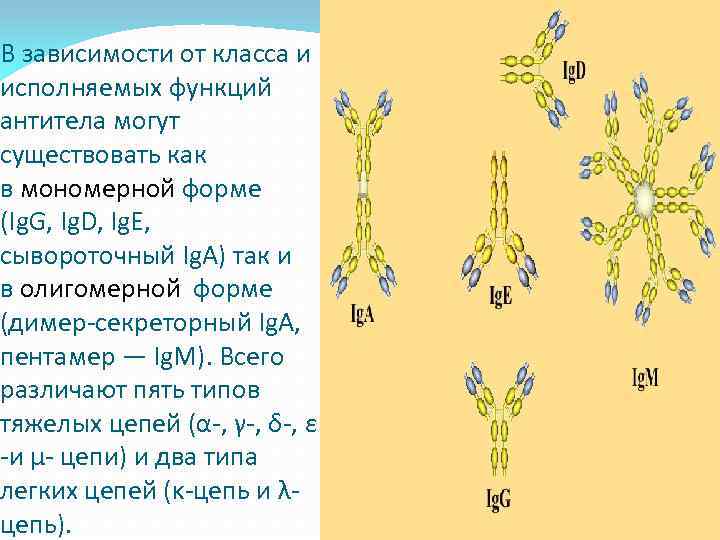 В зависимости от класса и исполняемых функций антитела могут существовать как в мономерной форме (Ig. G, Ig. D, Ig. E, сывороточный Ig. A) так и в олигомерной форме (димер-секреторный Ig. A, пентамер — Ig. M). Всего различают пять типов тяжелых цепей (α-, γ-, δ-, ε -и μ- цепи) и два типа легких цепей (κ-цепь и λцепь).
В зависимости от класса и исполняемых функций антитела могут существовать как в мономерной форме (Ig. G, Ig. D, Ig. E, сывороточный Ig. A) так и в олигомерной форме (димер-секреторный Ig. A, пентамер — Ig. M). Всего различают пять типов тяжелых цепей (α-, γ-, δ-, ε -и μ- цепи) и два типа легких цепей (κ-цепь и λцепь).
 Ig. A сывороточный Ig. A составляет 15 -20 % всей фракции иммуноглобулинов, при этом 80 % молекул Ig. A представлено в мономерной форме у человека. Секреторный Ig. A представлен в димерной форме в комплексе секреторным компонентом, содержится в серозно-слизистых секретах (например в слюне, слезах, молозиве, молоке, отделяемом слизистой оболочки мочеполовой и респираторной системы). Содержит 10 -12 % углеводов, молекулярная масса 500 к. Да
Ig. A сывороточный Ig. A составляет 15 -20 % всей фракции иммуноглобулинов, при этом 80 % молекул Ig. A представлено в мономерной форме у человека. Секреторный Ig. A представлен в димерной форме в комплексе секреторным компонентом, содержится в серозно-слизистых секретах (например в слюне, слезах, молозиве, молоке, отделяемом слизистой оболочки мочеполовой и респираторной системы). Содержит 10 -12 % углеводов, молекулярная масса 500 к. Да
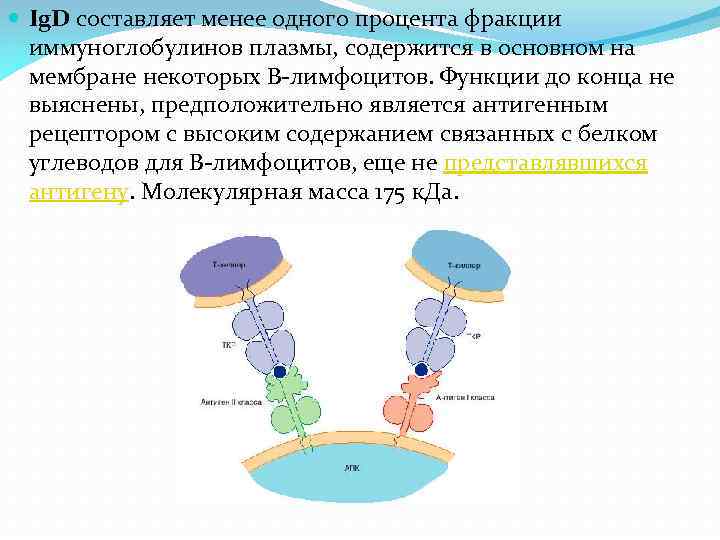 Ig. D составляет менее одного процента фракции иммуноглобулинов плазмы, содержится в основном на мембране некоторых В-лимфоцитов. Функции до конца не выяснены, предположительно является антигенным рецептором с высоким содержанием связанных с белком углеводов для В-лимфоцитов, еще не представлявшихся антигену. Молекулярная масса 175 к. Да.
Ig. D составляет менее одного процента фракции иммуноглобулинов плазмы, содержится в основном на мембране некоторых В-лимфоцитов. Функции до конца не выяснены, предположительно является антигенным рецептором с высоким содержанием связанных с белком углеводов для В-лимфоцитов, еще не представлявшихся антигену. Молекулярная масса 175 к. Да.
 Ig. E в свободном виде в плазме почти отсутствует. Способен осуществлять защитную функцию в организме от действия паразитарных инфекций, обуславливает многие аллергические реакции. Механизм действия Ig. E проявляется через связывание с высоким сродством (10− 10 М) с поверхностными структурами базофилов и тучных клеток, с последующим присоединением к ним антигена, вызывая дегрануляцию и выброс в кровь высоко активных аминов (гистамина и серотонина — медиаторов воспаления). 200 к. Да.
Ig. E в свободном виде в плазме почти отсутствует. Способен осуществлять защитную функцию в организме от действия паразитарных инфекций, обуславливает многие аллергические реакции. Механизм действия Ig. E проявляется через связывание с высоким сродством (10− 10 М) с поверхностными структурами базофилов и тучных клеток, с последующим присоединением к ним антигена, вызывая дегрануляцию и выброс в кровь высоко активных аминов (гистамина и серотонина — медиаторов воспаления). 200 к. Да.
 Ig. G является основным иммуноглобулином сыворотки здорового человека (составляет 70 -75 % всей фракции иммуноглобулинов), наиболее активен во вторичном иммунном ответе и антитоксическом иммунитете. Благодаря малым размерам (коэффициент седиментации 7 S, молекулярная масса 146 к. Да) является единственной фракцией иммуноглобулинов, способной к транспорту через плацентарный барьер и тем самым обеспечивающей иммунитет плода и новорожденного. В составе Ig. G 23 % углеводов ; два антигенсвязывающих Fab-фрагмента и один FC-фрагмент. Fab-фрагмент (50 -52 к. Да) состоит из целой L-цепи и N-концевой половины H-цепи, соединённых между собой дисульфидной связью , тогда как FC-фрагмент (48 к. Да) образован C-концевыми половинами H-цепей. Всего в молекуле Ig. G 12 доменов (участки, сформированные из βструктуры и α-спиралей полипептидных цепей Ig в виде неупорядоченных образований, связанных между собой дисульфидными мостиками аминокислотных остатков внутри каждой цепи): по 4 на тяжёлых и по 2 на лёгких цепях.
Ig. G является основным иммуноглобулином сыворотки здорового человека (составляет 70 -75 % всей фракции иммуноглобулинов), наиболее активен во вторичном иммунном ответе и антитоксическом иммунитете. Благодаря малым размерам (коэффициент седиментации 7 S, молекулярная масса 146 к. Да) является единственной фракцией иммуноглобулинов, способной к транспорту через плацентарный барьер и тем самым обеспечивающей иммунитет плода и новорожденного. В составе Ig. G 23 % углеводов ; два антигенсвязывающих Fab-фрагмента и один FC-фрагмент. Fab-фрагмент (50 -52 к. Да) состоит из целой L-цепи и N-концевой половины H-цепи, соединённых между собой дисульфидной связью , тогда как FC-фрагмент (48 к. Да) образован C-концевыми половинами H-цепей. Всего в молекуле Ig. G 12 доменов (участки, сформированные из βструктуры и α-спиралей полипептидных цепей Ig в виде неупорядоченных образований, связанных между собой дисульфидными мостиками аминокислотных остатков внутри каждой цепи): по 4 на тяжёлых и по 2 на лёгких цепях.
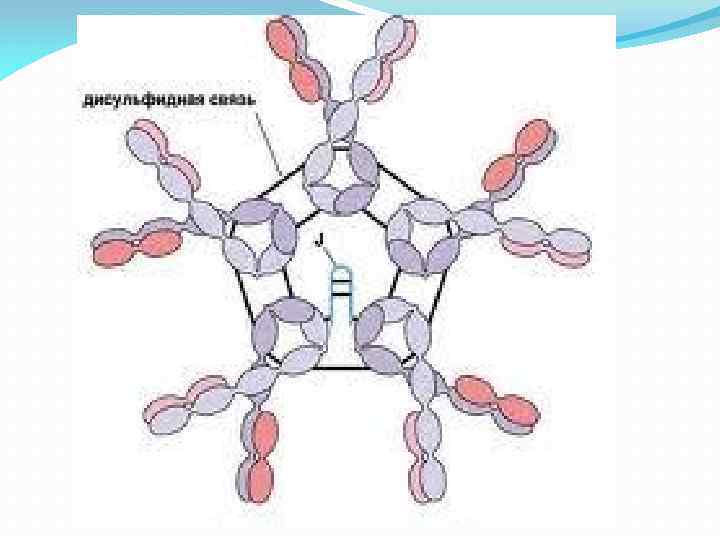
 Ig. M представляют собой пентамер основной четырехцепочечной единицы, содержащей две μ-цепи. При этом каждый пентамер содержит одну копию полипептида с J -цепью (20 к. Да), который синтезируется антителообразующей клеткой и ковалентно связывается между двумя соседними FC-фрагментами иммуноглобулина. Появляются при первичном иммунном ответе Bлимфоцитами на неизвестный антиген, составляют до 10 % фракции иммуноглобулинов. Являются наиболее крупными иммуноглобулинами (970 к. Да). Содержат 10 -12 % углеводов. Образование Ig. M происходит ещё в пре-B-лимфоцитах, в которых первично синтезируются из μ-цепи; синтез лёгких цепей в пре-B-клетках обеспечивает их связывание с μцепями, в результате образуются функционально активные Ig. M, которые встраиваются в поверхностные структуры плазматической мембраны, выполняя роль антиген распознающего рецептора; с этого момента клетки пре-Bлимфоцитов становятся зрелыми и способны участвовать в
Ig. M представляют собой пентамер основной четырехцепочечной единицы, содержащей две μ-цепи. При этом каждый пентамер содержит одну копию полипептида с J -цепью (20 к. Да), который синтезируется антителообразующей клеткой и ковалентно связывается между двумя соседними FC-фрагментами иммуноглобулина. Появляются при первичном иммунном ответе Bлимфоцитами на неизвестный антиген, составляют до 10 % фракции иммуноглобулинов. Являются наиболее крупными иммуноглобулинами (970 к. Да). Содержат 10 -12 % углеводов. Образование Ig. M происходит ещё в пре-B-лимфоцитах, в которых первично синтезируются из μ-цепи; синтез лёгких цепей в пре-B-клетках обеспечивает их связывание с μцепями, в результате образуются функционально активные Ig. M, которые встраиваются в поверхностные структуры плазматической мембраны, выполняя роль антиген распознающего рецептора; с этого момента клетки пре-Bлимфоцитов становятся зрелыми и способны участвовать в
 Вариабельность антител Антитела являются чрезвычайно вариабельными (в организме одного человека может существовать до 108 вариантов антител). Все разнообразие антител проистекает из вариабельности как тяжёлых цепей, так и лёгких цепей. У антител, вырабатываемых тем или иным организмом в ответ на те или иные антигены, выделяют: Изотипическая вариабельность — проявляется в наличии классов антител (изотипов), различающихся по строению тяжёлых цепей и олигомерностью, вырабатываемых всеми организмами данного вида; Аллотипическая вариабельность — проявляется на индивидуальном уровне в пределах данного вида в виде вариабельности аллелей иммуноглобулинов — является генетически детерминированным отличием данного организма от другого; Идиотипическая вариабельность — проявляется в различии аминокислотного состава антиген-связывающего участка. Это касается вариабельных и гипервариабельных доменов тяжёлой и лёгкой цепей, непосредственно контактирующих с антигеном.
Вариабельность антител Антитела являются чрезвычайно вариабельными (в организме одного человека может существовать до 108 вариантов антител). Все разнообразие антител проистекает из вариабельности как тяжёлых цепей, так и лёгких цепей. У антител, вырабатываемых тем или иным организмом в ответ на те или иные антигены, выделяют: Изотипическая вариабельность — проявляется в наличии классов антител (изотипов), различающихся по строению тяжёлых цепей и олигомерностью, вырабатываемых всеми организмами данного вида; Аллотипическая вариабельность — проявляется на индивидуальном уровне в пределах данного вида в виде вариабельности аллелей иммуноглобулинов — является генетически детерминированным отличием данного организма от другого; Идиотипическая вариабельность — проявляется в различии аминокислотного состава антиген-связывающего участка. Это касается вариабельных и гипервариабельных доменов тяжёлой и лёгкой цепей, непосредственно контактирующих с антигеном.
 Контроль пролиферации Наиболее эффективный контролирующий механизм заключается в том, что продукт реакции одновременно служит ее ингибитором. Этот тип отрицательной обратной связи имеет место при образовании антител. Действие антител нельзя объяснить просто нейтрализацией антигена, потому что целые молекулы Ig. G подавляют синтез антител намного эффективнее, чем F(ab')2 -фрагменты. Предполагают, что блокада продуктивной фазы T-зависимого B-клеточного ответа возникает в результате образования перекрестных связей между антигеном, Ig. G и Fc — рецепторами на поверхности B-клеток. Инъекция Ig. M, усиливает иммунный ответ. Так как антитела именно этого изотипа появляются первыми после введения антигена, то на ранней стадии иммунного ответа им приписывается усиливающая роль.
Контроль пролиферации Наиболее эффективный контролирующий механизм заключается в том, что продукт реакции одновременно служит ее ингибитором. Этот тип отрицательной обратной связи имеет место при образовании антител. Действие антител нельзя объяснить просто нейтрализацией антигена, потому что целые молекулы Ig. G подавляют синтез антител намного эффективнее, чем F(ab')2 -фрагменты. Предполагают, что блокада продуктивной фазы T-зависимого B-клеточного ответа возникает в результате образования перекрестных связей между антигеном, Ig. G и Fc — рецепторами на поверхности B-клеток. Инъекция Ig. M, усиливает иммунный ответ. Так как антитела именно этого изотипа появляются первыми после введения антигена, то на ранней стадии иммунного ответа им приписывается усиливающая роль.
 Классификация по антигенам антиинфекционные или антипаразитарные антитела, вызывающие непосредственную гибель или нарушение жизнедеятельности возбудителя инфекции либо паразита так называемые «антитела-свидетели заболевания» , наличие которых в организме сигнализирует о знакомстве иммунной системы с данным возбудителем в прошлом или о текущем инфицировании этим возбудителем, но которые не играют существенной роли в борьбе организма с возбудителем (не обезвреживают ни самого возбудителя, ни его токсины, а связываются со второстепенными белками возбудителя). аутоагрессивные антитела или аутологичные антитела, аутоантитела — антитела, вызывающие разрушение или повреждение нормальных, здоровых тканей самого организма хозяина и запускающие механизм развития аутоиммунных заболеваний.
Классификация по антигенам антиинфекционные или антипаразитарные антитела, вызывающие непосредственную гибель или нарушение жизнедеятельности возбудителя инфекции либо паразита так называемые «антитела-свидетели заболевания» , наличие которых в организме сигнализирует о знакомстве иммунной системы с данным возбудителем в прошлом или о текущем инфицировании этим возбудителем, но которые не играют существенной роли в борьбе организма с возбудителем (не обезвреживают ни самого возбудителя, ни его токсины, а связываются со второстепенными белками возбудителя). аутоагрессивные антитела или аутологичные антитела, аутоантитела — антитела, вызывающие разрушение или повреждение нормальных, здоровых тканей самого организма хозяина и запускающие механизм развития аутоиммунных заболеваний.
 аллореактивные антитела, или гомологичные антитела, аллоантитела — антитела против антигенов тканей или клеток других организмов того же биологического вида. Аллоантитела играют важную роль в процессах отторжения аллотрансплантантов, например, при пересадке почки, печени, костного мозга, и в реакциях на переливание несовместимой крови. гетерологичные антитела, или изоантитела — антитела против антигенов тканей или клеток организмов других биологических видов. Изоантитела являются причиной невозможности осуществления ксенотрансплантации даже между эволюционно близкими видами (например, невозможна пересадка печени шимпанзе человеку) или видами, имеющими близкие иммунологические и антигенные характеристики
аллореактивные антитела, или гомологичные антитела, аллоантитела — антитела против антигенов тканей или клеток других организмов того же биологического вида. Аллоантитела играют важную роль в процессах отторжения аллотрансплантантов, например, при пересадке почки, печени, костного мозга, и в реакциях на переливание несовместимой крови. гетерологичные антитела, или изоантитела — антитела против антигенов тканей или клеток организмов других биологических видов. Изоантитела являются причиной невозможности осуществления ксенотрансплантации даже между эволюционно близкими видами (например, невозможна пересадка печени шимпанзе человеку) или видами, имеющими близкие иммунологические и антигенные характеристики
 антиидиотипические антитела — антитела против антител, вырабатываемых самим же организмом. Причём это антитела не «вообще» против молекулы данного антитела, а именно против рабочего, «распознающего» участка антитела, так называемого идиотипа. Антиидиотипические антитела играют важную роль в связывании и обезвреживании избытка антител, в иммунной регуляции выработки антител. Кроме того, антиидиотипическое «антитело против антитела» зеркально повторяет пространственную конфигурацию исходного антигена, против которого было выработано исходное антитело. И тем самым антиидиотипическое антитело служит для организма фактором иммунологической памяти, аналогом исходного антигена, который остаётся в организме и после уничтожения исходных антигенов. В свою очередь, против антиидиотипических антител могут вырабатываться антиидиотипические антитела и т. д.
антиидиотипические антитела — антитела против антител, вырабатываемых самим же организмом. Причём это антитела не «вообще» против молекулы данного антитела, а именно против рабочего, «распознающего» участка антитела, так называемого идиотипа. Антиидиотипические антитела играют важную роль в связывании и обезвреживании избытка антител, в иммунной регуляции выработки антител. Кроме того, антиидиотипическое «антитело против антитела» зеркально повторяет пространственную конфигурацию исходного антигена, против которого было выработано исходное антитело. И тем самым антиидиотипическое антитело служит для организма фактором иммунологической памяти, аналогом исходного антигена, который остаётся в организме и после уничтожения исходных антигенов. В свою очередь, против антиидиотипических антител могут вырабатываться антиидиотипические антитела и т. д.



