АНТИТЕЛА 2.pptx
- Количество слайдов: 39

АНТИТЕЛА
Антителами называются сывороточные белки, образующиеся в ответ на действие антигена • Они относятся к сывороточным глобулинам, поэтому называются иммуноглобулинами (Ig). • Через них реализуется гуморальный тип иммунного ответа. : Антитела обладают 2 свойствами специфичностьюспособностью вступать во взаимодействие с АГ, аналогичным тому, который вызвал их образование; Гетерогенностью по физико-химическому строению, специфичности, генетической детерминированности образования (по происхождению).

Антитела (иммуноглобулины) это особый класс гликопротеинов, присутствующих на поверхности Вклеток в виде мембраносвязанных рецепторов и в сыворотке крови и тканевой жидкости в виде растворимых молекул. • Они являются важнейшим фактором специфического гуморального иммунитета. • Антитела используются иммунной системой для идентификации и нейтрализации чужеродных объектов Антитела выполняют функции: 1. антиген-связывающую – распознавание и/или блокирование АГ посредством активных центров (участвуют Fab фрагменты). 2. эффекторную – осуществление эффекта элиминации (реализуется Fc фрагментом). Вызывают тот или иной иммунный ответ, например, запускают классическую схему активации комплемента). Fc фрагменты Ig обеспечивают взаимодействие комплексов АГ —АТ с клетками, обеспечивающими деструкцию и удаление АГ из организма. Для этого существуют Fc рецепторы для Ig различных классов на поверхности макрофагов, лимфоцитов, нейтрофилов, эозино и базофилов, тучных, и К клеток. Взаимодействуя с Fc областью Ig, рецепторы стимулируют фагоцитоз, противоопухолевую активность, дегрануляцию тучных клеток. •

• Антитела синтезируются ПК, которыми становятся В-л в ответ на присутствие АГ • Для каждого АГ формируются соответствующие ему специализировавшиеся ПК, вырабатывающие специфичные для этого антигена антитела. • Антитела распознают АГ, связываясь с определённым эпитопом — характерным фрагментом поверхности или линейной аминокислотной цепи антигена. • Существенным и уникальным свойством АТ, отличающим их от других иммуноглобулинподобных структур, является способность взаимодействия с цельными (нативными или необработанными) АГ. Следовательно, не требуется времени на предварительную обработку и эффекторная функция осуществляется немедленно! Антитела — единственный фактор безотлагательной защиты организма, например, от сильных ЯДОВ.

Молекулы Ig одной и той же специфичности по антигену присутствуют в организме в трех формах: § растворимой (кровь и другие биологические жидкости); § на мембране В лимфоцита в составе рецептора для антигена — ВСR; § в связи с клетками, но не в трансмембранном варианте, а связанными за Fc фрагмент Fc pe цептором клетки.

Все иммуноглобулины являются иммунными, т. е. образуются в результате иммунизации, контакта с АГ Тем не менее по происхождению они делятся: • на нормальные (анамнестические) АТ, которые обнаруживаются в любом организме как результат бытовой иммунизации; • инфекционные АТ, которые накапливаются в организме в период инфекционной болезни; • постинфекционные АТ, которые обнаруживаются в организме после перенесенного инфекционного заболевания; • поствакцинальные АТ, которые возникают после искусственной иммунизации.

• Сила связи AT с АГ обозначают термином авидность (жадность) – суммарная сила взаимодействия цельной молекулы АТ со всеми антигенными эпитопами. Чем выше авидность, тем прочнее комплекс АТ АГ. • Аффинность — мера прочности этой связи – сила связывания одного эпитопа с одним активным центром Ig. Зависит от точности совпадения пространственной конфигурации активных центров молекул AT с АГ детерминантами. Чем выше аффинитет, тем специфичнее связь AT с АГ.
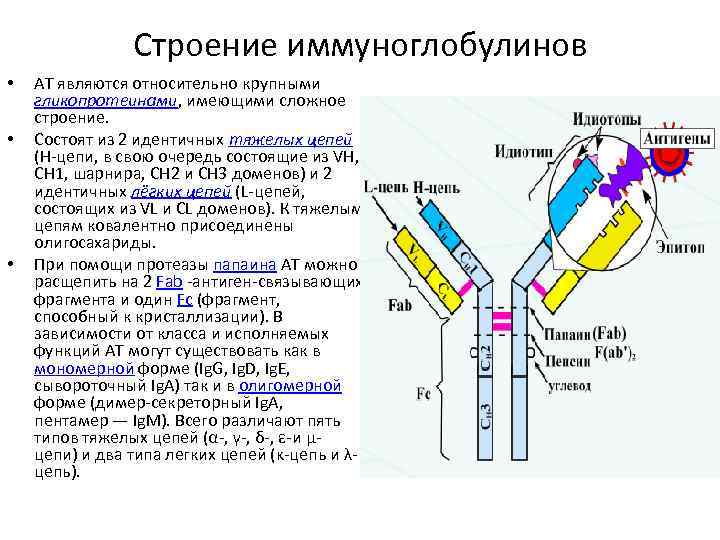
Строение иммуноглобулинов • • • АТ являются относительно крупными гликопротеинами, имеющими сложное строение. Состоят из 2 идентичных тяжелых цепей (H цепи, в свою очередь состоящие из VH, CH 1, шарнира, CH 2 и CH 3 доменов) и 2 идентичных лёгких цепей (L цепей, состоящих из VL и CL доменов). К тяжелым цепям ковалентно присоединены олигосахариды. При помощи протеазы папаина АТ можно расщепить на 2 Fab антиген связывающих фрагмента и один Fc (фрагмент, способный к кристаллизации). В зависимости от класса и исполняемых функций АТ могут существовать как в мономерной форме (Ig. G, Ig. D, Ig. E, сывороточный Ig. A) так и в олигомерной форме (димер секреторный Ig. A, пентамер — Ig. M). Всего различают пять типов тяжелых цепей (α , γ , δ , ε и μ цепи) и два типа легких цепей (κ цепь и λ цепь).

• Активный центр антител антигенсвязывающий участок Fab фрагмента Ig, образованный гипервариабельными участками Н и L цепей, связывает эпитопы АГ. • В активном центре имеются специфичные комплементарные участки к определенным антигенным эпитопам • Fc фрагмент может связывать комплемент, взаимодействует с мембранами клеток и участвует в переносе Ig. G через плаценту. • Домены антител компактные структуры, скрепленные дисульфидной связью. • Так, в Ig. G различают: V домены легких (VL) и тяжелых (VH) цепей АТ, расположенные в N концевои части Fab фрагмента; • С домены константных участков легких цепей (СL) ; • С домены константных участков тяжелых цепей (СH 1, СH 2, СH 3). Комплементсвязывающий участок находится в СH 2 домене.

• Антигенные свойства антител • Изотип антител (класс, подкласс иммуноглобулинов Ig. M, Ig. Gl, Ig. G 2, Ig. G 3, Ig. G 4, Ig. A 1, Ig. A 2, Ig. D, Ig. E) определяется С доменам тяжелых цепей; • Идиотип антител определяется антигенсвязывающими центрами Fab фрагментов антител, т. е. антигенными свойствами вариабельных участков (V областей). Идиотип состоит из набора идиотопов антигенных детерминант V области антитела.

ИЗОТИП, АЛЛОТИП, ИДИОТИП Антитела — это особые растворимые белки с определенной биохимической структурой (иммуноглобулины), которые присутствуют в сыворотке крови и других биологических жидкостях и которые организм вырабатывает для связывания АГ. Международная аббревиатура иммуноглобулинов — Ig. Заглавная буква один из пяти существующих классов иммуноглобулинов — М, A, G, E, D. Последующая арабская цифра обозначает субкласс. Субклассы есть лишь у иммуноглобулинов класса G —G 1, G 2, G 3, G 4 и Ig А — Al, A 2. Изотипы В зависимости от строения константных областей тяжелых цепей иммуноглобулины разделяют на основные группы, называемые классами Классы и подклассы, вместе взятые, называют изотипами. Таким образом, классов иммуноглобулинов 5, а изотипов — 9. Они различаются не только по аминокислотным последовательностям, но и по антигенной специфичности Аллотипы Этот тип разнообразия АТ обусловлен существованием аллельных форм (кодируемых аллельными генами одного локуса); Аллотипические детерминанты служат генетическими маркерами. Подобно тому как Эр у генетически различных индивидуумов могут различаться по системам АГ групп крови А, В, О, тяжелые цепи иммуноглобулинов различаются по экспрессии аллотипических групп Gm-маркеры на Ig. G. Аллотипические различия в конкретном локусе Gm обычно затрагивают одну или две аминокислоты полипептидной цепи. Возьмем, к примеру, локус Glm(a) на Ig. Gl. У особи с этим аллотипом каждая из молекул Ig. Gl будет содержать такую последовательность: Asp. Glu. Leu. Thr. Lys. У другой особи с иным аллотипом (a negative) имеют место две аминокислотные за мены: lu. Glu. Met. Thr. Lys. На сегодняшний G день на тяжелых у цепях обнаружено 25 маркеров Gm и три маркера на константных областях к цепей (Кт маркеры).

Идиотипы Мы убедились в том, что можно получить АТ, узнающие изотипические и аллотипические варианты; кроме того, можно получить антисыворотку, специфичную к конкретному АТ и способную отличить одно Мк. АТ от другого независимо от их изотипов и аллотипов. Такая антисыворотка определяет индивидуальные особенности, характерные для каждого АТ, в совокупности названные идиотипом. Неудивительно, что идиотипические детерминанты локализованы в вариабельной области антитела и ассоциированы с гипервариабельными участками. Антиидиотипические Ig, реагирующие только с одним определенным антителом, узнают частные (private) идиотипы, что подтверждает наличие у каждого АТ уникальной структуры. Часто молекулы АТ с похожими аминокислотными последовательностями вдобавок обладают одним и тем же идиотипом , и тогда мы говорим об общих (public) или перекрестно реагирующих идиотипах. Антиидиотипическая сыворотка служит удобным реагентом для обнаружения одной и той же вариабельной области на разных тяжелых цепях и в разных клетках, для идентификации специфических иммунных комплексов в сыворотке больных.
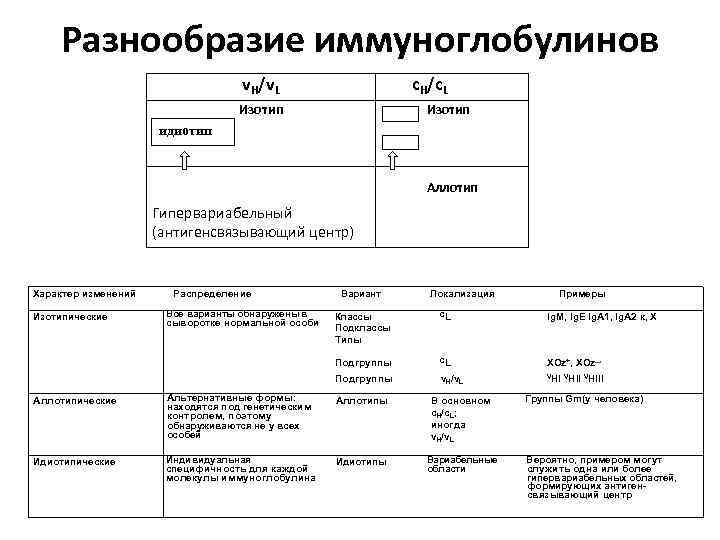
Разнообразие иммуноглобулинов v /v c /c H L H Изотип L Изотип идиотип Аллотип Гипервариабельный (антигенсвязывающий центр) Характер изменений Распределение Все варианты обнаружены в сыворотке нормальной особи Вариант Локализация Примеры Классы Подклассы Типы CL Ig. M, Ig. E lg. A 1, lg. A 2 к, X Подгруппы CL XOz+, XOz~ Подгруппы Изотипические v. H/v. L VHIII Аллотипические Альтернативные формы: находятся под генетическим контролем, поэтому обнаруживаются не у всех особей Аллотипы В основном c. H/c. L; иногда v. H/v. L Идиотипические Индивидуальная специфичность для каждой молекулы иммуноглобулина Идиотипы Вариабельные области Группы Gm(y человека) Вероятно, примером могут служить одна или более гипервариабельных областей, формирующих антигенсвязывающий центр

Классификация по тяжелым цепям • Различают пять классов (изотипов) иммуноглобулинов Ig. G, Ig. M, Ig. A, Ig. D, Ig. E, различающихся: • величиной • зарядом • последовательностью аминокислот • содержанием углеводов • Класс Ig. G классифицируют на четыре подкласса (Ig. G 1, Ig. G 2, Ig. G 3, Ig. G 4), • класс Ig. A — на два подкласса (Ig. A 1, Ig. A 2). Все классы и подклассы составляют девять изотипов, которые присутствуют в норме у всех индивидов. Каждый изотип определяется последовательностью аминокислот константной области тяжелой цепи.
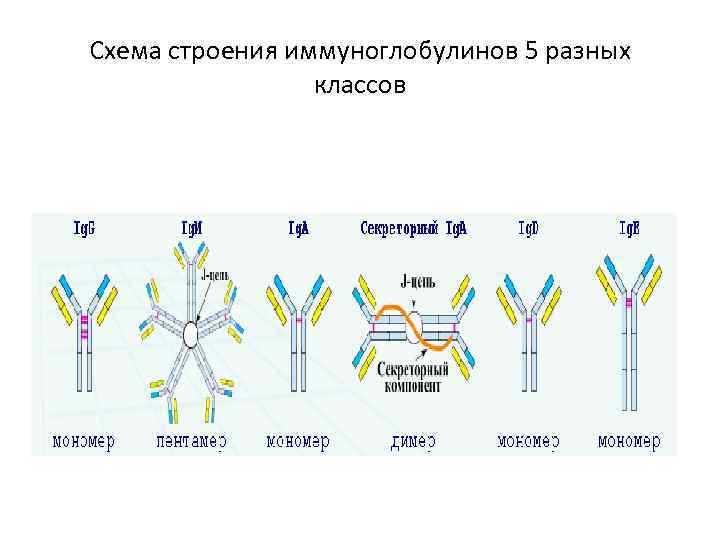
Схема строения иммуноглобулинов 5 разных классов
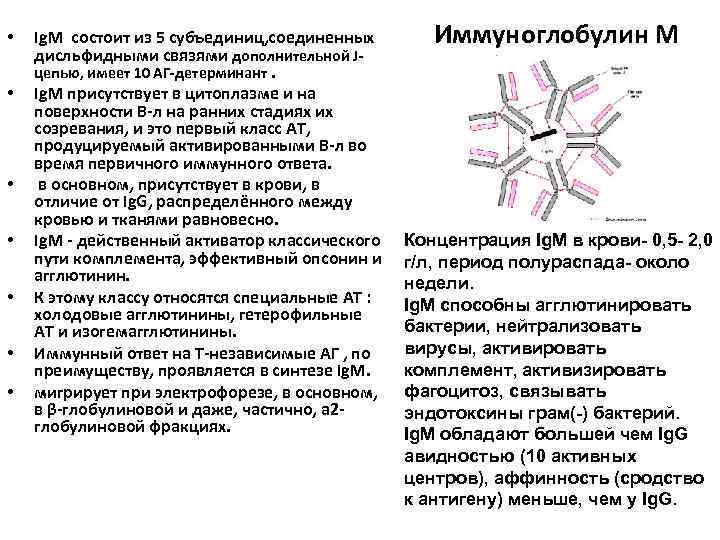
• • Ig. M состоит из 5 субъединиц, соединенных дисльфидными связями дополнительной J- цепью, имеет 10 АГ-детерминант. Ig. M присутствует в цитоплазме и на поверхности В-л на ранних стадиях их созревания, и это первый класс АТ, продуцируемый активированными В-л во время первичного иммунного ответа. в основном, присутствует в крови, в отличие от Ig. G, распределённого между кровью и тканями равновесно. Ig. M - действенный активатор классического пути комплемента, эффективный опсонин и агглютинин. К этому классу относятся специальные АТ : холодовые агглютинины, гетерофильные АТ и изогемагглютинины. Иммунный ответ на Т-независимые АГ , по преимуществу, проявляется в синтезе Ig. M. мигрирует при электрофорезе, в основном, в β-глобулиновой и даже, частично, a 2 глобулиновой фракциях. Иммуноглобулин М Концентрация Ig. M в крови- 0, 5 - 2, 0 г/л, период полураспада- около недели. Ig. M способны агглютинировать бактерии, нейтрализовать вирусы, активировать комплемент, активизировать фагоцитоз, связывать эндотоксины грам(-) бактерий. Ig. M обладают большей чем Ig. G авидностью (10 активных центров), аффинность (сродство к антигену) меньше, чем у Ig. G.

Ig М • Ig. M наиболее ранний класс антител, образующихся при первичном попадании антигена в организм. Наличие Ig. M антител к соответствующему возбудителю свидетельствует о свежем инфицировании (текущем инфекционном процессе). Антитела к антигенам грамотрицательных бактерий, жгутиковым антигенам преимущественно Ig. M антитела. Ig. M основной класс иммуноглобулинов, синтезируемых у новорожденных и младенцев. Ig. M у новорожденных это показатель внутриутробного заражения (краснуха, ЦМВ, токсоплазмоз и другие внутриутробные инфекции), поскольку материнские Ig. M через плаценту не проходят.
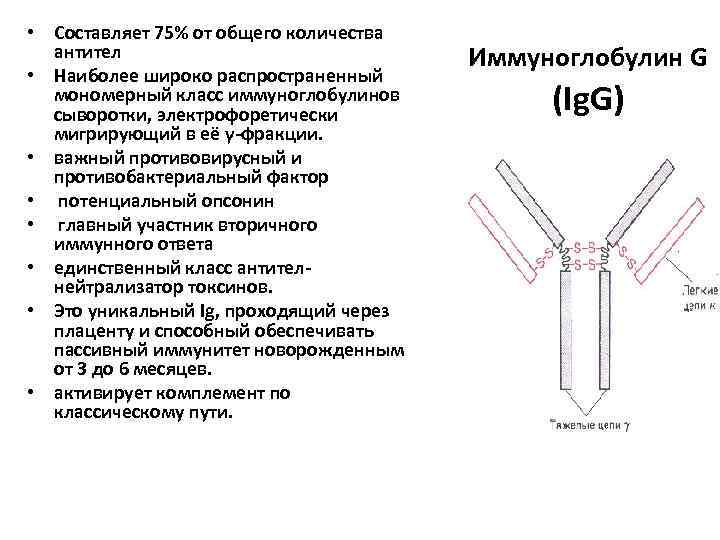
• Составляет 75% от общего количества антител • Наиболее широко распространенный мономерный класс иммуноглобулинов сыворотки, электрофоретически мигрирующий в её γ-фракции. • важный противовирусный и противобактериальный фактор • потенциальный опсонин • главный участник вторичного иммунного ответа • единственный класс антител- нейтрализатор токсинов. • Это уникальный Ig, проходящий через плаценту и способный обеспечивать пассивный иммунитет новорожденным от 3 до 6 месяцев. • активирует комплемент по классическому пути. Иммуноглобулин G (Ig. G)

Ig. G • Концентрация в крови- от 8 до 17 г/л, период полураспада- около 3 - 4 недель. Это основной класс иммуноглобулинов, защищающих организм от бактерий, токсинов и вирусов. В наибольшем количестве Ig. G- антитела вырабатываются на стадии выздоровления после инфекционного заболевания (поздние или 7 S антитела), при вторичном иммунном ответе. Ig. G 1 и Ig. G 4 специфически (через Fab- фрагменты) связывают возбудителей (опсонизация), благодаря Fc- фрагментам Ig. G взаимодействуют с Fc- рецепторам фагоцитов, способствуя фагоцитозу и лизису микроорганизмов. Ig. G способны нейтрализовать бактериальные экзотоксины, связывать комплемент. Только Ig. G способны транспортироваться через плаценту от матери к плоду (проходить через плацентарный барьер) и обеспечивать защиту материнскими антителами плода и новорожденного. В отличие от Ig. M- антител, Ig. G- антитела относятся к категории поздних- появляются позже и более длительно выявляются в крови.

Подклассы Ig. G • В зависимости от типа тяжёлой цепи, иммуноглобулины класса G подразделяются на 4 подкласса: Ig. G 1–Ig. G 4 • Ig. G 1 (70%) > Ig. G 2 (20%) > Ig. G 3 (6%) і Ig. G 4 (4%) • Структура шарнирного участка заметно отличается у представителей различных подклассов иммуноглобулина G (наиболее длинный – у Ig. G 3, самый короткий – у Ig. G 2. • В целом, гибкость и подвижность частей молекулы относительно друга у подклассов иммуноглобулина G снижается в ряду: Ig. G 3 > Ig. G 1 > Ig. G 4 > Ig. G 2

Функции подклассов Ig. G • наиболее активен подкласс Ig. G 3, шарнирная область которого обеспечивает молекуле антител максимальное число степеней свободы • По способности взаимодействовать с С 1 q на первом месте стоит подкласс Ig. G 3 • У человека все подклассы Ig. G способны активно проникать через плаценту в организм плода, создавая пассивный иммунитет • Ig. G 2 человека играет ключевую роль в инактивации инкапсулированных бактерий
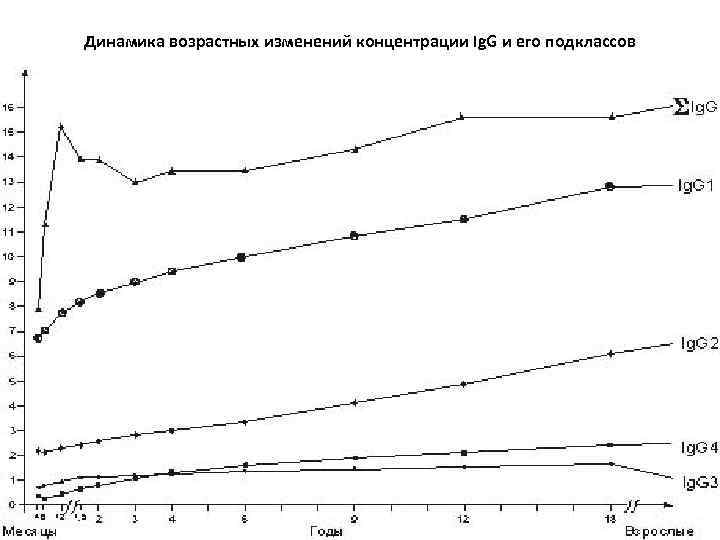
Динамика возрастных изменений концентрации Ig. G и его подклассов

Концентрация подклассов Ig. G у взрослых (г/л) • • Ig. G 1 - 4, 9– 11, 4; Ig. G 2 - 1, 5– 6, 4; Ig. G 3 - 0, 2– 1, 1; Ig. G 4 - 0, 08– 1, 4
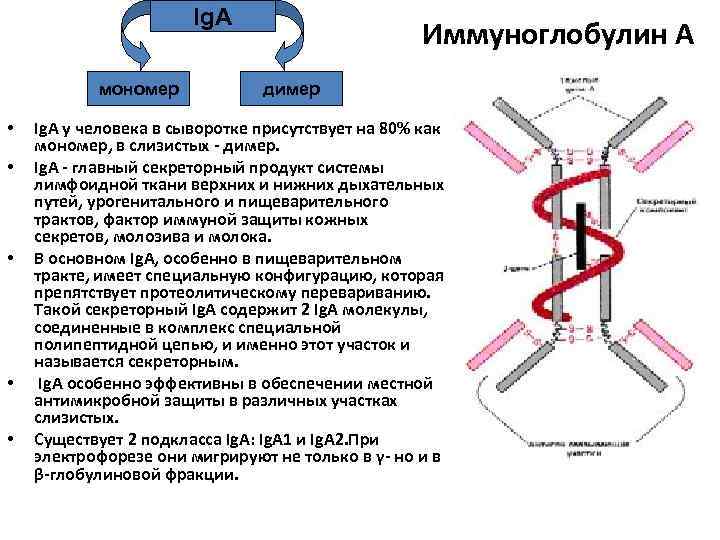
Ig. A мономер • • • Иммуноглобулин А димер Ig. A у человека в сыворотке присутствует на 80% как мономер, в слизистых - димер. Ig. A - главный секреторный продукт системы лимфоидной ткани верхних и нижних дыхательных путей, урогенитального и пищеварительного трактов, фактор иммуной защиты кожных секретов, молозива и молока. В основном Ig. A, особенно в пищеварительном тракте, имеет специальную конфигурацию, которая препятствует протеолитическому перевариванию. Такой секреторный Ig. A содержит 2 Ig. A молекулы, соединенные в комплекс специальной полипептидной цепью, и именно этот участок и называется секреторным. Ig. A особенно эффективны в обеспечении местной антимикробной защиты в различных участках слизистых. Существует 2 подкласса Ig. A: Ig. A 1 и Ig. A 2. При электрофорезе они мигрируют не только в γ- но и в β-глобулиновой фракции.

• Ig. A не проходит через плацентарный барьер, уровень его у новорожденных около 1% от концентрации у взрослых (а к году этот показатель составляет всего 20 % от уровня взрослых). Поэтому новорожденным в первые дни жизни секреторные Ig. A поступают с молозивом матери, защищая их дыхательный пути и желудочно кишечный тракт до тех пор, пока не сформируются механизмы его синтеза в собственном организме. • Возраст 3 мес. многими авторами определяется как критический период; этот период особенно важен для диагностики врожденной или транзиторной недостаточности местного иммунитета. Уровня, характерного для взрослого человека, достигает примерно к 5 летнему возрасту

• • • Выделяют сывороточные Ig. A (мономер) и секреторные Ig. A (Ig. As). Сывороточные Ig. A составляют 1, 4 4, 2 г/л. Секреторные Ig. As находятся в слюне, пищеварительных соках, секрете слизистой носа, в молозиве. Они являются первой линией защиты слизистых, обеспечивая их местный иммунитет. Ig. As состоят из Ig мономера, J цепи и гликопротеина (секреторного компонента). Выделяют два изотипа Ig. A 1 преобладает в сыворотке, субкласс Ig. A 2 — в экстраваскулярных секретах. Секреторный компонент вырабатывается эпителиальными клетками слизистых оболочек и присоединяется к молекуле Ig. A в момент прохождения последней через эпителиальные клетки. Механизм секреции Ig. A на поверхности слизистой оболочки. Клетки слизистой синтезируют иммуноглобулиновый рецептор, который встраивается в базальную мембрану. Димер Ig. A связывается с этим рецептором и транспортируется к апикальной поверхности клетки с помощью эндоцитарной вакуоли. При расщеплении рецептора высвобождается Ig. A, который все еще связан с частью рецептора, получившей название «секреторный компонент» (secretory piece). Секреторный компонент повышает устойчивость молекул Ig. As к действию протеолитических ферментов. Основная роль Ig. A- обеспечение местного иммунитета слизистых. Они препятствуют прикреплению бактерий к слизистым, обеспечивают транспорт полимерных иммунных комплексов с Ig. A, нейтрализуют энтеротоксин, активируют фагоцитоз и систему комплемента.
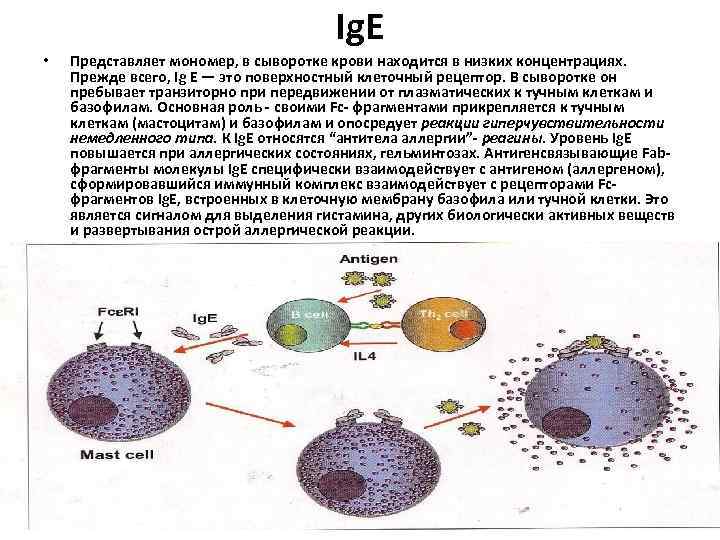
Ig. E • Представляет мономер, в сыворотке крови находится в низких концентрациях. Прежде всего, Ig E — это поверхностный клеточный рецептор. В сыворотке он пребывает транзиторно при передвижении от плазматических к тучным клеткам и базофилам. Основная роль - своими Fc- фрагментами прикрепляется к тучным клеткам (мастоцитам) и базофилам и опосредует реакции гиперчувствительности немедленного типа. К Ig. E относятся “антитела аллергии”- реагины. Уровень Ig. E повышается при аллергических состояниях, гельминтозах. Антигенсвязывающие Fab- фрагменты молекулы Ig. E специфически взаимодействует с антигеном (аллергеном), сформировавшийся иммунный комплекс взаимодействует с рецепторами Fc- фрагментов Ig. E, встроенных в клеточную мембрану базофила или тучной клетки. Это является сигналом для выделения гистамина, других биологически активных веществ и развертывания острой аллергической реакции.

Ig. D • Мономеры Ig. D обнаруживают на поверхности развивающихся В- лимфоцитов, в сыворотке находятся в крайне низких концентрациях (составляет менее 1% всех Ig сыворотки). Их биологическая роль точно не установлена. Полагают, что Ig. D участвуют в дифференциацировке В-клеток (мембранный Ig D вместе с Ig M являются критерием зрелости В лимфоцитов), способствуют развитию антиидиотипического ответа (участвуют в аутоиммунных процессах), развитии лимфопролиферативной патологии.

Роль антител в формировании иммунитета. Антитела имеют важное значение в формировании приобретенного постинфекционного и поствакцинального иммунитета. 1. Связываясь с токсинами, антитела нейтрализуют их, обеспечивая антитоксический иммунитет. 2. Блокируя рецепторы вирусов, антитела препятствуют адсорбции вирусов на клетках, участвуют в противовирусном иммунитете. 3. Комплекс антиген- антитело запускает классический путь активации комплемента с его эффекторными функциями (лизис бактерий, опсонизация, воспаление, стимуляция макрофагов). 4. Антитела принимают участие в опсонизации бактерий, способствуя более эффективному фагоцитозу. 5. Антитела способствуют выведению из организма (с мочой, желчью) растворимых антигенов в виде циркулирующих иммунных комплексов. Ig. G принадлежит наибольшая роль в антитоксическом иммунитете, Ig. M- в антимикробном иммунитете (фагоцитоз корпускулярных антигенов), особенно в отношении грамотрицательных бактерий, Ig. A- в противовирусном иммунитете (нейтрализация вирусов), Ig. As- в местном иммунитете слизистых оболочек, Ig. E- в реакциях гиперчувствительности немедленного типа.

Циркулирующие иммуноглобулины могут обеспечивать следующие формы антибактериальной защиты: • нейтрализацию бактериальных токсинов, например, столбнячного. • инактивацию факторов вирулентности и распространения бактерий, например, гиалуронидазы • блокаду бактериальных рецепторов ростовых факторов, например железосвязывающих белков. • опсонизирующий эффект для фагоцитоза бактерий • литический эффект через комплемент • блокаду подвижности бактериальных органоидов движения • предотвращение прикрепления бактерий к клеткам организма путём занятия соответствующих адгезивных молекул

МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА • настоящее время методами биотехнологии и/или генной инженерии получают иммуноглобулины, продуцируемые одним клоном клеток. • Они называются моноклональными антителами. Их продуценты — клетки-гибридомы, являющиеся потомками, полученными при скрещивании Влимфоцита (ПК) с опухолевой клеткой. • От плазматической клетки-гибридома наследуется способность к синтезу АТ, а от опухолевой клетки — способность длительно культивироваться вне организма.
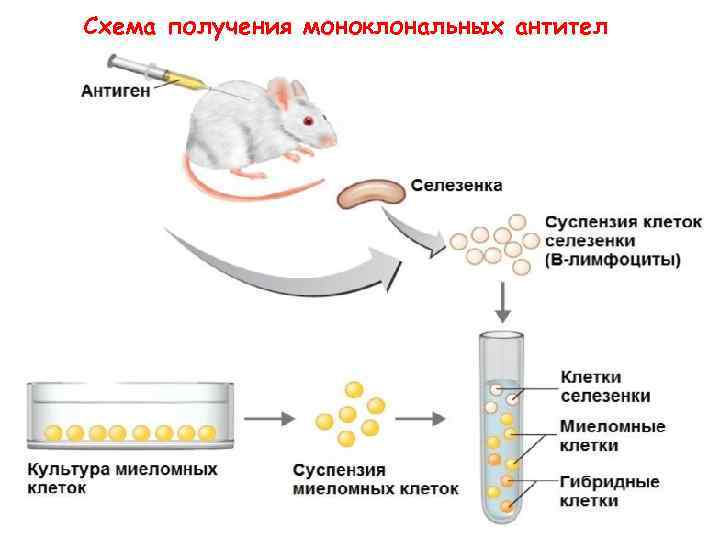
Схема получения моноклональных антител
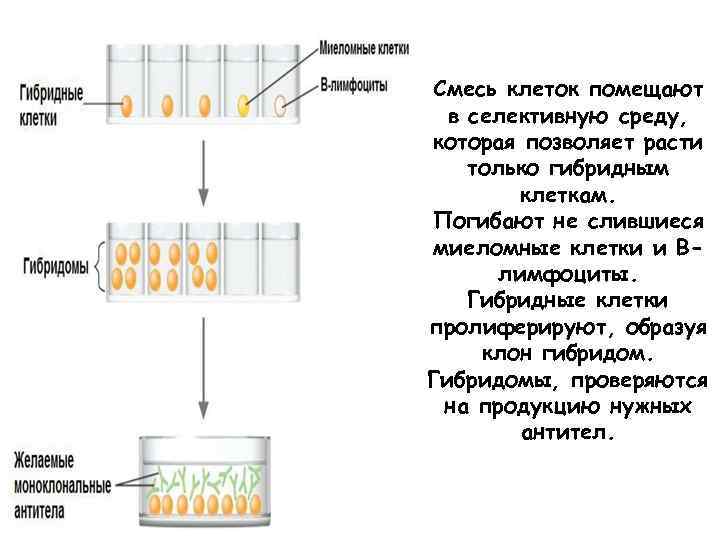
Смесь клеток помещают в селективную среду, которая позволяет расти только гибридным клеткам. Погибают не слившиеся миеломные клетки и Влимфоциты. Гибридные клетки пролиферируют, образуя клон гибридом. Гибридомы, проверяются на продукцию нужных антител.

«Мышиные фабрики» по производству моноклональных антител • Для получения больших объемов жидкости, содержащей моноклональные антитела, гибридомы могут быть введены внутрибрюшинно мышам реципиентам. • В результате в брюшной полости вырастает солидная опухоль и накапливается асцитическая жидкость, являющаяся источником моноклональных антител.

Применение МКАТ • • • Они являются наиболее четким инструментом поиска самых различных молекулярных структур клеток и тканей. С их помощью выявлена и продолжает изучаться молекулярная характеристика по CD антигенам клеток иммунной системы. Уточняются процессы дифференцировки иммунологически значимых клеток, их относительного участия в различных функциональных проявлениях, выясняется связь клеток иммунитета с клетками иных систем организма. В медицинской практике наибольшее применение нашли в онкологии. С помощью меченых АТ определяются метастазы различных форм опухолевого поражения для выработки наиболее адекватной терапии. Во всем мире ведутся обширные исследования в области использования МКАТ в качестве вектора, доставляющие фармакологические, токсические препараты в пораженные раковые и другие патологически измененные клетки. У нас в стране наиболее активно в этом направлении работает С. Г. Егорова (МГУ). Вклад Г. Келлера и Ц. Милыптейна в разработку технологии получения МАТ оценен присуждением им в 1984 г. Нобелевской премии по медицине.

Области применения моноклональных антител • идентификация субпопуляций лимфоцитов человека • выделение клеток • установление функций молекул клеточной поверхности • определение группы крови • диагностика опухолей и локализация опухолей • иммунорадиометрический анализ • анализ сложных смесей антигенов • анализ эмбрионального развития • анализ иммунного ответа • искусственные ферменты

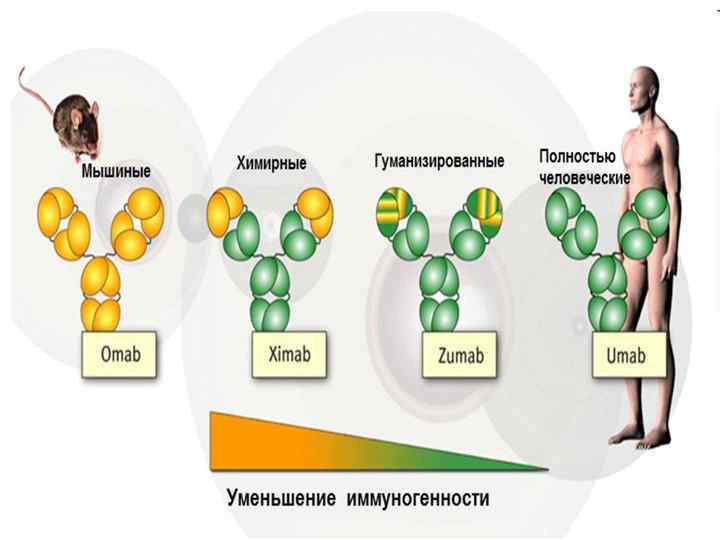
Терапевтические моноклональные антитела • • Ученые сумели принудить клетки грызунов к выработке антител с человеческими Fc-фрагментами (химерные АТ) Константная часть мышиных антител замещена соответствующей константной областью иммуноглобулина человека и в своей структуре имеют более 65% человеческого иммуноглобулина. Гуманизированные моноклональные антитела – до 95% состоят из человеческого иммуноглобулина. Трансгенные технологии (фаговый дисплей) были использованы для создания полностью человеческих моноклональных антител Моноклональные антитела, в отличие от традиционных препаратов, высокоспецифичны к определенным мишеням - антигенам. Поэтому, использование моноклональных антител в качестве терапевтических агентов стало для медицины стратегическим этапом в смене концепции лечения – от неспецифической к специфической (таргетной) терапии.
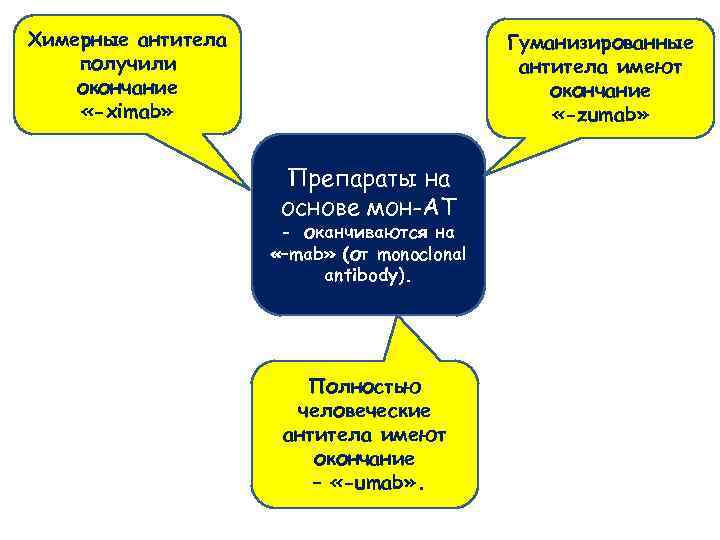
Химерные антитела получили окончание «-ximab» Гуманизированные антитела имеют окончание «-zumab» Препараты на основе мон-АТ - оканчиваются на «–mab» (от monoclonal antibody). Полностью человеческие антитела имеют окончание – «-umab» .
АНТИТЕЛА 2.pptx