ПиБАД_5_Антиокислители.ppt
- Количество слайдов: 17
 Антиокислители Современные представления о механизме окисления органических веществ, в том числе липидов, основаны на перекисной теории Баха. Энглера и теории цепных вырожденно разветвленных реакций Н. Н. Семенова В соответствии с молекулярно-кинетической теорией в реакцию способны вступать не все молекулы, а только активные, т. е. обладающие определенным избытком энергии. Такими свойствами обладают молекулы, имеющие свободную валентность – свободный радикалы.
Антиокислители Современные представления о механизме окисления органических веществ, в том числе липидов, основаны на перекисной теории Баха. Энглера и теории цепных вырожденно разветвленных реакций Н. Н. Семенова В соответствии с молекулярно-кинетической теорией в реакцию способны вступать не все молекулы, а только активные, т. е. обладающие определенным избытком энергии. Такими свойствами обладают молекулы, имеющие свободную валентность – свободный радикалы.
 Для отрыва водорода от метиленовой группы радикала жирных кислот или разрыва двойной связи требуется определенная энергия. Этой энергией может быть энергия света (фотохимическое инициирование) или теплота (нагревание) в случаях жидкофазного окисления – воздействие ионизирующей радиации (рентгеновских лучей, γ-лучей, быстрых электронов, αчастиц, нейтронов, протонов). Свободные радикалы в дальнейшем могут реагировать, например, с другими радикалами, образуя полимеры, или кислородом воздуха, с образованием первичных продуктов окисления – пероксидных радикалов, пероксидов или гидропероксидов.
Для отрыва водорода от метиленовой группы радикала жирных кислот или разрыва двойной связи требуется определенная энергия. Этой энергией может быть энергия света (фотохимическое инициирование) или теплота (нагревание) в случаях жидкофазного окисления – воздействие ионизирующей радиации (рентгеновских лучей, γ-лучей, быстрых электронов, αчастиц, нейтронов, протонов). Свободные радикалы в дальнейшем могут реагировать, например, с другими радикалами, образуя полимеры, или кислородом воздуха, с образованием первичных продуктов окисления – пероксидных радикалов, пероксидов или гидропероксидов.
 Пероксиды (гидропероксиды) являются нестойкими веществами и способны разрушаться с образованием вторичных продуктов окисления: альдегидов, кетонов, оксикислот, эпоксисоединений и т. д. Все продукты окисления являются токсичными для организма человека и животных, кроме того они изменяют в нежелательном направлении органолептические свойства продуктов. Поэтому в ходе технологического процесса необходимо обеспечить торможение процессов окисления.
Пероксиды (гидропероксиды) являются нестойкими веществами и способны разрушаться с образованием вторичных продуктов окисления: альдегидов, кетонов, оксикислот, эпоксисоединений и т. д. Все продукты окисления являются токсичными для организма человека и животных, кроме того они изменяют в нежелательном направлении органолептические свойства продуктов. Поэтому в ходе технологического процесса необходимо обеспечить торможение процессов окисления.
 Способы торможения процесса окисления Ø Ø Физические: - понижение температуры хранения; - ограничение доступа света; - уменьшение количества кислорода в таре. Химические: - устранение активаторов окисления; - уменьшение степени ненасыщенности липидов продукта; - введение антиокислителей.
Способы торможения процесса окисления Ø Ø Физические: - понижение температуры хранения; - ограничение доступа света; - уменьшение количества кислорода в таре. Химические: - устранение активаторов окисления; - уменьшение степени ненасыщенности липидов продукта; - введение антиокислителей.
 Классификация антиокислителей Кроме деления антиокислителей по происхождению на натуральные и синтетические, в настоящее время более часто применяется их классификация по принципу действия. По принципу действия антиокислители делятся на три группы: 1. АО фенольного типа; 2. Серосодержащие АО; 3. АО, образующие соединения-включения.
Классификация антиокислителей Кроме деления антиокислителей по происхождению на натуральные и синтетические, в настоящее время более часто применяется их классификация по принципу действия. По принципу действия антиокислители делятся на три группы: 1. АО фенольного типа; 2. Серосодержащие АО; 3. АО, образующие соединения-включения.
 Антиокислители фенольного типа Для их обозначения в научной литературе принято обозначение – In. H, т. е. ингибитор, имеющий «подвижный» атом водорода. Антиокислители фенольного типа вступают во взаимодействие со свободными радикалами, насыщая их валентность. Малоактивный свободный радикал ингибитора может взаимодействовать с другими радикалами (реакции 1. и 2) с образованием нетоксичных продуктов. Кроме того, при наличии в системе донора атома водорода, антиокислитель фенольного типа может восстановить свои свойства (реакция 3).
Антиокислители фенольного типа Для их обозначения в научной литературе принято обозначение – In. H, т. е. ингибитор, имеющий «подвижный» атом водорода. Антиокислители фенольного типа вступают во взаимодействие со свободными радикалами, насыщая их валентность. Малоактивный свободный радикал ингибитора может взаимодействовать с другими радикалами (реакции 1. и 2) с образованием нетоксичных продуктов. Кроме того, при наличии в системе донора атома водорода, антиокислитель фенольного типа может восстановить свои свойства (реакция 3).
 Преимущества и недостатки использования АО фенольного типа Ø Преимущества: - хорошая растворимость в жирах; - взаимодействуют со свободными радикалами, препятствуя образованию первичных и вторичных продуктов окисления. Ø Недостатки: - вызывают опасения с точки зрения токсикологии; - расходуются в процессе торможения окисления.
Преимущества и недостатки использования АО фенольного типа Ø Преимущества: - хорошая растворимость в жирах; - взаимодействуют со свободными радикалами, препятствуя образованию первичных и вторичных продуктов окисления. Ø Недостатки: - вызывают опасения с точки зрения токсикологии; - расходуются в процессе торможения окисления.
 Разрешенные в России АО фенольного типа n n n n n Е 306 Концентрат смеси токоферолов Е 307 Альфа-Токоферол Е 308 Гамма-Токоферол синтетический Е 309 Дельта-Токоферол синтетический Е 310 Пропилгаллат Е 311 Октилгаллат Е 312 Додецилгаллат Е 314 Гваяковая смола Е 320 Бутилгидроксианизол Е 321 Бутилгидрокситолуол ( «ионол» )
Разрешенные в России АО фенольного типа n n n n n Е 306 Концентрат смеси токоферолов Е 307 Альфа-Токоферол Е 308 Гамма-Токоферол синтетический Е 309 Дельта-Токоферол синтетический Е 310 Пропилгаллат Е 311 Октилгаллат Е 312 Додецилгаллат Е 314 Гваяковая смола Е 320 Бутилгидроксианизол Е 321 Бутилгидрокситолуол ( «ионол» )
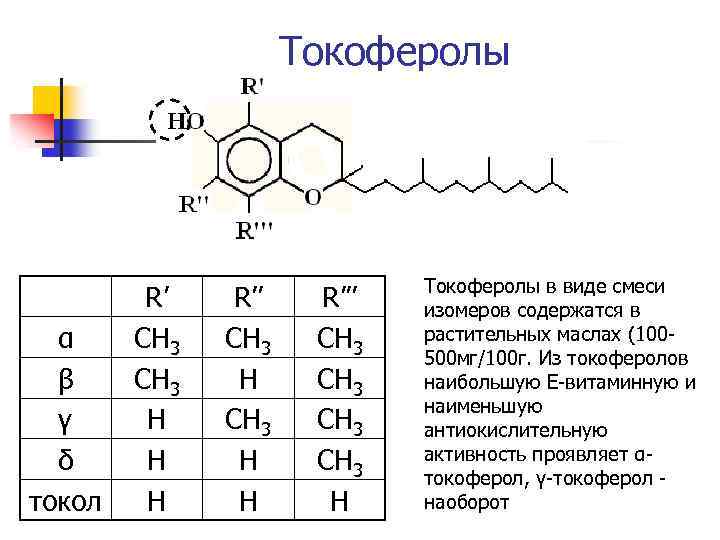 Токоферолы α β γ δ токол R’ СН 3 Н Н Н R’’ СН 3 Н Н R’’’ СН 3 Н Токоферолы в виде смеси изомеров содержатся в растительных маслах (100500 мг/100 г. Из токоферолов наибольшую Е-витаминную и наименьшую антиокислительную активность проявляет αтокоферол, γ-токоферол - наоборот
Токоферолы α β γ δ токол R’ СН 3 Н Н Н R’’ СН 3 Н Н R’’’ СН 3 Н Токоферолы в виде смеси изомеров содержатся в растительных маслах (100500 мг/100 г. Из токоферолов наибольшую Е-витаминную и наименьшую антиокислительную активность проявляет αтокоферол, γ-токоферол - наоборот
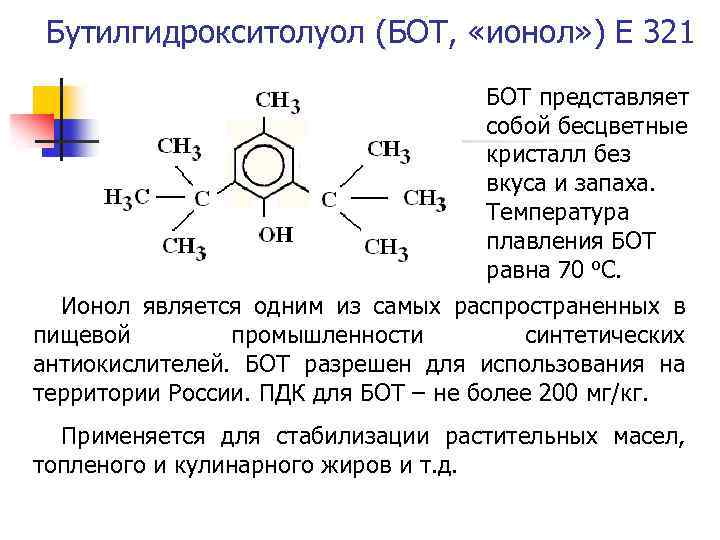 Бутилгидрокситолуол (БОТ, «ионол» ) Е 321 БОТ представляет собой бесцветные кристалл без вкуса и запаха. Температура плавления БОТ равна 70 о. С. Ионол является одним из самых распространенных в пищевой промышленности синтетических антиокислителей. БОТ разрешен для использования на территории России. ПДК для БОТ – не более 200 мг/кг. Применяется для стабилизации растительных масел, топленого и кулинарного жиров и т. д.
Бутилгидрокситолуол (БОТ, «ионол» ) Е 321 БОТ представляет собой бесцветные кристалл без вкуса и запаха. Температура плавления БОТ равна 70 о. С. Ионол является одним из самых распространенных в пищевой промышленности синтетических антиокислителей. БОТ разрешен для использования на территории России. ПДК для БОТ – не более 200 мг/кг. Применяется для стабилизации растительных масел, топленого и кулинарного жиров и т. д.
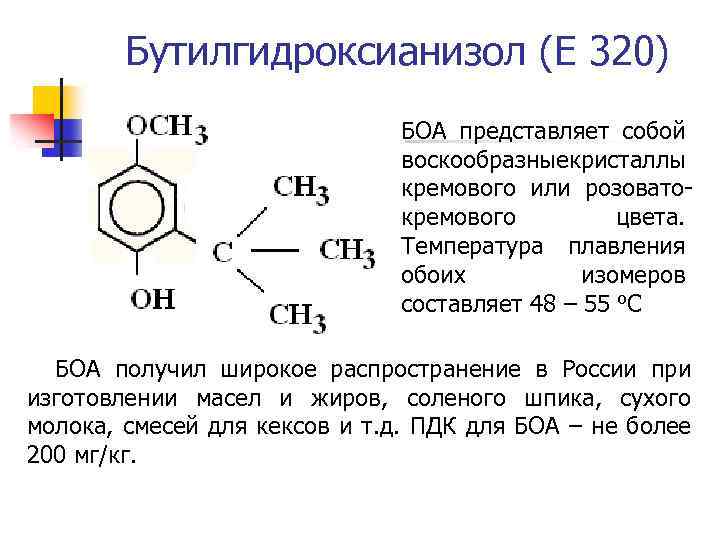 Бутилгидроксианизол (Е 320) БОА представляет собой воскообразные ристаллы к кремового или розоватокремового цвета. Температура плавления обоих изомеров составляет 48 – 55 о. С БОА получил широкое распространение в России при изготовлении масел и жиров, соленого шпика, сухого молока, смесей для кексов и т. д. ПДК для БОА – не более 200 мг/кг.
Бутилгидроксианизол (Е 320) БОА представляет собой воскообразные ристаллы к кремового или розоватокремового цвета. Температура плавления обоих изомеров составляет 48 – 55 о. С БОА получил широкое распространение в России при изготовлении масел и жиров, соленого шпика, сухого молока, смесей для кексов и т. д. ПДК для БОА – не более 200 мг/кг.
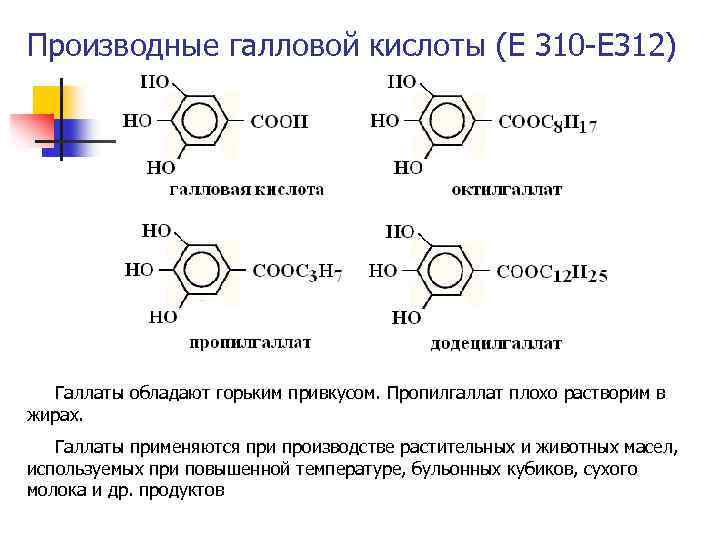 Производные галловой кислоты (Е 310 -Е 312) Галлаты обладают горьким привкусом. Пропилгаллат плохо растворим в жирах. Галлаты применяются при производстве растительных и животных масел, используемых при повышенной температуре, бульонных кубиков, сухого молока и др. продуктов
Производные галловой кислоты (Е 310 -Е 312) Галлаты обладают горьким привкусом. Пропилгаллат плохо растворим в жирах. Галлаты применяются при производстве растительных и животных масел, используемых при повышенной температуре, бульонных кубиков, сухого молока и др. продуктов
 Серосодержащие антиокислители взаимодействуют с пероксидами или гидропероксидами по следующей схеме: Серосодержащие антиокислители не разрешены к использованию в Российской Федерации. Одним из таких антиокислителей является Е 388 тиодипропионовая кислота
Серосодержащие антиокислители взаимодействуют с пероксидами или гидропероксидами по следующей схеме: Серосодержащие антиокислители не разрешены к использованию в Российской Федерации. Одним из таких антиокислителей является Е 388 тиодипропионовая кислота
 Преимущества и недостатки использования серосодержащих антиокислителей Преимущества: Ø взаимодействуют с пероксидами, блокируя атом кислорода; Ø хорошо растворяются в жирах. Недостатки: Ø не препятствуют образованию вторичных продуктов окисления; Ø вызывают опасения с точки зрения токсикологии; Ø расходуются в процессе торможения окисления.
Преимущества и недостатки использования серосодержащих антиокислителей Преимущества: Ø взаимодействуют с пероксидами, блокируя атом кислорода; Ø хорошо растворяются в жирах. Недостатки: Ø не препятствуют образованию вторичных продуктов окисления; Ø вызывают опасения с точки зрения токсикологии; Ø расходуются в процессе торможения окисления.
 Антиокислители, образующие соединения включения Карбамид (Е 927 b) В пищевой промышленности используется в настоящее время в качестве улучшителя при изготовлении муки и хлеба Карбамид взаимодействует со свободными жирными кислотами по следующей схеме:
Антиокислители, образующие соединения включения Карбамид (Е 927 b) В пищевой промышленности используется в настоящее время в качестве улучшителя при изготовлении муки и хлеба Карбамид взаимодействует со свободными жирными кислотами по следующей схеме:
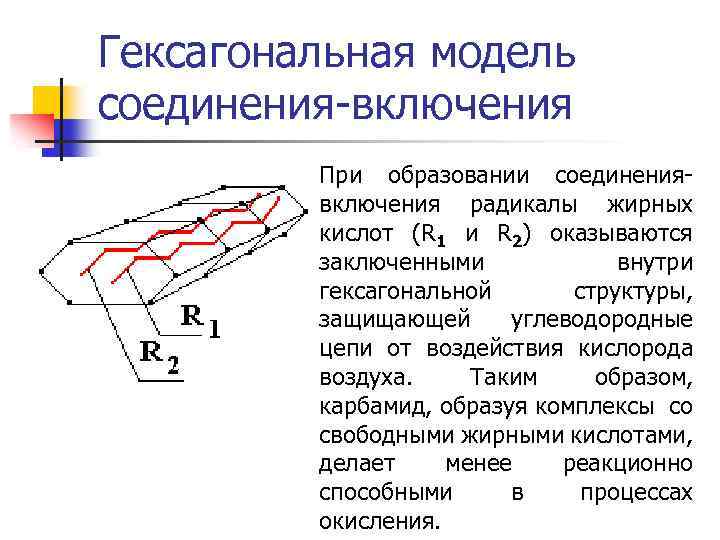 Гексагональная модель соединения-включения При образовании соединения- включения радикалы жирных кислот (R 1 и R 2) оказываются заключенными внутри гексагональной структуры, защищающей углеводородные цепи от воздействия кислорода воздуха. Таким образом, карбамид, образуя комплексы со свободными жирными кислотами, делает менее реакционно способными в процессах окисления.
Гексагональная модель соединения-включения При образовании соединения- включения радикалы жирных кислот (R 1 и R 2) оказываются заключенными внутри гексагональной структуры, защищающей углеводородные цепи от воздействия кислорода воздуха. Таким образом, карбамид, образуя комплексы со свободными жирными кислотами, делает менее реакционно способными в процессах окисления.
 Преимущества и недостатки использования карбамида Преимущества: Ø препятствует образованию первичных и вторичных продуктов окисления; Ø практически нетоксичен. Недостатки: Ø плохо растворим в жирах; Ø расходуется в процессе торможения окисления.
Преимущества и недостатки использования карбамида Преимущества: Ø препятствует образованию первичных и вторичных продуктов окисления; Ø практически нетоксичен. Недостатки: Ø плохо растворим в жирах; Ø расходуется в процессе торможения окисления.


