Арс.Кар-антидиабетические средства.pptx
- Количество слайдов: 25

«АНТИДИАБЕТИЧЕСКИЕ СРЕДСТВА» Выполнила: студентка 3 курса 14 группы Арсентьева Карина

АНТИДИАБЕТИЧЕСКИЕ СРЕДСТВА, ПОНИЖАЮТ СОДЕРЖАНИЕ САХАРА В КРОВИ. К НИМ ОТНОСЯТСЯ ИНСУЛИН И ПРЕПАРАТЫ НА ЕГО ОСНОВЕ, А ТАКЖЕ ПРОИЗВОДНЫЕ СУЛЬФОНИЛМОЧЕВИНЫ И БИГУАНИДИНА. ДЛЯ МЕД. ЦЕЛЕЙ ПРИМЕНЯЮТ ГЛ. ОБР. ИНСУЛИН, ПОЛУЧАЕМЫЙ ИЗ ПОДЖЕЛУДОЧНЫХ ЖЕЛЕЗ СВИНЕЙ И КРУПНОГО РОГАТОГО СКОТА. РАЗРАБОТАНЫ МЕТОДЫ БИОСИНТЕЗА ИНСУЛИНА ЧЕЛОВЕКА. ИНСУЛИНЫ РАЗЛ. ЖИВОТНЫХ И ЧЕЛОВЕКА НЕСК. ОТЛИЧАЮТСЯ ПО ИММУНОЛОГИЧ. СВВАМ. ВАЖНЕЙШИЙ ПОКАЗАТЕЛЬ КАЧ-ВА ПРЕПАРАТОВ ИНСУЛИНА-СТЕПЕНЬ ОЧИСТКИ ОТ БЕЛКОВЫХ ПРИМЕСЕЙ, ГЛ. ОБР. ОТ ПРОИНСУЛИНА.

КЛАССИФИКАЦИЯ ГИПОГЛИКЕМИЧЕСКИХ СРЕДСТВ: v производные сульфонилмочевины (глибенкламид, гликвидон, гликлазид, глимепирид, глипизид, хлорпропамид); v - меглитиниды (натеглинид, репаглинид); v - бигуаниды (буформин, метформин, фенформин); v - тиазолидиндионы (пиоглитазон, росиглитазон, циглитазон, энглитазон, троглитазон); v - ингибиторы альфа-глюкозидаз (акарбоза, миглитол); v - инкретиномиметики.

Фармакологическое действие сульфонилмочевины Действие производных сульфонилмочевины связано, главным образом, со стимуляцией бета-клеток поджелудочной железы, сопровождающейся мобилизацией и усилением выброса эндогенного инсулина. Основной предпосылкой для проявления их эффекта является наличие в поджелудочной железе функционально активных бета-клеток. На мембране бета-клеток производные сульфонилмочевины cвязываются со специфическими рецепторами, ассоциированными c АТФ-зависимыми калиевыми каналами. Ген рецептора сульфонилмочевины клонирован. Установлено, что классический высокоаффинный рецептор сульфонилмочевины (SUR-1) представляет собой белок с молекулярной массой 177 к. Да. В отличие от других производных сульфонилмочевины, глимепирид связывается с другим белком, сопряженным с АТФ-зависимыми калиевыми каналами и имеющим молекулярную массу 65 к. Да (SUR-X). Кроме того, в состав К+канала входит внутримембранная субъединица Kir 6. 2 (белок с молекулярной массой 43 к. Да), которая отвечает за транспорт ионов калия. Считают, что в результате этого взаимодействия происходит «закрытие» калиевых каналов бетаклеток. Повышение концентрации ионов К+ внутри клетки способствует деполяризации мембран, открытию потенциал-зависимых Ca 2+-каналов, увеличению внутриклеточного содержания ионов кальция. Результатом этого является высвобождение запасов инсулина из бета-клеток.

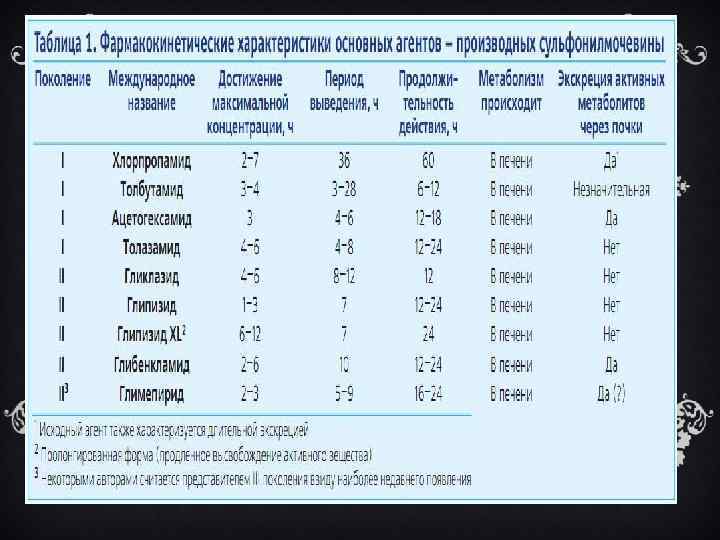
Производные сульфонилмочевины: I поколение: толбутамид, карбутамид, толазамид, ацетогексамид, хлорпропамид. II поколение: глибенкламид, глизоксепид, глиборнурил, гликвидон, гликлазид, глипизид. III поколение: глимепирид.


В настоящее время в России препараты сульфонилмочевины I поколения практически не применяют. Основное отличие препаратов II поколения от производных сульфонилмочевины I поколения — бóльшая активность (в 50– 100 раз), что позволяет использовать их в более низких дозах и, соответственно, снижает вероятность возникновения побочных эффектов. Отдельные представители гипогликемических производных сульфонилмочевины I и II поколения различаются по активности и переносимости. Так, суточная доза препаратов I поколения — толбутамида и хлорпропамида — 2 и 0, 75 г соответственно, а препаратов II поколения — глибенкламида — 0, 02 г; гликвидона — 0, 06– 0, 12 г. Препараты II поколения обычно лучше переносятся больными.

Гликлазид — второе по частоте назначения после глибенкламида пероральное гипогликемическое средство. Помимо того, что гликлазид оказывает гипогликемическое действие, он улучшает гематологические показатели, реологические свойства крови, положительно влияет на систему гемостаза и микроциркуляции; предупреждает развитие микроваскулитов, в т. ч. поражение сетчатой оболочки глаза; подавляет агрегацию тромбоцитов, значительно увеличивает индекс относительной дезагрегации, повышает гепариновую и фибринолитическую активность, увеличивает толерантность к гепарину, а также проявляет антиоксидантные свойства. Гликвидон является ЛС, которое можно назначать пациентам с умеренно выраженными нарушениями функции почек, т. к. через почки выводится лишь 5% метаболитов, остальное (95%) — через кишечник. Глипизид, обладая выраженным эффектом, представляет минимальную опасность в плане гипогликемических реакций, поскольку не кумулирует и не имеет активных метаболитов.
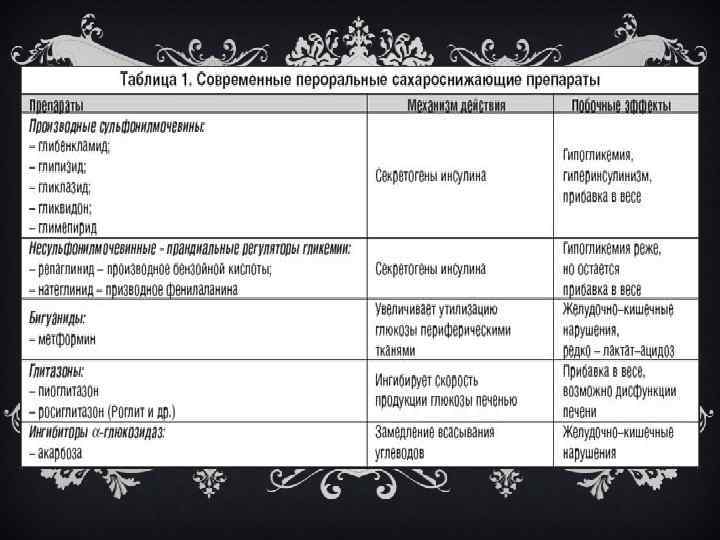

Меглитиниды — прандиальные регуляторы (репаглинид, натеглинид). Репаглинид — производное бензойной кислоты. Несмотря на отличие по химической структуре от производных сульфонилмочевины, он также блокирует АТФ-зависимые калиевые каналы в мембранах функционально активных бета-клеток островкового аппарата поджелудочной железы, вызывает их деполяризацию и открытие кальциевых каналов, индуцируя тем самым инкрецию инсулина. Инсулинотропный ответ на прием пищи развивается в течение 30 мин после применения и сопровождается понижением уровня глюкозы в крови в период приема пищи (концентрация инсулина между приемами пищи не повышается). Как и у производных сульфонилмочевины, основной побочный эффект — гипогликемия. С осторожностью назначают репаглинид больным с печеночной и/или почечной недостаточностью. Натеглинид — производное D-фенилаланина. В отличие от других пероральных сахароснижающих средств, эффект натеглинида на секрецию инсулина более быстрый, но менее стойкий. Применяют натеглинид преимущественно для снижения постпрандиальной гипергликемии при диабете типа 2.

Бигуаниды, которые начали использовать для лечения сахарного диабета типа 2 в 70 -е годы, не стимулируют секрецию инсулина бета-клетками поджелудочной железы. Их действие в основном определяется угнетением глюконеогенеза в печени (в т. ч. гликогенолиза) и повышением утилизации глюкозы периферическими тканями. Они также тормозят инактивирование инсулина и улучшают его связывание с инсулиновыми рецепторами (при этом повышается усвоение глюкозы и ее метаболизм). Бигуаниды (в отличие от производных сульфонилмочевины) не снижают уровень глюкозы в крови у здоровых людей и у больных диабетом типа 2 после ночного голодания, но существенно ограничивают его возрастание после приема пищи, не вызывая при этом гипогликемию

Гипогликемические бигуаниды — метформин и другие — также применяют при сахарном диабете типа 2. Помимо сахароснижающего действия, бигуаниды при длительном применении положительно влияют на липидный обмен. Препараты этой группы тормозят липогенез (процесс, при котором глюкоза и другие вещества превращаются в организме в жирные кислоты), активируют липолиз (процесс расщепления липидов, особенно содержащихся в жире триглицеридов, на составляющие их жирные кислоты под действием фермента липазы), понижают аппетит, способствуют уменьшению массы тела. В ряде случаев их применение сопровождается уменьшением содержания триглицеридов, холестерина и ЛПНП (определяемых натощак) в сыворотке крови. При сахарном диабете типа 2 нарушения углеводного обмена сочетаются с выраженными изменениями липидного обмена. Так, 85– 90% больных сахарным диабетом типа 2 имеют повышенную массу тела. Поэтому при сочетании сахарного диабета типа 2 с избыточной массой тела показаны ЛС, нормализующие липидный обмен.

Бигуаниды противопоказаны при наличии ацидоза и склонности к нему (провоцируют и усиливают накопление лактата), при состояниях, сопровождающихся гипоксией (в т. ч. сердечная и дыхательная недостаточность, острая фаза инфаркта миокарда, острая недостаточность мозгового кровообращения, анемия) и др. Побочные эффекты бигуанидов отмечаются чаще, чем у производных сульфонилмочевины (20% против 4%), прежде всего это побочные реакции со стороны ЖКТ: металлический привкус во рту, диспептические явления и др. В отличие от производных сульфонилмочевины, гипогликемия применении бигуанидов (например метформина) возникает очень редко. Лактацидоз, появляющийся иногда приеме метформина, относят к серьезным осложнениям, поэтому не следует назначать метформин при почечной недостаточности и состояниях, которые предрасполагают к его развитию — нарушение функции почек и/или печени, сердечная недостаточность, патология легких. Бигуаниды не следует назначать одновременно с циметидином, поскольку они конкурируют друг с другом в процессе канальцевой секреции в почках, что может привести к кумуляции бигуанидов, кроме того, циметидин снижает биотрансформацию бигуанидов в печени.


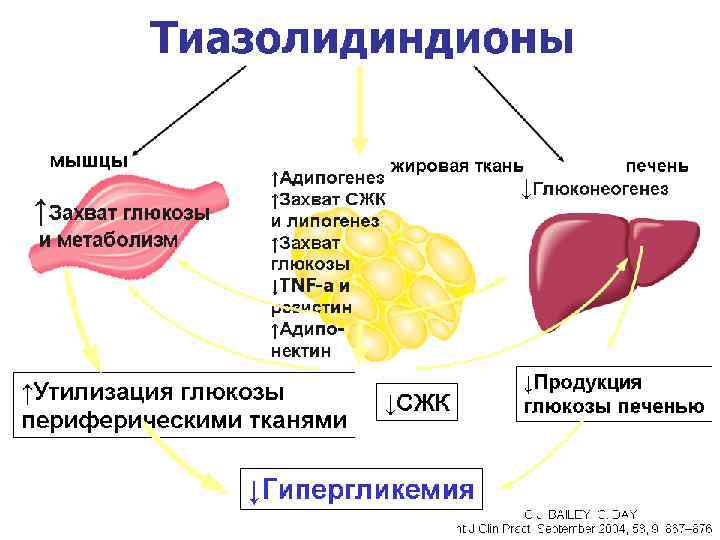
Тиазолидиндионы С 1997 года в клиническую практику вошли тиазолидиндионы (глитазоны), в основе химической структуры которых лежит тиазолидиновое кольцо. В эту новую группу противодиабетических средств входят пиоглитазон и росиглитазон. ЛС этой группы повышают чувствительность тканей-мишеней (мышцы, жировая ткань, печень) к инсулину, понижают синтез липидов в мышечных и жировых клетках. Тиазолидиндионы являются селективными агонистами ядерных рецепторов PPARγ (peroxisome proliferatoractivated receptor-gamma). У человека эти рецепторы находятся в основных для действия инсулина «тканях-мишенях» : в жировой ткани, в скелетной мускулатуре и печени. Ядерные рецепторы PPARγ регулируют транскрипцию инсулиноответственных генов, вовлеченных в контроль за продукцией, транспортом и утилизацией глюкозы
Для того чтобы тиазолидиндионы оказывали свой эффект, необходимо присутствие инсулина. Эти ЛС снижают инсулинорезистентность периферических тканей и печени, увеличивают расход инсулинозависимой глюкозы и уменьшают выброс глюкозы из печени; снижают средние уровни триглицеридов, увеличивают концентрацию ЛПВП и холестерина; предотвращают гипергликемию натощак и после приема пищи, а также гликозилирование гемоглобина.

Ингибиторы альфа-глюкозидаз (акарбоза, миглитол) тормозят расщепление поли- и олигосахаридов, уменьшая образование и всасывание глюкозы в кишечнике и предупреждая тем самым развитие постпрандиальной гипергликемии. Принятые с пищей углеводы в неизмененном виде попадают в нижние отделы тонкого и толстый кишечник, при этом всасывание моносахаридов пролонгируется до 3– 4 ч. В отличие от сульфонамидных гипогликемических средств они не увеличивают высвобождение инсулина и, следовательно, не вызывают гипогликеми

Показаниями к назначению ингибиторов альфаглюкозидаз являются сахарный диабет типа 2 при неэффективности диетотерапии (курс которой должен составлять не менее 6 мес), а также сахарный диабет типа 1 (в составе комбинированной терапии). Препараты этой группы могут вызывать диспептические явления, обусловленные нарушением переваривания и всасывания углеводов, которые метаболизируются в толстом кишечнике с образованием жирных кислот, углекислого газа и водорода. Поэтому при назначении ингибиторов альфаглюкозидаз необходимо строгое соблюдение диеты с ограниченным содержанием сложных углеводов, в т. ч. сахарозы

Инкретиномиметики В настоящее время появился принципиально новый класс гипогликемических средств — инкретиномиметики. Инкретины — гормоны, которые секретируются некоторыми типами клеток тонкого кишечника в ответ на прием пищи и стимулируют секрецию инсулина. Выделены два гормона — глюкагоноподобный полипептид (ГПП-1) и глюкозозависимый инсулинотропный полипептид (ГИП). К инкретиномиметикам относят 2 группы препаратов: - вещества, имитирующие действие (ГПП-1) — аналоги ГПП-1 (лираглутид, эксенатид, ликсисенатид); - вещества, пролонгирующие действие эндогенного ГПП-1 вследствие блокады дипептидилпептидазы-4 (ДПП-4) — фермента, разрушающего ГПП-1 — ингибиторы ДПП-4 (ситаглиптин, вилдаглиптин, саксаглиптин, линаглиптин, алоглиптин)

Агонисты ГПП-1 Эксенатид (Баета) был выделен из слюны гигантской ящерицы Gila monster. Аминокислотная последовательность эксенатида на 50% совпадает с человеческим ГПП-1. Исследования in vitro показали, что препарат связывается с рецепторами к ГПП-1 и устойчив к инактивации ДПП-4. Кроме того, при подкожном введении эксенатида пациентам с СД 2 -го типа пик концентрации в плазме достигался через 2– 3 часа, а период полужизни составлял 2– 6 часов. Эти фармакологические свойства эксенатида позволяют проводить терапию данным препаратом в виде двух подкожных инъекций в день перед завтраком и перед ужином, что достаточно эффективно снижает уровень гликемии на протяжении всех суток. Таким образом, лечение эксенатидом может рассматриваться как в качестве монотерапии СД 2 -го типа, так и в составе комбинированной сахароснижающей терапии.

Наиболее перспективной представляется комбинация ингибиторов ДПП-4 и метформина, что позволяет воздействовать на все основные патогенетические механизмы развития СД 2 -го типа — инсулинорезистентность, секреторный дефект бета-клеток и гиперпродукцию глюкозы печенью.
Арс.Кар-антидиабетические средства.pptx