4 Антибиотикорезистентность Основные правила.pptx
- Количество слайдов: 69

Антибиотикорезистентность Основные правила Ольга Ершова

Пациентка Б. Д. Возраст: 25, дата поступления: 23. 09. 2014 дата выбытия: 26. 05. 2016 Число койко‐дней: 611, выполнено 10 оперативных вмешательств на головном мозге, связанных с шунт‐системами 5 генов вирулентности клебсиелл – uge 2 wab. G, kfu, fim. H, alls Механизмы антибиотикорезистентности: Устойчивость к бета‐лактамам – гены бета‐лактамаз (SHV), БЛРС (CTX‐M), карбапенемаз (OXA‐ 48) Устойчивость к другим классам препаратов – интегроны (1 и 2 классов), модификация проницаемости

Hara G. L. et al. Detection, treatment, and prevention of carbapenemase‐producing Enterobacteriaceae: recommendations from an International Working Group //Journal of chemotherapy. – 2013. – Т. 25. – №. 3. – С. 129‐ 140.


Резистентность к карбапенемам K. pneumoniae, E. coli, E. cloacae, S. marcescens OXA‐ 48, NDM‐ 1, VIM‐ 1/4 Skleenova E. et al. ICAAC 2013 C 2‐ 1092

В США объявлено о первой смерти от супербактерии, устойчивой к 26 антибиотикам (Pan‐Resistant New Delhi Metallo‐Beta‐Lactamase‐Producing Klebsiella pneumoniae) Among >250 CRE isolate reports collected as part of the Emerging Infections Program, approximately 80% remained susceptible to at least one aminoglycoside and nearly 90% were susceptible to tigecycline. CDC recommends that when these bacteria are identified, facilities ensure that appropriate infection control contact precautions are instituted to prevent transmission and that health care contacts are evaluated for evidence of transmission. The patient in this report had inpatient health care exposure in India before receiving care in the United States. Health care facilities should obtain a history of health care exposures outside their region upon admission and consider screening for CRE when patients report recent exposure outside the United States or in regions of the United States known to have a higher incidence of CRE Chen L, Todd R, Kiehlbauch J, Walters M, Kallen A. Notes from the Field: Pan‐Resistant New Delhi Metallo‐Beta ‐Lactamase‐Producing Klebsiella pneumoniae — Washoe County, Nevada, 2016. MMWR Morb Mortal Wkly Rep 2017; 66: 33. DOI: http: //dx. doi. org/10. 15585/mmwr. mm 6601 a 7

• • • Коллеги, а что нынче с применением антисептиков при резистентных инфекциях? Когда‐то, помнится, спирт, гипохлорид На применяли. Что скажут фармакологи? 16 января 2017 21: 04 Полная резистентность ‐ явление крайне редкое. Это обнадёживает. А вот по поводу появления за короткое время столь агрессивных микробов с удивительным сочетанием самых негативных свойств ‐ это наверняка дело рук человеческих, бак. лабораторий. А не от того, что АБ широко применяют. Если бы в первые секунды произвели асептическую обработку раны, то ничего бы такого не произошло. Очередная страшилка для народа, Конечно же в таких случаях , надо использовать все изобретенные антибиотики, даже запрещенные. . Второй метод борьбы, думаю это изобретение метода пресечения образования штаммов или уничтожение памяти бактерии. http: //vrachirf. ru/away? key=51719 a 8 e‐b 270‐ 4551‐a 6 cc‐ 9 e 68 e 270 eefd&dist. Id=1717&to=http%3 a%2 f%2 fvrachirf. ru%2 f

Как мы оцениваем ситуацию с резистентностью бактерий?

Селекция резистентности MRSA Цефалоспорины III VRE MDR Enterobacteriacea Фторхинолоны MDR Pseudomonas spp MDR Acinetobacter spp Карбапенемы CR Enterobacteriacea CDI

Рациональное использование антибиотиков: баланс между пациентом и экологией отделения Кому? Когда? Как много? Как долго? то, что нужно тому, кому нужно в нужное время

Выбор антимикробного препарата Этиология инфекций Ведущие патогены Чувствительность к АМП

Что необходимо для назначения адекватной антибиотикотерапии 1. Гипотеза о локализации очага инфекции 2. Гипотеза о возбудителе инфекции 3. Ранний старт

Неадекватная антибиотикотерапия 1. Антибиотик не покрывают весь спектр возбудителей инфекции 2. Патоген обладает резистентностью к антибиотику 3. Поздний старт терапии 4. Неадекватная доза 5. Плохое проникновение в ткань очага инфекции 6. Отсутствовала комбинированная терапия, где это необходимо

Что следует учесть делая выбор антибактериального препарата? 1. Локализация очага инфекции 2. Вероятный возбудитель 3. Чувствительность возбудителя инфекции к антимикробным препаратам 4. Способность препарата проникать и накапливаться в различных тканях и жидкостях (СМЖ, легкие, мягкие ткани, кости…)

Антибактериальный препарат 1. Активен в отношении вероятного возбудителя 2. Способен проникать и накапливаться в различных тканях и жидкостях (СМЖ, легкие, мягкие ткани, кости…) 3. Путь введения

Польза и ограничения микробиологического исследования Микробиологическая лаборатория: Выделение возбудителя из образца – забор материала и преаналитика Определение чувствительности выделенной культуры к антибиотикам in vitro – фенотип резистентности

Польза и ограничения микробиологического исследования Лечащий врач: Оценка клинического значения выделенного патогена Оценка фенотипа резистентности и прогнозирование эффективности антимикробной терапии

IN VITRO IN VIVO

• Цель определения чувствительности ‐ прогнозирование эффективности антибактериальной терапии инфекций у пациентов • Существуют различия между микробиологической чувствительностью микроорганизмов и клинической эффективностью терапии

Отсутствие эффекта от АБ Нечувствительность к терапевтическим концентрациям АБ в биологических тканях и жидкостях Сохранение жизнеспособности отдельными изолятами при концентрациях АБ, которые подавляют рост большинства штаммов

Природная резистентность Анаэробные бактерии – аминогликозиды Enterococcus faecium – β‐лактамы Stenotrophomonas maltophilia – карбапенемы Serratia marcescens, Proteus spp. – полимиксин (колистин), тетрациклин (тайгециклин) • Pseudomonas aeruginosa – хлорамфеникол, триметоприм, тайгециклин • ………. • •

В пределах популяций бактерий EUCAST выделяет: «Дикий» тип (wild type ‐ WT), к которому относятся микроорганизмы, лишенные мутационных или других приобретенных механизмов устойчивости к конкретному антибактериальному препарату. «Недикий» тип (non‐wild type – NWT), к которому относятся микроорганизмы, обладающие мутационными или другими приобретенными механизмами устойчивости к конкретному антибактериальному препарату.

• Микроорганизм оценивается как чувствительный к антибактериальному препарату, если уровень активности последнего позволяет предположить высокую вероятность эффективности терапии.

• Микроорганизм оценивается как умеренно‐резистентный, если уровень активности антибактериального препарата связан с неопределенным результатом лечения.

• Микроорганизм оценивается как резистентный (устойчивый) к антибактериальному препарату, если уровень активности последнего позволяет предположить высокий риск неэффективности терапии

Необычные (редкие) фенотипы резистентности, требующие подтверждения Streptococcus pyogenes резистентнтный к пенициллину Staphylococcus aureus резистентнтный к ванкомицину Enterococcus faecium чувствительный к ампициллину Анаэробы резистентные к метронидазолу Serratia marcescens и Proteus spp чувствительные к колистину Enterococcus spp. устойчивые к линезолиду, даптомицину, тигециклину, телаванцину.

Как определить, что мы имеем дело с приобретенной резистентностью?

Фенотип Генотип Bacterial type IV secretion system structure reveals how antibiotics resistance genes move from one bacterium to another. Harry H. Low, Francesca Gubellini, Angel Rivera‐Calzada, Nathalie Braun, Sarah Connery, Annick Dujeancourt, Fang Lu, Adam Redzej, Rémi Fronzes, Elena V. Orlova, Gabriel Waksman. Structure of a type IV secretion system. Nature, 2014; DOI: 10. 1038/nature 13081

Локализация генов резистентности хромосомная плазмидная Локализация генов на конъюгативных плазмидах способствует их быстрому горизонтальному распространению

• В одной бактерии может быть много плазмид , и они чаще всего несут именно гены устойчивости к антибиотикам. • Бактерии способны обмениваться плазмидами. Проникновение плазмиды в бактериальную клетку называется трансформацией.

Горизонтальный перенос генов резистентности 1. Трансформацией – приобретением и интеграцией в собственный геном свободных фрагментов чужеродной ДНК 2. Конъюгацией – переносом генов путем прямого контакта между бактериальным клетками (наиболее частый и эффективный механизм переноса генов резистентности с помощью плазмид)

Некоторые бактериофаги могут быть посредниками, переносящими генетический материал между особями. Такой способ переноса называется трансдукцией. В ряде случаев геном бактериофага может встраиваться в геном бактерии, в течение нескольких поколений не убивая клетку

Транспозаза Tn 5: фермент, помогающий бактериям делиться устойчивостью к антибиотикам Транспозаза, осуществляет перемещение бактериального транспозона Tn 5. Транспозон Tn 5 — это один из первых обнаруженных транспозонов. Он был открыт при изучении устойчивости кишечной палочки (Escherichia coli) к антибиотику канамицину.

multidrug‐resistant (MDR), extensively drug‐resistant (XDR) pandrug‐resistant (PDR) bacteria Diagram showing the relationship of MDR, XDR and PDR to each other. Magiorakos A. P. et al. Multidrug‐resistant, extensively drug‐resistant and pandrug‐resistant bacteria: an international expert proposal for interim standard definitions for acquired resistance //Clinical Microbiology and Infection. – 2012. – Т. 18. – №. 3. – С. 268‐ 281.

• Полирезистентные MDR (multidrug‐resistant) – нечувствительность (НЧ) к препаратам (≥ 1) 3 классов АБ • Экстремально резистентные XDR (extensively drug‐resistant) – НЧ к препаратам (≥ 1) всех за исключением 1‐ 2 классов АБ • Панрезистентные PDR (pandrug‐resistant) – НЧ ко всем АБ всех классов

Механизм резистентности Выбор антибиотиков ЦЕЛЬ ‐ преодолеть механизм резистентности


Выделение MDR, XDR, PDR Грамположительные: • Staphylococcus spp. – выявление устойчивости к оксациллину (MRSA), ванкомицину (VISA) • Enterococcus spp. – выявление устойчивости к ванкомицину

Интерпретация результатов определения чувствительности Staphylococcus spp. Резистентность к оксациллину, опосредованная наличием гена mec. A Изоляты, резистентные к метициллину (оксациллину), являются резистентными ко всем β‐лактамным препаратам. Резистентность и к метициллину (оксациллину) обусловлена наличием гена mec. A. Изоляты, резистентные к метициллину (оксациллину), являются резистентными ко всем карабапенемам.

Интерпретация результатов определения чувствительности Staphylococcus spp. МПК ванкомицина 2 мг/л – значение эпидемиологической точки отсечения (ECOFF), разграничивающее популяцию "дикого" и "недикого типа". Клиническая эффективность терапии инфекций, вызванных такими штаммами, может быть сниженной. Терапия тяжелых инфекций, вызванных штаммами стафилококков с более высокими значениями МПК (умеренно резистентные штаммы, GISA), может быть неэффективной даже при использовании повышенных доз ванкомицина и тейкопланина.

Выделение MDR, XDR, PDR Грамотрицательные: • Enterobacteriaceae, Неферментирующие грамотрицательные бактерии ‐ НГОБ (Pseudomonas spp. , Acinetobacter spp. ) • Выявление ESBL, Аmp. C • Выявление карбапенемаз

• • • Клинически значимые приобретенные bla (b‐лактамазы) Β‐лактамазы расширенного спектра (ESBL) класс А и D CTX‐M, TEM, SHV у Enterobacteriaceae Плазмидные Amp. C цефалоспориназы (класс С) Металло‐β‐лактамазы (класс В) VIM, IMP, NDM у ГОБ OXA карбапенемазы (класс D) у Acinetobacter spp. and Enterobacteriaceae KPC карбапенемазы (класс А) у Enterobacteriaceae

β‐lactamases Bush K. Proliferation and significance of clinically relevant β‐lactamases //Annals of the New York Academy of Sciences. – 2013. – Т. 1277. – №. 1. – С. 84‐ 90.

Вторичные плазмидные Цефалоспориназы Amp. C , кодируемые хромосомными и плазмидными генами более эффективно гидролизуют цефалоспорины широкого спектра действия, чем ESBL В настоящее время этот механизм устойчивости недооценивают Diagram of Amp. C from E. coli complexed with acylated ceftazidime available at http: //www. ncbi. nlm. nih. gov Jacoby G. A. Amp. C β‐lactamases //Clinical microbiology reviews. – 2009. – Т. 22. – №. 1. – С. 161‐ 182.

European Committee on Antimicrobial Susceptibility Testing et al. EUCAST guidelines for detection of resistance mechanisms and specific resistances of clinical and/or epidemiological importance //EUCAST, Basel, Switzerland: http: //www. eucast. org/clinical_breakpoints. – 2013.

Приобретенные Аmp. C Молекулярный класс С Функциональная группа 1 Гидролизуют пенициллины и ЦС I‐III НЕ Чувствительны к ингибиторам или малочувствительны (клавуланата, сульбактам, тазобактам) • Множество генетических групп • Экспрессируют конститутционально • Распространены среди Энтеробактерий • •

Фенотип резистентности Ампициллин – R Амоксициллин/клавуланат – R Цефотаксим – R Цефтазидим – R Цефоперазон/сульбактам – R Цефокситин – R Цефепим – S устойчивость к ЦС III и цефокситину, отсутствие синергизма с клавуланатом могут указывать на наличие приобретенных Amp. C у E. coli, Klebsiella spp. , Proteus mirabilis

Enterobacter spp. , Citrobacter freundii, Serratia spp. и Morganella morganii Селекция Amp. C‐дерепресированных цефалоспорин‐резистентных мутантов может происходить во время терапии. Использование ЦС III поколения в комбинации с аминогликозидами также может быть клинически неэффективным из‐за селекции резистентных штаммов. Комбинации ЦС III поколения с фторхинолонами могут быть более эффективными. Риск селекции резистентых мутанных штаммов отсутствует или значительно снижается при использовании цефепима

• Продуценты ESBL часто относятся к категории чувствительных к комбинациям пенициллинов и ингибиторов β‐лактамаз. • Возможность использования комбинации этих препаратов остается спорной и требует осторожного подхода.

Правила интерпретации результатов определения чувствительности к бета‐лактамам у Enterobacteriaceae Если изолят резистентен или умеренно‐ резистентен к любому из ЦС III поколения (цефотаксим, цефтриаксон, цефтазидим) или ЦС IV поколения (цефепим) и чувствителен к амоксициллину‐клавуланату, ампициллину‐ сульбактаму или пиперациллину‐тазобактаму, то он расценивается в соответствии с полученнои категориеи чувствительности, но терапевтическом исходе не предсказуем для всех инфекции , за исключением ИМП

Правила интерпретации результатов определения чувствительности к аминогликозидам Все энтеробактерии, Pseudomonas aeruginosa и Acinetobacter baumannii : • При выявлении резистентности или умереннои ‐ резистентности к тобрамицину и чувствительности к гентамицину и амикацину, представители Enterobacteriaceae должны рассматриваться как умеренно‐резистентные к амикацину, а Pseudomonas aeruginosa и Acinetobacter baumannii – как резистентные к амикацину

Правила интерпретации результатов определения чувствительности к фторхинолонам Энтеробактерии Если изолят резистентен к ципрофлоксацину, то он рассматривается как резистентныи ко всем фторхинолонам

Выявление карбапенемаз • Тесты для выявления продукции карбапенемаз у клинических изолятов энтеробактерии рекомендуется использовать в случаях обнаружения пониженной чувствительности к меропенему • В целях получения эпидемиологических данных и осуществления инфекционного контроля, выявление карбапенемаз рекомендуется также проводить у всех нечувствительных к карбапенемам изолятов Pseudomonas и Acinetobacter spp.

Карбапенемазы • Металло‐β‐лактамазы (MBL) ‐ Класс В VIM IMP NDM • Сериновые карбапенемазы ‐ Класс А KPC ‐ Класс D группа OXA 48 – Энтеробактерии группа ОХА 23, 58, ‐ Ацинетобактер

Overview of Carbapenemase Enzyme Types in Enterobacteriaceae Карбапенемазы Энтеробактерий A (serine) KPC‐ Mainly found in Klebsiella pneumoniae (have been identified in other Enterobacteriaceae and nonfermenters) В Zinc binding thiol –“MBLs” NMD‐ 1 IMP‐I VIM‐ 1 Enterobacteriaceae and nonfermenters D (serine) OXA‐ 48 Enterobacteriaceae (other types of OXA carbapenemases mainly found in Acinetobacter spp. ) Morrill H. J. et al. Treatment options for carbapenem‐ resistant Enterobacteriaceae infections //Open forum infectious diseases. – Oxford University Press, 2015. – С. ofv 050.

Критерии оценки чувствительности Enterobacteriaceae к карбапенемам Пограничные значения МПК мг/л Россия МУК 4. 2‐ 2004 США CLSI ‐ 2014 Антибиотик S R S R Имипенем ≤ 4 ≥ 16 ≤ 1 ≥ 4 ≤ 2 > 8 Меропенем ≤ 4 ≥ 16 ≤ 1 ≥ 4 ≤ 2 > 8 Эртапенем ≤ 2 ≥ 8 ≤ 0, 5 ≥ 2 ≤ 0, 5 > 1 ≤ 1** > 2 Дорипенем ≤ 0, 5* Европа EUCAST ‐ 2014 Все ли ясно? * Kaniga K. et al. Worldwide experience with the use of doripenem against extended‐spectrum‐β‐lactamase‐producing and ciprofloxacin‐resistant Enterobacteriaceae: analysis of six phase 3 clinical studies //Antimicrobial agents and chemotherapy. – 2010. – Т. 54. – №. 5. – С. 2119‐ 2124. **The European Committee on Antimicrobial Susceptibility Testing. Breakpoint tables for interpretation of MICs and zone diameters. Version 6. 0, 2016. http: //www. eucast. org

The carbapenem breakpoints for Enterobacteriaceae will detect all clinically important resistance mechanisms (including the majority of carbapenemases). Carbapenemase detection and characterisation are recommended for public health and infection control purposes Пограничные значения для карбапенемов в большинстве случаев позволяют выявить клинически значимые механизмы резистентности (включая продукцию различных карбапенемаз). Однако при использовании этих пограничных значении некоторые изоляты, продуцирующие карбапенемазы, могут быть отнесены к категориям Ч и УР. В связи с этим, а также учитывая особое значение карбапенемаз и тенденцию роста их распространенности (в основном среди нозокомиальных штаммов), выявление продукции карбапенемаз является строго рекомендуемым The European Committee on Antimicrobial Susceptibility Testing. Breakpoint tables for interpretation of MICs and zone diameters. Version 6. 0, 2016. http: //www. eucast. org

Клинический пример ‐ Б. П. И. • Дата поступления: 17. 06. 2016 Возраст: 57 • Клинический диагноз: Тяжелая ЗЧМТ. Ушиб головного мозга тяжелой степени тяжести с формированием контузионного очага в правой лобно‐височной области головного мозга. Перелом нижней челюсти. Состояние после декомпрессивной трепанации черепа и удаления внутримозговой гематомы от 13. 06. 2016 и установки датчика ВЧД от 17. 06. 2016 г.

• ЧМТ получена в результате ДТП • На 4 сутки перевод в НИИ Нейрохирургии для дальнейшего лечения. • При поступлении ‐ уровень сознания‐ кома 1

ОАК Дата Эр Hb Hct Тром СОЭ Лейк Баз Эоз Мие Юн Пал Сегм Лим Мон 17. 06. 3. 34 107 30. 6 173 2016 21 9. 42 0. 0 1. 0 74. 0 17. 0 8. 0 20. 06. 2. 99 2016 35 8. 45 0. 0 1. 0 0. 0 4. 0 78. 0 95 28. 0 155 8. 0

БХК Дата Na 17. 06. 139 2016 17. 06. 142 2016 K Cl Гл Кр Моч 3. 8 106 5. 9 3. 8 106 3. 8 105 О. б. Альб Бил. о. Бил. п. АЛТ 5. 3 74 6. 9 58 28 12. 1 5. 0 73 7. 0 58 29 11. 9 АСТ ГГТП 53 23 58 51 25 56 ЩФ CRP 10. 3 73 10. 2

• Рентген легких от: 17. 06. 2016 • На обзорной рентгенограмме‐лежа‐ усилен легочный рисунок в нижних долях , прикорневых зонах. Корни легких неструктурные. Куполы диафрагмы четкие. Границы сердца не расширены. Аорта развернута, несколько расширена.
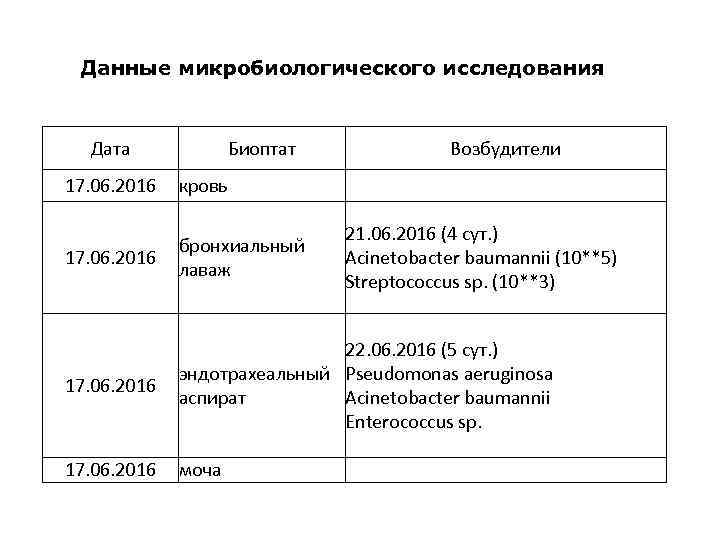
Данные микробиологического исследования Дата Биоптат Возбудители 17. 06. 2016 кровь бронхиальный 17. 06. 2016 лаваж 21. 06. 2016 (4 сут. ) Acinetobacter baumannii (10**5) Streptococcus sp. (10**3) 22. 06. 2016 (5 сут. ) эндотрахеальный Pseudomonas aeruginosa 17. 06. 2016 аспират Acinetobacter baumannii Enterococcus sp. 17. 06. 2016 моча

MBLs ‐ VIM

BLA ‐ OXA

Можно ли считать этот Acinetobacter baumannii возбудителем пневмонии? Можно ли использовать Карбапенемы? Аминогликозиды? Тайгециклин? Колистин? Комбинированную терапию?

Смертность при монотерапии колистином неприемлемо высока, но это не означает, что комбинированная терапия Paul M. et al. Combination therapy for carbapenem‐ работает лучше. resistant Gram‐negative bacteria //Journal of Antimicrobial Chemotherapy. – 2014. – С. dku 168.

Multidrug‐resistant Gram‐negative infections: what are the treatment options? While the pharmaceutical pipeline is waning, two revived old antibacterials (colistin and fosfomycin), a newer one (tigecycline) and an 'improved' member of an existing class (doripenem) are the only therapeutic options left. Колистин, фосфомицин, тигециклин и дорипенем остаются единственной возможностью для лечения Giamarellou H. , Poulakou G. Multidrug‐resistant gram‐negative infections //Drugs. – 2009. – Т. 69. – №. 14. – С. 1879‐ 1901.

4 Антибиотикорезистентность Основные правила.pptx