Антибиот.-1 2013.ppt
- Количество слайдов: 40

АНТИБИОТИКИ Лекция 4, 2013 А/Б – это органические соединения, продуцируемые любыми организмами (преимущественно микроорганизмами) или их модификации, обладающие способностью в НЕЗНАЧИТЕЛЬНЫХ КОНЦЕНТРАЦИЯХ ИЗБИРАТЕЛЬНО подавлять рост других м/о или убивать их (бактерии, грибы, простейшие, вирусы и др. ), или задерживать развитие злокачественных новообразований. А/Б отличаются от других ЛС гетерогенностью, т. е. многокомпонентностью состава. Например, гентамицин состоит из 3 компонентов: гентамицина А, гентамицина В и гентамицина С.

В солях бензилпенициллина сумма пенициллинов должна быть не менее 96, 0%, а содержание бензилпенициллина в нем – не менее 90, 0%. А/б, в отличие от некоторых других продуктов жизнедеятельности (кислоты, спирты, аммиак), характеризуются двумя основными признаками: - обладают высокой биологической активностью по отношению к чувствительным к ним организмам. Например, пенициллин даже в концентрации 1· 10 -6 г/мл оказывает четко выраженное бактерицидное действие;

- А/б избирательно действуют на м/о, не оказывая при этом заметного эффекта на другие формы живых существ. Так, бензилпенициллин задерживает развитие только грамположительных бактерий, не действуя на грамотрицательные бактерии и др. Он практически нетоксичен для организма человека и животных в присутствии гнилостных микробов. В этом отличие А/Б от ядов (сулема, мышьяк и др. ), подавляющих жизнедеятельность любого организма. А/Б относятся к химиотерапевтическим средствам, наряду с элементорганическими препаратами мышьяка, сульфаниламидами. Это препараты, которые проявляют бактерицидное или бактериостатическое действие в отношении м/о, не оказывая в терапевтических дозах действие на макроорганизм.

Явление антибиоса наблюдал Л. Пастер (1868 г), установивший гибель палочки сибирской язвы. В конце 19 века И. И. Мечников (1894 г). обобщил данные о лечении А/Б. Ему принадлежит идея бактериотерапии, то есть использования антагонизма бактерий. Он предложил использовать молочнокислые бактерии простокваши для подавления жизнедеятельности гнилостных бактерий, находящихся в толстом кишечнике человека. Шотландский микробиолог А. Флеминг (1928 г), случайно обнаружил на чашке Петри, засеянной Staphylococcus aureus, стерильные зоны вокруг колоний плесени. В Оксфорде в 1940 г. учёными Г. Флори и Э. Чейн был выделен чистый пенициллин.

1945 г. А. Флеминг, Г. Флори, Э. Чейн – Нобелевские лауреаты по физиологии и медицине

Пенициллин до сих пор считается «Королем» антибиотиков, а 40 -е годы 20 века стали началом развития науки об антибиотиках. В 1942 г. в Центральном институте малярии и медицинской паразитологии была создана первая в нашей стране специализированная лаборатория А/Б под руководством Г. Ф. Гаузе. В 1943 г. - опубликовано сообщение о новом перспективном для клиники антибактериальном веществе (полученном из подмосковной почвы) природного происхождения. В последствии оно получило название Грамицидин С (советский).

Историческая роль грамицидина С в том, что это один из первых А/Б, на котором разрабатывались приемы и методология исследования совершенно неизвестных до того времени антибиотических веществ природного происхождения. В последующем здесь были организованы работы по поиску противоопухолевых антибиотиков. В СССР пенициллин открыли самостоятельно (в военное время невозможно было получить из Англии образцы). В СССР группа Зинаиды Виссарионовны Ермольевой в 1942 году выделила первый отечественный пенициллин крустазин из Penicillium crustosum (этому открытию посвящен роман В. Каверина «Открытая книга» ; академик Зильберштейн – брат В. Каверина).

1942 г. З. В. Ермольева – первый отечественный пенициллин – крустазин (P. Сrustosum)

В 1943 г. Фармакологический комитет разрешил медицинское применение пенициллина. «Боевое крещение» отечественный пенициллин получил под руководством Н. Н. Бурденко (основоположник российской нейрохирургии) на Первом Прибалтийском фронте. В 1944 г. налажено производство антибиотика в Москве на химико-фармацевтическом заводе и мясокомбинатах Москвы и Ленинграда. В 1948 году в СССР был организован ВНИИ по пенициллину и другим антибиотикам, который в 1990 году он получил статус Государственного научного центра по антибиотикам (ГНЦА).

Благодаря работам этого института были разработаны и внедрены в промышленность методы получения большого количества А/Б, а медицинская практика получила современные пенициллины, тетрациклины, антибиотики аминогликозиды. К наиболее значимым достоинствам А/Б в современной медицине относят: - снижение детской смертности; - возрастание средней продолжительности жизни; - уменьшение тяжести течения и частоты возникновения гнойных осложнений в хирургии.

Открытие и внедрение в клинику современных А/Б привело к развитию новых отраслей медицины – трансплантологии, реконструктивной хирургии, а также позволило контролировать течение инфекций, протекающих на фоне иммунодефицита различного генеза.

Основные пути получения антибиотиков: - скрининг продуцентов новых природных веществ (бактерии – грамицидин, плесневые грибы – пенициллины, лучистые грибы – актиномицеты, эритроциты – эритромицин и другие); - химическая трансформация известных антибиотических структур (полусинтетические пенициллины, тетрациклины и другие); - полный химический фторхинолоны и другие). Большинство получается синтез антибиотиков было (левомицетин; получено и

Процесс ферментации проводят в асептических условиях в специальных приборах - ферментерах «глубинным способом» т. е. рост продуцента (плесени) и образование антибиотика идет по все толщине ферментационной массы при постоянном перемешивании и аэрации (через весь слой ферментационной массы снизу подаётся стерильный воздух, который перемешивает массу и насыщает кислородом). Регулируя состав ингредиентов питательной среды можно влиять на качественный и количественный выход антибиотиков.

Биосинтез включает следующие этапы: - изыскание штаммов продуцентов; - подбор питательных сред; - процесс ферментации; -выделение и очистка антибиотиков. -1 -я фаза биосинтеза - рост и размножение продуцента (в питательную среду вносят углеводы, соединения, содержащие азот (N), фосфор (P), серу (S) др. элементы, иногда воздействуют УФ-лучами и другими факторами); -2 -я фаза – замедление роста продуцента (из среды удаляются углеводы и фосфор; продуцент замедляет жизнедеятельность и в культуральной жидкости остается антибиотик);


3 -я фаза – выделение и очистка антибиотика (фильтрация, осаждение – сменой растворителей, экстракцией, хроматографическими методами – ТСХ, колоночная (ионообменная), перекристаллизация). Затем А/б подвергают химическому ( часто м-ды: ВЭЖХ, ГЖХ. спектроскопия ЯМР и др. ) и биологическому анализу. Наиболее объективными считаются биологические м -ды колич. опр-я А/Б. Они основаны на непосредственном биологическом действии А/Б на используемый стандартный тесторганизм.

Недостатки Биологических методов : - длительность проведения анализов; - зависимость точности результатов от многих внешних факторов; - наличие определенного штамма тест - микроорганизма и др. Точность биологических методов составляет около ± 10%. ОФС «Определение антимикробной активности антибиотиков методом диффузии в агар» Методика: в чашки Петри разливают расплавленные питательные среды определен. состава в один или два слоя. Нижний слой - незасеянные среды, верхний или один слой – агаровая среда, предварительно засеянная соответствующим тест-микробом.

На поверхности агара в чашке Петри расставляют 6 стерильных цилиндров из стали или алюминия одинаковых массы и размеров (высотой и внутренним диаметром) на равном расстоянии друг от друга и от края чашки. Вместо цилиндров можно использовать лунки диаметром от 6 до 8 мм, сделанные в толще агара. В цилиндры или лунки каждой чашки вносят равные объемы рабочих растворов ГСО и испытуемого образцов антибиотика. Чашки Петри инкубируют в термостате при температуре (36± 1)0 С в течение 16 -18 часов. Диаметры зон угнетения роста тест-микроба измеряют соответствующим прибором с точностью до 0, 1 мм. Вычисляют среднюю величину зоны угнетения роста для раствора испытуемого образца антибиотика и для раствора ГСО антибиотика.

Рассчитывают активность испытуемого А/Б относительно ГСО, либо графическим м-дом (по стандартной кривой) или с использованием соответствующих формул, приведенных в НД. Активность А/Б выражают в ЕД. Это обусловлено тем, что антибиотики в большинстве случаев представляют собой смесь нескольких родственных соединений. За единицу антибиотической активности принимают минимальное количество А/Б, способное подавить развитие или задержать рост определенного количества стандартного штамма тест-микроба в единице объема питательной среды.

Рациональное лечение антибиотиками должно проводиться следующим образом: 1. Применять А/б только для лечения конкретной инфекции (то есть составляются антибиотикограммы (спектр антибактериального действия) и определяется видовая принадлежность возбудителя заболевания). По данным ВОЗ более 75% А/б назначают нерационально. - 2. Выдерживать дозировку и соблюдать интервал между приемами; - 3. Не прекращать досрочно курс лечения При несоблюдении этих основных положений повторное применение антибиотиков может быть неэффективным.

К концу 40 -х годов было известно более 100 антибиотиков. К настоящему времени известно несколько тысяч антибиотиков. Однако медицинское применение нашли лишь несколько десятков из них в качестве лекарственных веществ. Другие были отсеяны из-за высокой токсичности, низкой эффективности, аллергенности и по другим причинам. В настоящее время антибиотики принадлежат к группе лекарственных веществ, механизм действия которых наиболее изучен. Они вмешиваются в жизненноважные процессы микробной клетки.

По этим процессам их можно разделить на три группы: - антибиотики, влияющие на биосинтез клеточной стенки - антибиотики, влияющие на синтез клеточного белка. - антибиотики, действующие на цитоплазматические мембраны. Это деление несколько неточное, т. к. до конца невозможно выяснить механизм биосинтеза клеточной стенки, белков, мембранной цитоплазмы.

По химическому строению, которое не полностью отражает механизм действия А/Б, их можно распределить на следующие группы: 1. β-лактамные антибиотики 2. Тетрациклины 3. Аминогликозиды 4. Макролиды 5. Линкозамиды 6. Гликопептиды 7. Оксазолидины Кроме того, антибиотики делят ещё на три группы: - А/Б, действующие на грам-положительные, - на грам-отрицательные микроорганизмы - действующие на обе группы микроорганизмов.

Эта классификация в большей степени относится к А/Б, которые нарушают синтез клеточной стенки. А/Б - уникальная группа ЛВ: - их мишень – рецептор находится не в тканях человека, а в клетке микроорганизма; -активность А/Б снижается со временем, так как с их применением формируется резистентность микроорганизмов к ним. Антибиотикорезистентность является неизбежным биологическим явлением, и предотвратить её практически невозможно.
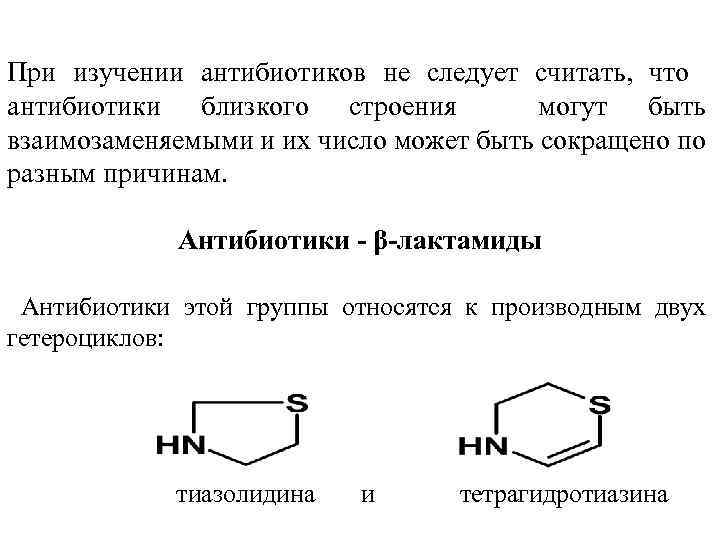
При изучении антибиотиков не следует считать, что антибиотики близкого строения могут быть взаимозаменяемыми и их число может быть сокращено по разным причинам. Антибиотики - β-лактамиды Антибиотики этой группы относятся к производным двух гетероциклов: тиазолидина и тетрагидротиазина
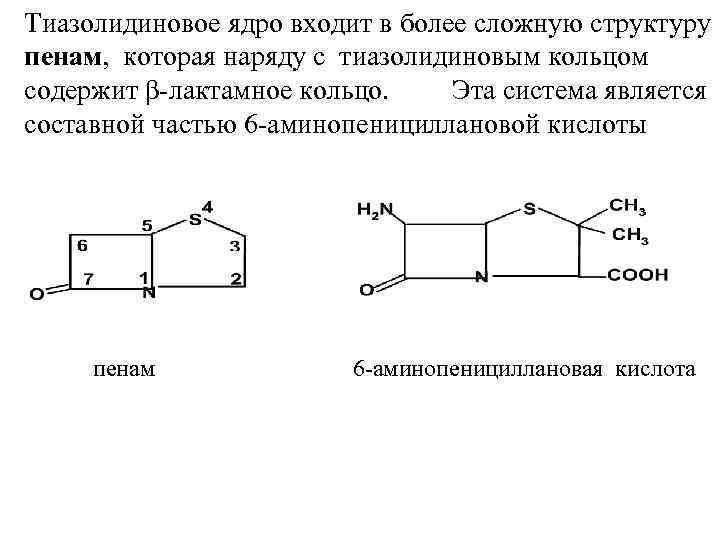
Тиазолидиновое ядро входит в более сложную структуру пенам, которая наряду с тиазолидиновым кольцом содержит β-лактамное кольцо. Эта система является составной частью 6 -аминопенициллановой кислоты пенам 6 -аминопенициллановая кислота
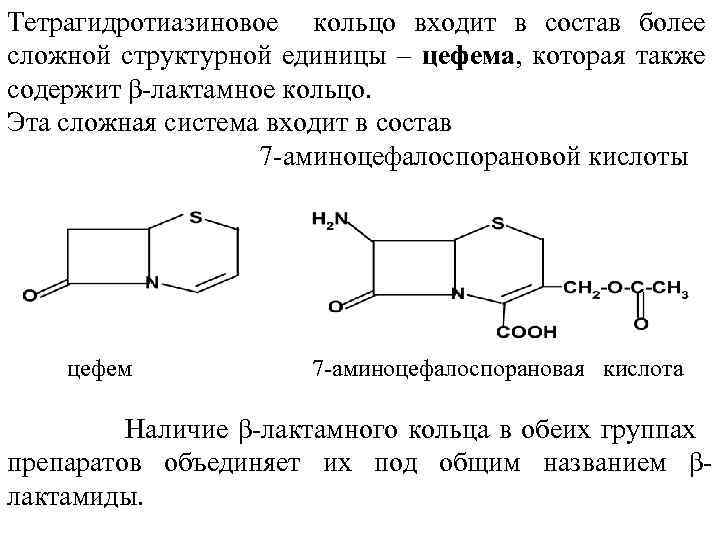
Тетрагидротиазиновое кольцо входит в состав более сложной структурной единицы – цефема, которая также содержит β-лактамное кольцо. Эта сложная система входит в состав 7 -аминоцефалоспорановой кислоты цефем 7 -аминоцефалоспорановая кислота Наличие β-лактамного кольца в обеих группах препаратов объединяет их под общим названием βлактамиды.
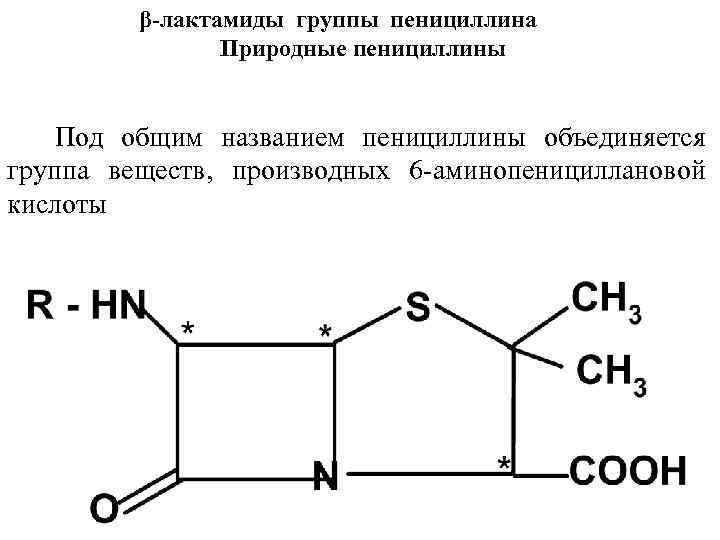
β-лактамиды группы пенициллина Природные пенициллины Под общим названием пенициллины объединяется группа веществ, производных 6 -аминопенициллановой кислоты

Бензилпенициллина натриевая соль Benzylpenicillin sodium Бензилпенициллина натриевая соль – бел. кристал. порошок, гигроскопический, легко р-мый в воде, практически нерастворимый в хлороформе и эфире. Подлинность: 1. Р-ция образования гидроксамовых кислот может протекать по амидной (1) и лактамной (2) группам.
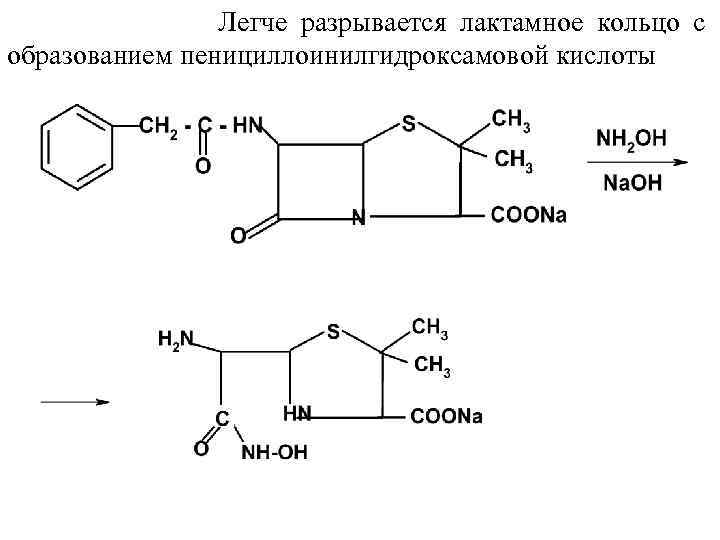
Легче разрывается лактамное кольцо с образованием пенициллоинилгидроксамовой кислоты
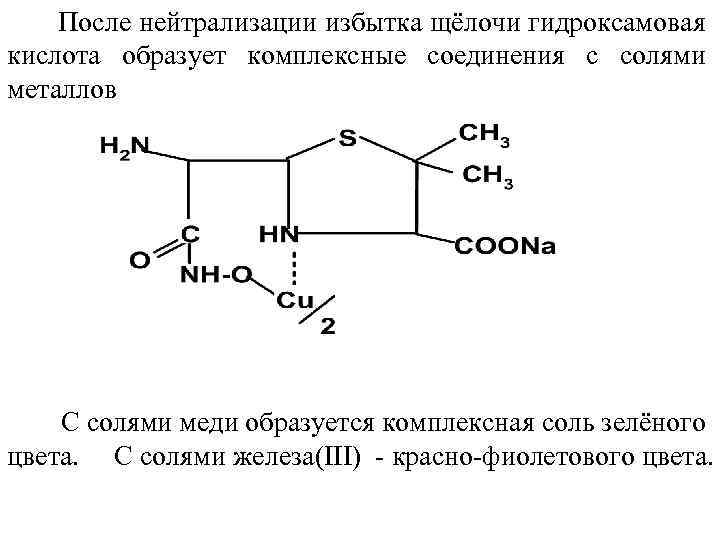
После нейтрализации избытка щёлочи гидроксамовая кислота образует комплексные соединения с солями металлов С солями меди образуется комплексная соль зелёного цвета. С солями железа(III) - красно-фиолетового цвета.

Сульфидную серу можно определить после сплавления с металлическим натрием и затем по реакции с раствором натрия нитропруссида. S 2 - + [Fe(CN)5 NO]2 - --> ¦ [Fe(CN)5 NOS]4 фиолетовое окраш. С раствором формальдегида в концентрированной кислоте серной при нагревании на водяной бане образуется красно-коричневое окрашивание.

По НД ИК-спектр поглощения ЛП сравнивают с ИКспектром CO или спектром, прилагаемым к НД. В ИК-спектре пенициллинов и цефалоспоринов наблюдается характерная полоса поглощен. при 1780 см-1. УФ-спектр - максимумы поглощен. при 257 и 263 нм (водный раствор). Удельное вращен. 2% водн. р-ра натриевой соли бензилпенициллина д. б. в пределах от +285 до + 3100. Ионы натрия с р-ром K[Sb(OH)6] – белый осадок. М-дом ТСХ подтверждают подлинность бензилпенициллина натриевой соли и наличие примесей.

Колич. опр-е - обратная йодометрия. Навеску ЛП р-ют в воде, добав. 1 М р-р Na. OH, через 20 минут 1 М р-р к-ты хлористоводородной, ацетатный буферный р-р и точное количество избытка титрованного 0, 005 М р-ра йода. Через 20 мин избыток йода титруют 0, 01 М р-ром натрия тиосульфата. Параллельно проводят контрольный опыт с таким же количеством ЛП не проводя щелочного гидролиза. Так определяется не только натриевая соль бензилпенициллина, но и другие окисляющиеся пенициллины. Методика определения основана на гидролизе бензилпенициллина в присутствии щёлочи до пенальдиновой кислоты и пеницилламина.
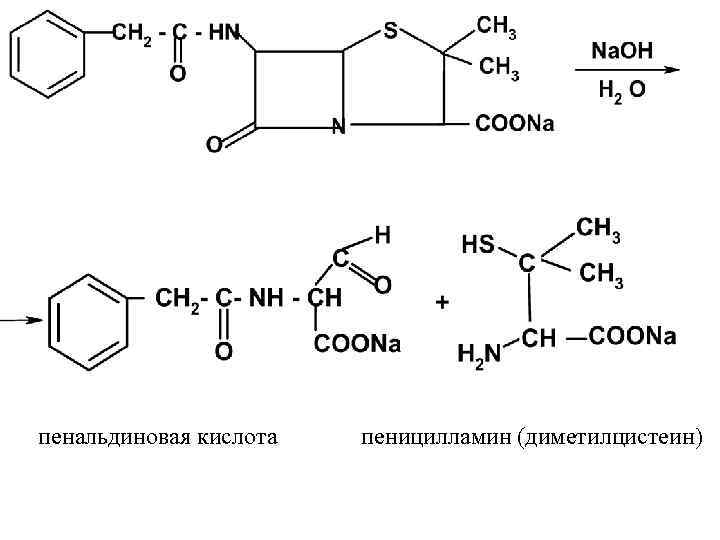
пенальдиновая кислота пеницилламин (диметилцистеин)
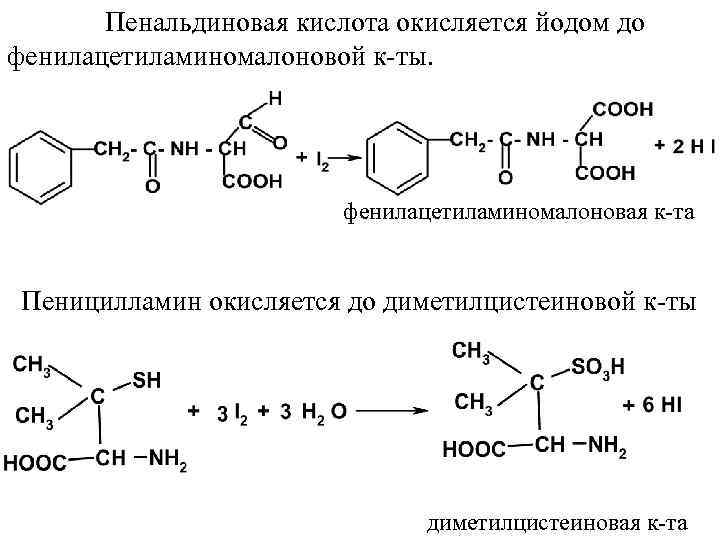
Пенальдиновая кислота окисляется йодом до фенилацетиламиномалоновой к-ты. фенилацетиламиномалоновая к-та Пеницилламин окисляется до диметилцистеиновой к-ты диметилцистеиновая к-та

Наиболее надёжным м-дом опред-я биологической активности бензилпенициллина натриевой соли является диффузия в агар-агар. Один из достоверных м-дов колич. опред. бензилпенициллина явл м-од ВЭЖХ с использованием СО бензилпенициллина. Теоретическая активность 1 мг натриевой соли бензилпенициллина соответствует 1670 ЕД. Бензилпенициллин быстро инактивируется в р-рах, особенно в присутствии кислот и щелочей. В сухом виде бензилпенициллин может храниться до 2 лет и более без потери активности. Натриевая соль бензилпенициллина является бактериостатическим антибиотиком.

Практически нетоксична, иногда может вызывать аллергические р-ции. Примен при пневмонии, менингите, гонорее, сепсисе и др. заболеваниях. Назначают бензилпенициллина натриевую соль в/м по 250 000 -500 000 ЕД, в тяжёлых случаях до 1 -2 млн ЕД. Выпускают бензилпенициллина натриевую соль во флаконах по 250 000, 500 000, 1 000 ЕД.
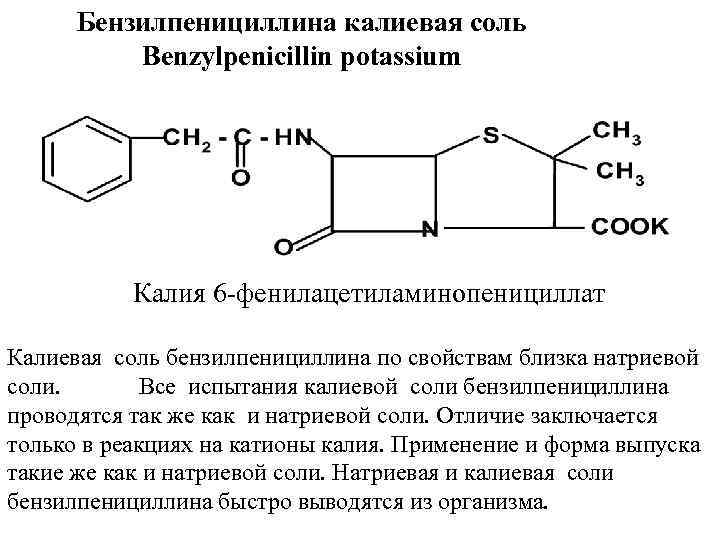
Бензилпенициллина калиевая соль Benzylpenicillin potassium Калия 6 -фенилацетиламинопенициллат Калиевая соль бензилпенициллина по свойствам близка натриевой соли. Все испытания калиевой соли бензилпенициллина проводятся так же как и натриевой соли. Отличие заключается только в реакциях на катионы калия. Применение и форма выпуска такие же как и натриевой соли. Натриевая и калиевая соли бензилпенициллина быстро выводятся из организма.
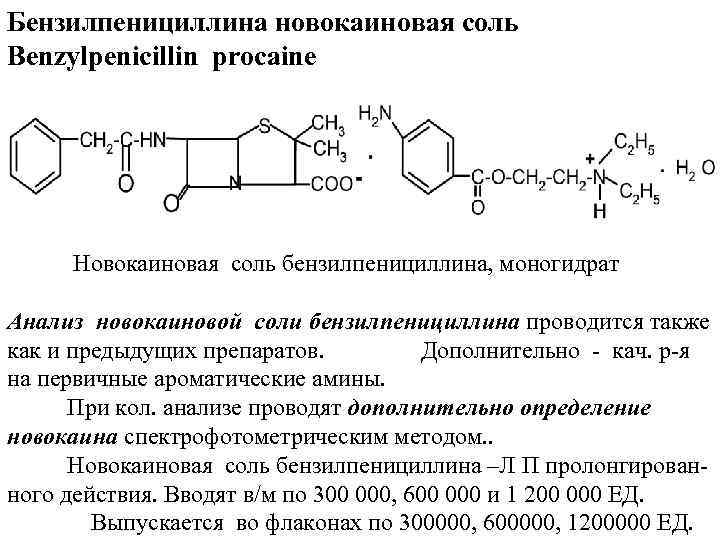
Бензилпенициллина новокаиновая соль Benzylpenicillin procaine Новокаиновая соль бензилпенициллина, моногидрат Анализ новокаиновой соли бензилпенициллина проводится также как и предыдущих препаратов. Дополнительно - кач. р-я на первичные ароматические амины. При кол. анализе проводят дополнительно определение новокаина спектрофотометрическим методом. . Новокаиновая соль бензилпенициллина –Л П пролонгированного действия. Вводят в/м по 300 000, 600 000 и 1 200 000 ЕД. Выпускается во флаконах по 300000, 600000, 1200000 ЕД.
Антибиот.-1 2013.ppt