Antibiotiki_-_GBSMP_-21_12_2010.ppt
- Количество слайдов: 135

Антибиотики Е. В. Орешников

Микроорганизмы, вызывающие инфекционные заболевания у человека n Бактерии – – – n n n Истинные бактерии Риккетсии и хламидии Микоплазмы Грибы Вирусы Простейшие

Микроорганизмы n Штамм – основная единица (чистая культура) n Вид – совокупность микробов с единым генотипом и сходными биологическими свойствами n Роды: Staphylococcus, Streptococcus – Staphylococcus aureus, Streptococcus pneumoniae n Staphylococcus spp. – S. aureus, S. epidermidis, S. saprophyticus

Инфекционная характеристика микробов • Патогенность – Патогенные бактерии • Bacillus anthracis, Yersinia pestis, Francisella tularensis – Условно-патогенные бактерии • Стафилококки, стрептококки, кишечная палочка – Непатогенные бактерии • бифидобактерии, большинство микробов почвы, воды • Вирулентность – Степень патогенности (способности вызывать инфекции) • Инвазивность – Способность диссеминировать в организме

Основные группы бактерий n Грамположительные n Грамотрицательные – Принципиальных различий в строении цитоплазматической мембраны и во внутреннем строении нет – Различия касаются строения клеточной стенки

Окраска по Граму Предложена в 1884 г. Христианом Грамом – При последовательной обработке кристалл виолетом и йодом клетки бактерий приобретают синее окрашивание § При последующем обесцвечивании спиртом некоторые виды микроорганизмы теряют синее окрашивание – При докраске фуксином приобретают красное окрашивание – Эмпирически обнаруженные различия в окраске отражают принципиальные различия в структуре клеточной стенки бактерий

Практические аспекты n Клеточная стенка грамотрицательных бактерий является препятствием для проникновения во внутреннюю среду бактерий экзогенных веществ, в том числе антибактериальных препаратов n Грамотрицательные бактерии более устойчивы к действию большинства антибактериальных препаратов n Липополисахарид, входящий в состав клеточной стенки грамотрицательных бактерий является одним из ведущих индукторов системной воспалительной реакции

Наиболее значимые микроорганизмы n Грамположительные – – – Стафилококки (Staphylococcus aureus и другие) Пневмококки (Streptococcus pneumoniae) Стрептококки § Группа А – бета-гемолитические (S. pyogenes) § Другие (S. viridans) – Энтерококки (E. faecalis) n Грамотрицательные – – Кишечная палочка Клебсиелла Гемофильная палочка Синегнойная палочка
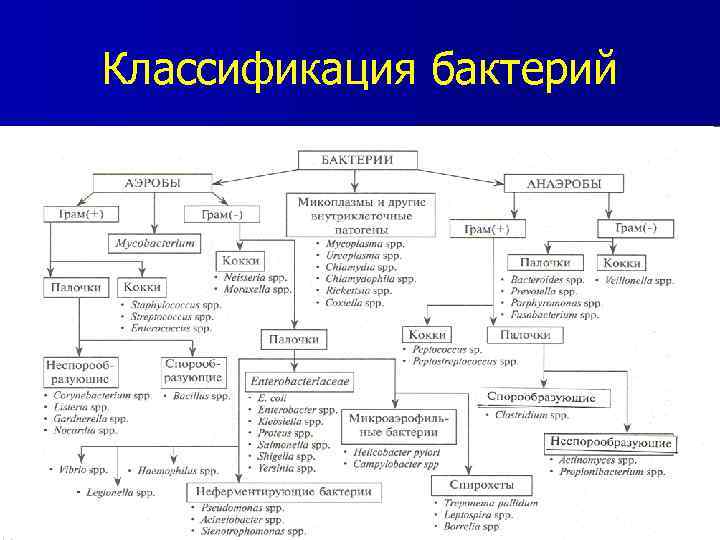
Классификация бактерий

Категории чувствительности микроорганизмов Чувствительный n лечение инфекции, вызванной данным микроорганизмом применении данного антибиотика вероятно будет эффективным Промежуточный n лечение инфекции, вызванной данным микроорганизмом применении данного антибиотика может быть эффективным при использовании повышенных доз и при локализации очага инфекции в том участке, где возможно формирование повышенных концентраций антибиотика Устойчивый n лечение инфекции, вызванной данным микроорганизмом применении данного антибиотика вероятно будет неэффективным

«Человек – микроб – антибиотик» n МПК – антимикробная активность антибиотика n Концентрации в крови/тканях - фармакокинетика n Отношении концентраций и МПК - фармакодинамика

Резистентность микроорганизмов • Природная (генетическая) – Легко прогнозируется – Абсолютная неэффективность антибиотика • Приобретенная – Первичная (до начала лечения) – Вторичная (на фоне лечения) • Сложно прогнозировать • Эффективность антибиотика слабо предсказуема

Инфекционный процесс n Инфекция – микробиологический и клинический феномен, характеризующийся воспалительным ответом на присутствие микроорганизмов или инвазией микроорганизмами стерильных тканей [Bone et al. , 1992] Первичная инфекция n Вторичная инфекция – Рецидив (тот же возбудитель, та же локализация) – Суперинфекция (другой возбудитель, любая локализация) n

Бактериальные инфекции • Внебольничные – Региональное сходство – Предсказуемость этиологии и чувствительности возбудителей • Эффективность антибиотиков прогнозируема • Госпитальные (нозокомиальные) – Различия между медицинскими учреждениями и лечебными отделениями – Этиология и чувствительность возбудителей менее предсказуемы • Эффективность антибиотиков варьирует

Антимикробная терапия n Антимикробная терапия – лечение вызванных микроорганизмами инфекционных заболеваний лекарственными препаратами, избирательно действующими на эти микроорганизмы n Эмпирическая и этиотропная терапия n Цель антимикробной терапии – эрадикация возбудителя заболевания

Микробиологические результаты антибиотикотерапии n Эрадикация (элиминация) – Исчезновение возбудителя на фоне лечения n Персистирование – Повторное выделение первоначального возбудителя на фоне лечения n Колонизация – Выделение новых микроорганизмов на фоне лечения без клинических признаков инфекции n Суперинфекция – Выделение новых микроорганизмов при клиническом рецидиве инфекции

От чего зависит эффект антибиотиков? Факторы микроба Факторы человека Факторы антибиотика Чувствительность Иммунитет ФК Способность формировать R Ответ на инфекцию Достижение киллинга in vivo

Факторы, ограничивающие эффективность антибиотиков n Низкая природная активность § Цефалоспорины III поколения – стафилококки § Карбапенемы - энтерококки n Тканевая фармакокинетика § Аминогликозиды – гнойный очаг § Бета-лактамы - клетки n Задержка назначения адекватной антибактериальной терапии § Пневмония n сепсис ПОН септический шок Неадекватный режим дозирования § Амоксициллин < 1 г в сутки § Цефуроксим < 1 г в сутки

Отличительные особенности антибиотиков как лекарственных средств • Мишень действия – микроорганизм • Избирательность действия на прокариотическую клетку • Снижение активности и эффективности со временем

Две задачи Тактическая – вылечить конкретного больного Стратегическая – предупредить формирование полирезистентной микрофлоры (иначе вылечишь одного, а умрут сотни! В том числе медработники!) «Больница – чашка Петри для выращивания резистентной флоры»

Три тактики антибиотикотерапии n Эскалация (больные без начальных признаков ГСО, тяжесть состояния которых не предполагает улучшения в течение ближайших недель) n Деэскалация (больные с явными признаками ГСО, угрожающими жизни) n Рестрикция (больные с быстрым восстановлением, без явных признаков ГСО, а также «выздоравливающие больные» ? )

Эффективная АБ-терапия - эмпирическое назначение антибиотиков n Эмпирический - это не «назначенный случайно» . n Эмпирический – это «назначенный на основании опыта» . n Тактика АБ-терапии - на основании клинической картины и мониторинга микрофлоры данного отделения!!!

Способы решения проблемы n Экстенсивный – новые АБ n Интенсивный – ротация АБ и повышение эффективных доз.
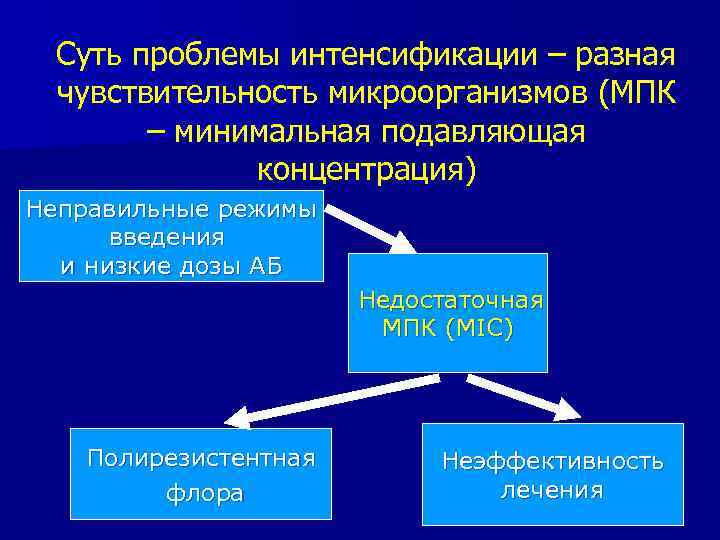
Суть проблемы интенсификации – разная чувствительность микроорганизмов (МПК – минимальная подавляющая концентрация) Неправильные режимы введения и низкие дозы АБ Недостаточная МПК (MIC) Полирезистентная флора Неэффективность лечения
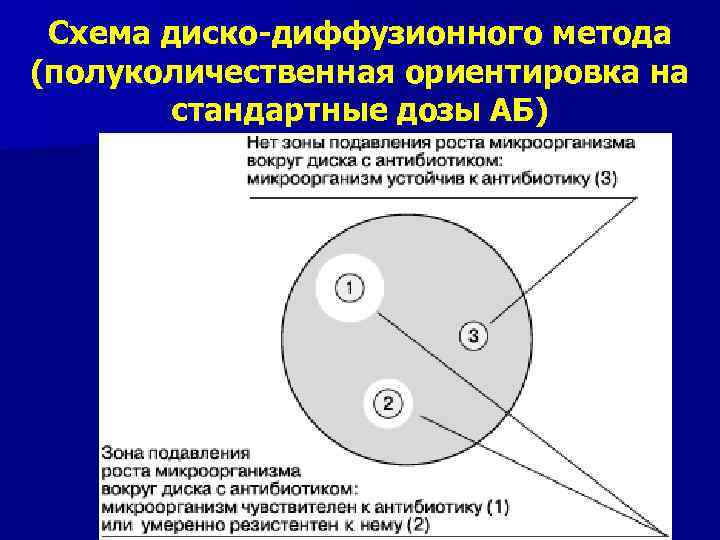
Схема диско-диффузионного метода (полуколичественная ориентировка на стандартные дозы АБ)

Как безопасно увеличить МПК? Учет фармакокинетических свойств n Учет биодоступности (расширение показаний к пероральному приему) n Повышение суточных доз (контроль и профилактика n побочных эффектов: лабораторный мониторинг, инфузионная терапия 40 -60 мл/кг)
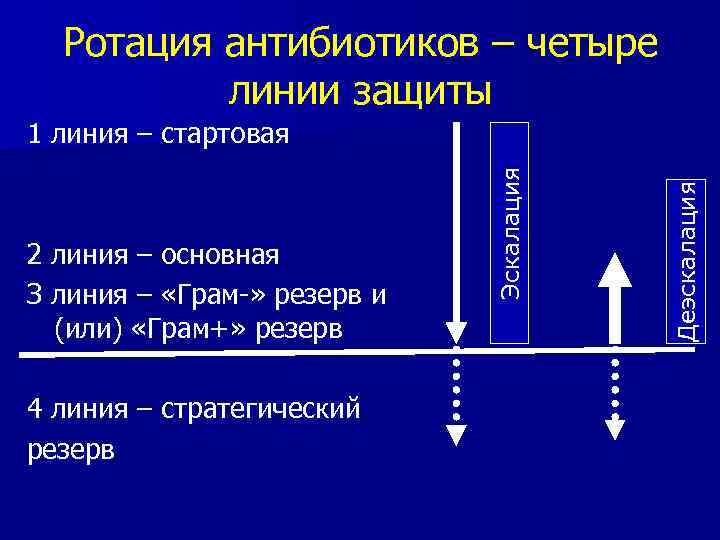
Ротация антибиотиков – четыре линии защиты 4 линия – стратегический резерв Деэскалация 2 линия – основная З линия – «Грам-» резерв и (или) «Грам+» резерв Эскалация 1 линия – стартовая

Пути повышения эффективности АБ-терапии n Выбор тактики n Контроль микрофлоры отделения (сеять всё вокруг! Даже мобильные телефоны и водопроводные краны!!!) n Повышение МПК за счет новых доз и новых режимов введения n Ротация АБ n Руки мыть!!! (И другие места тоже!!!)

Бета-лактамные антибиотики n Пенициллины n Цефалоспорины n Карбапенемы n Монобактамы азтреонам

Пенициллины n Бензилпенициллин до 20 -30 тыс. ЕД в сутки, на 6 введений – Стрептококковые инфекции (сепсис, инфекционный эндокардит (нативного клапана), рожа, ИКи. МТ) – Менингококковые инфекции (менингит) – Клостридиальные инфекции (газовая гангрена) n Оксациллин 8 -12 г в сутки, на 6 введений – Стафилокковые инфекции (ИОХВ, кожи и мягких тканей, инфекции костей и суставов, катетер-ассоциированные инфекции кровотока, инфекционный эндокардит (у наркоманов), менингит, сепсис) n Ампициллин 8 -12 г в сутки, на 6 введений – Энтерококковые инфекции (E. faecalis): сепсис, эндокардит , ИМП
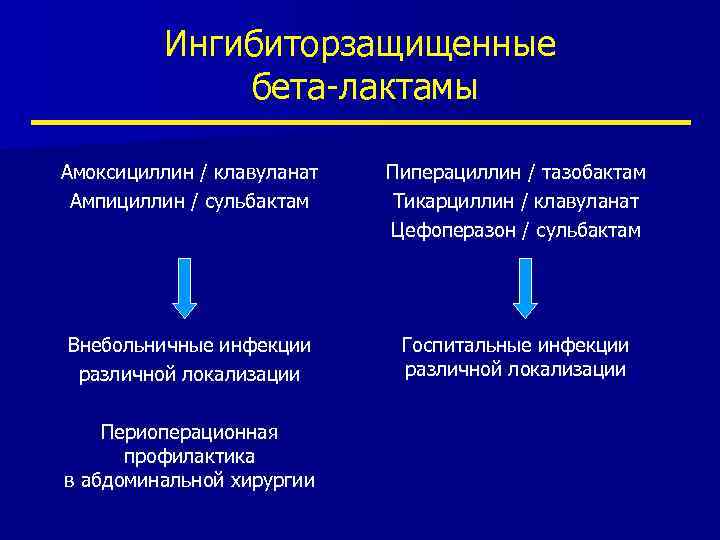
Ингибиторзащищенные бета-лактамы Амоксициллин / клавуланат Ампициллин / сульбактам Пиперациллин / тазобактам Тикарциллин / клавуланат Цефоперазон / сульбактам Внебольничные инфекции различной локализации Госпитальные инфекции различной локализации Периоперационная профилактика в абдоминальной хирургии

Пиперациллин/тазобактам (Тазоцин) Тазоцин 2, 25 г: Пиперациллин 2 г + Тазобактам 0, 25 г Тазоцин 4, 5 г: Пиперациллин 4 г + Тазобактам 0, 5 г Интервал дозирования: 6 -8 часов Разрешен у детей с 2 лет Дозирование: Внебольничные инфекции: 2, 25 г каждые 6 -8 часов Нозокомиальные инфекции: 4, 5 г каждые 6 -8 часов Нейтропения, P. aeruginosa: 4, 5 г каждые 6 часов

Пиперациллин/тазобактам (Тазоцин) n Широкий антимикробный спектр: – – – n Грам(+): стафилококки, стрептококки, энтерококки Грам(-): энтеробактерии, P. aeruginosa, Acinetobacter Анаэробы, вкл. Bacteroides spp. , Clostridium spp. § Возможность монотерапии полимикробных инфекций Активность против резистентных Грам(-) – Возможность применения при нозокомиальных инфекциях n Более высокая (по сравнению с сульперазоном и цефтазидимом) активность против Грам(+) – Возможность применения при внебольничных инфекциях n В отличие от цефалоспоринов III-IV и фторхинолонов не вызывает селекцию -продуцентов – Возможность замены ЦС III и ФХ в качестве базовой терапии НИ БЛРС
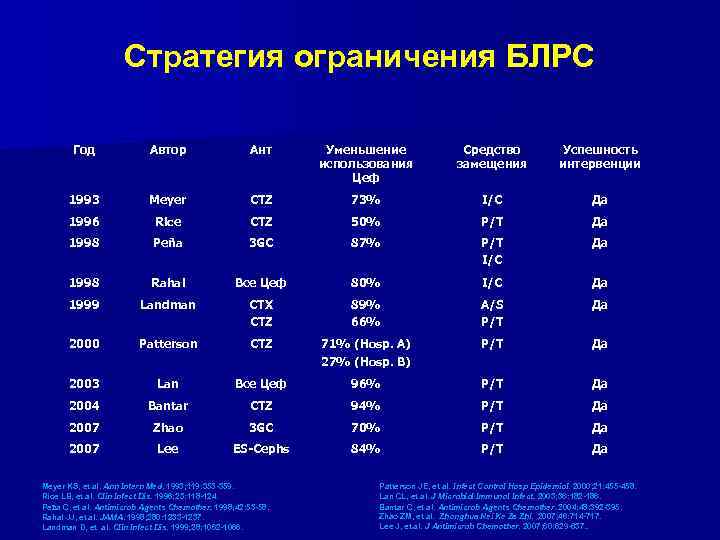
Стратегия ограничения БЛРС Год Автор Ант Уменьшение использования Цеф Средство замещения Успешность интервенции 1993 Meyer CTZ 73% I/C Да 1996 Rice CTZ 50% P/T Да 1998 Peña 3 GC 87% P/T I/C Да 1998 Rahal Все Цеф 80% I/C Да 1999 Landman CTX CTZ 89% 66% A/S P/T Да 2000 Patterson CTZ 71% (Hosp. A) 27% (Hosp. B) P/T Да 2003 Lan Все Цеф 96% P/T Да 2004 Bantar CTZ 94% P/T Да 2007 Zhao 3 GC 70% P/T Да 2007 Lee ES-Cephs 84% P/T Да Meyer KS, et al. Ann Intern Med. 1993; 119: 353 -359. Med. Rice LB, et al. Clin Infect Dis. 1996; 23: 118 -124. Dis. Peña C, et al. Antimicrob Agents Chemother. 1998; 42: 53 -58. Peñ Chemother. Rahal JJ, et al. JAMA. 1998; 280: 1233 -1237. JAMA. Landman D, et al. Clin Infect Dis. 1999; 28: 1062 -1066. Dis. Patterson JE, et al. Infect Control Hosp Epidemiol. 2000; 21: 455 -458. Epidemiol. Lan CL, et al. J Microbiol Immunol Infect. 2003; 36: 182 -186. Bantar C, et al. Antimicrob Agents Chemother. 2004; 48: 392 -395. Chemother. Zhao ZM, et al. Zhonghua Nei Ke Za Zhi. 2007; 46: 714 -717. Zhi. Lee J, et al. J Antimicrob Chemother. 2007; 60: 629 -637. . Chemother. 35

Пиперациллин/тазобактам (Тазоцин) • Средство 1 -го ряда эмпирической терапии НП, хирургических инфекций, нозокомиального сепсиса – Включен во все Практические рекомендации (Guidelines) в качестве средства 1 -й линии терапии • • • NP: ATS/IDSA 2005, РФ 2009 IAI: IDSA/SIS 2003 c. SSTI: IDSA 2005, РФ 2009 Сепсис: РФ 2009 Фебрильная нейтропения – Является эталонным препаратом сравнения при клинических исследованиях (FDA) • Относительно стабилен к БЛРС – Возможен инокулум-эффект – повышение МПК! • Сохраняется хорошая чувствительность P. aeruginosa
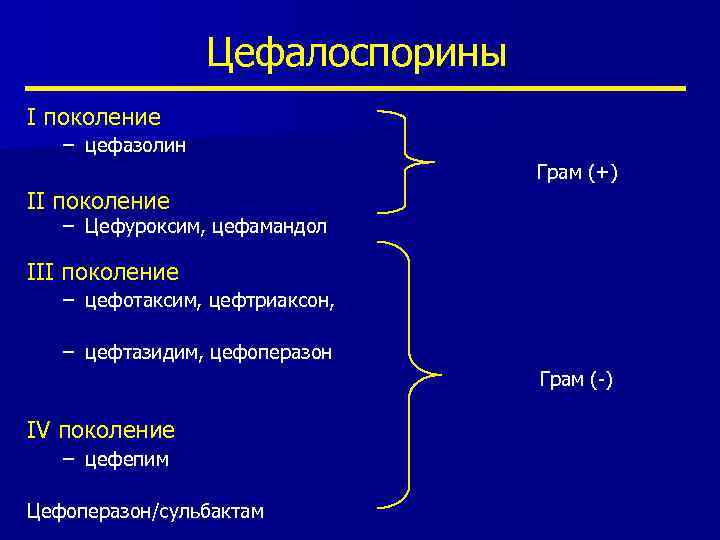
Цефалоспорины I поколение – цефазолин Грам (+) II поколение – Цефуроксим, цефамандол III поколение – цефотаксим, цефтриаксон, – цефтазидим, цефоперазон Грам (-) IV поколение – цефепим Цефоперазон/сульбактам

Показания для применения цефалоспоринов I - II поколения § Периоперационная профилактика в хирургии Цефазолин § Доказанные или предполагаемые стафилококковые инфекции при невысоком риске MRSA § (катетер-ассоциированный сепсис, эндокардит, мастит, инфекции кожи и мягких тканей, костей и суставов) Цефуроксим • Нетяжелые внебольничные инфекции кожи и мягких тканей, дыхательных и мочевыводящих путей Не назначать при госпитальных инфекциях !

Цефалоспорины III поколения Цефотаксим Цефтриаксон Цефтазидим Цефоперазон Высокая активность против пневмококков и Грам(-) Высокая активность против P. aeruginosa и Грам(-) Тяжелые внебольничные инфекции Тяжелые госпитальные инфекции различной локализации при подтвержденной или вероятной этиологической роли P. aeruginosa различной локализации Не применять при госпитальных инфекциях Фебрильная нейтропения Рост резистентности госпитальных штаммов Грам(-) бактерий (БЛРС)

Цефалоспорины IV поколения Цефепим • В отношении Гр (+) сходен с цефалоспоринами I – II • В отношении Гр (-) сходен с цефалоспоринами III • Сохраняет эффективность против некоторых резистентных к ЦС III энтеробактерий • Активен против P. aeruginosa (= цефтазидиму) Режим дозирования: 2 -4 г в сутки на 2 -4 введения

Цефоперазон / сульбактам (Сульперазон) • Расширение клинической активности цефоперазона на штаммы Грам(-) бактерий, продуцирующих БЛРС и устойчивых к незащищенным цефалоспоринам III • Возможность применения при госпитальных инфекциях, вызванных P. aeruginosa, Acinetobacter • Проявление клинической активности против анаэробов • – возможность применения в режиме монотерапии при смешанных инфекциях (интраабдоминальные, гинекологические, раневые инфекции) Режим дозирования: 4 г в сут в пересчете на цефоперазон
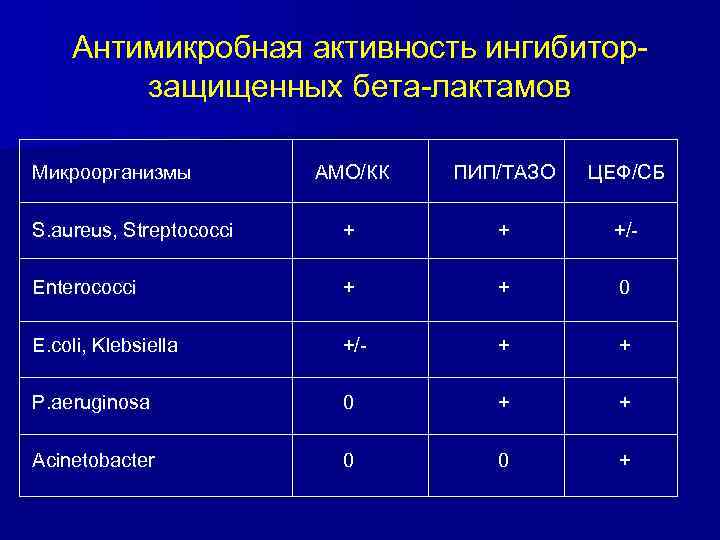
Антимикробная активность ингибиторзащищенных бета-лактамов Микроорганизмы АМО/КК ПИП/ТАЗО ЦЕФ/СБ S. aureus, Streptococci + + +/- Enterococci + + 0 E. coli, Klebsiella +/- + + P. aeruginosa 0 + + Acinetobacter 0 0 +

Анти-MRSA цефалоспорины n Цефтобипрол (Зефтера) и цефтаролин являются представителями V поколения цефалоспоринов n Обладают уникальной активностью в отношении широкого спектра возбудителей, включая активность в отношении MRSA

Анти-MRSA цефалоспорины n Клиническая эффективность Цефтобипрола при синдроме диабетической стопы равна эффективности комбинации ванкомицин+цефтазидим n Широкий спектр – MRSA + Enterobacteriaceae + Ps. aeruginosa § Кроме БЛРС

Аминогликозиды Резистентность Грам(-) бактерий к аминогликозидам: гентамицин, тобрамицин > нетилмицин > амикацин • • Гентамицин Стафилококковые инфекции • (только в комбинации с оксациллином или ванкомицином) Энтерококковые инфекции • (только в комбинации с ампициллином или ванкомицином!) Амикацин, сизомицин, тобрамицин Инфекции, вызванные P. aeruginosa • (только в комбинации с антисинегнойными бета-лактамами ) Нетилмицин • (при ХПН, слуховых и вестибулярных расстройствах)

Побочные эффекты аминогликозидов Гентамицин = Тобрамицин = Амикацин > Нетилмицин Нейротоксичность Нейромышечная блокада - усиливается при одновременном применении с анестетиками и миорелаксантами, большим количеством цитратной крови n Усиливают проявления паркинсонизма, миастении n При интравентрикулярном введении – вентрикулит n Нефротоксичность (12 - 15%) n n Ранние проявления: Энзимурия, Глюкозурия, Поздние проявления: Повышение мочевины и креатинина, реже ОПН Ото- и вестибулотоксичность (3 - 15%) Гентамицин - преобладание вестибулярных расстройств!!! (куда едет лифт? ? ? : -)) n Канамицин, Амикацин, Тобрамицин - слуховые расстройства n n Предрасполагающие факторы – Концентрации выше терапевтических, длительное применение, повторные курсы – Наличие ХПН, дегидратация, гиповолемия, возраст старше 70 – Комбинация с амфотерицином В, ванкомицином, цефалоспоринами, фуросемидом, НПВС

Требования к режиму дозирования аминогликозидов n n n стремление к достижению максимальных концентраций в пределах терапевтического диапазона при достаточно длительных интервалах между введениями Оптимальным является болюсное введение всей суточной дозы однократно внутривенно в виде короткой инфузии: Амикацин 15 - 25 мг/кг/сут Гентамицин 3 - 5 мг/кг/сут Нетилмицин 4 - 6 мг/кг/сут Тобрамицин 3 - 5 мг/кг/сут однократное введение всей суточной дозы аминогликозидов более эффективно и более безопасно, чем многократное введение

Фторхинолоны Ранние Преим. Гр(-) Ципрофлоксацин + синегнойная палочка + стафилококк Офлоксацин +стафилококк Пефлоксацин (менингит, ИЖВП, ХПН) n n n Госпитальные инфекции Новые Гр (-), Гр (+) n Левофлоксацин + стрептококк n Моксифлоксацин + стрептококк, анаэробы + внебольничные MRSA Тяжелые внебольничные инфекции Стафилококк (в т. ч. MRSA) Моксифлоксацин >Левофлоксацин = Ципрофлоксацин = Офлоксацин n Enterobacteriaceae (перекрестная резистентность) Ципрофлоксацин > Левофлоксацин > Моксифлоксацин > Офлоксацин n n P. аeruginosa Ципрофлоксацин >> Левофлоксацин > Офлоксацин

Ранние фторхинолоны (с 1981 г. ) Ципрофлоксацин (ципробай) n Офлоксацин (таривид) n Пефлоксацин (абактал) n n Антимикробная активность: преимущественно Грам(-) Основное применение n Госпитальные инфекции – Внебольничные инфекции § МВП § Кишечные § Респираторные – низкая анти. Грам(+)

Отличительные особенности ранних фторхинолонов Препарат Особенности Клиника Ципрофлоксацин Наиболее активен Базовый ФХ госпитальные инф. P. aeruginosa Офлоксацин Биодоступность Безопасность Инфекции МВП Хламидиоз Пефлоксацин Особая ФК Абдомин. инфекции Менингит

Современное значение ципрофлоксацина n Инфекции мочевыводящих путей – Пиелонефрит – Простатит n Инфекции, вызванные синегнойной палочкой – Муковисцидоз – Бронхоэктатическая болезнь – Сепсис (в комбинации с бета-лактамами) Госпитальные инфекции вне ОРИТ n Инфекции костей n – Остеомиелит

Новые фторхинолоны: «Антипневмококковые» «Респираторные» n Левофлоксацин 1997 (FDA) 1999 (РФ) – Таваник § Внутрь и внутривенно n Моксифлоксацин 1999 (FDA) 2000 (РФ) – Авелокс § Внутрь и внутривенно

Различия между ранними и новыми фторхинолонами n Более высокая природная активность новых фторхинолонов против грамположительных бактерий – Streptococcus pneumoniae (х 4 -12) – Staphylococcus aureus (х 2 -8) – Enterococcus faecalis (х 2 -4) n Более высокая природная активность против микоплазмы и хламидий (х 2 -4) n Появление у моксифлоксацина активности против анаэробных бактерий n Активность против Грам(-) бактерий сходная – Перекрестная устойчивость

Левофлоксацин n Первый фторхинолон с повышенной активностью против пневмококков – Рекомендован FDA 2000 г. для лечения ВП, вызванной PRSP – Различия между левофлоксацином и офлоксацином минимальные: МПК 1 и 2 мг/л n Левовращающий изомер офлоксацина

Моксифлоксацин (Авелокс) n 1999 год – регистрация FDA (США), ЕС – – – Внебольничная пневмония Обострение хронического бронхита Острый синусит n 2003 год – одобрен FDA для лечения ВП, вызванной PRSP n 2000 – 2006 годы – – Зарегистрирован в >90 странах Пероральная и внутривенная лекформы Ежегодно назначается >25 млн пациентам >3400 научных публикаций
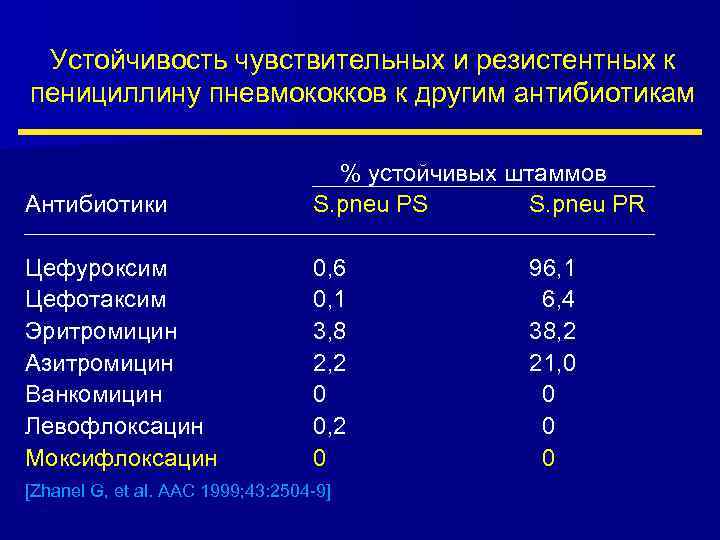
Устойчивость чувствительных и резистентных к пенициллину пневмококков к другим антибиотикам Антибиотики % устойчивых штаммов S. pneu PS S. pneu PR Цефуроксим Цефотаксим Эритромицин Азитромицин Ванкомицин Левофлоксацин Моксифлоксацин 0, 6 0, 1 3, 8 2, 2 0 0, 2 0 [Zhanel G, et al. AAC 1999; 43: 2504 -9] 96, 1 6, 4 38, 2 21, 0 0

Моксифлоксацин (Авелокс) Отсутствует устойчивость респираторных патогенов n Не способствует формированию устойчивых штаммов n Быстрый бактерицидный эффект в отношении Streptococcus pneumoniae n Наиболее надежное средство при тяжелой внебольничной пневмонии n Улучшает долговременный прогноз при ХОБЛ n Средство 1 -го ряда при синусите – более быстрое исчезновение симптомов – за счет антианаэробной активности n

Гликопептиды Ванкомицин Спектр активности: § резистентные Гр (+) MRSA, ARE § анаэробы (+ Clostridium difficile) Недостатки: – Медленное бактерицидное действие – Низкие концентрации в тканях, ликворе § Субклиническая эффективность (ИЭ) § Рецидивы инфекции – Переносимость и токсичность – Резистентные энтерококки (VREf) – Стафилококки со сниженной чувствительностью § Документированный неуспех терапии Режим дозирования: 30 -40 мг/кг/сут, не более 2 г/сут через 12 часов, продолжительность введения не менее 1 часа.

Побочные эффекты Ванкомицина n n n n n Гипотония Анафилаксия Псевдомембранозный колит Кожные реакции Лекарственная лихорадка Флебиты Нефротоксичность Ототоксичность Red-neck / red-man syndrome (синдром красной шеи ) Обусловлен выбросом гистамина при быстром введении ванкомицина. Не является показанием для отмены препарата. Профилактика: – Антигистаминные препараты перед введением – Медленное, дробное введение – Использование очищенных препаратов – Коррекция гиповолемии, сердечной недостаточности – Избегать комбинаций с нефро- или ототоксичными препаратами – Желательно мониторирование концентрации в крови

Липопептиды - даптомицин § Даптомицин имеет уникальный механизм действия, обеспечивает новый метод уничтожения Грам (+) бактерий путем прекращения целого ряда функций мембраны бактериальной клетки без проникновения в ее цитоплазму § Обратимо связывается с мембраной Грам (+) бактерий § § Кальций –зависимый механизм внедрения в мембрану клетки Олигомеризация для формирования пор или ионных каналов (амфифильная структура) § Быстрая деполяризация мембраны клетки § Эффлюкс ионов калия § Нарушение градиента концентрации ионов § Деполяризация приводит к гибели клетки § § Подавление синтеза ДНК и РНК Кубицин вызывает быстрый бактерицидный эффект без лизиса клетки (99% штаммов MSSA и MRSA погибают меньше, чем через 1 час, сохраняет бактерицидность 24 часа) Canepari et al. Antimicrob Agents Chemother 1990; 34: 1220– 1226; Silverman et al. Antimicrob Agents Chemother 2003; 47: 2538– 2544 Alborn et al. , Antimicrob Agents Chemother 1991; 35: 2282– 2287; Steenbergen et al. J Antimicrob Chemother 2005; 55: 283– 288 Jung et al. Chem Biol 2004; 11: 949– 957

Даптомицин (Кубицин) § Даптомицин является продуктом ферментации, выделенным из Streptomyces roseosporus § 1 раз в день, в/в § Первый препарат нового класса антибиотиков - циклических мембранодеполяризационных липопептидов с уникальным механизмом действия § Нет перекрестной резистентности с антибиотиками других классов § Нет известного механизма резистентности § Широкий спектр активности против Грам +бактерий, включая метициллин-резистентные Staphylococcus aureus (MRSA) § Быстрый бактерицидный эффект § Высокая клиническая эффективность у более, чем 325, 000 пациентов § США: одобрение в сентябре 2003 для лечения осложненных инфекций кожи и ее структур (c. SSSIs), в 2006 – одобрение для лечения S. aureus бактериемии и правостороннего инфекционного эндокардита § Европа: одобрение в январе 2006 для лечения осложненных инфекций кожи и мягких тканей (c. SSTIs) CUBICIN Summary of Product Characteristics 2006 La. Plante, Rybak. Exp Opin Pharmacother 2004; 5: 2321– 2331 Silverman et al. Antimicrob Agents Chemother 2003; 47: 2538– 2544 CUBICIN Prescribing Information

Оксазолидиноны • Первый представитель класса – линезолид (зивокс) • Антимикробная активность - Грам(+), вкл. MRSA • Сохраняет активность в отношении ванкомицинрезистентных энтерококков (VREf) и стафилококков со сниженной чувствительность к ванкомицину (VISA) • Резистентных к линезолиду штаммов в РФ не выявлено • Возможность парентерального и перорального применения • Режим дозирования: 600 мг с интервалом 12 часов

Линезолид (Зивокс) • Препарат выбора при НПивл, вызванной MRSA – Превосходит ванкомицин по клинической эффективности в 3 раза – Летальность на фоне линезолида в 2, 2 раза ниже по сравнению с ванкомицином [M. Kollef e. a. ICM 2004; 30: 388 -94] • Препарат выбора при MRSA инфекциях кожи и мягких тканей, осложненных сепсисом – Клиническая эффективность выше ванкомицина на 10% – Эрадикация MRSA на 22% выше ванкомицина (Р<0. 0001) [Weigelt e. a. , 2003]

Линезолид (Зивокс) • Другие клинические ситуации, при которых назначение линезолида обосновано и целесообразно: – Инфекции любой локализации, вызванные стафилококками, устойчивыми к ванкомицину • Всегда сохраняется чувствительность к линезолиду – Бактериемия или тяжелый сепсис, вызванный Enterococcus faecium • Возможен клинический неуспех ванкомицина в случае резистентных штаммов – Предшествующее применение ванкомицина • Риск селекции ванкомицин-резистентных штаммов – Инфекции MRSA у больных на гемодиализе* – Тяжелый сепсис/шок с ОПН* – MRSA-инфекции ЦНС, вкл. инфекцию шунтов* • Пенетрация линезолида в ликвор 66% [Myrianthefs, AAC; 50: 3971] * Не зарегистрированное показание

Макролиды n Streptococcus n Chlamydia, Mycoplasma – – – Активность высокая Устойчивость умеренная, но выше чем у пенициллина Различия между препаратами минимальны и клинически не значимы Активность высокая Различия между препаратами минимальны и клинически не значимы § Резистентность не документирована n Staphylococcus MS при непереносимости бета-лактамов n Haemophilus influenzae

Эритромицин vs. современные макролиды Параметр Азитро Кларитро Спиро, Джоза n Спектр Эри Эри n Уровень акт-ти Эри Эри n Эритро-R штаммы R n Стабильность > Эри n Биодоступность > Эри n Дозирование 1 кр. 2 кр. 2 - 3 кр. n Безопасность > Эри R > Эри S – R • Побочные эффекты макролидов Эритро > Кларитро > Джоза > Азитро = Спира = Мидеко = Рокситро • Стимуляция моторики ЖКТ (эритромицин > азитромицин > спирамицин) • Гепатит, холестаз (эритромицин) • Тромбофлебит при в/в введении • Лекарственные взаимодействия

Клиническое применение макролидов Основные показания n Тяжелая внебольничная пневмония в комбинации с бета-лактамами (Ц II - III, АКК) – Эритромицин или – Кларитромицин или – Азитромицин или – Спирамицин § § § § Урогенитальный хламидиоз и микоплазмоз Легионеллез Эрадикация H. pylori (Клар) Токсоплазмоз (Спир, Клар, Рокс, Азитро) Периодонтит (Спирамицин) Профилактика эндокардита (при непереносимости пенициллинов) Дифтерия, коклюш

В конце ХХ века сформировалось представление об особой форме организации микрофлоры организма человека - хорошо организованном взаимодействующем сообществе микроорганизмов, покрывающих поверхности кишечной стенки, других слизистых оболочек, кожи и зубов человека.

Оказалось, что микробы, во-первых, предпочитают жить, будучи прикрепленными к твердой поверхности, нежели свободно плавающими - как в водной среде, так и в воздухе. Во-вторых, они организованы в так называемые биопленки (Biofilm), сбалансированные по видовому составу и функциональному распределению членов сообщества. Фото: Комбинация биопленки, водорослей и солей кальция (фото выполнено конфокальным микроскопом) на стенке бассейна.

В природе биопленки распространены повсеместно. Также они выстилают нефтепроводы, аквариумы, постоянные катетеры, внутренние имплантаты, контактные линзы и протезы. Тонкое наслоение, формирующееся на зубах, пример, хорошо знакомый каждому. Формировать биопленки способны многие микроорганизмы, однако наибольшее клиническое значение имеют биопленки, формируемые Staphylococcus spp. , Pseudomonas aeruginosa. Из эукариотических микроорганизмов основное значение имеют Candida spp. С. В. Сидоренко Инфекционный процесс как "диалог" между хозяином и паразитом, 2001.
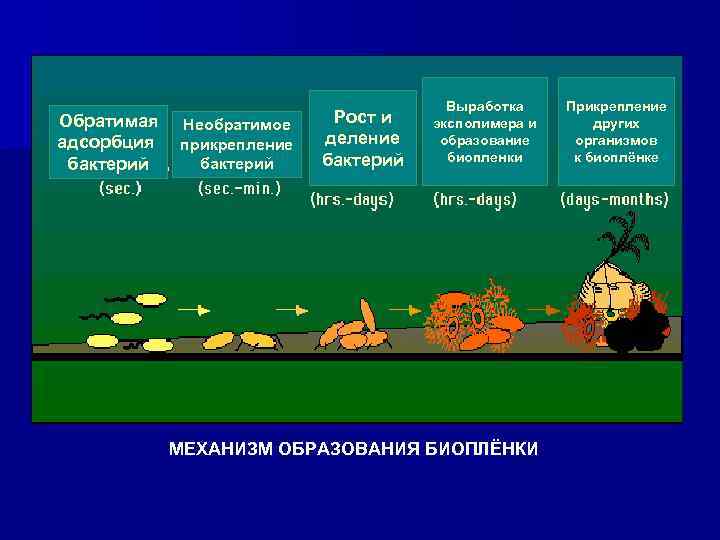
Обратимая адсорбция бактерий Необратимое прикрепление бактерий Рост и деление бактерий Выработка эксполимера и образование биопленки МЕХАНИЗМ ОБРАЗОВАНИЯ БИОПЛЁНКИ Прикрепление других организмов к биоплёнке

Биопленки могут оказаться и очень опасными. Болезнь легионеров, унесшая жизни 29 человек в Филадельфии в 1976 г. , оказалась связанной с бактериями биопленки, образовавшейся в системе кондиционирования воздуха. Легионеллёзная пневмония в Верхней Пышме в 2007 году (Свердловская область) была связана с биоплёнками в системе горячего водоснабжения. Миллионы долларов ежегодно расходуются в мире на работы по контролю за подобными биопленками.
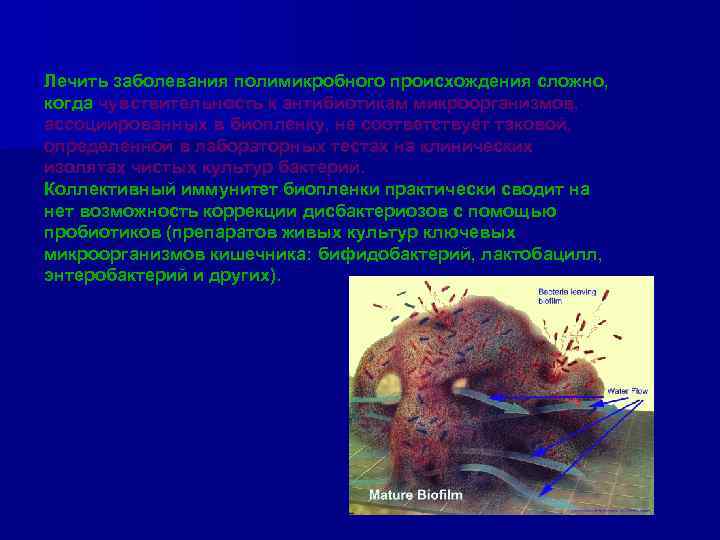
Лечить заболевания полимикробного происхождения сложно, когда чувствительность к антибиотикам микроорганизмов, ассоциированных в биопленку, не соответствует таковой, определенной в лабораторных тестах на клинических изолятах чистых культур бактерий. Коллективный иммунитет биопленки практически сводит на нет возможность коррекции дисбактериозов с помощью пробиотиков (препаратов живых культур ключевых микроорганизмов кишечника: бифидобактерий, лактобацилл, энтеробактерий и других).

Внутри плёнки существует движение, поток… Биоплёнка образованная Pseudomonas aeruginosa (синегнойная палочка)

Проблема резистентности биоплёнок Pseudomonas Aeruginosa(PA) Барьерный эффект Изменение внутренней среды в плёнке Другие подтипы резистентности Больше лактамаз: индукция выработки бета-лактамаз




Кларитромицин (Клацид) (разводить вначале в воде для инъекций, затем инфузия на физ. рре за 60 мин) n Противовоспалительный эффект n Иммуномодулирующий эффект n Стимуляция фагоцитоза n Разрушение биопленок !!!

Линкозамиды Клиндамицин превосходит Линкомицин по уровню антибактериальной активности и биодоступности n Спектр активности: – – – n Грам(+) (кроме госпитальных MRSA и энтерококков), анаэробы (устойчивость Bacteroides spp. 30% и более!) Внебольничные MRSA Показания: – – Нетяжелые стафилококковые и стрептококковые инфекции Некротизирующие инфекции мягких тканей Инфекции костей и суставов В сочетании с бета-лактамами при абдоминальных инфекциях и легочных нагноениях (эмпиема, абсцесс)

Тетрациклины n Современное применение ограничено ростом устойчивости микроорганизмов n Препараты выбора при хламидийных и микоплазменных инфекциях n В сочетании с бета-лактамами при эмпирической терапии воспалительных заболеваний органов малого таза
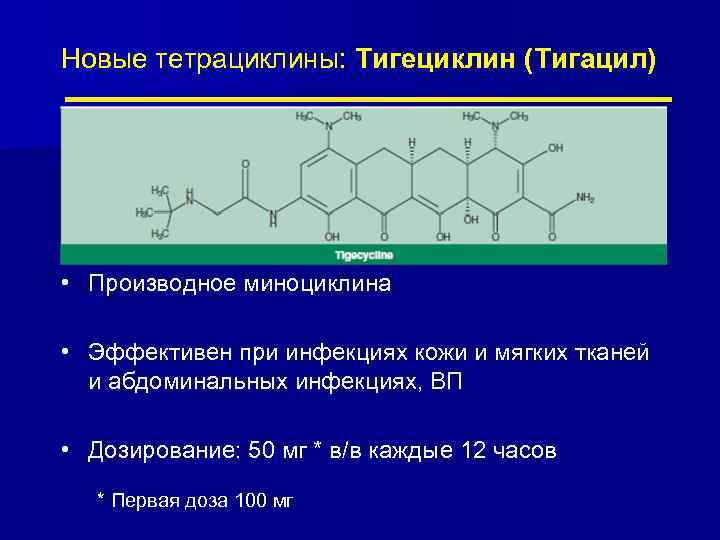
Новые тетрациклины: Тигециклин (Тигацил) • Производное миноциклина • Эффективен при инфекциях кожи и мягких тканей и абдоминальных инфекциях, ВП • Дозирование: 50 мг * в/в каждые 12 часов * Первая доза 100 мг

Тигециклин: первый анти-MRSA антибиотик с широким спектром: возможность монотерапии? Анти-MRSA активность + Грам(+) Грам(-) VRE PRSP Enterobacteriaceae: ESBL, KPC Acinetobacter baumanii Stenothrophomonas maltophilia Анаэробы

Отличительные свойства тицециклина n Широкий спектр: Грам(+), Грам(-), анаэробы + Возможность эмпирической монотерапии n Активность против резистентных возбудителей: MRSA, БЛРС, Acinetobacter, Stenotrophomonas, энтерококки (в т. ч. VREf) + Возможность эмпирической терапии нозокомиальных инфекций Природная устойчивость P. aeruginosa n Хорошая тканевая и в/клеточная ФК: Тк/Сыв = 5 -10; Нейтрофилы >20 -30; АМ > 80. n Низкие концентрации в крови n – Бактериемия? n Проявляет активность против микробов в биопленках

Клинические исследования тигециклина (Тигацил) Осложненные инфекции Ки. МТ Тигециклин = ванкомицин + азтреонам [Sacchidanant S, e. a. Intern J Infect Dis 2005; 9(5): 251 -61] Осложненные абдоминальные инфекции Тигециклин = имипенем [Babinchak T, e. a. Clin Infect Dis 2005; 41(Suppl 5): 354 -66]

Потенциал тигециклина (Тигацил®) в медицине • В качестве средства целенаправленной этиотропной терапии НИ, вызванных полирезистентными бактериями – – БЛРС: альтернатива карбапенемам Acinetobacter baumanii: альтернатива сульбактаму Klebsiella, E. coli, устойчивые к карбапенемам Stenotrophomonas maltophilia • Особые показания: полимикробные инфекции – MRSA + Грам(-) – Enterococci + Грам(-) • Монотерапия. Возможная комбинация: + ПИП/ТАЗО

Потенциал тигециклина (Тигацил®) в медицине В качестве средства эмпирической терапии • Абдоминальные инфекции – Послеоперационный перитонит с факторами риска R – Третичный перитонит • Инфекции кожи и мягких тканей – Некротические инфекции, диабетическая стопа, ИОХВ • Предшествующие антибиотики, полимикробная инфекция • Дозирование: 1 доза: 100 мг в/в, затем по 50 мг в/в каждые 12 часов

New-Deli Metallo-beta-lactamase 1 n По данным Агентства по охране здоровья (HPA), так называемые "супермикробы" (superbugs) - антибиотикоустойчивые микробы, обладающие геном NDM-1 - выделены у 50 пациентов британских больниц, многие из которых недавно подвергались хирургическим вмешательствам в Индии и Пакистане. Такие бактерии были найдены также у нескольких больных из разных городов США, Канады, Австралии, Нидерландов и Швеции. Ген NDM-1 (New Delhi metallo-beta-lactamase 1) кодирует фермент металло-беталактамазу. Она разрушает любые бета-лактамные антибиотики (пенициллины, цефалоспорины, карбапенемы и монобактамы) и ряд других – в эксперименте микробы оказались чувствительны только к тигециклину и полимиксину Е, часть изолятов – к азтреонаму. Впервые, как видно из названия, этот ген был найден в Нью-Дели, затем – в ряде других городов Индии, а также Пакистана и Бангладеш. NDM-1 был обнаружен у нескольких разновидностей кишечной палочки, протея и клебсиеллы. Таким образом, инфекция может поражать дыхательные пути, желудочно-кишечный тракт, мочеполовую систему и мягкие ткани, а также вызывать сепсис.

Метронидазол Спектр активности • Анаэробы • Helicobacter pylori • Простейшие Показания • • Анаэробная инфекция предполагаемая или подтвержденная: Периоперационная профилактика в абдоминальной хирургии Интраабдоминальные и инфекции органов малого таза Инфекции НДП (аспирац. пневмония, эмпиема плевры, абсцесс легкого) Инфекции ЦНС (менингит, абсцесс мозга) Инфекции полости рта Псевдомембранозный колит Антианаэробной активностью обладают также Ингибиторзащищенные пенициллины (Тик/Клав, Ам/Клав, Амп/Сульб, Пип/Тазо) Карбапенемы, Ванкомицин, Линезолид, Линкозамиды Моксифлоксацин

«Старые» (=добрые!) антибиотики n Полимиксины (колистин = полимиксин Е, полимиксин В) n Фосфомицин n Ко-тримоксазол (бисептол) n Фузидиевая кислота (и её соли)

Полимиксины n Незаменимы при инфекциях, вызванных 1) панрезистентными грамотрицательными неферментирующими бактериями 2) грамотрицательными энтеробактериями – продуцентами металлобеталактамаз плазмидного типа

Фосфомицин n n антибиотик бактерицидного действия ингибирует образование микробной стенки на ранних стадиях за счет подавления синтеза уридинфосфат-N-ацетилмурамовой кислоты не обладает тератогенным, мутагенным и эмбриотоксическим действием. В случае необходимости может назначаться беременным женщинам и новорожденным

Фосфомицин n n хорошо проникает в различные ткани и жидкости организма, включая почечную и костную ткань, ЦНС. Препарат обладает уникальным свойством препятствовать адгезии ряда бактерий к клеткам уроэпителия человека. Основной путь экскреции фосфомицина – почечный (90 -100% от введенной дозы в течение суток), Период полувыведения составляет 1, 5 -2 ч. (у детей – от 45 мин до 1, 5 часов, в зависимости от дозы).

Фосфомицин n Взрослые - парентерально в/в (медленно болюсно или в виде инфузии) по 1, 0 - 4, 0 г 4 раза в сутки. n Дети (начиная с периода новорожденности) - внутривенно 100 - 400 мг/кг/сутки в 3 -4 введения

Монобактамы - азтреонам n n синтетический антибиотик группы монобактамов для парентерального применения. уникален стабильностью к бета-лактамазам, фармакокинетикой и низкой токсичностью. обладает высокой бактерицидной активностью против грамотрицательных аэробов – практически всех. Enterobacteriaceae, Neisseria gonorrhoeae и Pseudomonas aeruginosa. демонстрирует высокую клиническую эффективность в лечении нозокомиальных инфекций, вызванных грамотрицательными бактериями, включая P. aeruginosa и K. pneumoniae.

Азтреонам n устойчив к гидролизу металло-бета-лактамазой NDM-1 (New Delhi metallo-beta-lactamase) n Эффективен в комбинации с пенициллинами, цефалоспоринами, гликопептидами, линкозамидами, метронидазолом, аминогликозидами n хорошо проникает и накапливается в различных тканях и жидкостях (в т. ч. плевральной и перитонеальной) организма n n Характерно увеличение проницаемости через ГЭБ при воспалении мозговых оболочек. Незначительно метаболизируется в печени. Обнаруживается в высоких концентрациях в моче. Период полувыведения составляет 1, 5 -2 ч.

Азтреонам n Взрослые - парентерально в/м или в/в (струйно медленно или в виде в/в инфузии) по 1, 0 -2, 0 г 3 -4 раза в сутки (при синегнойной инфекции до 12, 0 г в сутки). Дети - 30 мг/кг каждые 8 часов в/в или в/м; для лечения тяжелых и угрожающих жизни инфекций, а также инфекций у больных с муковисцидозом вводят по 30 мг/кг каждые 6 часов в/в. n Максимальная доза – 120 мг/кг/сутки. n

Карбапенемы n. Отдельный класс бета-лактамных антибиотиков – тиенамицины n. Производные тиенамицина соединения полученного из плесени (!) Streptomyces cattleya n. Самый широкий спектр действия из всех бета-лактамов n. Механизм действия сходен с другими бета-лактамами

Современное значение карбапенемов n Эмпирическая терапия в ОРИТ – Тяжелый сепсис, НПивл (APACHE >15 баллов) – Панкреонекроз – Посттравматический и послеоперационный менингит (меропенем) n Этиотропная терапия – Гр (-) бактерии, продуценты БЛРС (Klebsiella spp. , Enterobacter) Гр (-) бактерии, продуценты БЛРС – Acinetobacter spp. – P. aeruginosa, устойчивые к ЦС III—IV n Устойчивы к карбапенемам – – – MRSA Enterococcus faecium Stenotrophomonas maltophilia, Burkholderia cepacia Гр(-) бактерии, продуцирующие металло-беталактамазы Ps. aeruginosa – 40%

Карбапенемы - спектр активности n n n Гр(+) практически все, кроме MRSA, Enterococcus faecium Гр(-) практически все, кроме Stenotrophomonas maltophilia и Burkholderia cepacia Рs. aeruginosa изначально чувствительна, но в процессе лечения может развивать устойчивость. Не чувствительны атипичные возбудители - микоплазмы и хламидии – у них нет точки приложения ! Тиенам более активен в отношении гр(+) кокков, но менее активен в отношении гр(-)палочек Меронем, Дорипенем более активны в отношении гр(-) бактерий, но менее активны в отношении стафилококков и стрептококков

Классификация карбапенемов ГРУППА 1 Карбапенемы ГРУППА 2 (инфекции при Карбапенемы поступлении в стационар (Внутрибольничные – ограниченная инфекции– активность против неферментирующих Pseudomonas и грамотрицательных Acinetobacter) палочек) Эртапенем (Инванз) Имипенем Меропенем Дорипенем ГРУППА 3 Карбапенемы (активность против MRSA) CS-023 (исследуется) MRSA=S. аureus, резистентный к метициллину Адаптировано из Shah PM, Isaacs RD J Antimicrob Chemother 2003; 52: 538– 542; Thomson KS, Smith Moland E J Antimicrob Chemother 2004; 54: 557– 562; Mouton JW et al Clin Pharmacokinet 2000; 39: 185– 201.

Карбапенемы n Имипенем более активен против энтерококков и стафилококков Особые показания: n Меропенем более активен в отношении P. aeruginosa и Burkholderia cepacia Особые показания: – Менингит – P. aeruginosa – Инфекции костей и суставов – эндокардит n n Режим дозирования: 1 г в 3 -4 введения Режим дозирования: 0, 5 -1 г в 3 -4 введения

Карбапенемы: эртапенем n Не Антипсевдомонадный карбапенем ! – P. aeruginosa и Acinetobacter природно устойчивы Активность против Грам(+), Enterobacteriaceae и анаэробов сходна с имипенемом n Позиционирование: n – Тяжелые внебольничные и ранние нозокомиальные инфекции, вызванные Enterobacteriaceae - продуцентами БЛРС Режим дозирования: 1 г 1 раз в сутки

Свойства Эртапенема n Широкий спектр активности n Быстрый бактерицидный эффект n Надежная эффективность n Низкий уровень резистентности n Благоприятная фармакокинетика / фармакодинамика n Сохранение экологии стационара

Объективная потребность в новых антибиотиках n В структуре инфекций стали доминировать антибиотикорезистентные штаммы n Полирезистентные штаммы вышли за пределы ОРИТ и стационаров n Снижение клинической эффективности антибиотиков при лечении ИАИ, вызванных полирезистентными возбудителями n Регистрация устойчивых штаммов к антибиотикам резерва
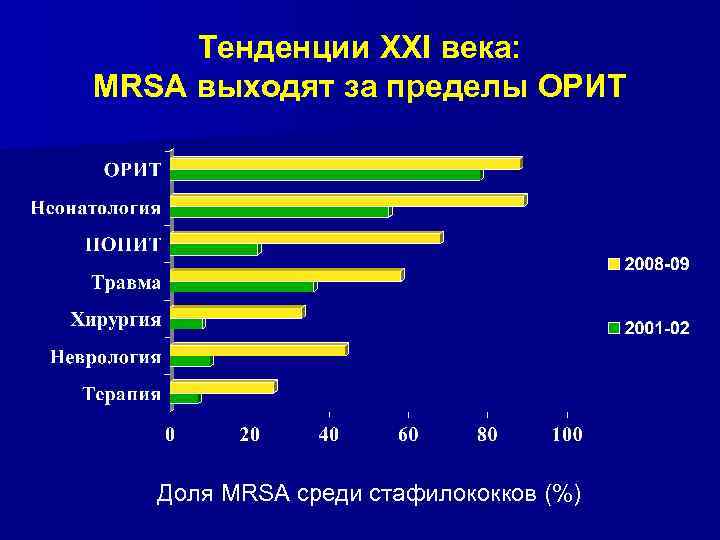
Тенденции XXI века: MRSA выходят за пределы ОРИТ Доля MRSA среди стафилококков (%)

Резистентность Enterobacteriaceae к ЦС III и продукция БЛРС в отделениях различного профиля 73, 7 94, 5 83, 2 60, 0 53, 6 * Штаммы, нечувствительные к цефтазидиму или цефотаксиму
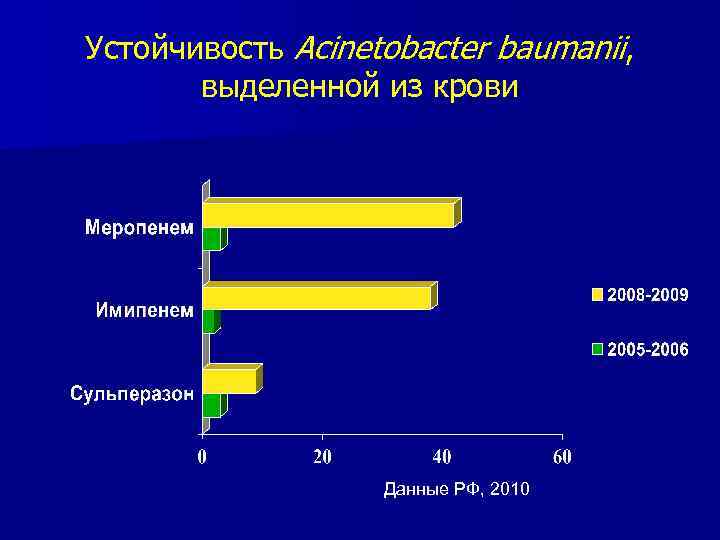
Устойчивость Acinetobacter baumanii, выделенной из крови Данные РФ, 2010
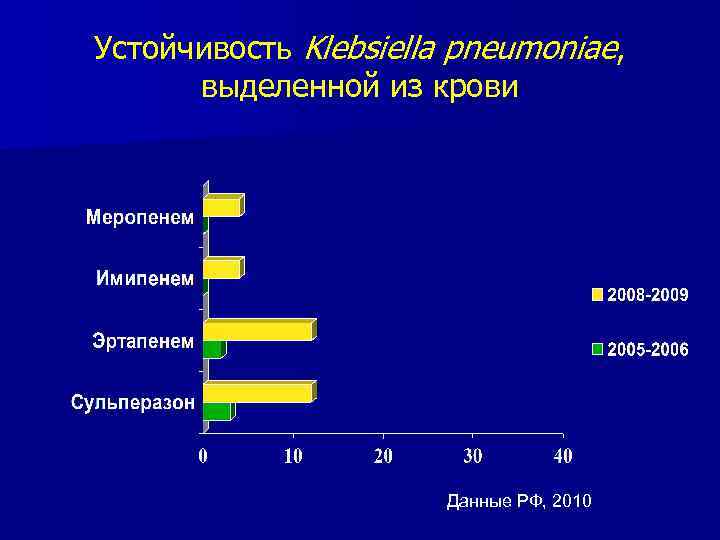
Устойчивость Klebsiella pneumoniae, выделенной из крови Данные РФ, 2010
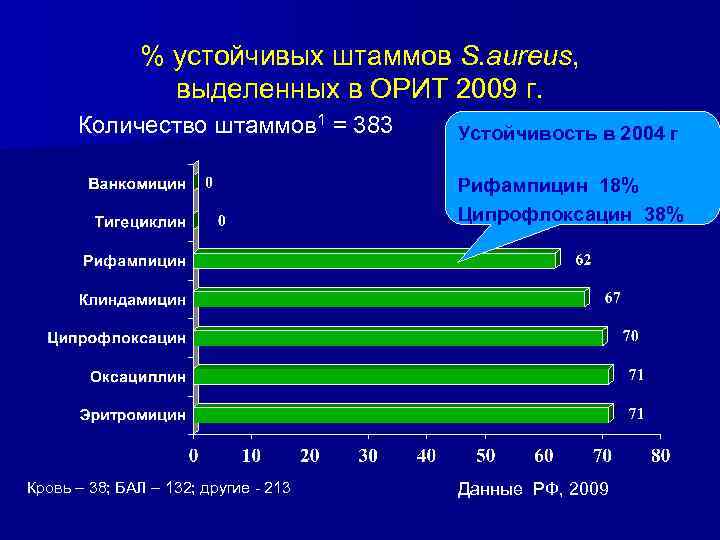
% устойчивых штаммов S. aureus, выделенных в ОРИТ 2009 г. Количество штаммов 1 = 383 Устойчивость в 2004 г Рифампицин 18% Ципрофлоксацин 38% Кровь – 38; БАЛ – 132; другие - 213 Данные РФ, 2009
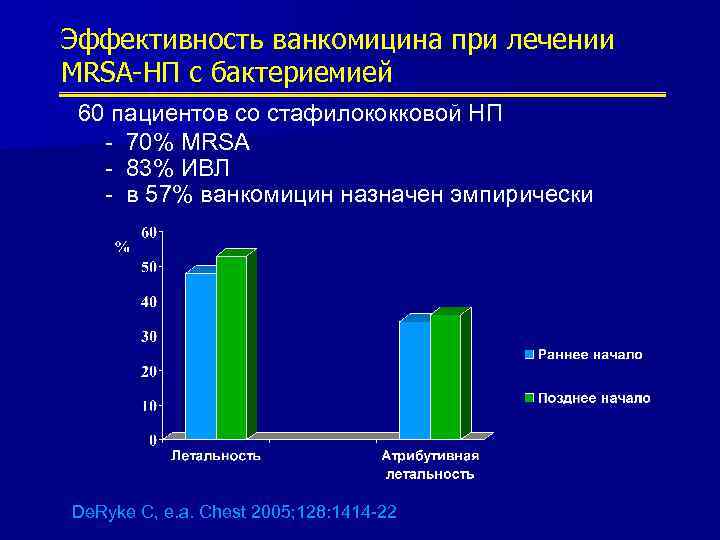
Эффективность ванкомицина при лечении MRSA-НП с бактериемией 60 пациентов со стафилококковой НП - 70% MRSA - 83% ИВЛ - в 57% ванкомицин назначен эмпирически De. Ryke C, e. a. Chest 2005; 128: 1414 -22
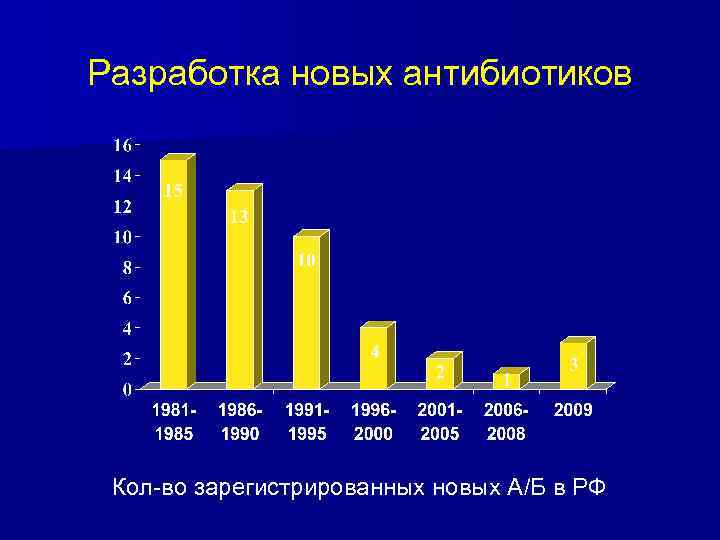
Разработка новых антибиотиков Кол-во зарегистрированных новых А/Б в РФ

Какие новые антибиотики нам нужны? • Энтеробактерии – БЛРС: альтернатива карбапенемам • Ацинетобактерии – Альтернатива сульперазону • Синегнойная палочка – Антибиотики с минимальным риском формирования устойчивости • MRSA, энтерококки – Повышение бактерицидности – Хорошая тканевая фармакокинетика

Новые антибактериальные препараты XXI века «Целевые» микроорганизмы Резистентные Грам(+) Грам(-) и Грам(+), в т. ч. MRSA Резистентные Грам(-) Тигециклин Цефтобипрол Дорипенем «ПИП/ТАЗО» Цефтаролин Разупенем Иклаприм Новые ингибиторы БЛ 2003 Линезолид 2009 Даптомицин После 2010 Телаванцин Далбаванцин
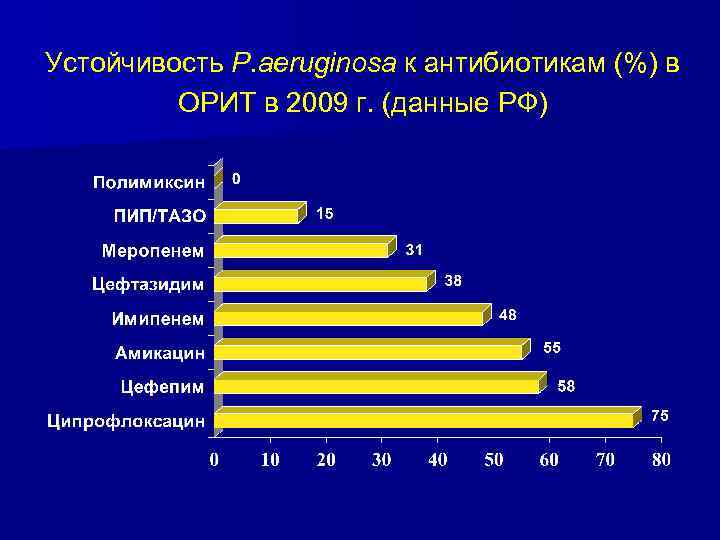
Устойчивость P. aeruginosa к антибиотикам (%) в ОРИТ в 2009 г. (данные РФ)
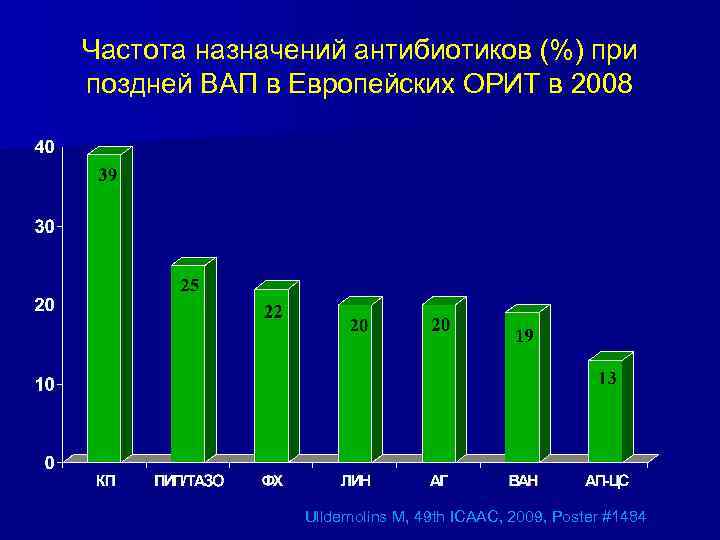
Частота назначений антибиотиков (%) при поздней ВАП в Европейских ОРИТ в 2008 Ulldemolins M, 49 th ICAAC, 2009, Poster #1484

Структура назначений антибиотиков для лечения ВАП в европейских ОРИТ 27 ОРИТ в 9 странах Европы 2436 пациентов Факторы, влияющие на выбор антибиотика врачом (многофакторный анализ) • Длительность Колистин (OR 5. 3) нахождения в ОРИТ Линезолид (2. 8) • Частота MRSA>10% Анти-MRSA (1. 5) • Acinetobacter >10% Колистин (115. 7) Карбапенем (3. 5) Не назначение антипсевдомонадного ЦС (2. 3) • Травма Ulldemolins M, 49 th ICAAC, 2009, Poster #1484
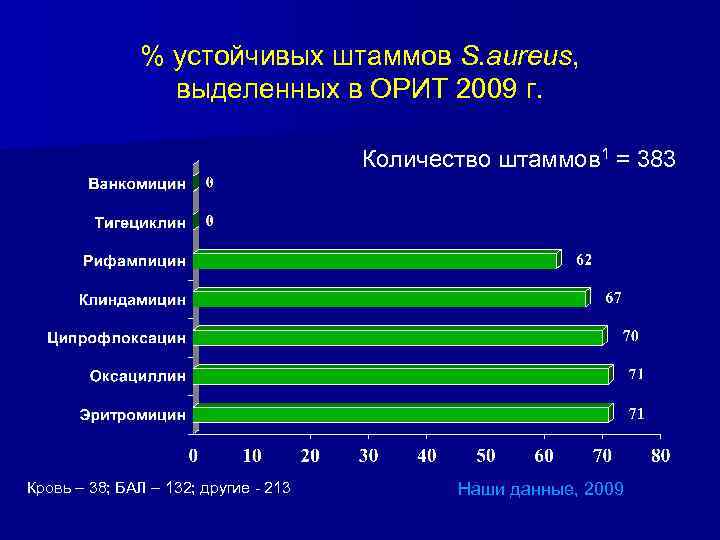
% устойчивых штаммов S. aureus, выделенных в ОРИТ 2009 г. Количество штаммов 1 = 383 Кровь – 38; БАЛ – 132; другие - 213 Наши данные, 2009
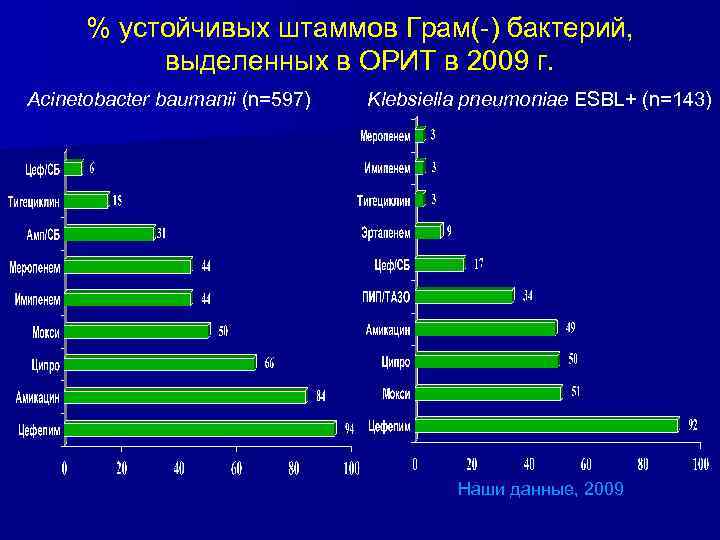
% устойчивых штаммов Грам(-) бактерий, выделенных в ОРИТ в 2009 г. Acinetobacter baumanii (n=597) Klebsiella pneumoniae ESBL+ (n=143) Наши данные, 2009
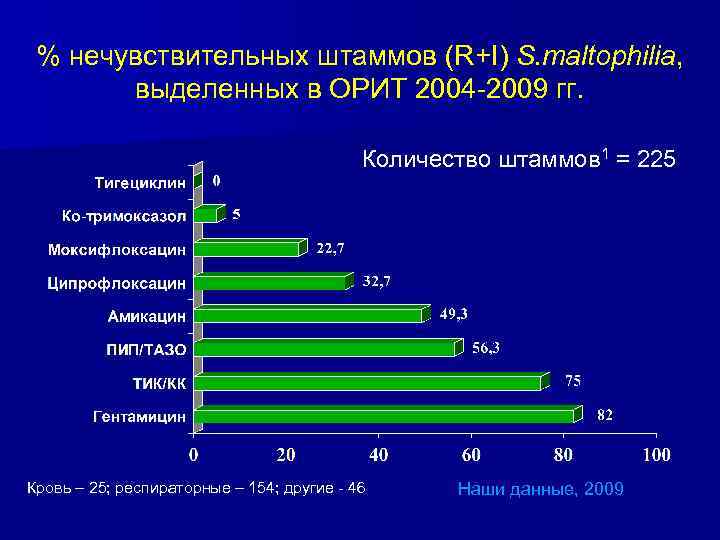
% нечувствительных штаммов (R+I) S. maltophilia, выделенных в ОРИТ 2004 -2009 гг. Количество штаммов 1 = 225 Кровь – 25; респираторные – 154; другие - 46 Наши данные, 2009

Феномен «Collateral damage» Экологический побочный эффект АБТ Селекция резистентных штаммов Цефалоспорины III-IV VRE E. coli, K. pneumonia (БЛРС+) Фторхинолоны Clostridium difficile MRSA Карбапенемы Ps. Aeruginosa Acinetobacter spp.

История болезни… n n n 69 -летняя женщина, бывший преподаватель высшей школы Острый неосложненный холецистит (хирургическое лечение, амокси/клав) Осложнения: спаечная кишечная непроходимость, абсцесс передней брюшной стенки, нагноение п/о раны Рост E. coli, Klebs. pneumoniae Антибиотикотерапия: Тиенам 1 г *3 р/сут Улучшение, планируемая выписка, НО!!!!

История болезни… n n n n Лихорадка до 38, 5 Диаррея 5 сут, отрицательные результаты посева крови Диффузная боль в животе Лейкоцитоз 14 тыс, СРБ+++ Нет аппетита, слабость, сонливость Кожа передней брюшной стенки: нет признаков инфекции Ожидаются результаты посева крови

История болезни… n КТ живота: множественные абсцессы печени

Что делать? n n Немедленная гемигепатэктомия + ванкомицин 2 г/сут Дренирование абсцессов под контролем КТ и эмпирическая терапия тигециклином Дренирование абсцессов под контролем КТ и эмпирическая терапия ПИП/ТАЗО Меропенем + эхинокандин, вмешательство отложить до стабилизации состояния

Ubi pus ibi evacua! Тигециклин 100 мг в/в, затем по 50 мг 2 раза/сут Посев содержимого абсцесса: E. faecium Гемокультура: E. faecium Контрастная КТ: 2 несообщающихся абсцесса печени

Клиническое течение n Нет добавочных абсцессов n Нет эндокардита n Медленный регресс абсцессов n Выписка через 6 нед n Через год: нет абсцессов, нет рецидивов n Нет роста E. faecium в посевах кала

Проблемные микробы Для каждой локализации – своя группа… Например, для осложненных ИАИ: n Энтерококки n MRSA (MRSE) n БЛРС (ESBL) - патогены n Ps. aeruginosa n Acinetobacter baumannii n Bacteroides fragilis

Мультирезистентные Энтерококки n E. faecalis: ампициллин/сульбактам, пиперациллин/тазобактам (Тазоцин), ванкомицин (Ванкоцин) n E. faecium: Линезолид (Зивокс), даптомицин (Кубицин), Тигециклин (Тигацил), Хинупристин/Дальфопристин (Синерцид)

MRSA Линезолид (Зивокс), даптомицин (Кубицин), Тигециклин (Тигацил), Хинупристин/Дальфопристин (Синерцид), ванкомицин (Ванкоцин) n Фузидин, рифампицин, тиенам+фосфомицин, ко-тримоксазол (бисептол) n Подозревать инфекцию, вызванную MRSA у колонизированных ранее лиц, на фоне гриппа, и применении антибиотиков (защищенных бета-лактамов и карбапенемов) в течение ближайших 3 -х месяцев n

БЛРС (ESBL) - патогены n n Резистентность ко всем цефалоспоринам, кроме цефоперазон/сульбактама, ассоциированная с резистентностью к фторхинолонам и аминогликозидам Формально противоречивые результаты в тесте чувствительности к антибиотикам (например: резист. к цефтриаксону и чувствит. к цефотаксиму – но так бывает только на бумаге!) Карбапенемы (в т. ч. Эртапенем - Инванз) , Тигециклин (Тигацил) В анамнезе – предшествующее лечение цефалоспроринами и фторхинолонами

Резистентная Ps. aeruginosa n Тиенам и меронем, тазоцин, цефтазидим (фортум), цефепим (максипим), ципрофлоксацин, амикацин, сизо-, тобрамицин, азтреонам n Нет антибиотика, к которому чувствительно более 90% n При панрезистентности - полимиксины

Резистентный Acinetobacter baumannii n Карбапенемы, аминогликозиды, ампициллин/сульбактам, цефоперазон/сульбактам n Тигециклин (тигацил) n Полимиксины

Резистентный Bacteroides fragilis n Метронидазол, тазоцин, карбапенемы n Резистентен к клиндамицину и моксифлоксацину

выводы?
Antibiotiki_-_GBSMP_-21_12_2010.ppt