анемии.ppt
- Количество слайдов: 83

Анемия снижение содержания гемоглобина и/или числа эритроцитов в крови по отношению к физиологическому уровню, необходимому для удовлетворения потребностей тканей в кислороде.

Классификация анемий по Идельсону Л. И. (1979 г) I. Анемии, связанные с кровопотерей: Острые постгеморрагические анемии Хронические постгеморрагические анемии II. Анемии, связанные с нарушенным кровообразованием: 1. Анемии, связанные с нарушением образования гемоглобина - анемии, связанные с дефицитом железа (железодефицитные) - анемии, связанные с нарушением синтеза или утилизации порфиринов (сидероахрестические) 2. Анемии, связанные с нарушением синтеза ДНК и РНК (мегалобластные) - анемии, связанные с дефицитом витамина В 12 (В 12 - дефицитная) - анемии, связанные с дефицитом фолиевой кислоты (фолиеводефицитная) 3. Анемии, связанные с нарушением процессов деления эритроцитов (дизэритропоэтические анемии): 4. Анемии, связанные с угнетением пролиферации клеток костного мозга (гипопластические и апластические анемии): III. Анемии, связанные с повышенным кроворазрушением (гемолитические анемии): 1. Наследственные гемолитические анемии 2. Приобретенные гемолитические анемии

Этиопатогенетическая классификация (Дворецкий Л. И. , Воробьёв П. А. , 1994). • • • I. Анемии вследствие кровопотери (постгеморрагические анемии): Острая постгеморрагическая анемия. Хроническая постгеморрагическая анемия. • • • II. Анемии вследствие нарушений процесса гемоглобинообразования или процессов эритропоэза: Железодефицитная анемия. Железоперераспределительная анемия (нарушение утилизации железа). Железонасыщенная (сидероахрестическая) анемия (нарушение синтеза и утилизации порфиринов). Мегалобластные анемии (нарушение синтеза ДНК и РНК), в том числе и В 12 - и фолиеводефицитные анемии. Гипопролиферативные анемии. Анемии, связанные с костно-мозговой недостаточностью, в том числе гипопластические (апластические) анемии, рефрактерная анемия при миелодиспластическом синдроме. Метапластические анемии, в том числе анемия при гемобластозах, анемия при метастазах рака в костный мозг. Дизэрйтропоэтические анемии. • • III. Анемии, вызванные усиленным распадом эритроцитов в организме (гемолитические): Наследственные, в том числе Минковского - Шоффара, серповидноклеточная анемия, гемоглобинозы, талассемия. Приобретенные, в том числе аутоиммунные, пароксизмальная ночная гемоглобинурия, лекарственные, травматические и микроанги-опатические, вследствие отравления гемолитическими ядами и бактериальными токсинами. IV. Анемии смешанные (полидефицитные), обусловленные сочетанным недостатком различных гемопоэтических факторов и действием ряда патологических механизмов (гемолиза, метаплазии, аутоиммунных конфликтов, кровопотери, сепсиса и др. ).

Нормальные показатели красной крови эритроциты у мужчин 4, 6 млн в мкл (4 -5, 1), у женщин - 4, 2 млн (3, 7 -4, 7); гемоглобин у мужчин 148 г/л (140 -160), у женщин - 130 г/л (120 -140), ретикулоциты 0, 7‰ (0, 2 -1, 2). средний объем эритроцита (MCV) 80 -96 f. L (фенталитр - один кубический мкл), ср. содержание гемоглобина в эритроците (МСН) 24 -35 пг ср. концентрация гемоглобина в эритроцитах (МСНС) 300 -380 г/л, гематокрит (Ht) у мужчин 0, 47, у женщин - 0, 42;

Среднее содержание гемоглобина в эритроците (MCH) MCH=Hb/B Hb - количество гемоглобина, г/л В – количество эритроцитов в литре крови

Средняя концентрация гемоглобина в эритроцитах (MCHС) MCHC=Hb/Ht Hb - количество гемоглобина, г/л Ht – гематокрит, %

Цветовой показатель (в норме 0, 85– 1, 05) Рассчитывается по формуле: Hbх3/В где Hb – содержание гемоглобина (в г/л), В – количество эритроцитов в литре.

Анемия По уровню ЦП Гипохромная ЦП < 0, 85 Железодефицитная Сидероахрестические Железоперераспреде лительные Нормохромная ЦП 0, 85 -1, 05 Гемолитическая Апластическая Острая постгеморрагическая Гиперхромная ЦП > 1, 05 В 12 дефицитная Фолиеводефицитная Анемии при миелодиспластическом синдроме
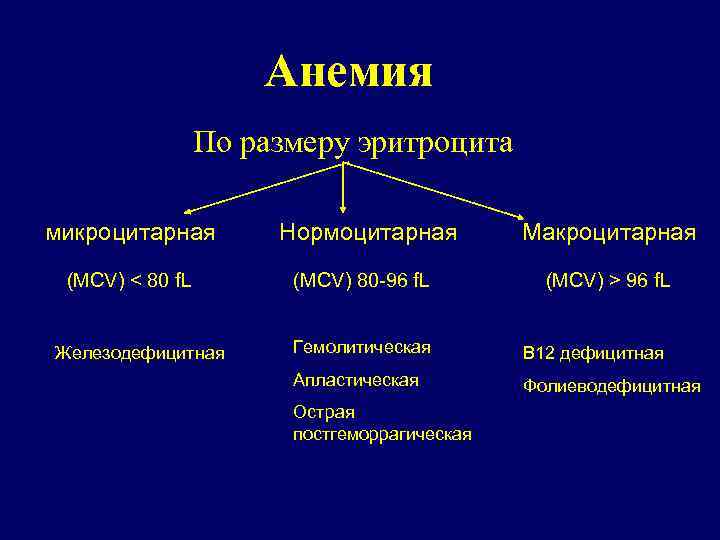
Анемия По размеру эритроцита микроцитарная (MCV) < 80 f. L Железодефицитная Нормоцитарная (MCV) 80 -96 f. L Макроцитарная (MCV) > 96 f. L Гемолитическая В 12 дефицитная Апластическая Фолиеводефицитная Острая постгеморрагическая

Классификация анемии по степени тяжести Легкая х 12 Кол-во эритроцитов 3, 0 -3, 5 10 /л; Нв – 110 -91 г/л Средней тяжести Тяжелая 12 х Кол-во эритроцитов 2, 0 -3, 0 10 /л; Нв – 90 -70 г/л х 12 Кол-во эритроцитов 1, 0 -2, 0 10 /л; Нв <70 г/л Крайне тяжелая 12 Кол-во эритроцитов менее 1, 0 10 /л

Железодефицитная анемия клинико-гематологический синдром, характеризующийся нарушением синтеза гемоглобина вследствие дефицита железа и проявляющийся анемией и сидеропенией.

Распространенность 1. железодефицитные анемии отмечаются примерно у 11% женщин детородного возраста 2. у мужчин больные железодефицитной анемией составляют около 2%. 3. скрытый дефицит железа в тканях - у 20 -25% По данным ВОЗ дефицит железа в той или иной степени выраженности имеется у 20% населения планеты.

В организме железо связано с белками. Железо содержат металлопротеины: ü белки, имеющие в своем составе гем (транспорт О 2) ü белки, переносящие и запасающие железо ü участвующие в окислительно-восстановительных реакциях В организме взрослого человека содержится 5 грамм железа: 1. В гемоглобине эритроцитов - 62% всего железа. 2. В миоглобине – 8% железа. 3. В тканевых ферментах – 5%. 4. 25% железа составляют его запасы (ферритин, гемосидерин и лабильный пул (плазма крови) Дефицит железа возникает при снижении его общего содержания (N сывороточного железа – 11, 6 -30 ммоль/л) Снижение уровня может протекать без функциональных нарушений, либо с развитием анемии.

Биодоступность железа. Различают: I. Гемовое железо. Всасывается в форме интактного порфиринового кольца. Обладает наивысшей биодоступностью (мясные продукты). Аскорбиновая кислота способствует всасыванию. II. Негемовое железо. Растворяется и становится компонентом пищевого пула ЖКТ. III. У пожилых снижается потребление мяса и снижается биодоступность железа. С возрастом снижается всасывание неорганического железа (для его всасывания необходим HCl). С возрастом повышается количество пациентов с атрофическим гастритом. Всосавшееся железо через 14 дней обнаруживается в молодых популяциях эритроцитов.

Дефицит железа возникает чаще всего при повышении потребления: • ускоренный рост (детский возраст) • интенсивные потери (беременность, лактация, менструация) Неизбежные физиологические потери – слущивание клеток кожи, ЖКТ, мочевыводящих путей, выделение с желчью. Уровень нормальной суточной экскреции железа равен 0, 61 -1, 02 мг При лактации потери железа достигают – 1, 22 -1, 33 мг Запасы железа – 30% сосредоточено в печени - 30% сосредоточено в красном костном мозге

Патогенез железодефицитной анемии. 1. Недостаточность потребления – не основная причина 2. Нарушение всасывания – имеет значение только при поражении желудка и начального отдела тонкой кишки: • Оперированный (резецированный) желудок, гастроеюностомия – ЖДА у 50 -60% больных (потеря резервуарной функции желудка и поступление пищи минуя 12 -перстную кишку приводят к анемии • Ахлоргидрия 3. Хроническая кровопотеря. Носовые кровотечения, кровохаркание, гематурия, маточные кровотечения Желудочно-кишечные кровотечения (скрытые) – основная причина ЖДА.

Стадия 1 ( Сниженные запасы железа): 1. Запасы железа в костном мозге и печени уменьшаются. 2. У пациента отсутствуют какие-либо клинические симптомы, уровень гемоглобина находится в пределах нормы. 3. Уровень ферритина сыворотки и количество железа в костном мозге снижены. 4. Основным физиологическим признаком истощения железа является повышение всасывания железа

Стадия 2 (Железодефицитный эритропоэз): 1. Активность эритропоэза снижается в связи с недостатком железа, необходимого для включения в гемовую часть молекулы гемоглобина. 2. Уровень гемоглобина начинает падать, свободный протопорфирин эритроцитов увеличивается. 3. Снижение количества запасов железа, низкий уровень железа сыворотки, повышение общей железосвязывающей способности сыворотки, и низкое насыщение трансферрина. 4. Показатели гематокрита практически не отличаются от нормальных.

Стадия 3 (Железодефицитная анемия): 1. Железодефицитная анемия является наиболее развернутой стадией заболевания. 2. Содержание ферритина и насыщение трансферрина находятся на очень низком уровне. 3. Снижаются количество запасов железа, уровень железа сыворотки. 4. Повышается общая железосвязывающая способность сыворотки (ОЖСС). 5. Снижается концентрация гемоглобина.

Клиническая картина железодефицитной анемии. 1. Клиника собственно анемии, связанная с недостатком кислорода на периферии: • бледность кожных покровов, слизистых, склер, • одышка, сердцебиение, • слабость, головокружение, утомляемость, головные боли. 2. Сидеропенический синдром (недостаток железа), который обусловлен снижением железа в цитохромоксидазе: • сухостью кожи, ломкостью волос и ногтей, • нарушением функции рецепторов ротовой полости (больные хотят есть мел, дерево, землю), • нарушением функции эпителия желудка, что ведет к нарушению продукции желудочного сока, что ведет к гипоацидным состояниям, а затем к дискинезии желчевыводящих путей. • Снижение железа в миоглобине ведет к мышечной слабости. • Снижение железа в миокардиоцитах - к кардиомиопатиям

Основными лабораторные критерии ЖДА (Перед исследованием обмена железа обязательно исключение приема препаратов железа на 7 -10 дней) 1. низкий цветовой показатель; 2. гипохромия эритроцитов, 3. микроцитоз; 4. снижение уровня сывороточного железа (норма - 1328 ммоль/л для мужчин; 11 -26 ммоль/л для женщин). 5. повышение общей железосвязывающей способности сыворотки (измеряется количеством железа, которое может связать 100 мл или 1 л сыворотки крови, в норме она равняется 30 - 80 мкмоль на литр или 3 -4 мг/л. ) 6. снижение содержания ферритина в сыворотке (норма у мужчин 21 -235 мкг/л, у женщин - 12 -128 мкг/л. )
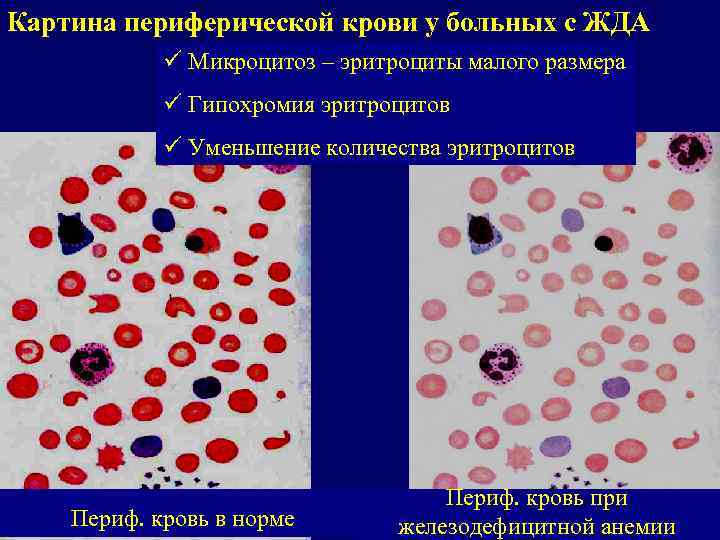
Картина периферической крови у больных с ЖДА ü Микроцитоз – эритроциты малого размера ü Гипохромия эритроцитов ü Уменьшение количества эритроцитов Периф. кровь в норме Периф. кровь при железодефицитной анемии

Примеры формулировки диагноза 1. Хроническая железодефицитная анемия вследствие меноррагий, средней тяжести. 2. Хроническая железодефицитная анемия на фоне хронического атрофического гастрита, легкой степени тяжести. Сопутствующий – язвенная болезнь желудка и 12 перстной кишки, ст. ремиссии, хр. Дуоденит. 3. Хроническая железодефицитная анемия на фоне неспецифического язвенного колита в стадии ремиссии, средней тяжести. 4. Хр. Геморрой, ст. обострения, хроническая железодефицитная анемия, средней тяжести.

Дифференциальный диагноз: Сидероахрестические анемии ( «железонасыщенные» ) (ахрезия – неиспользование). группа гипохромных анемий, при которых содержание железа в организме и его запасы в депо находятся в пределах нормы или даже повышены, однако в связи с нарушением включения его в молекулу гемоглобина (в силу различных причин) железо не используется для синтеза гема. Удельный вес их в структуре гипохромных анемий невелик.

Дифференциальный диагноз: Критерии сидероахрестических анемий: 1. низкий цветовой показатель; 2. гипохромия эритроцитов; 3. повышенное (реже нормальное) содержание железа в сыворотке; 4. нормальная или сниженная способность сыворотки; железосвязывающая 5. нормальное или повышенное содержание ферритина в сыворотке; 6. повышенное количество сидеробластов в костном мозге.

Дифференциальный диагноз: Железоперераспределительные анемии Анемии при воспалительных заболеваниях основной механизм развития анемии - перераспределение железа в клетки макрофагальной системы, активирующейся при различных воспалительных (инфекционных и неинфекционных) или опухолевых процессах. Поступающее в организм и высвобождающееся из разрушающихся эритроцитов железо переходит главным образом в депо, где и накапливается в макрофагальных клетках в виде железосодержащего белка ферритина.

Дифференциальный диагноз: Критерии железоперераспределительных анемий: 1. нормохромный или умеренно гипохромный характер анемии; 2. нормальное или умеренное сниженное содержание сывороточного железа; 3. нормальная или сниженная железосвязывающая способность сыворотки; 4. повышение содержания ферритина в сыворотке; 5. повышение количества сидеробластов в костном мозге; 6. клинико-лабораторные признаки активного процесса (воспалительного, опухолевого).

Лечение ЖДА: Чаще – амбулаторное лечение Показания к плановой госпитализации - 1. Анемия тяжелой степени тяжести 2. Рефрактерная к амбулаторному лечению анемия 3. Железодефицитная анемия неясного генеза 4. Железодефицитная анемия у пациентов, обследование которых в амбулаторных условиях не возможно 5. Социальные показания 6. Пациенты с тяжелыми сопутствующими заболеваниями

Основные принципы медикаментозного лечения хронической железодефицитной анемии 1) никогда не требуется переливаний эритроцитов; 2) практически никогда не нужно парентеральное введение железа (внутримышечно и внутривенно); 3) нет необходимости ничего добавлять к препаратам железа внутрь - ни витаминов в инъекциях, ни соляной кислоты, ни глюкозы внутривенно, ни "стимуляторов кроветворения", ни пищевых добавок; ни спец. Диеты (яблоки, орехи и т. д. ) 4) лечение проводится только длительным приемом препаратов двухвалентного железа внутрь в умеренных дозах, причем существенный прирост гемоглобина, в отличие от улучшения самочувствия, будет не скорым - через 4 -6 недель

Препараты железа могут вводиться внутривенно, внутримышечно и перорально. Терапию железом в основном следует проводить перорально. Причины заключаются в следующем: 1. Парентеральное применение железа не является эффективнее, чем пероральное. 2. Парентеральное лечение редко, но иногда может привести и к смертельному осложнению, анафилактическому приступу, отеку гортани, остановке дыхательной и сердечной деятельности.

Адекватная доза для адекватного прироста показателей гемоглобина для перорального приема препарата железа составляет 150 -180 мг желез в сутки Препарат Форма соединения железа в препарате Кол-во активного железа в препарате (мг) Ферро-градумет Сульфат железа 105 в 1 таблетке Актиферрин Сульфат железа 34, 5 в 1 капсуле 34, 5 в 5 мл сиропа Фенюльс Сульфат железа 45 в 1 капсуле Феррум лек Fe-гидроксид-полимальтоза 50 в 5 мл сиропа Все препараты железа основаны на включениях железа в виде сульфата, в соединении с витамином С, никотиновой или янтарной кислотами стимулируют пристеночное пищеварение. Доза железа должна пересчитываться на чистое железо.

Показания для применения ПЖ парентерально : - Нарушение всасывания при патологии кишечника (энтериты, синдром недостаточности всасывания, резекция тонкого кишечника, резекция желудка по Бильрот II с выключением двенадцатиперстной кишки); - Обострение язвенной болезни желудка или двенадцатиперстной кишки; - Непереносимость ПЖ для приема внутрь, не позволяющая дальнейшее продолжение лечения; - Необходимость более быстрого насыщения организма железом, например у больных ЖДА, которым предстоят оперативные вмешательства (миома матки, геморрой и др. ). - Состояния после резекции желудка, тонкого кишечника - Неспецифический язвенный колит - Хронический энтероколит - Социальные причины

Доза ПЖ для внутримышечного и внутривенного введения, рассчитывается по формуле: А=К х (100 - 6 х Нb) х 0, 0066 где А – число ампул, К – масса больного в кг, Нb – содержание гемоглобина в г %. При этом в 1 -й день вводят 1/2 ампулы (2, 5 мл), во 2 -й день – 1 ампулу (5 мл), в 3 -й день – 2 ампулы (10 мл). В последующем препарат вводят 2 раза в неделю до достижения необходимой рассчитанной общей дозы.

При внутривенном введении железа должен быть жесткий контроль уровня сывороточного железа во время всей терапии, так как избыточное количество железа откладывается в гемосидерин, что ведет к развитию гемохроматоза с поражением поджелудочной железы, развитием цирроза, поражением миокарда. Гемотрансфузии не используются, так как железо из гема плохо утилизируется и оно переходит в гемосидерин, также увеличивается масса эритроцитов, что ведет к торможению активности костного мозга.

Эффект от терапии отмечается через 3 -4 недели от начала лечения: объективными критериями эффективности являются: · ретикулоцитоз на периферии, что говорит об активации эритропоэза · нарастание количества эритроцитов · увеличение цветного показателя. Терапия препаратами железа должна продолжаться до полного восстановления уровня гемоглобина. После его восстановления лечение препаратами железа продолжается ещё 2 месяца для восстановления запасов железа под контролем уровня железа сыворотки крови.

Мегалобластные анемии – состояния, общим признаком которых служит обнаружение в костном мозге эритроцитов, находящихся на последних этапах созревания, но содержащих ядра (в норме эритроцит теряет ядро при созревании), , характеризующиеся ослаблением синтеза ДНК, в результате чего нарушается деление всех быстропролиферирующих клеток (гемопоэтических клеток, клеток кожи, клеток ЖКТ, слизистых оболочек). В-12 дефицитная анемия Фолиеводефицитная анемия

Обмен витамина В-12 в организме. 1. Витамин B 12, или цианокобаламин, представляет собой сложную молекулу, которая включает в себя атом кобальта. 2. В пище В-12 содержится в продуктах животного происхождения (печень, яйца, молоко). 3. Запасы В-12 в организме взрослого человека (главным образом в печени) около 5 мг. 4. Суточная потеря витамина В-12 мочой и калом составляет 5 мкг. 5. Дефицит витамина при значительном снижении его поступления и (или) усвоения развивается лишь через 3 - 6 лет. Проявления дефицита возникают значительно позже нарушения усвоения витамина в желудочно-кишечном тракте 6. Минимальная суточная потребность в этом витамине составляет 1 мкг. Так как из пищи всасывается не весь витамин В 12, содержащийся в ней, суточный рацион должен составлять 3 -7 мкг витамина в день.

Обмен витамина В-12 в организме. 7. Попадая в желудок, В-12 связывается (на фоне кислой реакции среды) с внутренним фактором — гликопротеином и позже всасывается в тонкой кишке (при щелочном значении р. Н ). 8. Максимальная способность всасывания витамина В 12 при помощи внутреннего фактора ограничена. У человека единовременно может всасываться не более 1, 5 мг, а за сутки – 6 -9 мг витамина В 12. 9. Часть витамина B 12 синтезируется бактериями в толстой кишке, однако из этого отдела кишечника он практически не всасывается. 10. Всосавшийся В-12 соединяется с белком-носителем — транскобаламином, который его доставляет к клеткам различных тканей. 11. Основное депо В-12 – печень. Существует кишечнопеченочная рециркуляция витамина B 12 при условии недостаточного поступления В-12 с пищей.

Причины формирования дефицита В-12. 1. Нарушение всасывания В-12 2. Повышенная потребность в витамине В 12 3. Нарушение транспорта витамина В 12 4. Неправильный прием некоторых медикаментов (ПАСК, неомицин, метформин). 5. Алиментарная недостаточность (редкая причина), главным образом в детском возрасте, при длительном парентеральном питании без дополнительного введения витаминов.

Причины нарушения всасывания В-12. 1. атрофический гастрит, приводящий к отсутствию внутреннего фактора Кастла, обеспечивающего всасывание витамина В 12, 2. рак желудка, 3. нарушение всасывания витамина В 12 при заболеваниях кишечника, 4. резекции подвздошной кишки (основной плацдарм, где происходит всасывание витамина В 12), 5. гастрэктомия. 6. энтериты с нарушением всасывания, 7. спру, целиакия; 8. панкреатиты с внешнесекреторной недостаточностью

Причины повышенной потребности в витамине В 12 1. инвазия широким лентецом; 2. дивертикулез толстой кишки, приводящий к размножению бактериальной флоры в кишечнике, потребляющей витамин В 12, 3. дисбактериоз кишечника; 4. быстрый рост (у детей); 5. гипертиреоз; 6. хронические заболевания печени (гепатиты, циррозы).

Причины нарушения транспорта витамина В 12 1. дефицит транскобаламина II (аутосомно-рециссивно наследуемый дефект, проявляющийся в раннем детском возрасте)

дефицит витамина В 12 нарушается синтез ДНК в кроветворных клетках неэффективный мегалобластический эритропоэз (в норме существует только у плода) с продукцией нестойких макроцитов и мегалоцитов

Клиническая картина Для клинического проявления характерна триада: · изменение крови · поражение ЖКТ · поражение нервной системы

Клиническая картина. Изменения крови. 1. высокий цветовой показатель; 2. макроцитоз, мегалоцитоз (эритроциты крупных размеров с диаметром более 15 мкм ); 3. эритроциты с остатками ядер (тельца Жолли, кольца Кэбота); 4. ретикулоцитопения; 5. гиперсегментация нейтрофилов; 6. лейкопения (нейтропения); 7. тромбоцитопения; 8. повышение содержания железа в сыворотке; 9. гипербилирубинемия с желтухой или без нее. 10. мегалобластическое кроветворение в костном мозге

Клиническая картина. Поражения ЖКТ. 1. Есть признаки глоссита - участки воспаления и атрофии сосочков языка, лакированный язык, болезненность языка. 2. Иногда имеются участки воспаления на поверхности языка или щек – афты. 3. Желудочная секреция резко снижения. 4. При фиброгастроскопии выявляется атрофия слизистой оболочки желудка, которая подтверждается и гистологически. 5. При рентгеноскопии желудка нередко обнаруживаются нарушения эвакуаторной деятельности желудка, уплощенные и сглаженные складки 6. Иногда отмечается небольшое увеличение селезенки, а иногда и печени
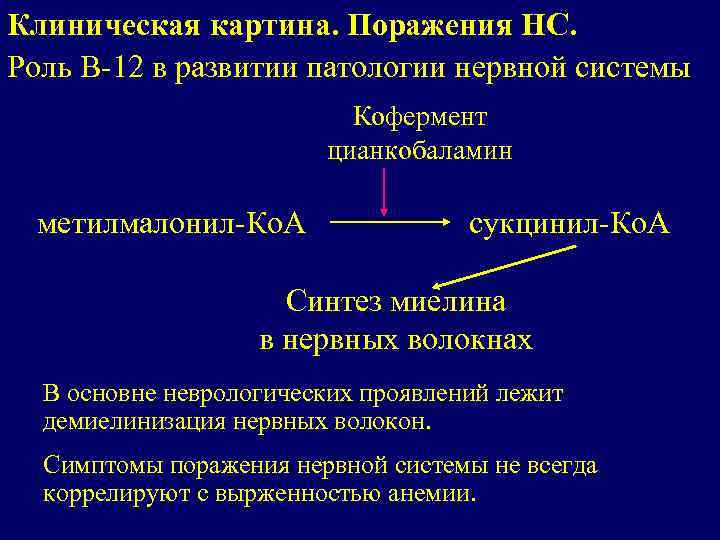
Клиническая картина. Поражения НС. Роль В-12 в развитии патологии нервной системы Кофермент цианкобаламин метилмалонил-Ко. А сукцинил-Ко. А Синтез миелина в нервных волокнах В основне неврологических проявлений лежит демиелинизация нервных волокон. Симптомы поражения нервной системы не всегда коррелируют с вырженностью анемии.

Клиническая картина. Поражения НС. Клинические проявления дистальных полиневритов: 1. 2. 3. 4. 5. дистальные парестезии, периферическая полиневропатия, расстройства чувствительности, повышение сухожильных рефлексов нарушения чувствительности с постоянными легкими болевыми ощущениями, напоминающими покалывание булавок или иголок, 6. ощущение холода, онемение в конечностях, 7. ощущение "ватных ног", ползания мурашек 8. опоясывающие боли, 9. признаки выраженной мышечной слабости, 10. могут развиться мышечные атрофии

Клиническая картина. Поражения НС. Клинические проявления поражения спинного мозга: Дегенерация задне-боковых столбов спинного мозга ). 1. Нижние конечности поражаются в первую очередь. 2. Поражение может распространяться на область живота и выше. 3. Руки поражаются редко, степень поражения их всегда значительно меньше, чем поражение ног 4. Поражение чаще вceгo симметричное. 5. Нарушаются поверхностная чувствительность, способность отличать холодное от горячего, снижается болевая чувствительность. 6. При глубоком поражении нарушаются вибрационная и глубокая чувствительность. 7. Некоторые больные теряют обоняние, слух, у них нарушаются вкусовые ощущения.

Диагностика В-12 дефицитной анемии. 1. Основной метод диагностики - исследование костного мозга (выявление мегалобластического эритропоэза). 2. Пункция костного мозга обязательна так как такая картина на периферии может быть при лейкозе, гемолитической анемии, апластических и гипопластических состояниях (однако гиперхромия характерна именно для В 12 -дефицитной анемии). 3. Данное исследование должно проводиться до назначения витамина В 12,
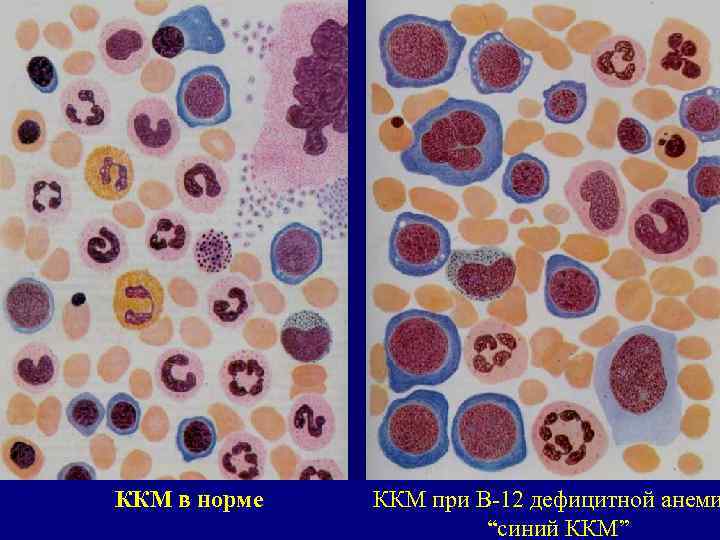
ККМ в норме ККМ при В-12 дефицитной анеми “синий ККМ”

Диагностика В-12 дефицитной анемии. Характеристики ККМ про В-12 дефицитной анемии: 1. Главный критерий постановки диагноза В 12 -дефицитная анемия типичные мегалобласты (клетки с "ядерно-цитоплазматической диссоциацией" (при зрелой гемоглобинизированной цитоплазме нежное, сетчатого строения ядро с нуклеолами)); 2. Костный мозг клеточный, 3. Число ядросодержащих эритроидных элементов увеличено в 2 -3 раза 4. Эритропоэз неэффективный(сниженное число ретикулоцитов и эритроцитов на периферии и укорочение их продолжительности жизни (в норме эритроцит живет 120 -140 дней). 5. Клетки гранулоцитарного ряда большого размера и гигантские мегакариоциты.

Диагностика В-12 дефицитной анемии. При невозможности выполнить данное исследование допустимо пробное назначение витамина В 12 (цианокобаламин) с исследованием количества ретикулоцитов в крови через 3 -5 дней (не позже). Если анемия связана с дефицитом витамина В 12, то под влиянием нескольких инъекций препарата происходит трансформация мегалобластического кроветворения в нормобластическое, что отражается значительным увеличением в периферической крови количества ретикулоцитов (ретикулоцитарный криз). по сравнению с исходным

Лечение В-12 дефицитной анемии. Принципы терапии: · насытить организм витамином · поддерживающая терапия · предупреждение возможного развития анемии

Лечение В-12 дефицитной анемии. Всем пациентам с В-12 дефицитной анемией показано длительное лечение витамином В 12 (цианокобаламин, гидроксикобаламин).

Лечение В-12 дефицитной анемии. Препараты витамина B 12 содержат его в количестве 30, 100, 200 и 500 мкг в 1 мл и вводятся внутримышечно: при неосложненной анемии — по 500 мкг при осложненной форма – 1000 мкг ежедневно или через день в течение 10 -14 сут, затем по 250 мкг еженедельно до полного восстановления количества эритроцитов. В дальнейшем вводят ежемесячно эту же дозу или 500 мкг 1 раз в 2 мес.

Лечение В-12 дефицитной анемии. ØГемотрансфузии можно применять лишь по жизненным показаниям при значительном снижении гемоглобина, когда больные находятся в коматозном состоянии или при резком нарушении гемодинамики. ØРекомендуется вводить эритроцитную массу по 250 - 300 мл (5 - 6 трансфузий).

Эффективность лечение В-12 дефицитной анемии. К ранним признакам наступающей ремиссии: ØБыстрое, иногда скачкообразное уменьшение СОЭ, ØЗначительно опережающее восстановление красной крови – эритроседиментационный криз (характеризуется восстановлением физических свойств эритроцитов). Эритроседиментационный криз или совпадает по времени с ретикулоцитарным кризом или отстает от него на 23 сут. Признаки полноценной ремиссии: Øполное восстановление показателей крови (происходит через 1. 5 - 2 месяца) Ø ликвидация неврологических нарушений (в течение полугода)
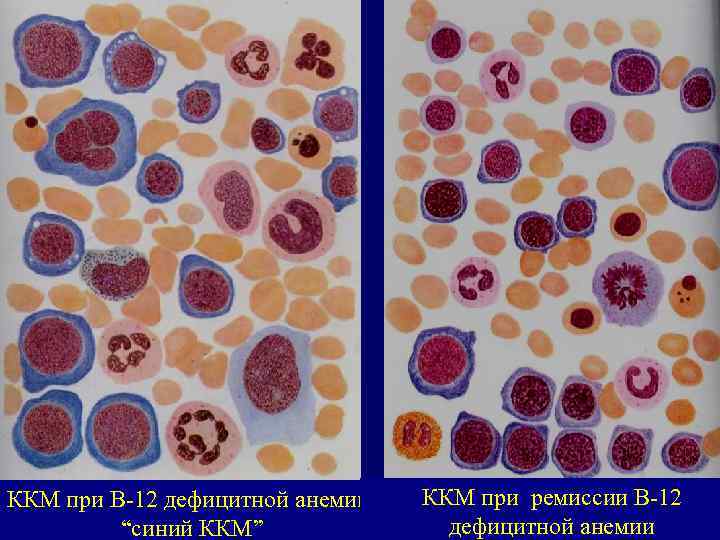
ККМ при В-12 дефицитной анемии “синий ККМ” ККМ при ремиссии В-12 дефицитной анемии

Поликлинический этап лечения В-12 дефицитной анемии. Цель 1 – контроль состояния При длительном поддерживающем лечении содержание гемоглобина следует контролировать не реже, чем раз в полгода. Цель 2 - противорецидивное лечение. ü В большинстве случаев лучше всего обязательные ежемесячные пожизненные(!) введения 300 -500 мкг витамина В 12, ü Альтернативное лечение - короткие профилактические курсы лечения (2 -3 нед в году вводится витамин В 12 ежедневно или через день в той же суточной дозе).

Фолиеводефицитные анемии Обмен фолиевой кислоты в организме. 1. Сама фолиевая кислота (водорастворимый витамин) неактивна. 2. В организме она превращается в биологически активный коэнзим — тетрагидрофолиевую кислоту, которая играет важную роль в биосинтезе амино- и нуклеиновых кислот и вследствие этого в делении клеток.

Обмен фолиевой кислоты в организме. 3. Фолиевая кислота широко распространена в зеленых овощах, грибах, печени, дрожжах. 4. В пище она содержится в конъюгированной форме (полиглютамат). 5. Фолиевая кислота синтезируется бактериями в толстой кишке, однако эта часть ее остается практически неиспользованной 6. Во многих тканях имеется фермент, который высвобождает фолиевую кислоту из этого конъюгата. 7. Запасы фолатов составляют 5 -10 мг 8. Минимальная суточная потребность человека в ней — 50 мкг, или 400 мкг поликлютамата. 9. Запасы фолиевой кислоты в организме достаточны для нормальной жизнедеятельности в течение нескольких месяцев. .

Причинами дефицита фолатов могут быть: 1. Недостаточное поступление · скудный рацион · нервно-психическая анорексия · парентеральное питание · несбалансированное питание у пожилых 2. Нарушение всасывания · мальабсорбция · изменения слизистой оболочки кишечника · целиакия и спру · болезнь Крона, регионарный илеит · лимфома кишечника · уменьшение реабсорбирующей поверхности после резекции тощей кишки · прием антиконвульсантов 3. Увеличение потребности · беременность- потребность до 100 мкг (800 мкг полиглютамата) · гемолитическая анемия · эксфолиативный дерматит и псориаз 4. Нарушение утилизации · алкоголизм · антагонисты фолатов: триметоприм и метотрексат · врожденные нарушения метаболизма фолатов

Патогенез дефицита фолиевой кислоты. Недостаточность фолиевой кислоты обусловливает нарушение синтеза и структуры ДНК (фолиевая кислота в своей метаболически активной форме - в виде тетрагидрофолиевой кислоты необходима для синтеза тимидинмонофосфата, а также включения в молекулу ДНК уридина и оротовой кислоты) Это сопровождается переходом нормобластического типа кроветворения на мегалобластический.

Дифференциальный диагноз фолиеводефицитной анемии. Диф. диагностика проводится с другими видами макроцитарных анемий и в первую очередь с В-12 дефицитной анемией. Основной дифференциальный признак - отсутствуют гастроэнтероколитический и неврологический синдромы

Диагностика фолиеводефицитной анемии. ØДиагноз фолиеводефицитной анемии подтверждается определением содержания фолиевой кислоты в сыворотке крови и эритроцитах. ØВ норме содержание фолиевой кислоты в эритроцитах колеблется от 100 до 450 нг/л

Лечение фолиево-дефицитной анемии. üфолиевая кислота в виде таблеток по 5 -15 мг/сут üДлительность лечения регламентируется темпами восстановления показателей крови.

Гипопластические состояния: 1. Апластическая анемия это состояние, возникающее в результате повреждения стволовой клетки миелопоза костного мозга и характеризующееся снижением гематопоэтической активности (депрессией) костного мозга с развитием периферической панцитопении (эритроцитопения, гранулоцитопения, тромбоцитпения) 2. Гипопластическая, парциальная анемия a. Парциальная аплазия - это парциальная красноклеточная аплазия, когда поврежден только эритроидный росток. b. Острый агранулоцитоз - поражен только гранулоцитарный росток. c. Амегакариоцитарная пурпура - страдает изолированной мегакариоцитарный росток. -

Апластическая анемия. Общие положения. • Апластическая анемия достаточно редкое заболевание • Частота составляет 5 случаев на 1 млн населения в год. • Апластическая анемия встречается чаще у лиц молодого возраста, одинаково часто у мужчин и женщин.
Апластическая анемия Врожденная Приобретенная 1. Врожденные анемии встречаются редко 1. Приобретенные анемии встречаются чаще 2. Чаще с этими вариантами встречаются педиатры, потому что заболевание манифестирует в детском возрасте. 2. Подразделяются на - 1. идиопатическую врожденную анемию (этиология не ясна). - 2. анемию с установленным этиологическим фактором: 3. С этими вариантами встречаются врачи любых специальностей (терапевт, гастроэнтеролог, инфекционист и т. д. )

Клиническая картина Складывается из синдромов депрессии кроветворения: 1. Геморрагического 2. Анемического 3. Нейтропенического (синдрома инфекционных осложнений)

Клиника апластической анемии. Геморрагический синдром. геморрагический синдром является следствием тромбоцитопении, Выраженность зависит от степени цитопении: 1. спонтанные - некупируемые маточные кровотечения, 2. геморроидальные кровотечения, 3. желудочные кровотечения, 4. кровоточивостью из десен; 5. спонтанно возникающие петехиальные кровоизлияния на слизистой губ, языка 6. спонтанно возникающие кровоизлияния в кожу, подкожную клетчатку 7. кровоизлияния в сетчатку бывают причиной полной слепоты больного Степень геморрагического синдрома может быть разной ( вплоть до кровоизлияний в мозг).

Клиника апластической анемии. Анемический синдром. Развитие анемии связано: 1. Угнетение гемопоэза 2. Постгеморрагические состояния Отмечаются Ø Ø Ø Ø Ø повышенная утомляемость слабость головокружение шум в ушах плохая переносимость душных помещений бледность кожных покровов одышка тахикардия выслушивается систолический шум в области сердца При идиопатической форме болезни селезенка не пальпируется. Ее увеличение может иметь место при аутоиммунной форме и при гемосидерозе, развивающемся в результате массивных трансфузий крови.

Клиника апластической анемии. Нейтропенический синдром. Гранулоцитопения приводит к развитию вторичной инфекции, которая может быть бактериальной и грибковой и может трансформироваться в септические осложнения. ü При сепсисе идут микроотсевы в кожу , другие органы. ü В ротовой полости и ЖКТ существует сапрофитная флора, которая при гранулоцитопении возникают проявления язвенного поражения слизистой. ü Микробы обладают протеолитическими ферментами, и воспаления у таких больных как правило носит некротический характер. ü Частые пневмонии, отиты, пиелиты и другие воспалительные процессы ü Антибактериальная терапия назначенная неправильно у таких больных часто приводит к осложнениям - грибковое поражение ЖКТ, кандидосепсис и др.

Диагностика апластической анемии. Клинический анализ крови. Ø Апластическая анемия чаще всего нормохромная, макроцитарная Ø Средний объем эритроцита (СЭО) - 94 мкм отмечается примерно у 60 - 65 % больных) Ø Концентрация гемоглобина может падать до 20 -30 г/л Ø Содержание ретикулоцитов от 0 до 5 %, чаще свидетельствует об иммунной форме болезни. ретикулоцитоз Ø Эритрокариоциты в периферической крови появляются редко. Ø Характерна выраженная гранулоцитопения. Иногда количество гранулоцитов снижается до 200 в 1 мкл, Ø Имеет место снижение абсолютного количества моноцитов. Ø Уровень лимфоцитов в большинстве случаев остается нормальным. Ø Количество тромбоцитов снижается иногда до нуля. При этом удлиняется время кровотечения, развивается геморрагический синдром. Ø У большинства больных возрастает СОЭ до 30 - 50 мм/ч.

Диагностика апластической анемии. Биохимический анализ крови. 1. Содержание железа в сыворотке крови нормальное или повышенное, 2. Насыщение трансферрина близко к 100%. 3. В ряде случаев отмечается повышение уровня фетального гемоглобина (в норме НЬР составляет до 15% от общего гемоглобина) и эритропоэтина.

Диагностика апластической анемии. Изменения ККМ. У здорового человека гистологическая картина костного мозга представлена следующим образом 50% гемопоэтической ткани, 50% - стромальные клетки ( жир, эпителиодные клетки). При апластической анемии в ККМ: 1. Гематогенные клетки представлены крайне скудно: в небольшом количестве встречаются эритроидные и гранулоцитарные предшественники. 2. Мегакариоциты отсутствуют. 3. Уменьшено количество миелокариоцитов, главным образом за счет предшественников клеток миелоидного ряда. 4. Бывает иногда раздражение красного ростка. Увеличено количество лимфоцитов, плазматических клеток, тучных клеток. 5. Участки ККМ с полным исчезновением костномозговых элементов и замещением их жировой тканью, содержание которой может достигать 90%, и участки ККМ, где наблюдаются небольшие очаги кроветворения на фоне значительного опустошения костного мозга.
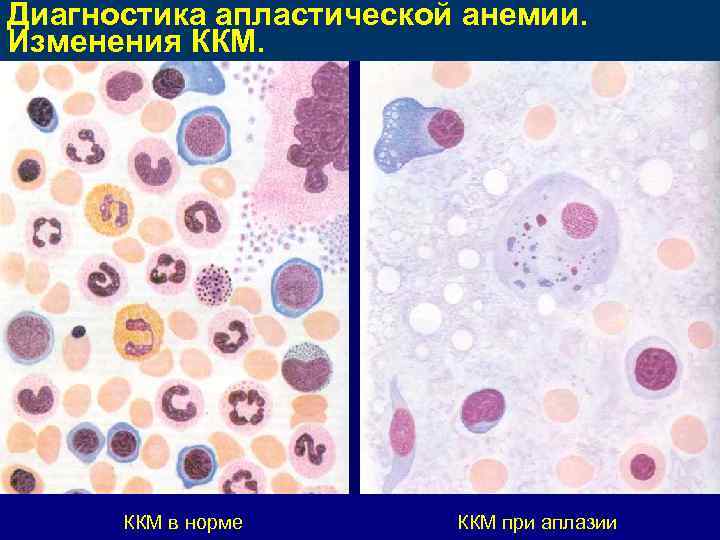
Диагностика апластической анемии. Изменения ККМ в норме ККМ при аплазии

Диагностика апластической анемии. Степени тяжести. Апластическую анемию подразделяют по степени тяжести § тяжелая апластическая анемия - клеточность костного мозга <25% от нормальной, - нейтрофилы в периферической крови < 0. 5 x 10^9/л, - тромбоциты в периферической крови < 20 x 10^9/л, - ретикулоцитоз < 1% Данная степень устанавливается при наличии хотя бы одного критерия. § нетяжелая апластическая анемия

Лечение апластической анемии. Принципы лечения: 1. Коррекция цитопенического синдрома и костномозговой недостаточности 2. Борьба с инфекционными осложнениями.

Лечение апластической анемии. ü Трансплантация костного мозга показана лицам молодого возраста, особенно с тяжелыми, прогностически неблагоприятными формами болезни ü Трансплантация при наличии подходящего донора должна быть ранней, когда аллоиммунизация вследствие заместительной терапии еще невелика. ü В настоящее время применяют трансплантацию костного мозга, подобранного по системам HL-A и MLc. ü Ремиссию получают у половины больных (лимфоциты больных апластической анемией тормозят образование эритроидных колоний донорского костного мозга). ü Для профилактики отторжения применяют большие дозы циклофосфана, тотальное облучение, антилимфоцитарный глобулин.

Лечение апластической анемии. Ø Вначале отменяют все лекарственные средства, к которым у больного имеется индивидуальная повышенная чувствительность и которые могут быть причастны к развитию анемии. Ø При тяжелой анемии проводят заместительные трансфузии отмытых эритроцитов, при выраженной тромбоцитопении и геморрагиях – переливания тромбоцитарной массы (лучше от одного донора). Ø При инфекционных осложнениях применяют антибиотики широкого спектра действия. Ø Кортикостероидные гормоны, в частности преднизолон должны быть применены для лечения у всех больных апластическим синдромом, так как в части случаев применение их оказывает хороший терапевтический эффект. При этом дозы преднизолона должны быть достаточно велики (60 - 100 мг в сутки).

Лечение апластической анемии. Спленэктомия Ø Широко применяется для лечения апластического синдрома. Ø Эффект спленэктомии, по всей вероятности, связан с тем, что селезенка - основной лимфоидный орган. В ней вырабатываются антитела, содержатся лимфоциты, участвующие в клеточных цитотоксических реакциях. Ø Эффект спленэктомии при апластическом синдроме наступает не сразу (через 2 – 5 мес после операции) и не более чем у половины больных. Ø Спленэктомия показана при менее тяжелых формах болезни – отсутствии большой кровоточивости и признаков сепсиса. Ø После спленэктомии проводят лечение анаболическими гормонами (неробол по 20 мг/сут, анаполон по 200 мг/сут в течение полугода).
анемии.ppt