KF_titration_Malytska.ppt
- Количество слайдов: 20
 Аналізатори води в органічних речовинах (метод Фішера) Підготувала Малицька Ю. Ю.
Аналізатори води в органічних речовинах (метод Фішера) Підготувала Малицька Ю. Ю.
 Методи визначення води v. Висушування v. Карбідний метод Ca. C 2 + 2 H 2 О = C 2 H 2 + Ca (OH) 2 v. Метод дистиляції (Діна-Старка) v. Газохроматографічний метод v. Метод Фішера 2
Методи визначення води v. Висушування v. Карбідний метод Ca. C 2 + 2 H 2 О = C 2 H 2 + Ca (OH) 2 v. Метод дистиляції (Діна-Старка) v. Газохроматографічний метод v. Метод Фішера 2
 Йодометричне визначення (метод Фішера) Титрування Карла Фішера – метод кількісного аналізу загального вмісту води у сполуках, що широко використовується в аналітичній хімії Карл Фішер (1901 – 1958) Публікація 1935 р. Реакція Бунзена: 2 H 2 O + SO 2 + I 2 = H 2 SO 4 + 2 HI 3
Йодометричне визначення (метод Фішера) Титрування Карла Фішера – метод кількісного аналізу загального вмісту води у сполуках, що широко використовується в аналітичній хімії Карл Фішер (1901 – 1958) Публікація 1935 р. Реакція Бунзена: 2 H 2 O + SO 2 + I 2 = H 2 SO 4 + 2 HI 3
 Реактив Фішера Розчинник – робоче середовище, тобто розчинник чи суміш розчинників, в яких розчиняється проба і проводиться КФтитрування (метанол, пропанол, етиленгліколь) Буфер – для підтримання р. Н в діапазоні 5 – 7 (піридин, імідазол, первинні аміни) o р. Н <5 – повільно відбувається реакція o р. Н >7 – побічні реакції Титрант I 2, SO 2 4
Реактив Фішера Розчинник – робоче середовище, тобто розчинник чи суміш розчинників, в яких розчиняється проба і проводиться КФтитрування (метанол, пропанол, етиленгліколь) Буфер – для підтримання р. Н в діапазоні 5 – 7 (піридин, імідазол, первинні аміни) o р. Н <5 – повільно відбувається реакція o р. Н >7 – побічні реакції Титрант I 2, SO 2 4
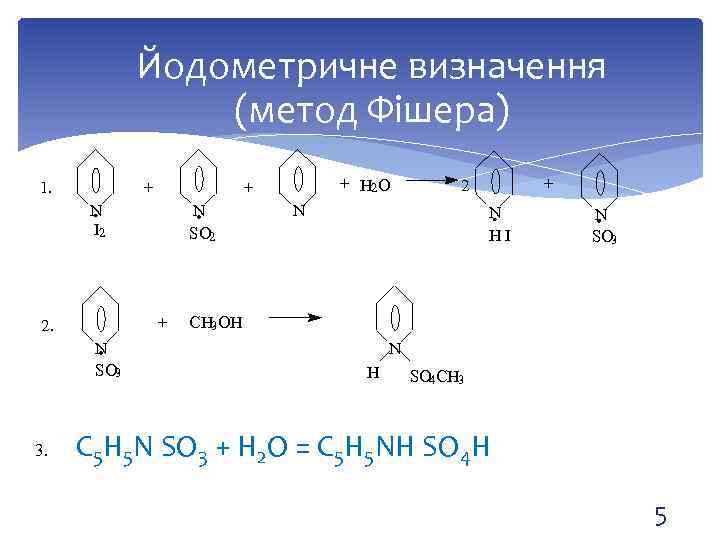 Йодометричне визначення (метод Фішера) 1. + N I 2 N SO 2 + 2. N SO 3 + H 2 O + + 2 N N HI N SO 3 CH 3 OH N H SO 4 CH 3 3. C 5 H 5 N SO 3 + H 2 O = C 5 H 5 NH SO 4 H 5
Йодометричне визначення (метод Фішера) 1. + N I 2 N SO 2 + 2. N SO 3 + H 2 O + + 2 N N HI N SO 3 CH 3 OH N H SO 4 CH 3 3. C 5 H 5 N SO 3 + H 2 O = C 5 H 5 NH SO 4 H 5
 Автоматичні аналізатори Фішера - аналізатор - комірка для титрування - порт введення проби - електроди - магнітна мішалка - хлоркальцієва трубка - блок живлення 6
Автоматичні аналізатори Фішера - аналізатор - комірка для титрування - порт введення проби - електроди - магнітна мішалка - хлоркальцієва трубка - блок живлення 6
 Переваги методу Висока точність і відтворюваність Селективність по воді Малі кількості необхідних зразків Швидкий аналіз Широкий діапазон вимірювання (1 ppm - 100%) Придатний для аналізу: o твердих речовин o рідин o газів 7 7
Переваги методу Висока точність і відтворюваність Селективність по воді Малі кількості необхідних зразків Швидкий аналіз Широкий діапазон вимірювання (1 ppm - 100%) Придатний для аналізу: o твердих речовин o рідин o газів 7 7
 Обмеження титрування КФ Реагент Фішера нестійкий до дії світла і вологи. Потрібна стандартизація перед кожним використанням Робочий інтервал p. H 5 – 8 Погано розчинні у метанолі сполуки (наприклад, жири, вуглеводні) розчиняють у вищих спиртах або хлороформі, можливі також добавки формаміду (для полярних речовин). Слід уникати титрування речовин, які здатні реагувати з компонентами реактиву Фішера (наприклад, альдегіди і кетони, сильні кислоти і основи, окисники і відновники, сполуки, що реагують з компонентами реактиву Фішера з утворенням води). 8
Обмеження титрування КФ Реагент Фішера нестійкий до дії світла і вологи. Потрібна стандартизація перед кожним використанням Робочий інтервал p. H 5 – 8 Погано розчинні у метанолі сполуки (наприклад, жири, вуглеводні) розчиняють у вищих спиртах або хлороформі, можливі також добавки формаміду (для полярних речовин). Слід уникати титрування речовин, які здатні реагувати з компонентами реактиву Фішера (наприклад, альдегіди і кетони, сильні кислоти і основи, окисники і відновники, сполуки, що реагують з компонентами реактиву Фішера з утворенням води). 8
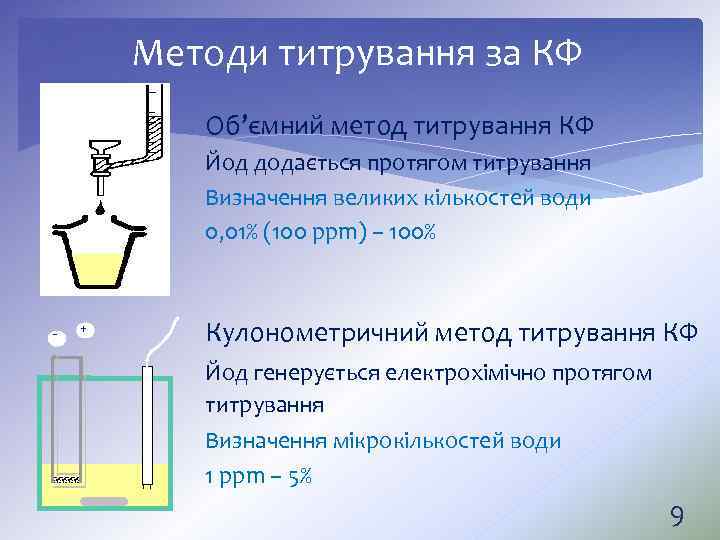 Методи титрування за КФ Об’ємний метод титрування КФ Йод додається протягом титрування Визначення великих кількостей води 0, 01% (100 ppm) – 100% - + Кулонометричний метод титрування КФ Йод генерується електрохімічно протягом титрування Визначення мікрокількостей води 1 ppm – 5% 9
Методи титрування за КФ Об’ємний метод титрування КФ Йод додається протягом титрування Визначення великих кількостей води 0, 01% (100 ppm) – 100% - + Кулонометричний метод титрування КФ Йод генерується електрохімічно протягом титрування Визначення мікрокількостей води 1 ppm – 5% 9
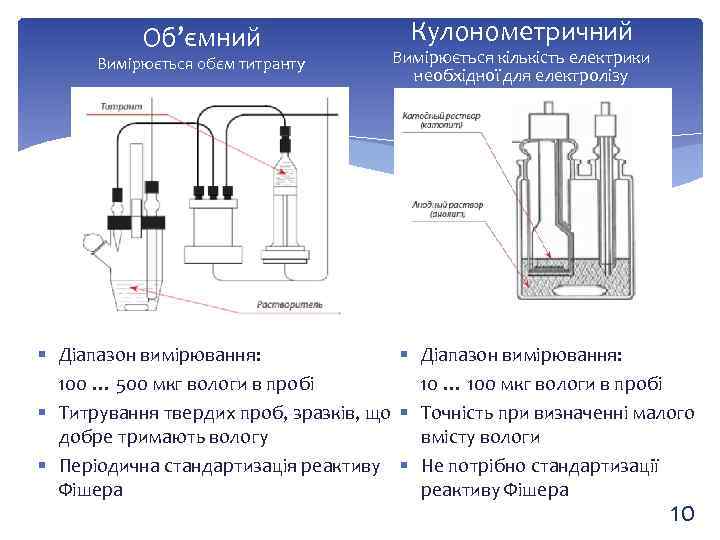 Об’ємний Вимірюється обєм титранту Кулонометричний Вимірюється кількість електрики необхідної для електролізу § § Діапазон вимірювання: 100 … 500 мкг вологи в пробі § Титрування твердих проб, зразків, що § добре тримають вологу § Періодична стандартизація реактиву § Фішера Діапазон вимірювання: 10 … 100 мкг вологи в пробі Точність при визначенні малого вмісту вологи Не потрібно стандартизації реактиву Фішера 10
Об’ємний Вимірюється обєм титранту Кулонометричний Вимірюється кількість електрики необхідної для електролізу § § Діапазон вимірювання: 100 … 500 мкг вологи в пробі § Титрування твердих проб, зразків, що § добре тримають вологу § Періодична стандартизація реактиву § Фішера Діапазон вимірювання: 10 … 100 мкг вологи в пробі Точність при визначенні малого вмісту вологи Не потрібно стандартизації реактиву Фішера 10
 Об’ємний метод титрування КФ Вимірюється об’єм титранту, витрачений на титрування § Однокомпонентний реактив § Титрант: I 2 , SO 2, буфер §Розчинник: спирт § Двокомпонентний реактив § Титрант: I 2 , метанол §Розчинник: SO 2, буфер, спирт 11
Об’ємний метод титрування КФ Вимірюється об’єм титранту, витрачений на титрування § Однокомпонентний реактив § Титрант: I 2 , SO 2, буфер §Розчинник: спирт § Двокомпонентний реактив § Титрант: I 2 , метанол §Розчинник: SO 2, буфер, спирт 11
 Кулонометричне титрування КФ - + Йод, необхідний для КФ-реакції утворюється внаслідок анодного окислення йодиду: 2 I- -2 e = I 2 12
Кулонометричне титрування КФ - + Йод, необхідний для КФ-реакції утворюється внаслідок анодного окислення йодиду: 2 I- -2 e = I 2 12
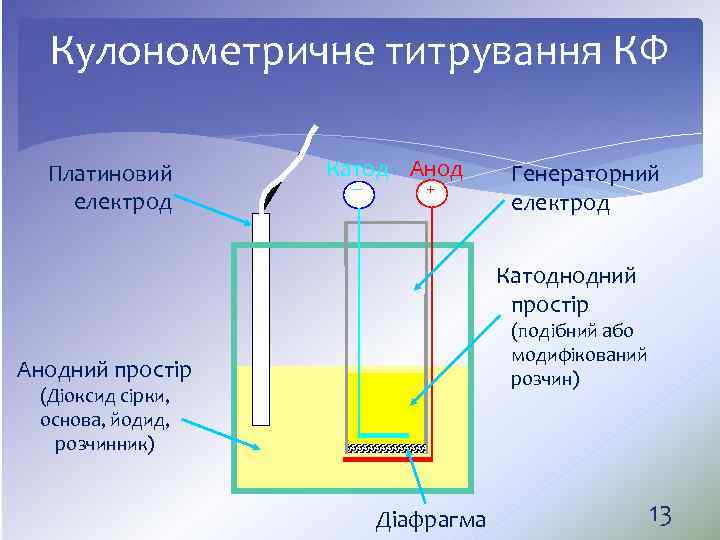 Кулонометричне титрування КФ Платиновий електрод Катод Анод – + Генераторний електрод Катоднодний простір (подібний або модифікований розчин) Анодний простір (Діоксид сірки, основа, йодид, розчинник) Діафрагма 13
Кулонометричне титрування КФ Платиновий електрод Катод Анод – + Генераторний електрод Катоднодний простір (подібний або модифікований розчин) Анодний простір (Діоксид сірки, основа, йодид, розчинник) Діафрагма 13
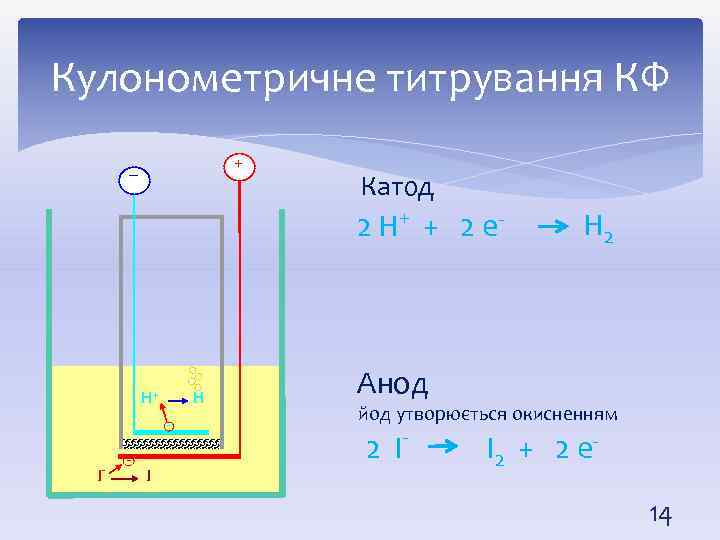 Кулонометричне титрування КФ + – Катод 2 H+ + 2 e- H+ H - I - - I H 2 Анод йод утворюється окисненням - 2 I I 2 + 2 e 14
Кулонометричне титрування КФ + – Катод 2 H+ + 2 e- H+ H - I - - I H 2 Анод йод утворюється окисненням - 2 I I 2 + 2 e 14
 Кулонометричні титратори З діафрагмою Без діафрагми -- можливість потрапляння йоду до + йод лише в анодному просторі катоду і відновлення в йодид реагує з водою + дозволяє використовувати один + висока точність вимірювання навіть при низькому вмісті вологи 15 реагент (замість аноліту і католіту), що спрощує та здешевлює процес титрування 15
Кулонометричні титратори З діафрагмою Без діафрагми -- можливість потрапляння йоду до + йод лише в анодному просторі катоду і відновлення в йодид реагує з водою + дозволяє використовувати один + висока точність вимірювання навіть при низькому вмісті вологи 15 реагент (замість аноліту і католіту), що спрощує та здешевлює процес титрування 15
 Аналіз нерозчинних чи складних зразків Сушильна піч DO 308 об’єм зразків до 10 см 3 діапазон температур 40 - 300 0 С Продувний газ переносить випарену вологу в комірку титратора DL 39 – Stromboli З автосамплером діапазон температур 40 - 300 0 С Вода вивільнюється і переноситься в титр-комірку потоком газу носія Гомогенізатор Вміст води 1 ppm – 5% 16
Аналіз нерозчинних чи складних зразків Сушильна піч DO 308 об’єм зразків до 10 см 3 діапазон температур 40 - 300 0 С Продувний газ переносить випарену вологу в комірку титратора DL 39 – Stromboli З автосамплером діапазон температур 40 - 300 0 С Вода вивільнюється і переноситься в титр-комірку потоком газу носія Гомогенізатор Вміст води 1 ppm – 5% 16
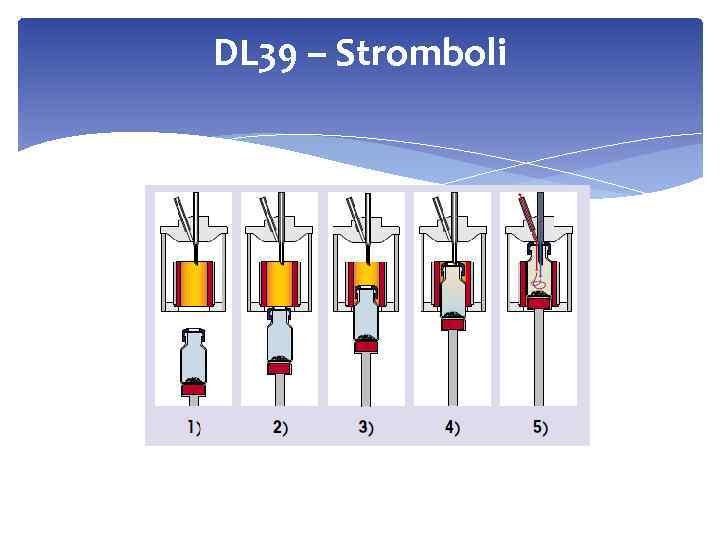 DL 39 – Stromboli
DL 39 – Stromboli
 Застосування титраторів КФ Виробництво полімерів Масла і мастила Фармацевтика 18
Застосування титраторів КФ Виробництво полімерів Масла і мастила Фармацевтика 18
 Список використаної літератури 1. 2. 3. 4. 5. Д. Скуг, Д. Уест Основи аналитической химии, т. 2 М. : Мир, 1979 р. – с. 215 -222 Пассет Б. В. , Антипов М. А. - Практикум по техническому анализу и контролю в производстве химико-фармацевтических препаратов и антибиотиков. - М. : Медицина, 1981, 272 с Руководство по применению реактивов HYDRANAL / Реактивы для титрования по Карлу Фишеру Riedel-de-Haёn http: //www. alsi. ua/ Оборудование современних лабораторий M. Lanz, A. De Agostini, C. A. De Caro, K. Rüegg Coulometric Karl Fischer titration: diaphragm-free cell, cell design and applications // Мettler-Toledo Gmb. H, Analytical CH-8603 Schwerzenbach, Switzerland 19
Список використаної літератури 1. 2. 3. 4. 5. Д. Скуг, Д. Уест Основи аналитической химии, т. 2 М. : Мир, 1979 р. – с. 215 -222 Пассет Б. В. , Антипов М. А. - Практикум по техническому анализу и контролю в производстве химико-фармацевтических препаратов и антибиотиков. - М. : Медицина, 1981, 272 с Руководство по применению реактивов HYDRANAL / Реактивы для титрования по Карлу Фишеру Riedel-de-Haёn http: //www. alsi. ua/ Оборудование современних лабораторий M. Lanz, A. De Agostini, C. A. De Caro, K. Rüegg Coulometric Karl Fischer titration: diaphragm-free cell, cell design and applications // Мettler-Toledo Gmb. H, Analytical CH-8603 Schwerzenbach, Switzerland 19
 Дякую за увагу : )
Дякую за увагу : )


