346a2dc274d163fae500d46fc0f1241f.ppt
- Количество слайдов: 63

Анализ результатов ОГЭ по химии в Свердловской области в 2017 г. И. В. Гофенберг доцент кафедры естественнонаучного образования ГАОУ ДПО СО «ИРО» , канд. хим. наук,

Информационная справка: В ОГЭ по химии в 2017 г приняло участие 4485 человек (в 2016 г. – 4450 чел. , в 2015 г. – 868 чел)

Результаты ОГЭ по предмету «Химия» в 2017 г. (2016 г. ) Не преодолели минимального балла 0, 84% (12, 32%) Средний балл 4, 04 (3, 64) Отметка « 3» 31, 57% Отметка « 4» Отметка « 5» 35, 93% (33, 24%) 32, 5% (21, 37%)

Содержательные блоки КИМ по предмету «Вещество» , «Химическая реакция» «Элементарные основы неорганической химии. Представления об органических веществах» «Методы познания веществ и химических явлений» , «Химия и жизнь» .

В центре внимания КИМ для ГИА-9 по химии в 2017 г. находились вопросы, связанные с усилением практической направленности контрольных измерительных материалов. В последние годы увеличена доля заданий, которые наряду с проверкой усвоения элементов предметного содержания ориентированы на проверку сформированности отдельных общеучебных интеллектуальных умений, способствующих приобретению опыта творческой и поисковой деятельности, к примеру, таких как умение работать с информацией, представленной в различных формах (рисунки, диаграммы, графики и т. п. ), умения сравнивать, сопоставлять изученные объекты, делать выводы и заключения и т. д.

Одним из результатов освоения курса химии на данном этапе его изучения должно стать «овладение умением объяснять причины многообразия веществ, зависимость их свойств от состава и строения, а также обусловленность применения веществ особенностями их свойств» ; «приобретение опыта применения химических методов изучения веществ и их превращений: наблюдение за свойствами веществ, условиями протекания химических реакций.

В экзаменационной работе ГИА-9 2017 г. на проверку сформированности названных умений ориентированы задания базового уровня сложности, с выбором ответа (задания 13 и 14) и повышенного уровня сложности (задания 18 и 19), с развернутым ответом (задание 22)

§ В соответствии с демонстрационным вариантом ОГЭ по химии в 2017 г. на выбор органам управления образованием субъектов предложены две модели экзаменационной работы, принципиальное различие которых заключается только в способах предъявления практико-ориентированных заданий части 2: § - модель № 1 без изменений повторяет экзаменационные модели предыдущих лет; § - модель № 2 предусматривает выполнение реального химического эксперимента (задания 22 и 23)

Часть I: задания базового сложности (1 -15) 1 2 Знание общих свойств классов Неорганических соединений Знание языка науки, основные химические понятий, 4 Признаки классификации веществ 3 5 Признаки классификации химических реакций Знание общих свойств металлов и неметаллов 6 7 Виды химических связей Расчет массовой доли элемента

Часть I: задания повышенного уровня сложности (16 -19) • закономерности изменения свойств химических элементов и образуемых ими соединений по группам и периодам Периодической системы химических элементов Д. И. Менделеева; • химические свойства основных классов неорганических соединений; • качественные реакции на ионы; • первоначальные сведения об органических веществах

Часть I: задания повышенного уровня сложности (16 -19) В экзаменационной работе 2017 г. предложены два задания на выбор нескольких правильных ответов из предложенного перечня (множественный выбор) и два задания на установление соответствия позиций, представленных в двух множествах. Правильный ответ записывается в виде набора цифр.

Часть I: задания повышенного уровня сложности (16 -19) В экзаменационной работе 2016 г. предложены два задания на выбор нескольких правильных ответов из предложенного перечня (множественный выбор) и два задания на установление соответствия позиций, представленных в двух множествах. Правильный ответ записывается в виде набора цифр.

Часть II: задания высокого уровня сложности 20 Окислительновосстановительные реакции 21 22 Расчетные задачи с использованием понятия массовая доля растворенного вещества Способы получения и химические свойства различных классов неорганических соединений, взаимосвязь веществ различных классов
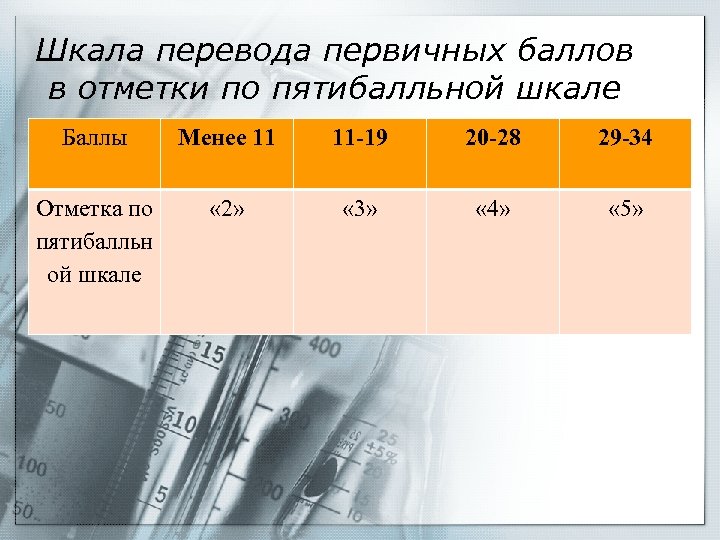
Шкала перевода первичных баллов в отметки по пятибалльной шкале Баллы Менее 11 11 -19 20 -28 29 -34 Отметка по пятибалльн ой шкале « 2» « 3» « 4» « 5»
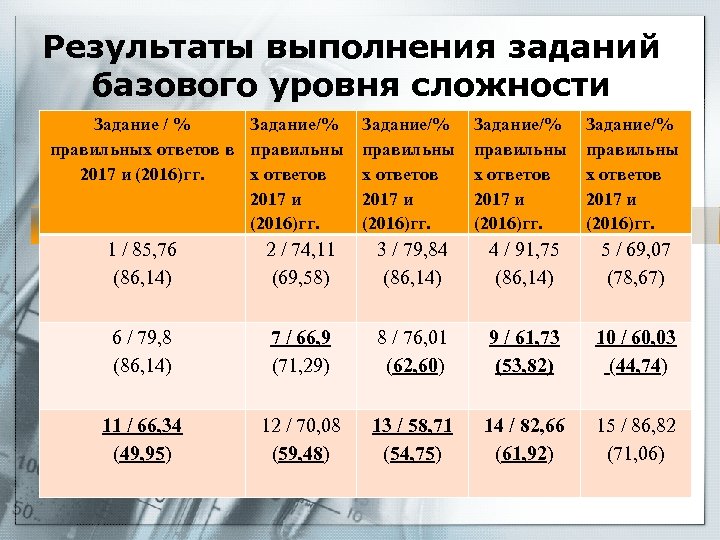
Результаты выполнения заданий базового уровня сложности Задание / % Задание/% правильных ответов в правильны 2017 и (2016)гг. х ответов 2017 и (2016)гг. Задание/% правильны х ответов 2017 и (2016)гг. 1 / 85, 76 (86, 14) 2 / 74, 11 (69, 58) 3 / 79, 84 (86, 14) 4 / 91, 75 (86, 14) 5 / 69, 07 (78, 67) 6 / 79, 8 (86, 14) 7 / 66, 9 (71, 29) 8 / 76, 01 (62, 60) 9 / 61, 73 (53, 82) 10 / 60, 03 (44, 74) 11 / 66, 34 (49, 95) 12 / 70, 08 (59, 48) 13 / 58, 71 (54, 75) 14 / 82, 66 (61, 92) 15 / 86, 82 (71, 06)

Средний результат (процент верно выполненных заданий) составил 74, 02% (против 68, 16% в 2016 г. ). Если средний балл за выполнение заданий базового уровня сложности в 2016 г. приближался к критическому значению (60%), то в 2017 г. показатель верно выполненных заданий базового уровня сложности существенно вырос. .

Задание 7 охватывает следующие элементы содержания курса химии: электролиты и неэлектролиты. Катионы и анионы. Электролитическая диссоциация кислот, щелочей и солей (средних). Школьники должны объяснять сущность процесса электролитической диссоциации и реакций ионного обмена. Как показывает практика, качество выполнения задания во многом определяется метапредметными умениями анализа и прогнозирования результата химической реакции.

§ Помимо знания условий протекания таких реакций, необходима сформированость умений прогнозировать состав исходных веществ по продуктам реакции, оценивать возможность протекания реакций между предложенными в задании ионами. Обычно школьники хорошо определяют возможность выпадения осадка, ориентируясь на таблицу растворимости. Возможность образования газа диагностируется труднее.

Наиболее низок балл для образовательных организаций всех видов задания 9, которое охватывает элементы содержания курса химии, касающиеся свойств простых веществ (металлов и неметаллов). Как показывает практика, качество выполнения задания во многом определяется метапредметными умениями анализировать (например, активность металла по ряду напряжений или галогенов по группе) и прогнозировать результат химической реакции.

§ В том случае, если задание содержит отрицание, оно приобретает дополнительную сложность. Так, например, если необходимо определить вещество из набора: аммиак, медь, оксид углерода (II), гидроксид натрия, которое не взаимодействует с кислородом, то уровень сложности задания возрастает.

Раздел курса неорганической химии, связанный со свойствами оксидов (задание 10), как ни странно, всегда оказывается сложным для выпускников. Непонимание признаков классификации, а также традиционные трудности определения веществ по названию (в соответствии номенклатурой) являются причиной резкого снижения качества выполнения этого задания. Выпускники затрудняются с определением свойств, прежде всего, амфотерных оксидов, которые имеют двойственный характер.

Задание 11 предполагало выявление понимания выпускниками характерных химических свойств оснований и кислот. Так, в одном из вариантов задание 11 предусматривало определение продуктов реакции гидроксида бария с каждым из двух веществ, указанных в перечне. Сложность задания заключалась в том, что были предложены не формулы, а названия веществ. Вопросы, связанные с номенклатурой веществ, традиционно относятся к трудным заданиям.

Качество выполнения задания 13, представленного в виде двух суждений, составляет 58, 71%. Участники экзамена затруднились ответить на вопрос о первой помощи при химических ожогах и о правилах хранения легковоспламеняющихся жидкостей, например, ацетона. Это задание имеет практикоориентированный характер. В основе правильного ответа – знание физических свойств веществ и способов хранения и обращения, умение привлекать свой жизненный опыт и здравый смысл.

Примеры заданий 13: верны ли следующие суждения? 1. А) При нагревании жидкости необходимо закрыть пробирку пробкой Б) При приготовлении раствора серной кислоты в концентрированную серную кислоту необходимо добавлять воду. 2. А) Фильтровальная бумага используется в процессе дистилляции Б) Отходы от использования синтетических моющих средств можно выливать в природные водоемы

3. А) В лаборатории запрещается принимать пищу Б) В лаборатории запрещается находиться без защитных очков 4. А) Запрещается переливать излишек взятого вещества обратно в исходную склянку Б) Чтобы погасить пламя спиртовки, следует его задуть

5. А) При нагревании пробирки с раствором ее следует располагать строго вертикально. Б) При проведении опытов с растворами кислот необходимо всегда надевать резиновые перчатки 6. А) Пробирка с газоотводной трубкой используется для отвода теплоты, выделяющейся в химической реакции Б) Зубная паста, содержащая ионы кальция, способствует укреплению зубной эмали

Результаты выполнения заданий повышенного уровня сложности Задание % правильных ответов в 2016 и (2015)гг. 16 95, 28% (77, 84%) 84, 56% (54, 24%) 67, 63% (38, 74%) 61, 58% (38, 49%) 17 18 19

Результат выполнения заданий повышенного уровня сложности оказался существенно выше показателя 2016 г. : средний показатель качества составил 77, 25% (в 2016 г. - 52, 33).

Качество выполнения большинства заданий повышенного уровня сложности значительно выше, чем в 2016 г. , хотя еще есть резервы повышения качества их выполнения (задания 18 и 19). Периодический закон и закономерности изменения свойств химических элементов и их соединений достаточно хорошо понят выпускниками. Традиционно сложнее для участников экзамена оказывается задание 17, связанное с первоначальными сведениями об органических веществах.

Пример задания 17: § Для уксусной кислоты характерно: 1) плохая растворимость в воде 2) взаимодействие с цинком 3) наличие в молекуле двойной связи между атомами углерода 4) наличие в молекуле четырех атомов водорода 5) взаимодействие с оксидом кремния

Анализ результатов выполнения задания 18 свидетельствует о том, что элемент содержания, связанный с качественными реакциями и признаками реакций освоен на значительно более высоком уровне: 67, 63% участников экзамена справились с заданием абсолютно правильно (в 2016 г. только 38, 74% участников экзамена получили за него 2 балла).

Задание 18 также было представлено двумя множествами и предполагало две формы: определение реагентов для идентификации предложенных веществ или установление признаков реакции.

Пример: установите соответствие между названиями реагирующих веществ и признаками реакции Названия веществ Признаки реакции А Медь и концентрированная серная кислота Б Гидрокарбонат кальция и 2) соляная кислота Нитрат бария и сульфат 3) меди образование голубого осадка образование белого осадка 4) выделение бурого газа В 1) выделение бесцветного газа

В содержательный блок «Неорганическая химия» включены элементы содержания, которые связаны с характерными химическими свойствами металлов, неметаллов и основных классов неорганических соединений. Задание 19 позволяет проверить усвоение этих элементов на другом, более высоком уровне сложности, чем задания 9, 10 и 11.

Формула вещества Реагенты А) P 2 O 5 1) Ca. CI 2, HNO 3 Б) Na 2 CO 3 2) Kl, Cu В) Br 2 3) H 2 O, Ca. O 4) O 2, Fe. SO 4

Часть II: задания высокого уровня сложности (20 -22) Выполнение заданий высокого уровня сложности предполагает сформированность комплексных умений: -составлять электронный баланс и уравнение окислительно-восстановительной реакции; -объяснять обусловленность свойств и способов получения веществ их составом и строением, взаимосвязь неорганических веществ; -проводить комбинированные расчеты -по химическим уравнениям
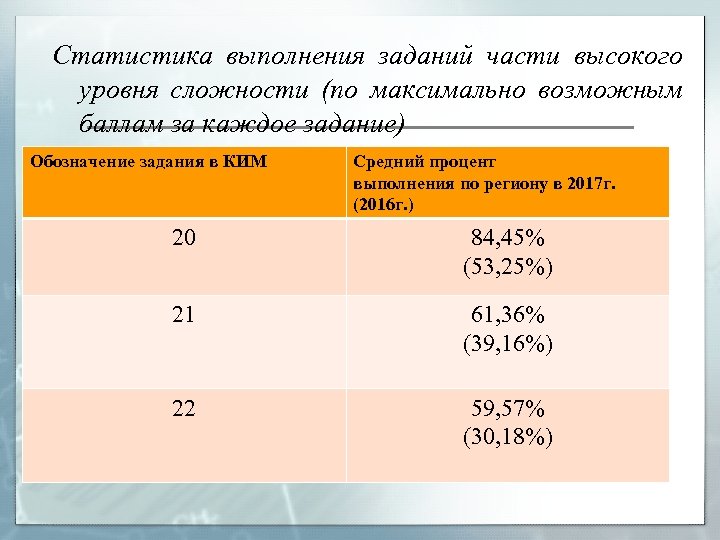
Статистика выполнения заданий части высокого уровня сложности (по максимально возможным баллам за каждое задание) Обозначение задания в КИМ Средний процент выполнения по региону в 2017 г. (2016 г. ) 20 84, 45% (53, 25%) 21 61, 36% (39, 16%) 22 59, 57% (30, 18%)

Средний показатель качества выполнения заданий с развернутым ответом (по максимально возможным баллам за каждое задание) составил 68, 46% (в 2016 г. – 40, 86%).

Используя метод электронного баланса, составьте уравнение реакции § NO 2 + О 2 + КОН → КNO 3 + H 2 O Определите окислитель и восстановитель 4 NO 2 + О 2 + 4 КОН = 4 КNO 3 + 2 H 2 O





К числу наиболее часто встречающихся ошибок следует отнести отсутствие коэффициентов в полуреакциях, путаницу в понимании роли частицы (окислитель или восстановитель) и процесса (окисление или восстановление). Значительная часть участников экзамена определяет как частицы, так и процесс. Причем зачастую название процесса противоречит электронному балансу. Это свидетельствует о недостаточном уровне сформированности понятий окислитель и восстановитель и может быть основанием для снижения балла.

Уравнения, которые были предложены в заданиях 20, не встречаются в систематическом курсе химии основной школы и призваны выявить умение участников экзамена действовать в новой учебной ситуации, используя необходимые элементы содержания курса химии. Na. Mn. O 4 + Na. OH → Na 2 Mn. O 4 + O 2 + H 2 O HCI + Pb. O 2 → Pb. CI 2 + H 2 O

Выпускники основной школы алгоритмом вычислительных операций владеют заметно увереннее. Ошибки, главным образом, допускаются при написании уравнений реакции: вместо газа SO 2, например, указан газ H 2 S, вместо карбоната натрия – сульфат натрия. В данном случае причиной ошибок является недостаточный уровень освоения номенклатуры веществ.

К 252 г раствору сульфита натрия с массовой долей соли 5% добавили избыток соляной кислоты. Вычислите объем (н. у. ) выделившегося газа.




Особенностью задания 22 является и то, что обычно дан избыточный перечень реактивов. Кроме того, требуемое вещество из предлагаемых реагентов можно получить и в одну стадию. Однако задание предполагает получение целевого продукта в две стадии. К числу типичных ошибок, допущенных участниками экзамена при выполнении задания 22, следует отнести получение нужного вещества в одну стадию, а также отсутствие описания признаков реакции: выделение осадка определенного характера и цвета, образование газа специфического запаха и др.

§ Особенностью задания 22 является и то, что решение является вариативным и допускает несколько способов. Даже в критериях оценивания в некоторых вариантах приводились несколько способов решения задания. Однако выпускники предлагали и свой алгоритм решения, с химической точки зрения абсолютно верный.

Пример задания 22. § Даны вещества: Fe, Fe 2(SO 4)3, Mg. SO 4, Na. CI, Ba. CI 2, раствор H 2 SO 4. Используя воду и необходимые вещества только из этого списка, получите в две стадии раствор хлорида железа (II). Запишите уравнения проведенных химических реакций. Опишите признаки этих реакций. Для реакции ионного обмена напишите сокращенное ионное уравнение. §

Критерии оценивания 1) Fe + H 2 SO 4 = Fe. SO 4 + H 2↑ 2) Fe. SO 4+ Ba. CI 2 = Ba. SO 4↓+ Fe. CI 2 Ва 2+ + SO 42 - = Ba. SO 4↓ Или 1) H 2 SO 4 + Ba. CI 2 = Ba. SO 4 + 2 НCI 2) Fe + 2 НCI = Fe. CI 2 + H 2↑ Ва 2+ + SO 42 - = Ba. SO 4↓



§ При согласовании единых подходов к оцениванию территориальными комиссиями было определено, что при описании свойств веществ необходимо использовать два признака: цвет газа и запах, цвет и характер осадка и т. п. В критериях оценивания приводятся как по одному, так по двум и даже по трем признакам веществ. Это делает критерии размытыми и требует единообразия подходов в оценивании.

Элементы содержания, уровень освоения которых соответствует требованиям стандарта базового уровня сложности Строение атома. Периодический закон и Периодическая система химических элементов Д. И. Менделеева Строение молекул, химическая связь. Валентность элементов. Степень окисления Простые и сложные вещества. Основные классы веществ. Химическая реакция. Условия и признаки протекания химических реакций. Химические уравнения. Вычисление массовой доля химического элемента в веществе.

Элементы содержания, уровень освоения которых соответствует требованиям стандарта повышенного и высокого уровней сложности Закономерности изменения свойств элементов по их положению в Периодической системе Степень окисления. Окислитель и восстановитель. Окислительно-восстановительные реакции. Основные классы веществ. Химическая реакция. Условия и признаки протекания химических реакций. Химические уравнения. Расчеты по уравнению реакции.

Элементы содержания, усвоение которых в целом нельзя считать достаточным - электролиты и неэлектролиты. Катионы и анионы. Электролитическая диссоциация кислот, щелочей и солей (средних). - взаимосвязь различных классов неорганических веществ; - качественные реакции на неорганические вещества и ионы -номенклатура неорганических веществ (систематическая и тривиальная)

- чистые вещества и смеси. Правила безопасной работы в школьной лаборатории. Лабораторная посуда и оборудование. Человек в мире веществ, материалов и химических реакций. Проблемы безопасного использования веществ и химических реакций в повседневной жизни. Разделение смесей и очистка веществ. Приготовление растворов. Химическое загрязнение окружающей среды и его последствия.
Умения и виды деятельности, уровень сформированности которых нельзя считать достаточным Умение выявлять взаимосвязь понятий Умение использовать химические понятия для объяснения фактов и явлений Объяснять зависимость свойств веществ от их состава и строения
Недостаточный уровень сформированности общеучебных умений: умение прогнозировать ход процесса умение устанавливать причинно-следственные связи умение анализировать текст и выделять ключевые слова, которые лежат в основе определения химизма процесса
346a2dc274d163fae500d46fc0f1241f.ppt