Лекции по АХ.ppt
- Количество слайдов: 103
 Аналитическая химия (количественный анализ) курс лекций Волков А. В. , Филимонов Д. А. , Березина Н. М. , Базанов М. И. ГОУ ВПО «ИГХТУ» Кафедра аналитической химии ПЛ 097/П
Аналитическая химия (количественный анализ) курс лекций Волков А. В. , Филимонов Д. А. , Березина Н. М. , Базанов М. И. ГОУ ВПО «ИГХТУ» Кафедра аналитической химии ПЛ 097/П
 Список литературы: Васильев, В. П. Аналитическая химия. Кн. 1. - М. : Дрофа, 2003. n Лабораторные работы по химическим методам анализа. : метод. указания / Кочергина Л. А. , Ю. А. Жуков; Иван. хим. -технол. ин-т. Иваново, 1991. /библ. № 370/. n Аналитическая химия: лабораторный практикум / В. П. Васильев, Р. П. Морозова, Л. А. Кочергина. М. : Дрофа, 2004. n Аналитическая химия: сборник вопросов, упражнений и задач / В. П. Васильев, Л. А. Кочергина, Т. Д. Орлова - М. : Дрофа, 2003. n
Список литературы: Васильев, В. П. Аналитическая химия. Кн. 1. - М. : Дрофа, 2003. n Лабораторные работы по химическим методам анализа. : метод. указания / Кочергина Л. А. , Ю. А. Жуков; Иван. хим. -технол. ин-т. Иваново, 1991. /библ. № 370/. n Аналитическая химия: лабораторный практикум / В. П. Васильев, Р. П. Морозова, Л. А. Кочергина. М. : Дрофа, 2004. n Аналитическая химия: сборник вопросов, упражнений и задач / В. П. Васильев, Л. А. Кочергина, Т. Д. Орлова - М. : Дрофа, 2003. n
 n. Лурье Ю. Ю. Справочник по аналитической химии. - М. : Химия, 1985. n. Раздаточный материал к лекционному курсу по аналитической химии (количественный анализ). : метод. указания / М. И. Базанов и др. ; Иван. гос. хим. -технол. ун-т. Иваново, 2004. /библ. № 933/. n. Расчеты в количественном анализе. : метод. указания / М. И. Базанов, Л. А. Кочергина, Т. Д. Орлова; Иван. гос. хим. -технол. ун-т. Иваново, 2005. /библ. № 949/. n. Задания для экспресс-опроса студентов при изучении курса «Аналитической химии» . : метод. указания / Л. А. Кочергина и др. ; Иван. гос. хим. технол. ун-т. Иваново, 2005. /библ. № 958/.
n. Лурье Ю. Ю. Справочник по аналитической химии. - М. : Химия, 1985. n. Раздаточный материал к лекционному курсу по аналитической химии (количественный анализ). : метод. указания / М. И. Базанов и др. ; Иван. гос. хим. -технол. ун-т. Иваново, 2004. /библ. № 933/. n. Расчеты в количественном анализе. : метод. указания / М. И. Базанов, Л. А. Кочергина, Т. Д. Орлова; Иван. гос. хим. -технол. ун-т. Иваново, 2005. /библ. № 949/. n. Задания для экспресс-опроса студентов при изучении курса «Аналитической химии» . : метод. указания / Л. А. Кочергина и др. ; Иван. гос. хим. технол. ун-т. Иваново, 2005. /библ. № 958/.
 Аналитическая химия - наука о методах определения химического состава вещества и его структуры. Предметом аналитической химии является разработка методов анализа и их практическое выполнение, а также широкое исследование теоретических основ аналитических методов. 4
Аналитическая химия - наука о методах определения химического состава вещества и его структуры. Предметом аналитической химии является разработка методов анализа и их практическое выполнение, а также широкое исследование теоретических основ аналитических методов. 4
 Аналитическая химия 1. Качественный анализ. 2. Количественный анализ. P = f(c) Р – аналитический сигнал (измеряемое свойство). а) Р –V(объем) – титриметрический анализ. б) Р – m (массы) – гравиметрический анализ. 5
Аналитическая химия 1. Качественный анализ. 2. Количественный анализ. P = f(c) Р – аналитический сигнал (измеряемое свойство). а) Р –V(объем) – титриметрический анализ. б) Р – m (массы) – гравиметрический анализ. 5
 Титриметрический анализ основан на точном измерении объема стандартного раствора пошедшего на реакцию с определяемым веществом. Стандартным раствором называют раствор, концентрация которого известна с высокой точностью (± 0, 1%). Титрование – процесс постепенного прибавления титранта (стандартный раствор) к определяемому веществу для определения точки эквивалентности. Точка эквивалентности – момент титрования, когда количество титранта химически эквивалентно количеству анализируемого вещества.
Титриметрический анализ основан на точном измерении объема стандартного раствора пошедшего на реакцию с определяемым веществом. Стандартным раствором называют раствор, концентрация которого известна с высокой точностью (± 0, 1%). Титрование – процесс постепенного прибавления титранта (стандартный раствор) к определяемому веществу для определения точки эквивалентности. Точка эквивалентности – момент титрования, когда количество титранта химически эквивалентно количеству анализируемого вещества.
 Эквивалент – реальная или условная частица, соответствующая одному протону или другому одноразрядному иону в данной реакции. Фактор эквивалентности показывает, какая доля реальной или условной частицы соответствует одному протону или другому однозарядному иону в данной реакции. Мэкв = fэкв ∙ М(А) Na 2 CO 3 + HCl = Na. HCO 3 + Na. Cl fэкв(Na 2 CO 3) = 1 Мэкв = 1 ∙ М(Na 2 CO 3) = 105, 99 Na 2 CO 3 + 2 HCl = H 2 CO 3 + 2 Na. Cl fэкв(Na 2 CO 3) = ½ Мэкв = ½ ∙ М(Na 2 CO 3) = 52, 99
Эквивалент – реальная или условная частица, соответствующая одному протону или другому одноразрядному иону в данной реакции. Фактор эквивалентности показывает, какая доля реальной или условной частицы соответствует одному протону или другому однозарядному иону в данной реакции. Мэкв = fэкв ∙ М(А) Na 2 CO 3 + HCl = Na. HCO 3 + Na. Cl fэкв(Na 2 CO 3) = 1 Мэкв = 1 ∙ М(Na 2 CO 3) = 105, 99 Na 2 CO 3 + 2 HCl = H 2 CO 3 + 2 Na. Cl fэкв(Na 2 CO 3) = ½ Мэкв = ½ ∙ М(Na 2 CO 3) = 52, 99
 Основное правило титриметрических методов анализа (закон эквивалентов) В точке эквивалентности число моль эквивалента титранта равно числу моль эквивалента определяемого вещества n (титранта) = n (определяемого вещества) 8
Основное правило титриметрических методов анализа (закон эквивалентов) В точке эквивалентности число моль эквивалента титранта равно числу моль эквивалента определяемого вещества n (титранта) = n (определяемого вещества) 8
 Способы выражения концентрации 1. Молярная (моль/л) с(HCl) = 0, 1 М с(H 2 SO 4) = 1 M 2. Молярная концентрация эквивалента (нормальность) (моль·экв/л) с(f. A) с(HCl) = 0, 1 н с(1/5 KMn. O 4) = 0, 1 н с(1/2 H 2 SO 4) = 1 н
Способы выражения концентрации 1. Молярная (моль/л) с(HCl) = 0, 1 М с(H 2 SO 4) = 1 M 2. Молярная концентрация эквивалента (нормальность) (моль·экв/л) с(f. A) с(HCl) = 0, 1 н с(1/5 KMn. O 4) = 0, 1 н с(1/2 H 2 SO 4) = 1 н
 3. Титр (г/мл) Т(HCl) = 0. 005026 4. Титр по определяемому веществу (г/мл) Т(А/В)(условный титр) – сколько грамм вещества В соответствует 1 мл титранта А. Т(HCl/Ca. O) = 0. 002914
3. Титр (г/мл) Т(HCl) = 0. 005026 4. Титр по определяемому веществу (г/мл) Т(А/В)(условный титр) – сколько грамм вещества В соответствует 1 мл титранта А. Т(HCl/Ca. O) = 0. 002914
 Требования, предъявляемые к реакциям в титриметрическом анализе n Реакция должна протекать с большой скоростью. n Константа равновесия должна быть велика, т. е. реакция должна протекать полностью. n Должны отсутствовать побочные реакции. n Возможность фиксирования точки эквивалентности (т. э. ). 11
Требования, предъявляемые к реакциям в титриметрическом анализе n Реакция должна протекать с большой скоростью. n Константа равновесия должна быть велика, т. е. реакция должна протекать полностью. n Должны отсутствовать побочные реакции. n Возможность фиксирования точки эквивалентности (т. э. ). 11
 Приемы титриметрического анализа • прямое титрование; • обратное титрование (титрование по остатку); • титрование по замещению (титрование заместителя). 12
Приемы титриметрического анализа • прямое титрование; • обратное титрование (титрование по остатку); • титрование по замещению (титрование заместителя). 12
 1. В методах прямого титрования определяемое вещество непосредственно реагирует с титрантом. Типичным примером прямого титрования является титрование щелочи кислотой. n(Na. OH) = n(HCl) c(Na. OH) ∙ V(Na. OH) = c(HCl) ∙ V(HCl) 13
1. В методах прямого титрования определяемое вещество непосредственно реагирует с титрантом. Типичным примером прямого титрования является титрование щелочи кислотой. n(Na. OH) = n(HCl) c(Na. OH) ∙ V(Na. OH) = c(HCl) ∙ V(HCl) 13
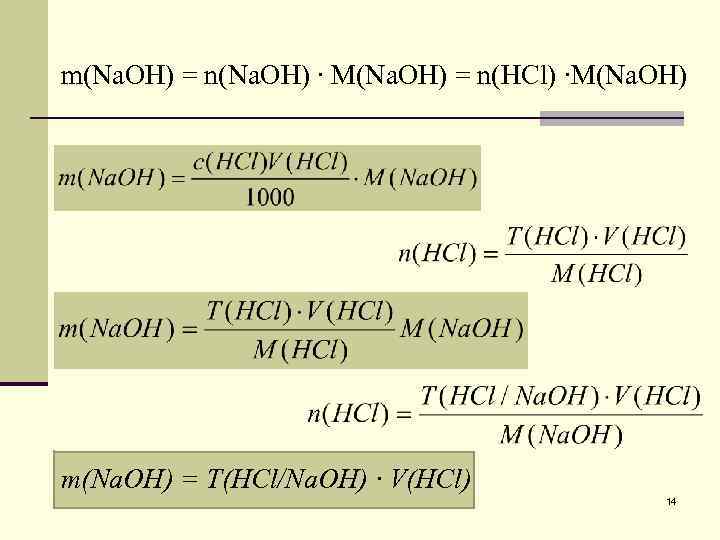 m(Na. OH) = n(Na. OH) ∙ M(Na. OH) = n(HCl) ∙M(Na. OH) m(Na. OH) = Т(HCl/Na. OH) ∙ V(HCl) 14
m(Na. OH) = n(Na. OH) ∙ M(Na. OH) = n(HCl) ∙M(Na. OH) m(Na. OH) = Т(HCl/Na. OH) ∙ V(HCl) 14
 2. В методах обратного титрования используется два титрованных рабочих раствора — основной и вспомогательный. Пример 1. Ca. CO 3 + 2 HCl(изб – № 1) = Ca. Cl 2+ H 2 O + CO 2 + (HClост) HClост + Na. OH № 2 = Na. Cl + H 2 O n(1/2 Ca. CO 3) = n(HCl) – n(Na. OH) 15
2. В методах обратного титрования используется два титрованных рабочих раствора — основной и вспомогательный. Пример 1. Ca. CO 3 + 2 HCl(изб – № 1) = Ca. Cl 2+ H 2 O + CO 2 + (HClост) HClост + Na. OH № 2 = Na. Cl + H 2 O n(1/2 Ca. CO 3) = n(HCl) – n(Na. OH) 15
 Пример 2. Определение солей аммония и азота в органических соединениях по Кьельдалю а) Н 2 SO 4 изб. + 2 NH 3 = (NH 4)2 SO 4 + (Н 2 SO 4 ост) Н 2 SO 4 ост + 2 Na. OH = Na 2 SO 4 + 2 H 2 O n(NH 4+) = n(1/2 Н 2 SO 4 ) – n(Na. OH) 16
Пример 2. Определение солей аммония и азота в органических соединениях по Кьельдалю а) Н 2 SO 4 изб. + 2 NH 3 = (NH 4)2 SO 4 + (Н 2 SO 4 ост) Н 2 SO 4 ост + 2 Na. OH = Na 2 SO 4 + 2 H 2 O n(NH 4+) = n(1/2 Н 2 SO 4 ) – n(Na. OH) 16
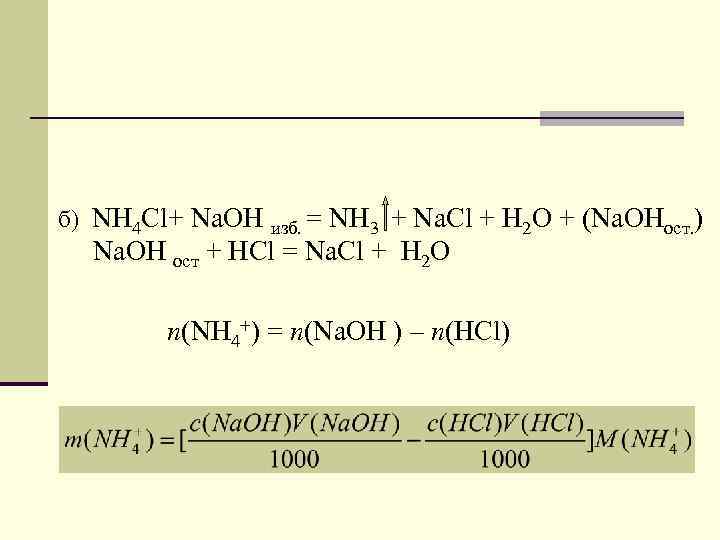 б) NH 4 Сl+ Na. OH изб. = NH 3 + Na. Cl + H 2 O + (Na. OHост. ) Na. OH ост + HCl = Na. Cl + H 2 O n(NH 4+) = n(Na. OH ) – n(HCl)
б) NH 4 Сl+ Na. OH изб. = NH 3 + Na. Cl + H 2 O + (Na. OHост. ) Na. OH ост + HCl = Na. Cl + H 2 O n(NH 4+) = n(Na. OH ) – n(HCl)
 3. Tитрование заместителя или титрование по замещению В этом методе к определяемому веществу добавляют специальный реагент, вступающий с ним в реакцию. Один из продуктов взаимодействия оттитровывается рабочим раствором.
3. Tитрование заместителя или титрование по замещению В этом методе к определяемому веществу добавляют специальный реагент, вступающий с ним в реакцию. Один из продуктов взаимодействия оттитровывается рабочим раствором.
 Примеры: 1) При иодометрическом определении меди к анализируемому раствору добавляется заведомый избыток KI и происходит реакция: 2 Сu 2+ + 4 I- = 2 Cu. I + I 2 Выделившийся иод оттитровывают тиосульфатом: I 2 + 2 S 2 O 42 - = 2 I- + S 4 O 622) Определение NH 4+ 4 NH 4+ + 6 CH 2 O = 6(CH 2)N 4↓ + 4 H+ + 6 H 2 O Образовавшуюся кислоту оттитровывают щелочью.
Примеры: 1) При иодометрическом определении меди к анализируемому раствору добавляется заведомый избыток KI и происходит реакция: 2 Сu 2+ + 4 I- = 2 Cu. I + I 2 Выделившийся иод оттитровывают тиосульфатом: I 2 + 2 S 2 O 42 - = 2 I- + S 4 O 622) Определение NH 4+ 4 NH 4+ + 6 CH 2 O = 6(CH 2)N 4↓ + 4 H+ + 6 H 2 O Образовавшуюся кислоту оттитровывают щелочью.
 3) Определение Ca: Сa. C 2 O 4 + H 2 SO 4 = Сa. SO 4 + H 2 C 2 O 4 5 H 2 C 2 O 4 + 2 Mn. O 4 - + 6 H+ =10 CO 2+ 2 Mn 2++ 8 H 2 O n(½Ca. C 2 O 4) = n(½H 2 C 2 O 4) = n(1/5 KMn. O 4) 20
3) Определение Ca: Сa. C 2 O 4 + H 2 SO 4 = Сa. SO 4 + H 2 C 2 O 4 5 H 2 C 2 O 4 + 2 Mn. O 4 - + 6 H+ =10 CO 2+ 2 Mn 2++ 8 H 2 O n(½Ca. C 2 O 4) = n(½H 2 C 2 O 4) = n(1/5 KMn. O 4) 20
 Методы титриметрического анализа: I. Кислотно-основное титрование Н+ +ОН- = Н 2 О II. Комплексометрическое титрование Hg 2+ + 2 Cl- = Hg. Cl 2 (меркуриметрия) M 2+ + H 2 ЭДТА 2 - = МЭДТА 2 - + 2 Н+ (комплексонометрия) III. Осадительное титрование Аg+ + Cl- = Ag. Cl (аргентометрия) Hg 22++ 2 Cl- = Hg 2 Cl 2 (меркурометрия) IV. Окислительно-восстановительное титрование (редоксиметрия) 5 Fe 2+ + Mn. O 4 - + 8 H+ = 5 Fe 3+ + Mn 2+ + 4 H 2 O 21
Методы титриметрического анализа: I. Кислотно-основное титрование Н+ +ОН- = Н 2 О II. Комплексометрическое титрование Hg 2+ + 2 Cl- = Hg. Cl 2 (меркуриметрия) M 2+ + H 2 ЭДТА 2 - = МЭДТА 2 - + 2 Н+ (комплексонометрия) III. Осадительное титрование Аg+ + Cl- = Ag. Cl (аргентометрия) Hg 22++ 2 Cl- = Hg 2 Cl 2 (меркурометрия) IV. Окислительно-восстановительное титрование (редоксиметрия) 5 Fe 2+ + Mn. O 4 - + 8 H+ = 5 Fe 3+ + Mn 2+ + 4 H 2 O 21
 I. Кислотно-основное титрование Н+ +ОН- = Н 2 О Титранты: • Сильные кислоты - HCl, HNO 3, Н 2 SO 4 • Сильные основания - Na. OH, KOH Определяемые вещества: кислоты, основания, соли. В процессе титрования происходит изменение р. Н p. Н = - lg a. H+ = - lg( H+] ∙ H+); p. Н - lg H+]. Кривая титрования - это графическая зависимость р. Н раствора от объема добавленного титранта (р. Н = f(Vтитранта)).
I. Кислотно-основное титрование Н+ +ОН- = Н 2 О Титранты: • Сильные кислоты - HCl, HNO 3, Н 2 SO 4 • Сильные основания - Na. OH, KOH Определяемые вещества: кислоты, основания, соли. В процессе титрования происходит изменение р. Н p. Н = - lg a. H+ = - lg( H+] ∙ H+); p. Н - lg H+]. Кривая титрования - это графическая зависимость р. Н раствора от объема добавленного титранта (р. Н = f(Vтитранта)).
 Расчет кривой титрования сильного основания сильной кислотой 100 мл 0, 1 М Na. OH + V мл 0, 1 М HCl; Vобщ = const (100 мл) Na. OH + HCl = Na. Cl + H 2 O 1) V(HCl) = 0 мл, ОН- = Na. ОН = 0, 1 моль/л р. ОН = -lg 0, 1 = 1; р. Н = 14 -1= 13 2) V(HCl) = 50, 0 мл, р. ОН = -lg 0, 05 = 1, 3; р. Н = 12, 7 3) V(HCl) = 90, 0 мл, р. ОН = -lg 0, 01 = 2; р. Н = 12 23
Расчет кривой титрования сильного основания сильной кислотой 100 мл 0, 1 М Na. OH + V мл 0, 1 М HCl; Vобщ = const (100 мл) Na. OH + HCl = Na. Cl + H 2 O 1) V(HCl) = 0 мл, ОН- = Na. ОН = 0, 1 моль/л р. ОН = -lg 0, 1 = 1; р. Н = 14 -1= 13 2) V(HCl) = 50, 0 мл, р. ОН = -lg 0, 05 = 1, 3; р. Н = 12, 7 3) V(HCl) = 90, 0 мл, р. ОН = -lg 0, 01 = 2; р. Н = 12 23
 4) V(HCI)=99, 0 мл; p. OH=3; р. Н = 11 5) V(HCl) = 99, 9 мл; р. ОН = 4; р. Н = 10 6) V(HCl) = 100, 0 мл – т. э. ; ОН- = Н+ = 10 -7 моль/л; р. Н = 7 7) V(HCl) = 100, 1 мл; р. Н = 4
4) V(HCI)=99, 0 мл; p. OH=3; р. Н = 11 5) V(HCl) = 99, 9 мл; р. ОН = 4; р. Н = 10 6) V(HCl) = 100, 0 мл – т. э. ; ОН- = Н+ = 10 -7 моль/л; р. Н = 7 7) V(HCl) = 100, 1 мл; р. Н = 4
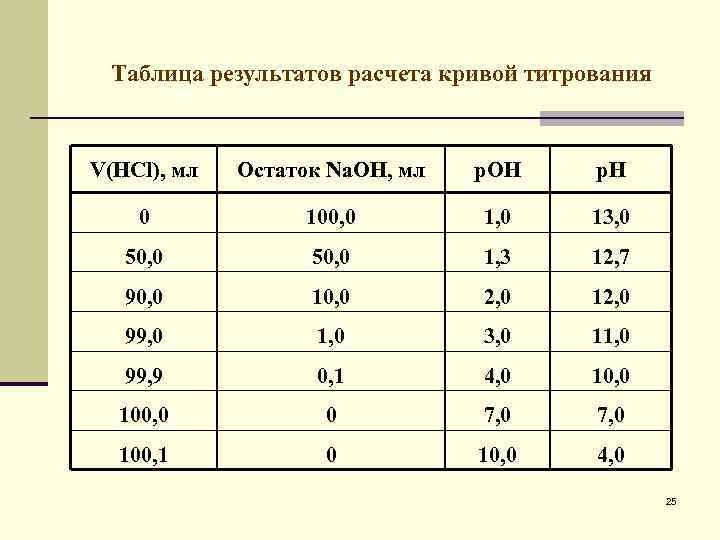 Таблица результатов расчета кривой титрования V(HCl), мл Остаток Na. ОН, мл р. ОН р. Н 0 100, 0 13, 0 50, 0 1, 3 12, 7 90, 0 10, 0 2, 0 12, 0 99, 0 1, 0 3, 0 11, 0 99, 9 0, 1 4, 0 100, 0 0 7, 0 100, 1 0 10, 0 4, 0 25
Таблица результатов расчета кривой титрования V(HCl), мл Остаток Na. ОН, мл р. ОН р. Н 0 100, 0 13, 0 50, 0 1, 3 12, 7 90, 0 10, 0 2, 0 12, 0 99, 0 1, 0 3, 0 11, 0 99, 9 0, 1 4, 0 100, 0 0 7, 0 100, 1 0 10, 0 4, 0 25
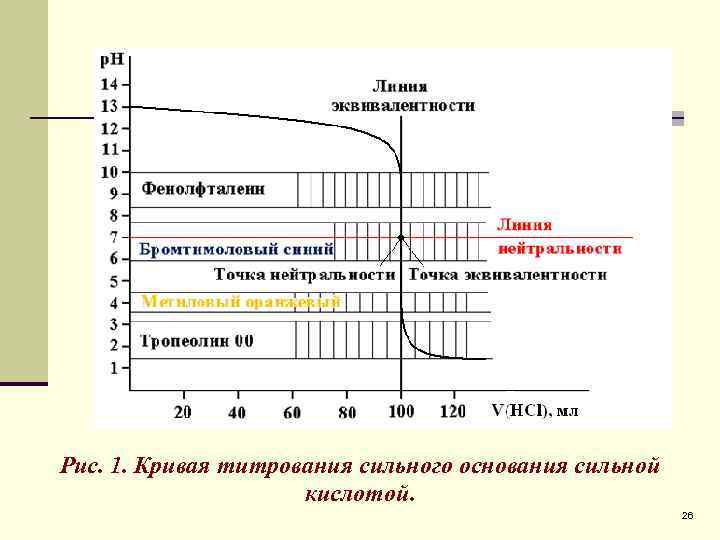 Рис. 1. Кривая титрования сильного основания сильной кислотой. 26
Рис. 1. Кривая титрования сильного основания сильной кислотой. 26
 Пересечение линии эквивалентности (Л. Э. ) с линией нейтральности (Л. Н. ) дает точку нейтральности (Т. Н. ). В данном случае, при титровании сильного основания сильной кислотой Т. Н. и Т. Э. совпадают. Резкое изменение р. Н вблизи Т. Э. называется скачком титрования (С. Т. ). Точка на кривой титрования, когда раствор недотитрован на 0, 1% называется началом С. Т. , когда раствор перетитрован на 0, 1% - конец С. Т.
Пересечение линии эквивалентности (Л. Э. ) с линией нейтральности (Л. Н. ) дает точку нейтральности (Т. Н. ). В данном случае, при титровании сильного основания сильной кислотой Т. Н. и Т. Э. совпадают. Резкое изменение р. Н вблизи Т. Э. называется скачком титрования (С. Т. ). Точка на кривой титрования, когда раствор недотитрован на 0, 1% называется началом С. Т. , когда раствор перетитрован на 0, 1% - конец С. Т.
 Факторы, влияющие на величину скачка титрования а) Концентрация с(Na. ОН) = с(НСl) = 1 M V(HCl) = 99, 9 мл; р. ОН = 3; р. Н = 11 V(HCl) = 100, 1 мл; р. Н = 3 Скачок титрования : 11 – 3 = 8 единиц р. Н. С увеличением концентрации скачка титрования увеличивается. величина 28
Факторы, влияющие на величину скачка титрования а) Концентрация с(Na. ОН) = с(НСl) = 1 M V(HCl) = 99, 9 мл; р. ОН = 3; р. Н = 11 V(HCl) = 100, 1 мл; р. Н = 3 Скачок титрования : 11 – 3 = 8 единиц р. Н. С увеличением концентрации скачка титрования увеличивается. величина 28
 б) Температура t = 25 0 C Kw = 10 -14 t = 60 0 C Kw = 10 -13 V(HCl) = 99, 9 мл, ОН- = 10 -3 моль/л; р. ОН = 3; р. Н = 10 V(HCl) = 100, 1 мл, Н+ = 10 -3 моль/л; р. Н = 3 При 60 0 C Δр. Н =10 - 3 = 7 С ростом температуры, величина скачка титрования уменьшается. 29
б) Температура t = 25 0 C Kw = 10 -14 t = 60 0 C Kw = 10 -13 V(HCl) = 99, 9 мл, ОН- = 10 -3 моль/л; р. ОН = 3; р. Н = 10 V(HCl) = 100, 1 мл, Н+ = 10 -3 моль/л; р. Н = 3 При 60 0 C Δр. Н =10 - 3 = 7 С ростом температуры, величина скачка титрования уменьшается. 29
 Расчет кривой титрования слабой кислоты сильным основанием 100 мл 0, 1 М СН 3 СООН + V мл 0, 1 М Na. OH; Vобщ = const (100 мл) 1) VNa. OH = 0 мл СН 3 СООН + Н 2 О =СН 3 СОО- +Н 3 О+ СН 3 СООН =СН 3 СОО- +Н+ Ca-x х х Ка = 1, 74 ∙ 10 -5 т. к. х << Сa, Сa-x ~ Ca х = [H+] = 1, 32 ∙ 10 -3 моль/л; р. Н = 2, 89 р. ОН = 11, 11 30
Расчет кривой титрования слабой кислоты сильным основанием 100 мл 0, 1 М СН 3 СООН + V мл 0, 1 М Na. OH; Vобщ = const (100 мл) 1) VNa. OH = 0 мл СН 3 СООН + Н 2 О =СН 3 СОО- +Н 3 О+ СН 3 СООН =СН 3 СОО- +Н+ Ca-x х х Ка = 1, 74 ∙ 10 -5 т. к. х << Сa, Сa-x ~ Ca х = [H+] = 1, 32 ∙ 10 -3 моль/л; р. Н = 2, 89 р. ОН = 11, 11 30
 0 < V(Na. OH) < 100 мл – буферная область СН 3 СООН = СН 3 СОО- + Н+ Ca-x Cs+x x 2) VNa. OH = 9, 0 мл Образовалось: СН 3 СОО- = Сs = Остаток: СН 3 СООН = Сa = р. Н = 3, 75 . 31
0 < V(Na. OH) < 100 мл – буферная область СН 3 СООН = СН 3 СОО- + Н+ Ca-x Cs+x x 2) VNa. OH = 9, 0 мл Образовалось: СН 3 СОО- = Сs = Остаток: СН 3 СООН = Сa = р. Н = 3, 75 . 31
 3) VNa. OH = 50, 0 мл Образовалось: СН 3 СОО- = СS = 0, 05 моль/л, Остаток: СН 3 СООН = СА = 0, 05 моль/л р. Н = 4, 76 р. ОН = 9, 24 4) VNa. OH = 90, 0 мл Образовалось: СН 3 СОО- = СS = 0, 09 моль/л, Остаток: СН 3 СООН = СА = 0, 01 моль/л р. Н = 5, 71 р. ОН = 8, 29 32
3) VNa. OH = 50, 0 мл Образовалось: СН 3 СОО- = СS = 0, 05 моль/л, Остаток: СН 3 СООН = СА = 0, 05 моль/л р. Н = 4, 76 р. ОН = 9, 24 4) VNa. OH = 90, 0 мл Образовалось: СН 3 СОО- = СS = 0, 09 моль/л, Остаток: СН 3 СООН = СА = 0, 01 моль/л р. Н = 5, 71 р. ОН = 8, 29 32
 5) VNa. OH = 99, 9 мл Образовалось: СН 3 СОО- = СS = 0, 0999 моль/л, Остаток: СН 3 СООН = СА = 0, 0001 моль/л р. Н = 7, 76 р. ОН = 6, 24 33
5) VNa. OH = 99, 9 мл Образовалось: СН 3 СОО- = СS = 0, 0999 моль/л, Остаток: СН 3 СООН = СА = 0, 0001 моль/л р. Н = 7, 76 р. ОН = 6, 24 33
 6) VNa. OH = 100 мл – эквивалентное количество Образовалось: СН 3 СОО- = СS = 0, 1 моль/л, Остаток: СН 3 СООН = СА = 0 моль/л СН 3 СОО- + Н 2 O = СН 3 СООН + ОН- Н+ = 10 -14/ (7, 6 ∙ 10 -6) = 1, 32 ∙ 10 -9 моль/л р. Н = 8, 88 р. ОН = 5, 12 34
6) VNa. OH = 100 мл – эквивалентное количество Образовалось: СН 3 СОО- = СS = 0, 1 моль/л, Остаток: СН 3 СООН = СА = 0 моль/л СН 3 СОО- + Н 2 O = СН 3 СООН + ОН- Н+ = 10 -14/ (7, 6 ∙ 10 -6) = 1, 32 ∙ 10 -9 моль/л р. Н = 8, 88 р. ОН = 5, 12 34
 7) VNa. OH = 100, 1 мл (избыток 0, 1 мл) OН- = 0, 1 ∙ 0, 1/100 = 1, 0 ∙ 10 -4 моль/л р. ОН = 4; р. Н = 10 35
7) VNa. OH = 100, 1 мл (избыток 0, 1 мл) OН- = 0, 1 ∙ 0, 1/100 = 1, 0 ∙ 10 -4 моль/л р. ОН = 4; р. Н = 10 35
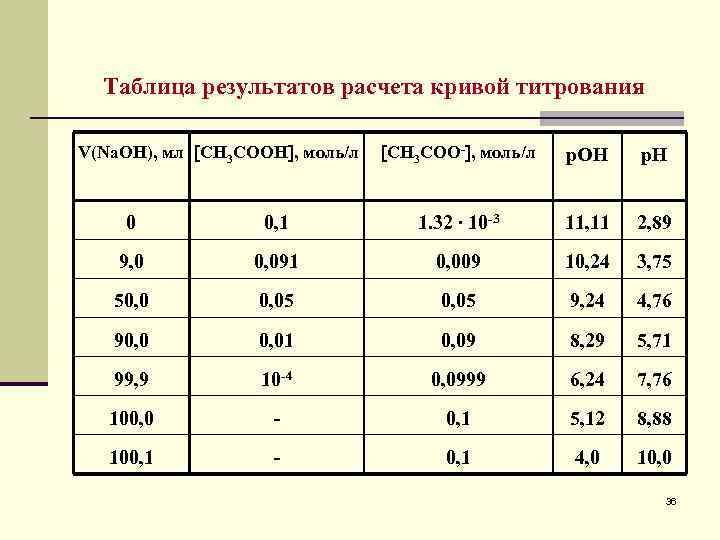 Таблица результатов расчета кривой титрования V(Na. ОН), мл СН 3 СООН , моль/л СН 3 СОО- , моль/л р. ОН р. Н 0 0, 1 1. 32 ∙ 10 -3 11, 11 2, 89 9, 0 0, 091 0, 009 10, 24 3, 75 50, 05 9, 24 4, 76 90, 01 0, 09 8, 29 5, 71 99, 9 10 -4 0, 0999 6, 24 7, 76 100, 0 - 0, 1 5, 12 8, 88 100, 1 - 0, 1 4, 0 10, 0 36
Таблица результатов расчета кривой титрования V(Na. ОН), мл СН 3 СООН , моль/л СН 3 СОО- , моль/л р. ОН р. Н 0 0, 1 1. 32 ∙ 10 -3 11, 11 2, 89 9, 0 0, 091 0, 009 10, 24 3, 75 50, 05 9, 24 4, 76 90, 01 0, 09 8, 29 5, 71 99, 9 10 -4 0, 0999 6, 24 7, 76 100, 0 - 0, 1 5, 12 8, 88 100, 1 - 0, 1 4, 0 10, 0 36
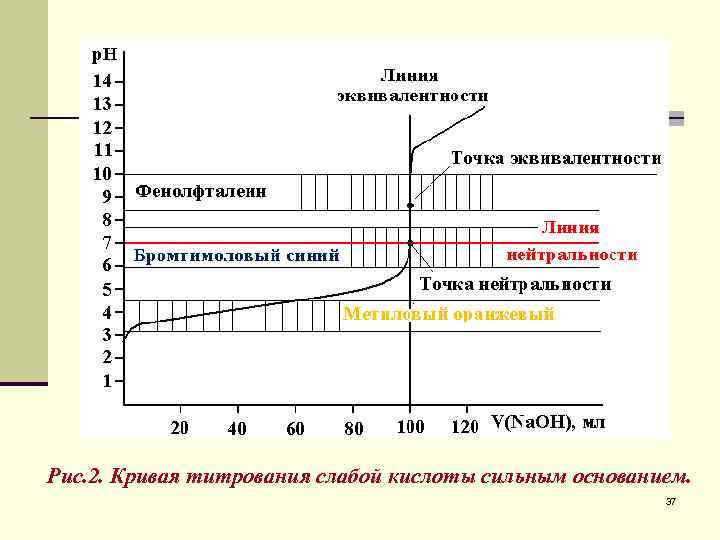 Рис. 2. Кривая титрования слабой кислоты сильным основанием. 37
Рис. 2. Кривая титрования слабой кислоты сильным основанием. 37
 Кривая титрования слабого основания сильной кислотой 0, 1 М NH 3 + 0, 1 М НCl, Кb = 1, 76 ∙ 10 -5; Ка = 5, 68∙ 10 -10; р. Н = 14 – р. Кb + lg ([NH 3] / [NH+4]) V(НCl), мл 0 50, 0 99, 9 100, 0 100, 1 остаток NН 3 , моль/л р. ОН р. Н 100, 0 50, 0 1, 0 0, 1 0 0 2, 9 4, 7 6, 7 7, 7 8, 9 10, 0 11, 1 9, 3 7, 3 6, 3 5, 1 4. 0 Точка эквивалентности находится в кислой области. 38
Кривая титрования слабого основания сильной кислотой 0, 1 М NH 3 + 0, 1 М НCl, Кb = 1, 76 ∙ 10 -5; Ка = 5, 68∙ 10 -10; р. Н = 14 – р. Кb + lg ([NH 3] / [NH+4]) V(НCl), мл 0 50, 0 99, 9 100, 0 100, 1 остаток NН 3 , моль/л р. ОН р. Н 100, 0 50, 0 1, 0 0, 1 0 0 2, 9 4, 7 6, 7 7, 7 8, 9 10, 0 11, 1 9, 3 7, 3 6, 3 5, 1 4. 0 Точка эквивалентности находится в кислой области. 38
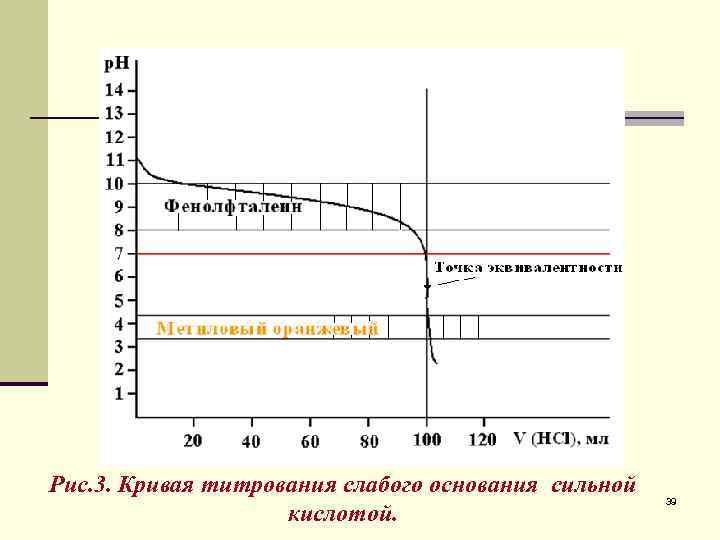 Рис. 3. Кривая титрования слабого основания сильной кислотой. 39
Рис. 3. Кривая титрования слабого основания сильной кислотой. 39
 Факторы, влияющие на величину скачка титрования: 1. Концентрация реагирующих веществ; 2. Температура (t°); 3. Природа реагирующих веществ (Kдисс). 40
Факторы, влияющие на величину скачка титрования: 1. Концентрация реагирующих веществ; 2. Температура (t°); 3. Природа реагирующих веществ (Kдисс). 40
 Титрование смеси двух кислот 1. Титрование смеси двух сильных кислот. Оттитровать отдельно одну сильную кислоту в присутствии другой сильной кислоты невозможно. Можно определить только общую кислотность (щелочность). 2. Титрование смеси сильной и слабой кислот (оснований). Оттитровать сильную кислоту в присутствии слабой с погрешностью в 1% можно, если Ka слабой кислоты ≤ 10 -5. HCl + CH 3 COOH; Kа = 1, 74 ∙ 10 -5 HCl + C 6 H 5 COOH; Kа = 6, 6 ∙ 10 -5 41
Титрование смеси двух кислот 1. Титрование смеси двух сильных кислот. Оттитровать отдельно одну сильную кислоту в присутствии другой сильной кислоты невозможно. Можно определить только общую кислотность (щелочность). 2. Титрование смеси сильной и слабой кислот (оснований). Оттитровать сильную кислоту в присутствии слабой с погрешностью в 1% можно, если Ka слабой кислоты ≤ 10 -5. HCl + CH 3 COOH; Kа = 1, 74 ∙ 10 -5 HCl + C 6 H 5 COOH; Kа = 6, 6 ∙ 10 -5 41
 3. Титрование смеси двух слабых кислот НХ; HУ титрант – щелочь. Предположим, что одну слабую кислоту в присутствии другой слабой кислоты можно оттитровать с точностью в 1%. НХ – оттитрована на 99% HУ – оттитрована на 1% 42
3. Титрование смеси двух слабых кислот НХ; HУ титрант – щелочь. Предположим, что одну слабую кислоту в присутствии другой слабой кислоты можно оттитровать с точностью в 1%. НХ – оттитрована на 99% HУ – оттитрована на 1% 42
 НХ = Н+ + Х- НУ = Н+ + У-
НХ = Н+ + Х- НУ = Н+ + У-
 Kнх ∙ 10 -2 = Kну ∙ 102 ; Т. о. Оттитровать одну слабую кислоту в присутствии другой слабой кислоты с точностью в 1% можно, если отношение величин Ka этих кислот отличается больше, чем на четыре порядка. 44
Kнх ∙ 10 -2 = Kну ∙ 102 ; Т. о. Оттитровать одну слабую кислоту в присутствии другой слабой кислоты с точностью в 1% можно, если отношение величин Ka этих кислот отличается больше, чем на четыре порядка. 44
![Выведем формулу для расчета р. Н в т. э. [H+]2 = Kнх ∙ Kну; Выведем формулу для расчета р. Н в т. э. [H+]2 = Kнх ∙ Kну;](https://present5.com/presentation/148288599_132358591/image-45.jpg) Выведем формулу для расчета р. Н в т. э. [H+]2 = Kнх ∙ Kну;
Выведем формулу для расчета р. Н в т. э. [H+]2 = Kнх ∙ Kну;
 Титрование многоосновных кислот 100 мл 0, 1 м Н 3 РО 4 + V мл 0, 1 м Na. OH Н 3 РО 4 Н+ + Н 2 РО-4 К 1 = 7, 58 ∙ 10 -3 р. К 1 = 2, 12 Н 2 РО-4 Н+ + НРО 2 -4 К 2 = 6, 16 ∙ 10 -8 р. К 2 = 7, 21 НРО 2 -4 Н+ + РО 3 -4 К 3 = 4, 26 ∙ 10 -13 р. К 3 = 12, 38 VNa. OH = 100 мл - I т. э. VNa. OH = 200 мл - II т. э VNa. OH = 300 мл III т. э В области третьей точки эквивалентности скачка не наблюдается, т. к. К 3 очень мала.
Титрование многоосновных кислот 100 мл 0, 1 м Н 3 РО 4 + V мл 0, 1 м Na. OH Н 3 РО 4 Н+ + Н 2 РО-4 К 1 = 7, 58 ∙ 10 -3 р. К 1 = 2, 12 Н 2 РО-4 Н+ + НРО 2 -4 К 2 = 6, 16 ∙ 10 -8 р. К 2 = 7, 21 НРО 2 -4 Н+ + РО 3 -4 К 3 = 4, 26 ∙ 10 -13 р. К 3 = 12, 38 VNa. OH = 100 мл - I т. э. VNa. OH = 200 мл - II т. э VNa. OH = 300 мл III т. э В области третьей точки эквивалентности скачка не наблюдается, т. к. К 3 очень мала.
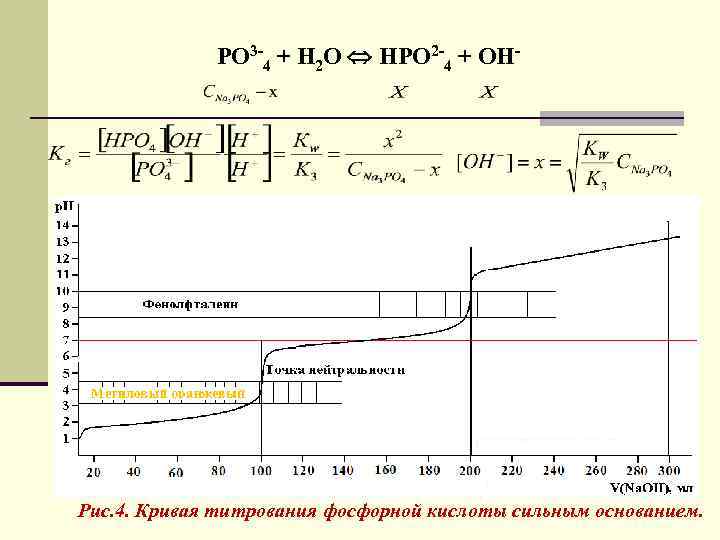 РО 3 -4 + Н 2 О НРО 2 -4 + ОН- Рис. 4. Кривая титрования фосфорной кислоты сильным основанием.
РО 3 -4 + Н 2 О НРО 2 -4 + ОН- Рис. 4. Кривая титрования фосфорной кислоты сильным основанием.
 Титрование солей многоосновных кислот 100 мл 0, 1 М Na 2 CO 3 + V мл 0, 1 М HCl 48
Титрование солей многоосновных кислот 100 мл 0, 1 М Na 2 CO 3 + V мл 0, 1 М HCl 48
 2) 0 V(HCl) 100 мл – 1 я буферная область. 3) V(HCl)=100 мл – 1 я точка эквивалентности. 49
2) 0 V(HCl) 100 мл – 1 я буферная область. 3) V(HCl)=100 мл – 1 я точка эквивалентности. 49
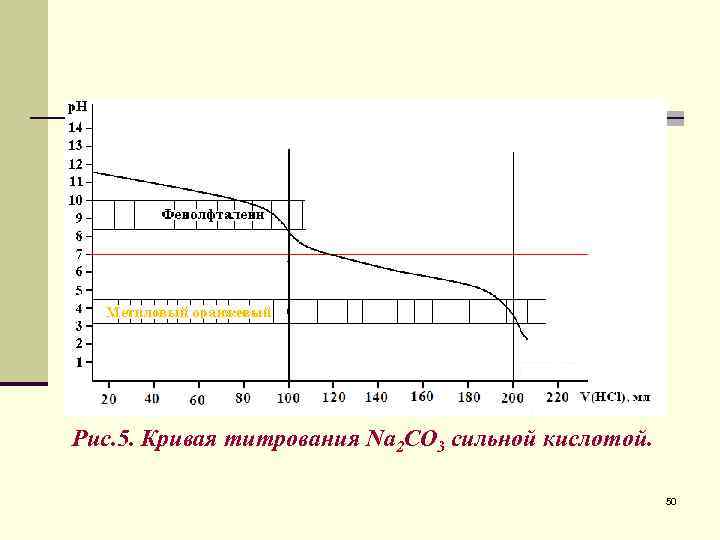 Рис. 5. Кривая титрования Na 2 CO 3 сильной кислотой. 50
Рис. 5. Кривая титрования Na 2 CO 3 сильной кислотой. 50
 Индикаторы кислотно-основного титрования Кислотно-основные индикаторы – это органические соединения сложной структуры, которые изменяют свою окраску в зависимости от р. Н раствора.
Индикаторы кислотно-основного титрования Кислотно-основные индикаторы – это органические соединения сложной структуры, которые изменяют свою окраску в зависимости от р. Н раствора.
 Ионная теория Hind H+ + Indкр желт Интервал p. H, при котором индикатор изменяет свою окраску, называется интервалом перехода индикатора.
Ионная теория Hind H+ + Indкр желт Интервал p. H, при котором индикатор изменяет свою окраску, называется интервалом перехода индикатора.
 Хромофорная теория В соответствии с этой теорией изменение цвета индикатора связано с существенным изменением его молекулярной структуры. Окраска соединений связана с наличием хромофорных групп: -NO 2 - , -N=N- т. д. , и ауксохромных групп, которые в присутствии хромофорных также влияют на окраску. Структурные изменения в растворах метилового оранжевого при изменении р. Н можно представить схемой: В воде, нейтральном и щелочном растворе метиловый оранжевый имеет желтую окраску (форма Ind-), при подкислении структура молекулы изменяется и индикатор приобретает красную окраску (форма HInd).
Хромофорная теория В соответствии с этой теорией изменение цвета индикатора связано с существенным изменением его молекулярной структуры. Окраска соединений связана с наличием хромофорных групп: -NO 2 - , -N=N- т. д. , и ауксохромных групп, которые в присутствии хромофорных также влияют на окраску. Структурные изменения в растворах метилового оранжевого при изменении р. Н можно представить схемой: В воде, нейтральном и щелочном растворе метиловый оранжевый имеет желтую окраску (форма Ind-), при подкислении структура молекулы изменяется и индикатор приобретает красную окраску (форма HInd).
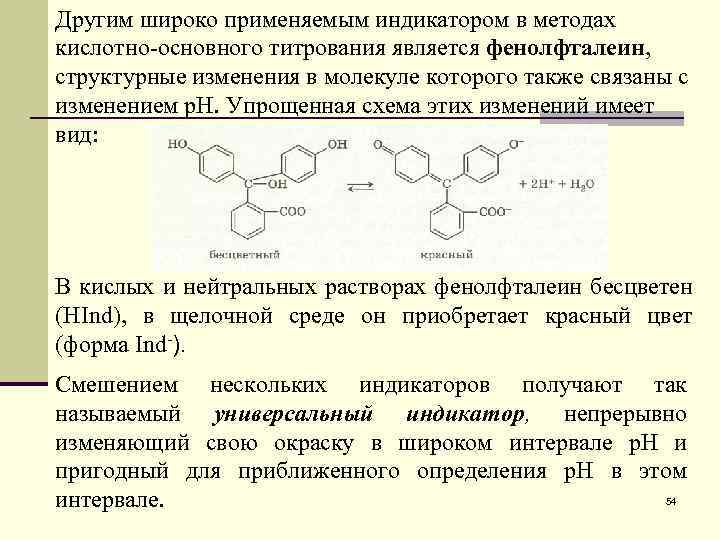 Другим широко применяемым индикатором в методах кислотно-основного титрования является фенолфталеин, структурные изменения в молекуле которого также связаны с изменением р. Н. Упрощенная схема этих изменений имеет вид: В кислых и нейтральных растворах фенолфталеин бесцветен (HInd), в щелочной среде он приобретает красный цвет (форма Ind-). Смешением нескольких индикаторов получают так называемый универсальный индикатор, непрерывно изменяющий свою окраску в широком интервале р. Н и пригодный для приближенного определения р. Н в этом 54 интервале.
Другим широко применяемым индикатором в методах кислотно-основного титрования является фенолфталеин, структурные изменения в молекуле которого также связаны с изменением р. Н. Упрощенная схема этих изменений имеет вид: В кислых и нейтральных растворах фенолфталеин бесцветен (HInd), в щелочной среде он приобретает красный цвет (форма Ind-). Смешением нескольких индикаторов получают так называемый универсальный индикатор, непрерывно изменяющий свою окраску в широком интервале р. Н и пригодный для приближенного определения р. Н в этом 54 интервале.
 Условия выбора индикатора 1. По кривой титрования. 2. По показателю титрования. Показатель титрования – это то значение р. Н, при котором заканчивают титрование с данным индикатором. Показатель титрова 6 ния должен находиться в пределах скачка титрования р. Т р. Н в т. э. 3. По индикаторной ошибке. 55
Условия выбора индикатора 1. По кривой титрования. 2. По показателю титрования. Показатель титрования – это то значение р. Н, при котором заканчивают титрование с данным индикатором. Показатель титрова 6 ния должен находиться в пределах скачка титрования р. Т р. Н в т. э. 3. По индикаторной ошибке. 55
 Индикаторные ошибки титрования Тип ошибки Причина ошибки Водородная Н+ -ошибка, Н+ Избыток ионов Н+ вследствие недотитрования сильной кислоты или перетитрования основания (сильного или слабого) сильной кислотой. ионов ОНвследствие Гидроксильная Избыток ОН- - ошибка, недотитрования сильного основания или перетитрования кислоты (сильной или ОНслабой) сильным основанием. V 1 – объем анализируемого раствора, взятый для титрования; V 2 – объем раствора в конце титрования; Сн – нормальная концентрация анализируемого раствора; р. К – показатель константы диссоциации слабого электролита; р. Т – показатель титрования индикатора.
Индикаторные ошибки титрования Тип ошибки Причина ошибки Водородная Н+ -ошибка, Н+ Избыток ионов Н+ вследствие недотитрования сильной кислоты или перетитрования основания (сильного или слабого) сильной кислотой. ионов ОНвследствие Гидроксильная Избыток ОН- - ошибка, недотитрования сильного основания или перетитрования кислоты (сильной или ОНслабой) сильным основанием. V 1 – объем анализируемого раствора, взятый для титрования; V 2 – объем раствора в конце титрования; Сн – нормальная концентрация анализируемого раствора; р. К – показатель константы диссоциации слабого электролита; р. Т – показатель титрования индикатора.
 Индикаторные ошибки титрования Кислотная НА – ошибка, НА Щелочная МОН-ошибка, МОН Избыток молекул НА слабой кислоты при её недотитровании Избыток молекул слабого основания МОН при его недотитровании V 1 – объем анализируемого раствора, взятый для титрования; V 2 – объем раствора в конце титрования; Сн – нормальная концентрация анализируемого раствора; р. К – показатель константы диссоциации слабого электролита; р. Т – показатель титрования индикатора.
Индикаторные ошибки титрования Кислотная НА – ошибка, НА Щелочная МОН-ошибка, МОН Избыток молекул НА слабой кислоты при её недотитровании Избыток молекул слабого основания МОН при его недотитровании V 1 – объем анализируемого раствора, взятый для титрования; V 2 – объем раствора в конце титрования; Сн – нормальная концентрация анализируемого раствора; р. К – показатель константы диссоциации слабого электролита; р. Т – показатель титрования индикатора.
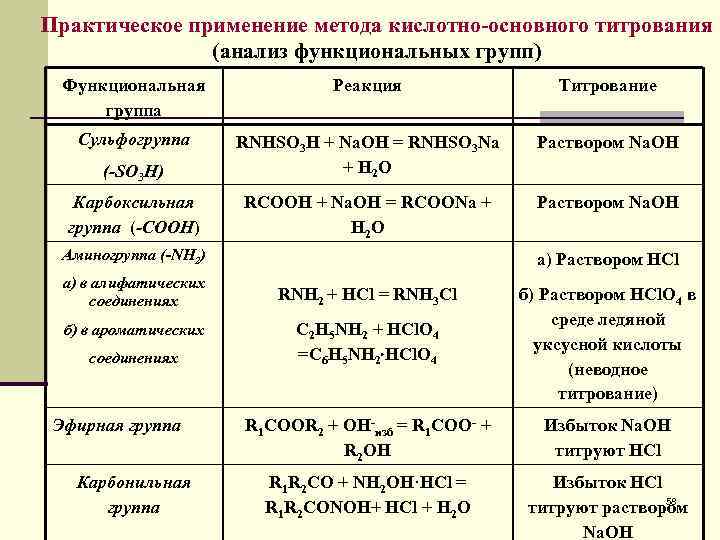 Практическое применение метода кислотно-основного титрования (анализ функциональных групп) Функциональная группа Реакция Титрование Сульфогруппа Раствором Na. OH (-SO 3 H) RNHSO 3 H + Na. OH = RNHSO 3 Na + H 2 O Карбоксильная группа (-COOH) RCOOH + Na. OH = RCOONa + H 2 O Раствором Na. OH Аминогруппа (-NH 2) а) в алифатических соединениях б) в ароматических соединениях Эфирная группа Карбонильная группа а) Раствором HCl RNH 2 + HCl = RNH 3 Cl С 2 H 5 NH 2 + HCl. O 4 =С 6 H 5 NH 2 HCl. O 4 б) Раствором HCl. O 4 в среде ледяной уксусной кислоты (неводное титрование) R 1 COOR 2 + OH-изб = R 1 COO- + R 2 OH Избыток Na. OH титруют НСl R 1 R 2 CO + NH 2 OH·HCl = R 1 R 2 CONOH+ HCl + H 2 O Избыток HCl 58 титруют раствором Na. OH
Практическое применение метода кислотно-основного титрования (анализ функциональных групп) Функциональная группа Реакция Титрование Сульфогруппа Раствором Na. OH (-SO 3 H) RNHSO 3 H + Na. OH = RNHSO 3 Na + H 2 O Карбоксильная группа (-COOH) RCOOH + Na. OH = RCOONa + H 2 O Раствором Na. OH Аминогруппа (-NH 2) а) в алифатических соединениях б) в ароматических соединениях Эфирная группа Карбонильная группа а) Раствором HCl RNH 2 + HCl = RNH 3 Cl С 2 H 5 NH 2 + HCl. O 4 =С 6 H 5 NH 2 HCl. O 4 б) Раствором HCl. O 4 в среде ледяной уксусной кислоты (неводное титрование) R 1 COOR 2 + OH-изб = R 1 COO- + R 2 OH Избыток Na. OH титруют НСl R 1 R 2 CO + NH 2 OH·HCl = R 1 R 2 CONOH+ HCl + H 2 O Избыток HCl 58 титруют раствором Na. OH
 II. Комплексометрическое титрование 1. Меркуриметрия Титрант – Hg(NO 3)2 Определяемые вещества – Cl-, Br-, SCN-, CNИндикаторы – нитропруссид натрия, дифенилкарбазид, дифенилкарбазон Hg 2+ + 2 Г- Hg. Г 2 - константа устойчивости Hg. Г 2 59
II. Комплексометрическое титрование 1. Меркуриметрия Титрант – Hg(NO 3)2 Определяемые вещества – Cl-, Br-, SCN-, CNИндикаторы – нитропруссид натрия, дифенилкарбазид, дифенилкарбазон Hg 2+ + 2 Г- Hg. Г 2 - константа устойчивости Hg. Г 2 59
 2. Комплексонометрия (хелатометрия) Основными титрантами являются комплексоны. Комплексонами называют группу аминополикарбоновых кислот. Простейшим комплексоном иминодиуксусная кислота: является Для целей количественного анализа наиболее часто в качестве титранта используется двухзамещенная натриевая соль этилендиаминтетраксусной кислоты – комплексон III (трилон Б, ЭДТА): 60
2. Комплексонометрия (хелатометрия) Основными титрантами являются комплексоны. Комплексонами называют группу аминополикарбоновых кислот. Простейшим комплексоном иминодиуксусная кислота: является Для целей количественного анализа наиболее часто в качестве титранта используется двухзамещенная натриевая соль этилендиаминтетраксусной кислоты – комплексон III (трилон Б, ЭДТА): 60
 Метод комплексонометрии основан на образовании прочных комплексных соединений ионов металлов с комплексоном III (комплексонатов металлов) в соотношении M: L = 1: 1 по схеме: M 2+ + H 2 Edta 2 - = MEdta 2 - + 2 H+ M 3+ + H 2 Edta 2 - = MEdta- + 2 H+
Метод комплексонометрии основан на образовании прочных комплексных соединений ионов металлов с комплексоном III (комплексонатов металлов) в соотношении M: L = 1: 1 по схеме: M 2+ + H 2 Edta 2 - = MEdta 2 - + 2 H+ M 3+ + H 2 Edta 2 - = MEdta- + 2 H+
 Условия комплексонометрического титрования 1. p. H 3 титровать нельзя, т. к. образуются менее прочные кислые комплексы. 2. p. H 10 титровать нельзя. М(ОН)2 3. Оптимальное значение p. H = 8 10 в среде аммонийного буфера (NH 3+NH 4 Cl) M 2+ + H 2 Y 2 - = MY 2 - + 2 H+; H 2 Y 2 - - комплексон; MY 2 - - комплексонат. 4. Аммиак кроме части буферного раствора является также дополнительным лигандом. M(NH 3)42+ + H 2 Y 2 - = MY 2 - + 2 NH 4+ + 2 NH 3 5. Маскировка мешающих ионов металлов с помощью солей органических кислот. 62
Условия комплексонометрического титрования 1. p. H 3 титровать нельзя, т. к. образуются менее прочные кислые комплексы. 2. p. H 10 титровать нельзя. М(ОН)2 3. Оптимальное значение p. H = 8 10 в среде аммонийного буфера (NH 3+NH 4 Cl) M 2+ + H 2 Y 2 - = MY 2 - + 2 H+; H 2 Y 2 - - комплексон; MY 2 - - комплексонат. 4. Аммиак кроме части буферного раствора является также дополнительным лигандом. M(NH 3)42+ + H 2 Y 2 - = MY 2 - + 2 NH 4+ + 2 NH 3 5. Маскировка мешающих ионов металлов с помощью солей органических кислот. 62
 Условная константа устойчивости Zn 2+ + L 4 - Zn. L 2 - - истинная константа устойчивости. При наличии дополнительных лигандов и ионов Н+ возможно наличие конкурирующих равновесий. - условная константа устойчивости Zn 2+ / и L 4 - / - условные концентрации. 63
Условная константа устойчивости Zn 2+ + L 4 - Zn. L 2 - - истинная константа устойчивости. При наличии дополнительных лигандов и ионов Н+ возможно наличие конкурирующих равновесий. - условная константа устойчивости Zn 2+ / и L 4 - / - условные концентрации. 63
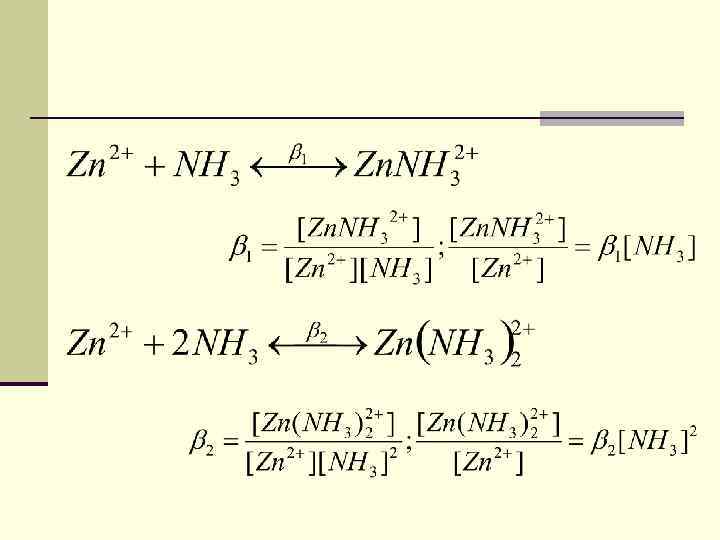
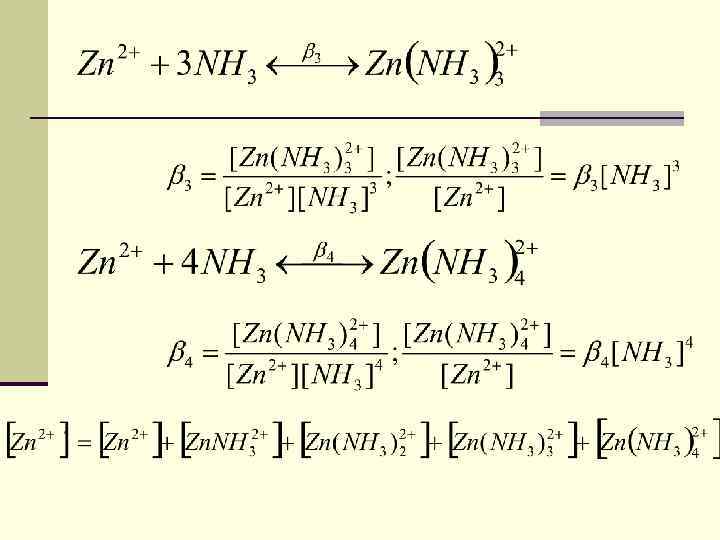
 - коэффициент побочных реакций для металла.
- коэффициент побочных реакций для металла.
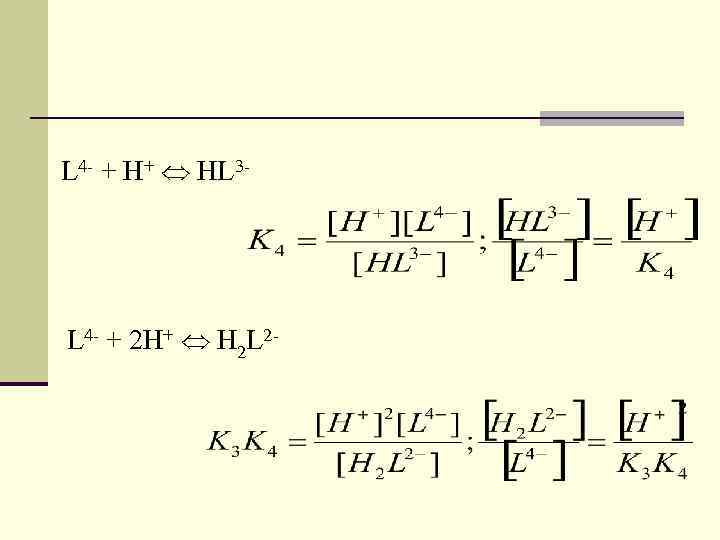 L 4 - + H+ HL 3 - L 4 - + 2 H+ H 2 L 2 -
L 4 - + H+ HL 3 - L 4 - + 2 H+ H 2 L 2 -
 L 4 - + 3 H+ H 3 L- L 4 - + 4 H+ H 4 L
L 4 - + 3 H+ H 3 L- L 4 - + 4 H+ H 4 L
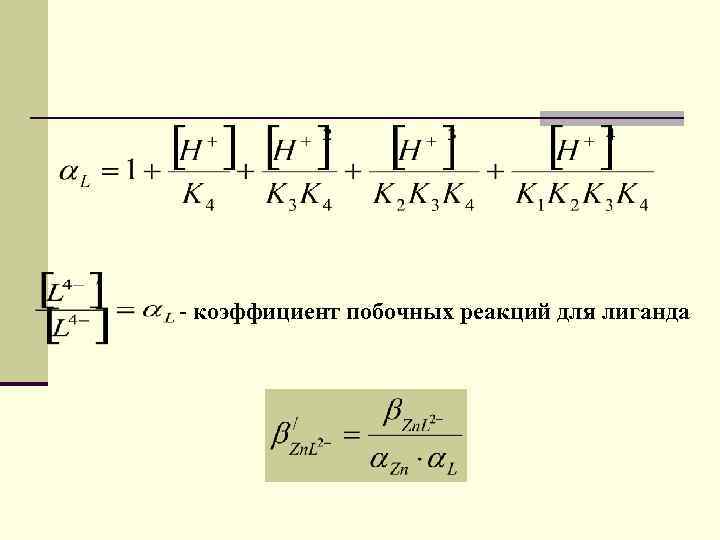 - коэффициент побочных реакций для лиганда
- коэффициент побочных реакций для лиганда
 Расчет скачка титрования 100 мл 0, 01 М Са 2+ + V мл 0, 01 М трилона Б. Са 2+ + Y 4 - =Ca. Y 2 -; 10 -5 -х х 0, 00999 -х 1) Vтр. Б = 99, 9 мл р. Са 2+ = 5 2) Vтр. Б = 100 мл – т. э. Са. Y 2 - =Ca 2+ + Y 40, 01 -х х = 5 10 -7 моль/л; р. Са = 6, 3 70
Расчет скачка титрования 100 мл 0, 01 М Са 2+ + V мл 0, 01 М трилона Б. Са 2+ + Y 4 - =Ca. Y 2 -; 10 -5 -х х 0, 00999 -х 1) Vтр. Б = 99, 9 мл р. Са 2+ = 5 2) Vтр. Б = 100 мл – т. э. Са. Y 2 - =Ca 2+ + Y 40, 01 -х х = 5 10 -7 моль/л; р. Са = 6, 3 70
 3) Vтр. Б = 100, 1 мл Са. Y 2 - =Ca 2+ + Y 40, 01 -х х х+10 -5 х = 2, 5 10 -8 моль/л; р. Са = 7, 7 Кривую титрования строят в координатах р. Са – Vтитранта. 71
3) Vтр. Б = 100, 1 мл Са. Y 2 - =Ca 2+ + Y 40, 01 -х х х+10 -5 х = 2, 5 10 -8 моль/л; р. Са = 7, 7 Кривую титрования строят в координатах р. Са – Vтитранта. 71
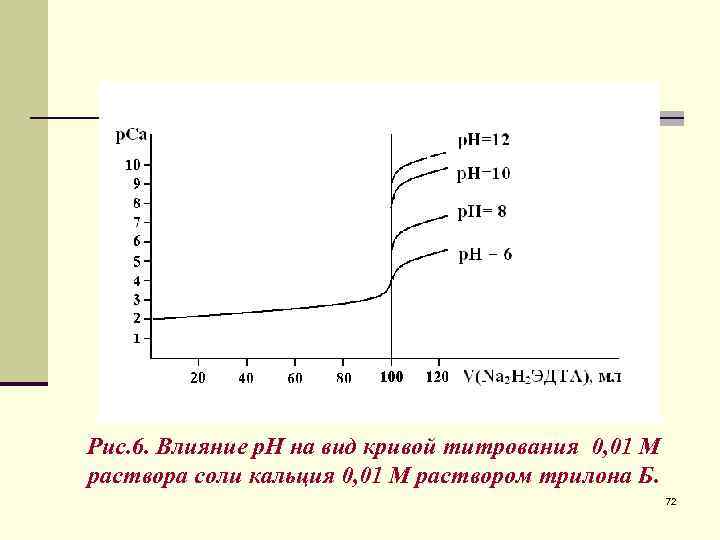 Рис. 6. Влияние р. Н на вид кривой титрования 0, 01 М раствора соли кальция 0, 01 М раствором трилона Б. 72
Рис. 6. Влияние р. Н на вид кривой титрования 0, 01 М раствора соли кальция 0, 01 М раствором трилона Б. 72
 Металлохромные индикаторы Применяются в методе комплексонометрии, представляют собой слабые органические кислоты, которые образуют окрашенные комплексы с металлами, устойчивость которых ниже, чем устойчивость соответствующих комплексонатов (мурексид, эриохром черный Т, ксиленовый оранжевый и др. ). Эриохром черный Т (Н 3 Ind): р. Н 6 р. Н = 8 10 красн голуб р. Н 11 оранж Zn 2+ + NH 3 + HInd 2 - = Zn. Ind- (кр-фиол) + NH 4+ Zn. Ind- + NH 3 + H 2 Y 2 - = Zn. Y 2 - + NH 4+ + HInd 2 -(голуб) При выборе индикатора необходимо учитывать правило: 73
Металлохромные индикаторы Применяются в методе комплексонометрии, представляют собой слабые органические кислоты, которые образуют окрашенные комплексы с металлами, устойчивость которых ниже, чем устойчивость соответствующих комплексонатов (мурексид, эриохром черный Т, ксиленовый оранжевый и др. ). Эриохром черный Т (Н 3 Ind): р. Н 6 р. Н = 8 10 красн голуб р. Н 11 оранж Zn 2+ + NH 3 + HInd 2 - = Zn. Ind- (кр-фиол) + NH 4+ Zn. Ind- + NH 3 + H 2 Y 2 - = Zn. Y 2 - + NH 4+ + HInd 2 -(голуб) При выборе индикатора необходимо учитывать правило: 73
 Применение метода комплексонометрии 1. Прямое титрование Zn 2+ ; Ca 2+ ; Ni 2+ ; Co 2+ ; Cd 2+ ; Mg 2+ и др. с аммонийным буфером и эриохромом черным Т. Fe 3+ ; Zr 4+ - в кислой среде с ксиленовым оранжевым. Прямое титрование использовать нельзя, если: а) возможно образование гидроксидов металлов. б) реакция медленно. комплексообразования протекает в) нет подходящего металлохромного индикатора. г) возможно блокирование индикатора. 74
Применение метода комплексонометрии 1. Прямое титрование Zn 2+ ; Ca 2+ ; Ni 2+ ; Co 2+ ; Cd 2+ ; Mg 2+ и др. с аммонийным буфером и эриохромом черным Т. Fe 3+ ; Zr 4+ - в кислой среде с ксиленовым оранжевым. Прямое титрование использовать нельзя, если: а) возможно образование гидроксидов металлов. б) реакция медленно. комплексообразования протекает в) нет подходящего металлохромного индикатора. г) возможно блокирование индикатора. 74
 2. Косвенное титрование а) обратное титрование M 2+ + H 2 Y 2 -(изб. )=MY 2 -+ 2 H+ + (H 2 Y 2 -(ост. )) H 2 Y 2 -(ост. )+ Zn 2+=Zn. Y 2 -+ 2 H+ n(M 2+) = n(H 2 Y 2 -) – n(Zn 2+) Определяют: Hg 2+, Al 3+; Cr 3+ и др. б) титрование по замещению M 2+ + Mg. Y 2 - = MY 2 - + Mg 2+ + H 2 Y 2 - = Mg. Y 2 - + 2 H+ n(M 2+) = n(Mg 2+) = n(H 2 Y 2 -) Определяют: Hg 2+, Th 4+; Cu 2+ и др.
2. Косвенное титрование а) обратное титрование M 2+ + H 2 Y 2 -(изб. )=MY 2 -+ 2 H+ + (H 2 Y 2 -(ост. )) H 2 Y 2 -(ост. )+ Zn 2+=Zn. Y 2 -+ 2 H+ n(M 2+) = n(H 2 Y 2 -) – n(Zn 2+) Определяют: Hg 2+, Al 3+; Cr 3+ и др. б) титрование по замещению M 2+ + Mg. Y 2 - = MY 2 - + Mg 2+ + H 2 Y 2 - = Mg. Y 2 - + 2 H+ n(M 2+) = n(Mg 2+) = n(H 2 Y 2 -) Определяют: Hg 2+, Th 4+; Cu 2+ и др.
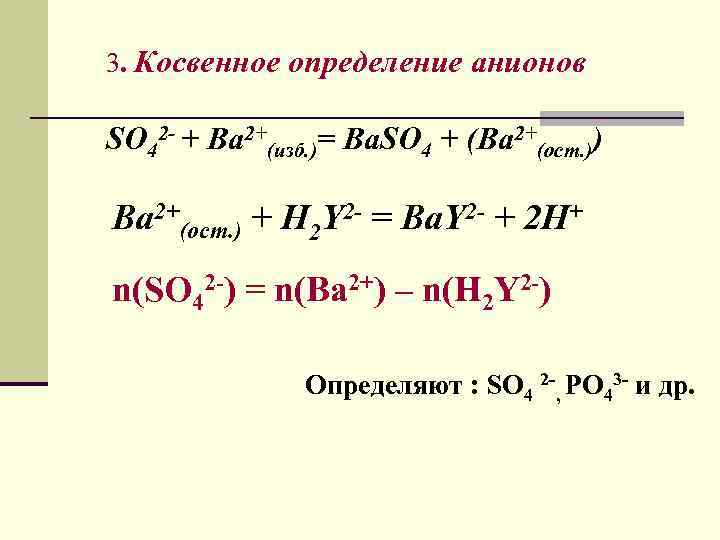 3. Косвенное определение анионов SO 42 - + Ba 2+(изб. )= Ba. SO 4 + (Ba 2+(ост. )) Ba 2+(ост. ) + H 2 Y 2 - = Ba. Y 2 - + 2 H+ n(SO 42 -) = n(Ba 2+) – n(H 2 Y 2 -) Определяют : SO 4 2 -, PO 43 - и др.
3. Косвенное определение анионов SO 42 - + Ba 2+(изб. )= Ba. SO 4 + (Ba 2+(ост. )) Ba 2+(ост. ) + H 2 Y 2 - = Ba. Y 2 - + 2 H+ n(SO 42 -) = n(Ba 2+) – n(H 2 Y 2 -) Определяют : SO 4 2 -, PO 43 - и др.
 III. Осадительное титрование Требования к реакциям осаждения: 1. Малая растворимость осадка. 2. Высокая скорость образования осадков. 3. Явление адсорбции и окклюзии должно быть минимальным. 4. Возможность фиксирования точки эквивалентности. 77
III. Осадительное титрование Требования к реакциям осаждения: 1. Малая растворимость осадка. 2. Высокая скорость образования осадков. 3. Явление адсорбции и окклюзии должно быть минимальным. 4. Возможность фиксирования точки эквивалентности. 77
![Аргентометрия Титрант – Ag. NO 3. Ag+ + X- = Ag. X ПРAg. X=[Ag+][X-]; Аргентометрия Титрант – Ag. NO 3. Ag+ + X- = Ag. X ПРAg. X=[Ag+][X-];](https://present5.com/presentation/148288599_132358591/image-78.jpg) Аргентометрия Титрант – Ag. NO 3. Ag+ + X- = Ag. X ПРAg. X=[Ag+][X-]; Определяемые ионы - X = Cl-, Br-, I-, SCN-. 1. Безиндикаторные методы. Метод равного помутнения (Гей-Люссака). 2. Метод Мора (индикатор K 2 Cr. O 4). Ag+ + Cl- = Ag. Cl Индикаторная реакция: Cr. O 42 - + 2 Ag+ = Ag 2 Cr. O 4 Условия: р. Н 6, 5 10 р. Н 6, 5 Cr. O 42 - + Н+ = НCr. O 4 р. Н 10 Ag 2 O (черный осадок) кирпично-красный осадок 78
Аргентометрия Титрант – Ag. NO 3. Ag+ + X- = Ag. X ПРAg. X=[Ag+][X-]; Определяемые ионы - X = Cl-, Br-, I-, SCN-. 1. Безиндикаторные методы. Метод равного помутнения (Гей-Люссака). 2. Метод Мора (индикатор K 2 Cr. O 4). Ag+ + Cl- = Ag. Cl Индикаторная реакция: Cr. O 42 - + 2 Ag+ = Ag 2 Cr. O 4 Условия: р. Н 6, 5 10 р. Н 6, 5 Cr. O 42 - + Н+ = НCr. O 4 р. Н 10 Ag 2 O (черный осадок) кирпично-красный осадок 78
 3. Метод Фольгарда (тиоционатометрия) Индикатор - Обратное титрование (рабочие растворы-Ag. NO 3, КSCN или NH 4 SCN): Cl- + Ag+(изб) Ag. Cl + Ag+(ост) + SCN- Ag. SCN Индикаторная реакция: Fe 3+ + n. SCN-(изб) = n (Cl-)= n (Ag+) -n (SCN-) 79
3. Метод Фольгарда (тиоционатометрия) Индикатор - Обратное титрование (рабочие растворы-Ag. NO 3, КSCN или NH 4 SCN): Cl- + Ag+(изб) Ag. Cl + Ag+(ост) + SCN- Ag. SCN Индикаторная реакция: Fe 3+ + n. SCN-(изб) = n (Cl-)= n (Ag+) -n (SCN-) 79
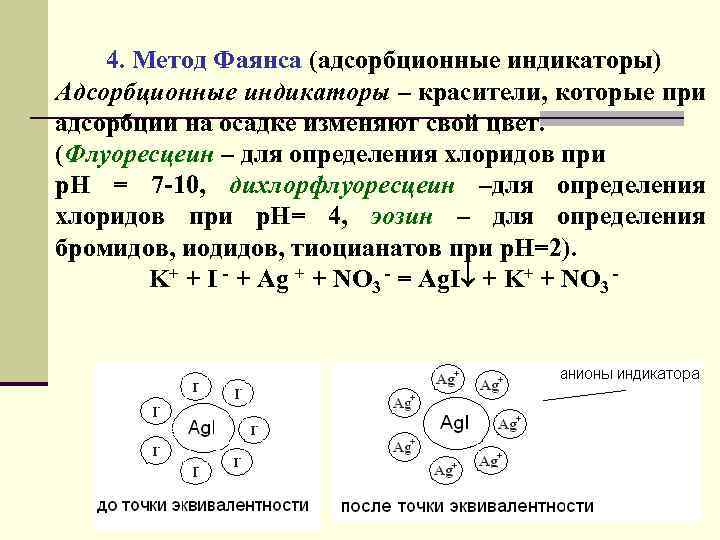 4. Метод Фаянса (адсорбционные индикаторы) Адсорбционные индикаторы – красители, которые при адсорбции на осадке изменяют свой цвет. (Флуоресцеин – для определения хлоридов при р. Н = 7 -10, дихлорфлуоресцеин –для определения хлоридов при р. Н= 4, эозин – для определения бромидов, иодидов, тиоцианатов при р. Н=2). K+ + I - + Ag + + NO 3 - = Ag. I + K+ + NO 3 - 80
4. Метод Фаянса (адсорбционные индикаторы) Адсорбционные индикаторы – красители, которые при адсорбции на осадке изменяют свой цвет. (Флуоресцеин – для определения хлоридов при р. Н = 7 -10, дихлорфлуоресцеин –для определения хлоридов при р. Н= 4, эозин – для определения бромидов, иодидов, тиоцианатов при р. Н=2). K+ + I - + Ag + + NO 3 - = Ag. I + K+ + NO 3 - 80
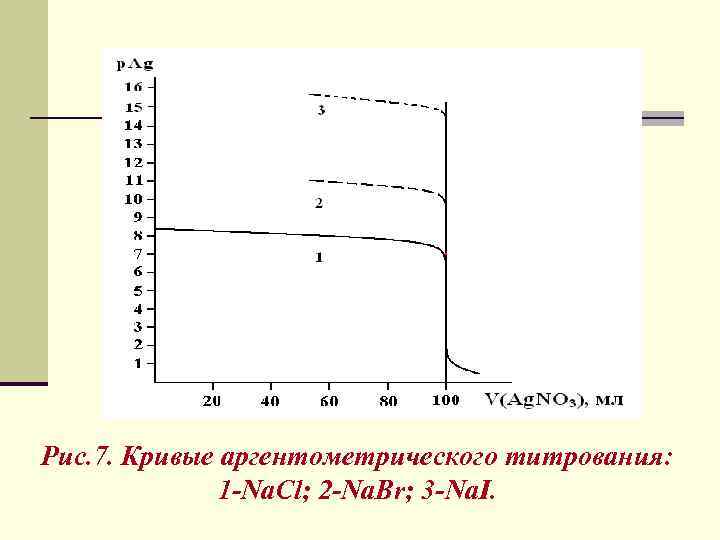 Рис. 7. Кривые аргентометрического титрования: 1 -Na. Cl; 2 -Na. Br; 3 -Na. I.
Рис. 7. Кривые аргентометрического титрования: 1 -Na. Cl; 2 -Na. Br; 3 -Na. I.
 Факторы, влияющие на величину скачка титрования в методах осаждения 1. Концентрация реагентов. 2. Температура. 3. Произведение растворимости (ПР). 4. Ионная сила раствора (I). 82
Факторы, влияющие на величину скачка титрования в методах осаждения 1. Концентрация реагентов. 2. Температура. 3. Произведение растворимости (ПР). 4. Ионная сила раствора (I). 82
 Меркурометрия Рабочий раствор – Hg 2(NO 3)2 Hg 22+ + 2 X- = Hg 2 X 2 ; X= Cl -, Br -, SCN -; ПР=[Hg 22+][X-]2 1. Индикатор – Fe. SCN 2+ 2 Fe. SCN 2+ + Hg 22+ = Hg 2(SCN)2 + 2 Fe 3+ ; Fe. SCN 2+- кроваво-красный, Hg 2(SCN)2 – белый. 2. Индикатор дифенилкарбазон – адсорбционный индикатор, который окрашивает суспензию Hg 2 Cl 2 в сине-фиолетовый цвет. 83
Меркурометрия Рабочий раствор – Hg 2(NO 3)2 Hg 22+ + 2 X- = Hg 2 X 2 ; X= Cl -, Br -, SCN -; ПР=[Hg 22+][X-]2 1. Индикатор – Fe. SCN 2+ 2 Fe. SCN 2+ + Hg 22+ = Hg 2(SCN)2 + 2 Fe 3+ ; Fe. SCN 2+- кроваво-красный, Hg 2(SCN)2 – белый. 2. Индикатор дифенилкарбазон – адсорбционный индикатор, который окрашивает суспензию Hg 2 Cl 2 в сине-фиолетовый цвет. 83
 IV. Окислительно-восстановительное титрование Фактор эквивалентности – доля условной или реальной частицы, которая соответствует 1 электрону в окислительно-восстановительной реакции. fэкв(Fe 2+) = 1 В реакциях окисления-восстановления существует 2 редокс-пары. Окислительно-восстановительная система характеризуется окислительно-восстановительным потенциалом. 84
IV. Окислительно-восстановительное титрование Фактор эквивалентности – доля условной или реальной частицы, которая соответствует 1 электрону в окислительно-восстановительной реакции. fэкв(Fe 2+) = 1 В реакциях окисления-восстановления существует 2 редокс-пары. Окислительно-восстановительная система характеризуется окислительно-восстановительным потенциалом. 84
 Уравнение Нернста
Уравнение Нернста
 Величина Е зависит от следующих факторов: 1. t ; 2. Концентрация; 3. Величина р. Н; 4. От реакций протекающих совместно:
Величина Е зависит от следующих факторов: 1. t ; 2. Концентрация; 3. Величина р. Н; 4. От реакций протекающих совместно:
 а) образование труднорастворимых соединений: Cu 2+ + e → Cu+ 2 Cu 2+ + 4 I- = 2 Cu. I + I 2
а) образование труднорастворимых соединений: Cu 2+ + e → Cu+ 2 Cu 2+ + 4 I- = 2 Cu. I + I 2
 б) реакции комплексообразования: 88
б) реакции комплексообразования: 88
 Константа равновесия окислительновосстановительных реакций Кр – константа равновесия реакции; Eox 0 - стандартный потенциал пары окислителя; Ered 0 - стандартный потенциал пары восстановителя; m – наименьшее общее кратное из числа принятых и отданных электронов. 89
Константа равновесия окислительновосстановительных реакций Кр – константа равновесия реакции; Eox 0 - стандартный потенциал пары окислителя; Ered 0 - стандартный потенциал пары восстановителя; m – наименьшее общее кратное из числа принятых и отданных электронов. 89
 Расчет скачка титрования 100 мл 0, 1 М Fe. Cl 2 + V мл 0, 1 н KMn. O 4; Н+ = 1 моль/л, р. Н=0 и [H+]=0, 1 моль/л, р. Н=1 0, 1 н КMn. O 4 = 0, 02 М КMn. O 4
Расчет скачка титрования 100 мл 0, 1 М Fe. Cl 2 + V мл 0, 1 н KMn. O 4; Н+ = 1 моль/л, р. Н=0 и [H+]=0, 1 моль/л, р. Н=1 0, 1 н КMn. O 4 = 0, 02 М КMn. O 4
 1) V(KMn. O 4) = 99, 9 мл 91
1) V(KMn. O 4) = 99, 9 мл 91
 2) V(KMn. O 4) = 100 мл - точка эквивалентности, а) Н+ = 1 моль/л, р. Н =0 а, в – число принятых и отданных электронов. б) Н+ = 0, 1 моль/л, р. Н=1 Кр = 1062, 7 = 5 1062
2) V(KMn. O 4) = 100 мл - точка эквивалентности, а) Н+ = 1 моль/л, р. Н =0 а, в – число принятых и отданных электронов. б) Н+ = 0, 1 моль/л, р. Н=1 Кр = 1062, 7 = 5 1062
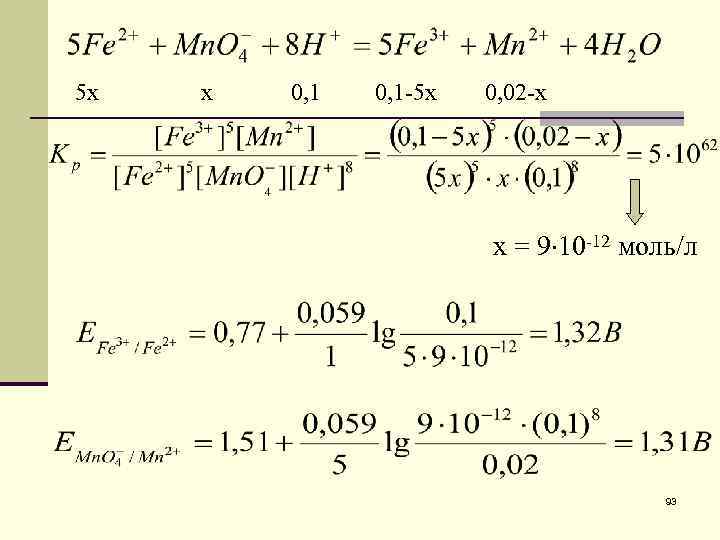 5 х х 0, 1 -5 х 0, 02 -х х = 9 10 -12 моль/л 93
5 х х 0, 1 -5 х 0, 02 -х х = 9 10 -12 моль/л 93
 3) V(KMn. O 4) = 100, 1 мл а) Н+ = 1 моль/л б) Н+ = 0, 1 моль/л Величина скачка титрования зависит от р. Н. Кривую титрования строят в координатах Е – Vтитранта. 94
3) V(KMn. O 4) = 100, 1 мл а) Н+ = 1 моль/л б) Н+ = 0, 1 моль/л Величина скачка титрования зависит от р. Н. Кривую титрования строят в координатах Е – Vтитранта. 94
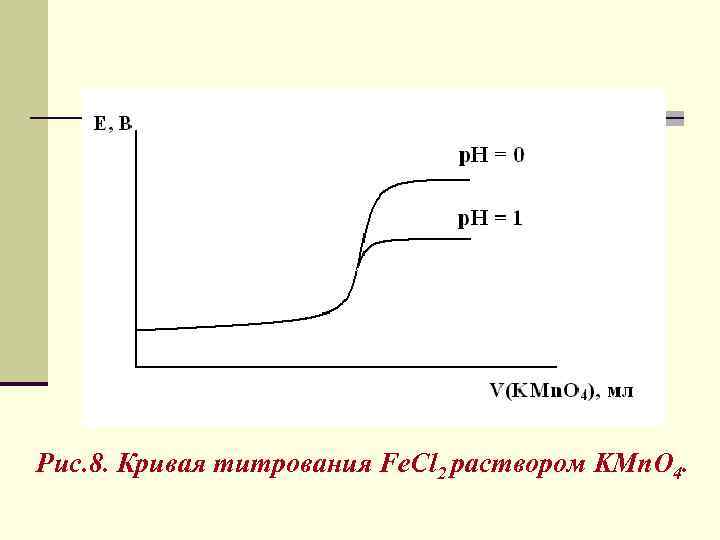 Рис. 8. Кривая титрования Fe. Cl 2 раствором KMn. O 4.
Рис. 8. Кривая титрования Fe. Cl 2 раствором KMn. O 4.
 Методы окислительно-восстановительного титрования • Перманганатометрия KMn. O 4 (безиндикаторный); • Иодометрия I 2 , Na 2 S 2 O 3 (индикатор - крахмал); • Хроматометрия K 2 Cr 2 O 7 (индикатор - дифениламин); • Броматометрия KBr. O 3 (индикаторы метиловый оранжевый, метиловый красный). 96
Методы окислительно-восстановительного титрования • Перманганатометрия KMn. O 4 (безиндикаторный); • Иодометрия I 2 , Na 2 S 2 O 3 (индикатор - крахмал); • Хроматометрия K 2 Cr 2 O 7 (индикатор - дифениламин); • Броматометрия KBr. O 3 (индикаторы метиловый оранжевый, метиловый красный). 96
 Гравиметрический анализ Гравиметрический метод анализа основан на измерении массы вещества, полученного в результате химической реакции. а) Метод отгонки. Состоит в переводе одного из компонентов в летучее соединение и его последующем удалении б) Метод осаждения. Состоит в выделении определяемого вещества в осадок в виде малорастворимого соединения. 97
Гравиметрический анализ Гравиметрический метод анализа основан на измерении массы вещества, полученного в результате химической реакции. а) Метод отгонки. Состоит в переводе одного из компонентов в летучее соединение и его последующем удалении б) Метод осаждения. Состоит в выделении определяемого вещества в осадок в виде малорастворимого соединения. 97
 Соединение, в виде которого определяемый компонент осаждают из анализируемого раствора, называют формой осаждения, которая должна отвечать требованиям: 1. Полнота осаждения. 2. Легкая фильтруемость. 3. Чистота осадка. 98
Соединение, в виде которого определяемый компонент осаждают из анализируемого раствора, называют формой осаждения, которая должна отвечать требованиям: 1. Полнота осаждения. 2. Легкая фильтруемость. 3. Чистота осадка. 98
 Соединение, в виде которого определяемое вещество взвешивают, называют гравиметрической формой. Требования к гравиметрической форме: 1. Состав гравиметрической формы должен соответствовать химической формуле. 2. Гравиметрическая форма должна иметь большую молекулярную массу для определения меньшего количества вещества с большей точностью. 3. Гравиметрическая форма должна быть устойчива и не должна взаимодействовать с окружающей средой.
Соединение, в виде которого определяемое вещество взвешивают, называют гравиметрической формой. Требования к гравиметрической форме: 1. Состав гравиметрической формы должен соответствовать химической формуле. 2. Гравиметрическая форма должна иметь большую молекулярную массу для определения меньшего количества вещества с большей точностью. 3. Гравиметрическая форма должна быть устойчива и не должна взаимодействовать с окружающей средой.
 Условия аналитического осаждения кристаллических осадков Размер частиц кристаллического осадка связан с величиной относительного пересыщения (О. П. ) раствора в процессе осаждения, которая определяется по формуле: Чем меньше величина О. П. , тем больше размер кристаллов.
Условия аналитического осаждения кристаллических осадков Размер частиц кристаллического осадка связан с величиной относительного пересыщения (О. П. ) раствора в процессе осаждения, которая определяется по формуле: Чем меньше величина О. П. , тем больше размер кристаллов.
 Основной причиной, вызывающей загрязнение осадков, является соосаждение – выпадение в осадок вместе с определяемым веществом примесей, для которых в условиях осаждения произведение растворимости не достигнуто. Соосаждение примесей на поверхности осадка называют адсорбцией. Соосаждение, при котором примеси или маточный раствор захватываются внутрь кристалла, называют окклюзией.
Основной причиной, вызывающей загрязнение осадков, является соосаждение – выпадение в осадок вместе с определяемым веществом примесей, для которых в условиях осаждения произведение растворимости не достигнуто. Соосаждение примесей на поверхности осадка называют адсорбцией. Соосаждение, при котором примеси или маточный раствор захватываются внутрь кристалла, называют окклюзией.
 Кристаллические осадки осаждают медленно из горячих, разбавленных растворов разбавленным раствором осадителя при интенсивном перемешивании в присутствии солей аммония. Аморфные осадки осаждают быстро из горячих, концентрированных растворов в присутствии солей аммония с последующим разбавлением. Горячие растворы сразу фильтруют.
Кристаллические осадки осаждают медленно из горячих, разбавленных растворов разбавленным раствором осадителя при интенсивном перемешивании в присутствии солей аммония. Аморфные осадки осаждают быстро из горячих, концентрированных растворов в присутствии солей аммония с последующим разбавлением. Горячие растворы сразу фильтруют.
 Определение сульфата гравиметрическая форма и форма осаждения F – фактор перерасчета Погрешность метода не более 0, 5%, масса определяемого вещества 0, 01 1, 00 гр. , при процентном отношении не менее 0, 1%. 103
Определение сульфата гравиметрическая форма и форма осаждения F – фактор перерасчета Погрешность метода не более 0, 5%, масса определяемого вещества 0, 01 1, 00 гр. , при процентном отношении не менее 0, 1%. 103


