IM-lektsia_1.pptx
- Количество слайдов: 71
 Аналитическая химия II. Инструментальные методы анализа Майстренко В. Н. Башкирский государственный университет Кафедра аналитической химии V_maystrenko@mail. ru Тел: 229 -97 -12
Аналитическая химия II. Инструментальные методы анализа Майстренко В. Н. Башкирский государственный университет Кафедра аналитической химии V_maystrenko@mail. ru Тел: 229 -97 -12
 Аналитическая химия – наука об определении химического состава веществ и отчасти их химического строения Химические методы анализа Физико-химические методы анализа Физические методы анализа Инструментальные методы анализа
Аналитическая химия – наука об определении химического состава веществ и отчасти их химического строения Химические методы анализа Физико-химические методы анализа Физические методы анализа Инструментальные методы анализа
 Инструментальные методы анализа — методы аналитической химии, для выполнения которых требуется электрохимическая, оптическая, радио-химическая и иная аппаратура. К инструментальным методам анализа относятся: электрохимические методы - потенциометрия (ионометрия), кулонометрия, вольтамперометрия, кондуктометрия и др. ; методы, основанные на испускании или погло-щении электромагнитного излучения – эмиссионная, абсорбционная, флуоресцентная атомная и молеку-лярная спектроскопия, фотометрические методы, рентгеноспектральный анализ и др. ; масс-спектральный анализ; ЯМР, ЭПР, методы, основанные на измерении радиоактивности и др.
Инструментальные методы анализа — методы аналитической химии, для выполнения которых требуется электрохимическая, оптическая, радио-химическая и иная аппаратура. К инструментальным методам анализа относятся: электрохимические методы - потенциометрия (ионометрия), кулонометрия, вольтамперометрия, кондуктометрия и др. ; методы, основанные на испускании или погло-щении электромагнитного излучения – эмиссионная, абсорбционная, флуоресцентная атомная и молеку-лярная спектроскопия, фотометрические методы, рентгеноспектральный анализ и др. ; масс-спектральный анализ; ЯМР, ЭПР, методы, основанные на измерении радиоактивности и др.
 Рекомендуемые учебники
Рекомендуемые учебники
 Дефиниция y = f(x) х y • Аналитический сигнал Сигнал, содержащий количественную информацию о величине, функционально связанной с содержанием определяемого компонента, и регистрируемый в ходе анализа вещества или материала "Контроль объекта аналитический. Термины и определения. " ГОСТ Р 52361– 2005.
Дефиниция y = f(x) х y • Аналитический сигнал Сигнал, содержащий количественную информацию о величине, функционально связанной с содержанием определяемого компонента, и регистрируемый в ходе анализа вещества или материала "Контроль объекта аналитический. Термины и определения. " ГОСТ Р 52361– 2005.
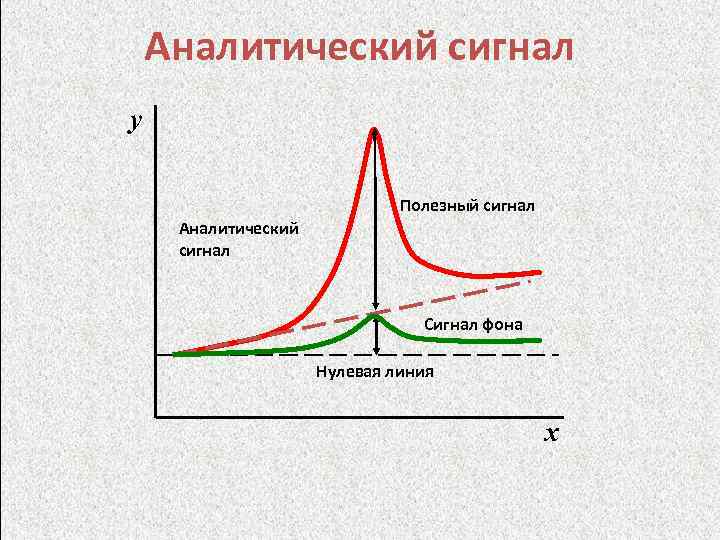 Аналитический сигнал y Полезный сигнал Аналитический сигнал Сигнал фона Нулевая линия x
Аналитический сигнал y Полезный сигнал Аналитический сигнал Сигнал фона Нулевая линия x
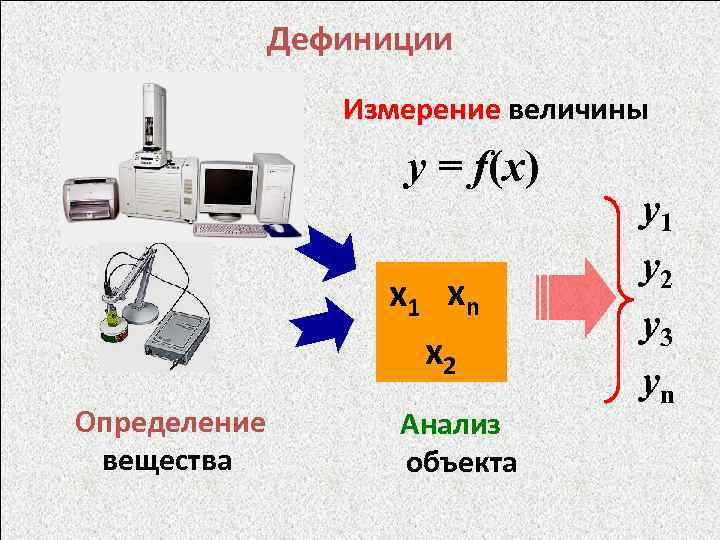 Дефиниции Измерение величины y = f(x) х1 хn х2 Определение вещества Анализ объекта y 1 y 2 y 3 yn
Дефиниции Измерение величины y = f(x) х1 хn х2 Определение вещества Анализ объекта y 1 y 2 y 3 yn
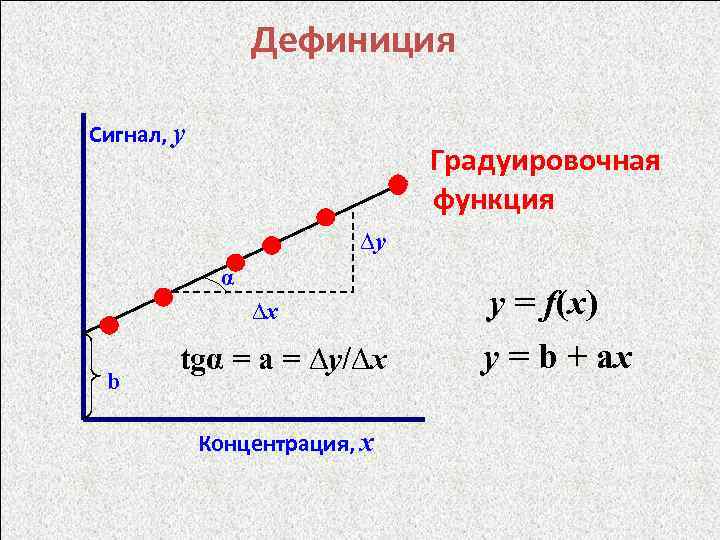 Дефиниция Сигнал, y Градуировочная функция ∆y α ∆х b tgα = а = ∆y/∆х Концентрация, х y = f(x) y = b + аx
Дефиниция Сигнал, y Градуировочная функция ∆y α ∆х b tgα = а = ∆y/∆х Концентрация, х y = f(x) y = b + аx
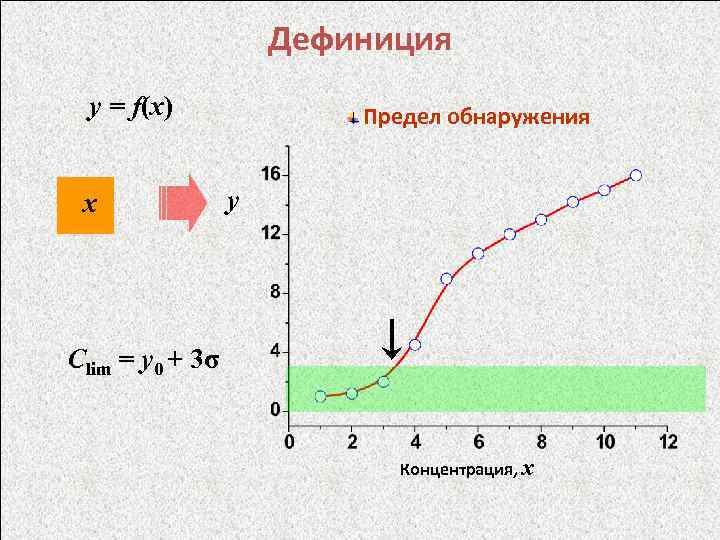 Дефиниция y = f(x) х Предел обнаружения y Сlim = y 0 + 3σ Концентрация, x
Дефиниция y = f(x) х Предел обнаружения y Сlim = y 0 + 3σ Концентрация, x
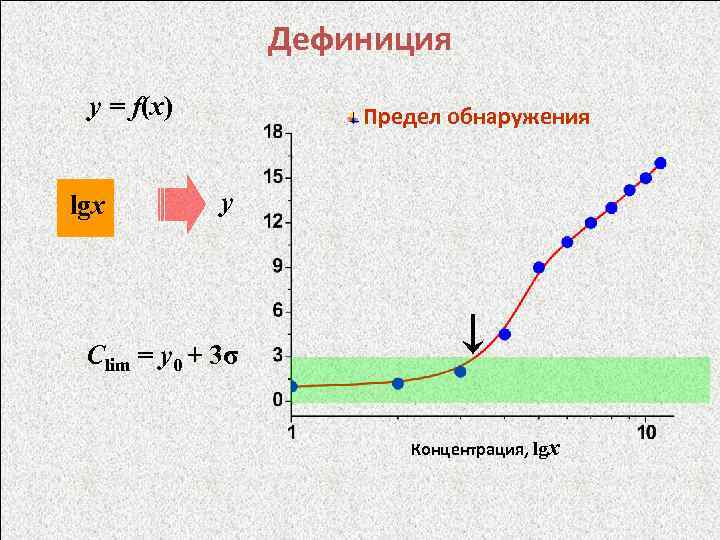 Дефиниция y = f(x) lgх Предел обнаружения y Сlim = y 0 + 3σ Концентрация, lgx
Дефиниция y = f(x) lgх Предел обнаружения y Сlim = y 0 + 3σ Концентрация, lgx
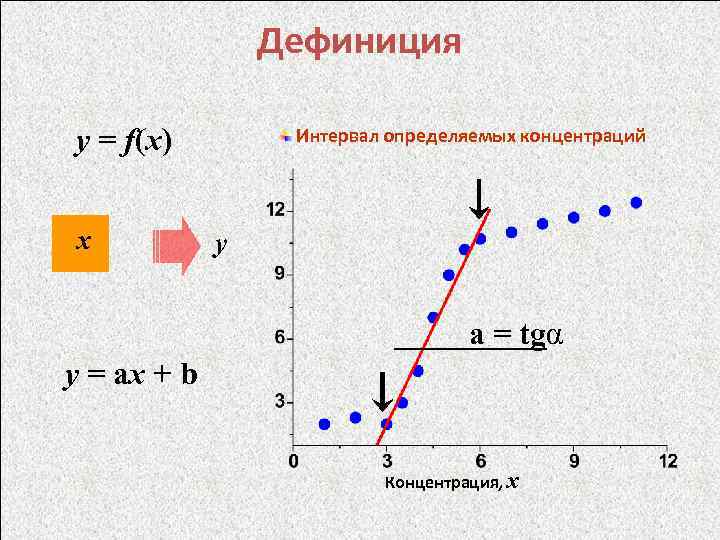 Дефиниция y = f(x) х Интервал определяемых концентраций y a = tgα y = ax + b Концентрация, x
Дефиниция y = f(x) х Интервал определяемых концентраций y a = tgα y = ax + b Концентрация, x
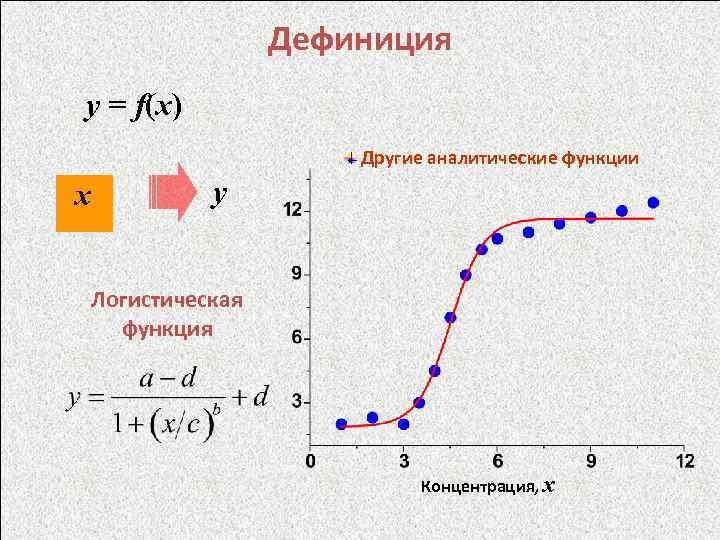 Дефиниция y = f(x) Другие аналитические функции х y Логистическая функция Концентрация, x
Дефиниция y = f(x) Другие аналитические функции х y Логистическая функция Концентрация, x
 Метод и методика анализа • Метод анализа – достаточно универсальный и теоретически обоснованный способ определения состава безотносительно к определяемому компоненту и (обычно) к анализируемому объекту. • Методика анализа – подробное описание анализа данного объекта с использованием выбранного метода. "Контроль объекта аналитический. Термины и определения. " ГОСТ Р 52361– 2005.
Метод и методика анализа • Метод анализа – достаточно универсальный и теоретически обоснованный способ определения состава безотносительно к определяемому компоненту и (обычно) к анализируемому объекту. • Методика анализа – подробное описание анализа данного объекта с использованием выбранного метода. "Контроль объекта аналитический. Термины и определения. " ГОСТ Р 52361– 2005.
 Методы аналитической химии • Методы отбора проб (пробоотбора) • Методы разложения проб • Методы разделения компонентов • Методы концентрирования • Методы обнаружения (идентификации) • Методы определения
Методы аналитической химии • Методы отбора проб (пробоотбора) • Методы разложения проб • Методы разделения компонентов • Методы концентрирования • Методы обнаружения (идентификации) • Методы определения
 Проба • Проба – или образец – предмет исследования аналитика, объект, взятый для анализа. • По ГОСТ: проба - часть вещества (материала), являющегося объектом аналитического контроля, отобранная для анализа и/или исследования его структуры, и/или определе-ния свойств, отражающая его химический состав и/или структуру, и/или свойства. • Представительная проба вещества или материала - объекта аналитического контроля – проба, которая по химическому составу и/или свойствам, и/или структуре идентична объекту аналитического контроля, от которого она отобрана.
Проба • Проба – или образец – предмет исследования аналитика, объект, взятый для анализа. • По ГОСТ: проба - часть вещества (материала), являющегося объектом аналитического контроля, отобранная для анализа и/или исследования его структуры, и/или определе-ния свойств, отражающая его химический состав и/или структуру, и/или свойства. • Представительная проба вещества или материала - объекта аналитического контроля – проба, которая по химическому составу и/или свойствам, и/или структуре идентична объекту аналитического контроля, от которого она отобрана.
 Классификация проб • В зависимости от способа получения: • • разовая, точечная (единичная, частная), мгновенная, суточная и т. п. • В зависимости от стадии первичной обработки: • • исходная, промежуточная, объединенная, средняя, сокращенная, лабораторная, аналитическая и др. • В зависимости от назначения: • • контрольная, рабочая, резервная, арбитражная и др.
Классификация проб • В зависимости от способа получения: • • разовая, точечная (единичная, частная), мгновенная, суточная и т. п. • В зависимости от стадии первичной обработки: • • исходная, промежуточная, объединенная, средняя, сокращенная, лабораторная, аналитическая и др. • В зависимости от назначения: • • контрольная, рабочая, резервная, арбитражная и др.
 Абсолютные и относительные методы анализа Абсолютные методы – не требуют градуировки и стандартных образцов (гравиметрия, кулонометрия и т. д. ). Относительные методы – параметры градуировочной функции определяют экспериментально (потенциометрия, вольтамперометрия и т. д. ) с использованием стандартных образцов.
Абсолютные и относительные методы анализа Абсолютные методы – не требуют градуировки и стандартных образцов (гравиметрия, кулонометрия и т. д. ). Относительные методы – параметры градуировочной функции определяют экспериментально (потенциометрия, вольтамперометрия и т. д. ) с использованием стандартных образцов.
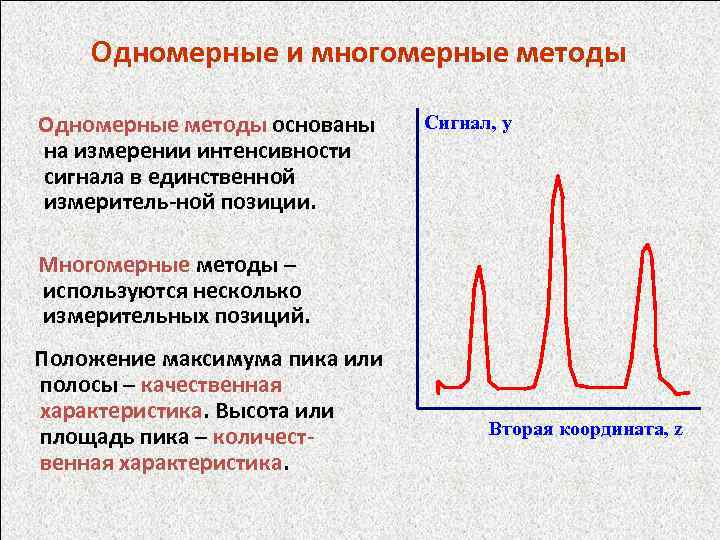 Одномерные и многомерные методы Одномерные методы основаны на измерении интенсивности сигнала в единственной измеритель-ной позиции. Сигнал, y Многомерные методы – используются несколько измерительных позиций. Положение максимума пика или полосы – качественная характеристика. Высота или площадь пика – количественная характеристика. Вторая координата, z
Одномерные и многомерные методы Одномерные методы основаны на измерении интенсивности сигнала в единственной измеритель-ной позиции. Сигнал, y Многомерные методы – используются несколько измерительных позиций. Положение максимума пика или полосы – качественная характеристика. Высота или площадь пика – количественная характеристика. Вторая координата, z
 Классификация методов анализа общая классификация по способу регистрации по способу измерения по объекту
Классификация методов анализа общая классификация по способу регистрации по способу измерения по объекту
 Классификация методов анализа Общая классификация качественный / количественный элементный / изотопный / молекулярный / структурно-групповой валовый / распределительный (локальный) / вещественный / фазовый контактный / дистанционный деструктивный / недеструктив-ный макро- > 0. 1 г полумикро- 0. 1 - 0. 01 г микро- 0. 01 – 0. 001 г ультрамикро- 10 -6 г субмикро- 10 -9 г макро- / полумикро- / ультрамикро- / субмикро-
Классификация методов анализа Общая классификация качественный / количественный элементный / изотопный / молекулярный / структурно-групповой валовый / распределительный (локальный) / вещественный / фазовый контактный / дистанционный деструктивный / недеструктив-ный макро- > 0. 1 г полумикро- 0. 1 - 0. 01 г микро- 0. 01 – 0. 001 г ультрамикро- 10 -6 г субмикро- 10 -9 г макро- / полумикро- / ультрамикро- / субмикро-
 Классификация методов анализа По способу регистрации сигнала Химические (погрешность < 0. 1 - 0. 2 %) Физические (погрешность 2 - 5 %) Биологические Химические Гравиметрия Титриметрия Электрохимические Биохимические
Классификация методов анализа По способу регистрации сигнала Химические (погрешность < 0. 1 - 0. 2 %) Физические (погрешность 2 - 5 %) Биологические Химические Гравиметрия Титриметрия Электрохимические Биохимические
 Классификация методов анализа По способу регистрации сигнала Химические (погрешность < 0. 1 - 0. 2 %) Физические (погрешность 2 - 5 %) Биологические Физические Спектральные Масс-спектральные Основанные на измерении радиоактивности Термический анализ
Классификация методов анализа По способу регистрации сигнала Химические (погрешность < 0. 1 - 0. 2 %) Физические (погрешность 2 - 5 %) Биологические Физические Спектральные Масс-спектральные Основанные на измерении радиоактивности Термический анализ
 Классификация методов анализа По способу регистрации сигнала Химические (погрешность < 0. 1 - 0. 2 %) Физические (погрешность 2 - 5 %) Биологические Биотестирование Биоиндикация Микробиологический анализ Биосенсоры
Классификация методов анализа По способу регистрации сигнала Химические (погрешность < 0. 1 - 0. 2 %) Физические (погрешность 2 - 5 %) Биологические Биотестирование Биоиндикация Микробиологический анализ Биосенсоры
 Классификация методов анализа По способу регистрации сигнала Химические Физические Биологические Физико-химические Спектроскопические Масс-спектральные Основанные на радиоактивности Электрохимические Биохимические Термические
Классификация методов анализа По способу регистрации сигнала Химические Физические Биологические Физико-химические Спектроскопические Масс-спектральные Основанные на радиоактивности Электрохимические Биохимические Термические
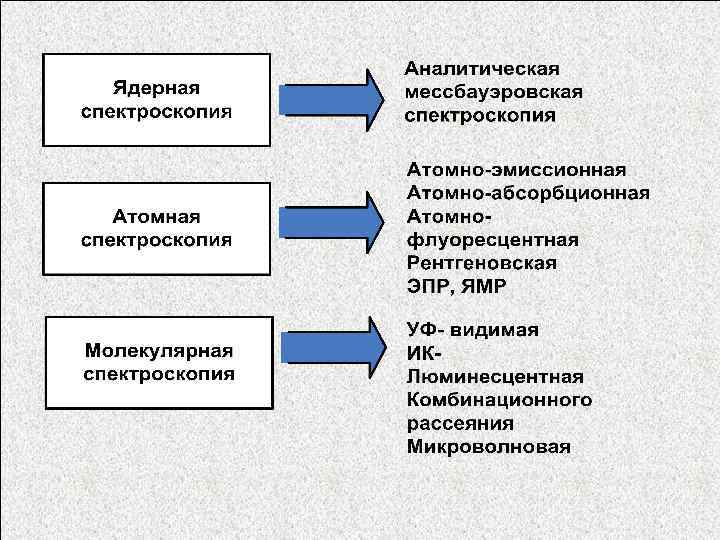
 По способу измерения сигнала • • Спектроскопия Молекулярная Атомная Ядерная • Электрохимические методы • Вольтамперометрия • Потенциометрия • Кондуктометрия • Кулонометрия • Хронопотенциометрия, хроноамперометрия
По способу измерения сигнала • • Спектроскопия Молекулярная Атомная Ядерная • Электрохимические методы • Вольтамперометрия • Потенциометрия • Кондуктометрия • Кулонометрия • Хронопотенциометрия, хроноамперометрия
 Классификация • По объекту анализа х по агрегатному состоянию по химической природе по происхождению объекта по степени распространенности и важности по степени чистоты
Классификация • По объекту анализа х по агрегатному состоянию по химической природе по происхождению объекта по степени распространенности и важности по степени чистоты
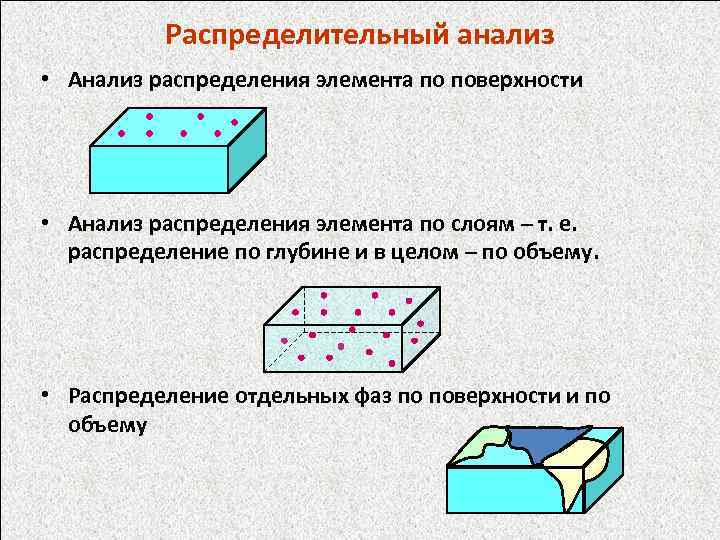 Распределительный анализ • Анализ распределения элемента по поверхности • Анализ распределения элемента по слоям – т. е. распределение по глубине и в целом – по объему. • Распределение отдельных фаз по поверхности и по объему
Распределительный анализ • Анализ распределения элемента по поверхности • Анализ распределения элемента по слоям – т. е. распределение по глубине и в целом – по объему. • Распределение отдельных фаз по поверхности и по объему
 Критерии сравнения Аналитические характеристики Метрологические характеристики Требования к пробоподготовке Особенности приборного оснащения Специальные требования, связанные с природой объекта контроля • Экономические характеристики • • •
Критерии сравнения Аналитические характеристики Метрологические характеристики Требования к пробоподготовке Особенности приборного оснащения Специальные требования, связанные с природой объекта контроля • Экономические характеристики • • •
 Литература 1. Основы аналитической химии. Кн. 2. Методы химического анализа. / Под ред. Ю. А. Золотова. 2 -е изд. М. : Высшая школа, 2004. 2. Аналитическая химия. Физические и физико-химические методы анализа. Под ред. О. М. Петрухина. М. : Химия, 2001. 3. Васильев В. П. Аналитическая химия. Кн. 2. Физико-химические методы анализа. М. : Дрофа, 2004. Дополнительная литература 1. Кристиан Г. Аналитическая химия. В 2 -х т. М. : БИНОМ, 2009. 2. Аналитическая химия. Проблемы и подходы: В 2 -х т. / Под ред. Р. Кельнера, Ж-М. Мерме, М. Отто, Н. Видмера. М. : Мир, 2004. 3. Отто М. Современные методы аналитической химии. В 2 т. М. : Техносфера, 2003.
Литература 1. Основы аналитической химии. Кн. 2. Методы химического анализа. / Под ред. Ю. А. Золотова. 2 -е изд. М. : Высшая школа, 2004. 2. Аналитическая химия. Физические и физико-химические методы анализа. Под ред. О. М. Петрухина. М. : Химия, 2001. 3. Васильев В. П. Аналитическая химия. Кн. 2. Физико-химические методы анализа. М. : Дрофа, 2004. Дополнительная литература 1. Кристиан Г. Аналитическая химия. В 2 -х т. М. : БИНОМ, 2009. 2. Аналитическая химия. Проблемы и подходы: В 2 -х т. / Под ред. Р. Кельнера, Ж-М. Мерме, М. Отто, Н. Видмера. М. : Мир, 2004. 3. Отто М. Современные методы аналитической химии. В 2 т. М. : Техносфера, 2003.
 Инструментальные методы анализа: спектры атомов и молекул Майстренко В. Н. Башкирский государственный университет Кафедра аналитической химии V_maystrenko@mail. ru Тел: 229 -97 -12
Инструментальные методы анализа: спектры атомов и молекул Майстренко В. Н. Башкирский государственный университет Кафедра аналитической химии V_maystrenko@mail. ru Тел: 229 -97 -12
 В арсенале современной аналитической химии важнейшее место занимают методы атомной оптической спектроскопии, основанные на измерении интенсивности электромагнитного излучения, испускаемого или поглощаемого атомами элементов, которые находятся в газо- или парообразном состоянии. Эти методы являются многоэлементными и широко используются для установления состава различных объектов – сплавов, минералов, руд, пищевых продуктов, объектов окружающей среды и др.
В арсенале современной аналитической химии важнейшее место занимают методы атомной оптической спектроскопии, основанные на измерении интенсивности электромагнитного излучения, испускаемого или поглощаемого атомами элементов, которые находятся в газо- или парообразном состоянии. Эти методы являются многоэлементными и широко используются для установления состава различных объектов – сплавов, минералов, руд, пищевых продуктов, объектов окружающей среды и др.
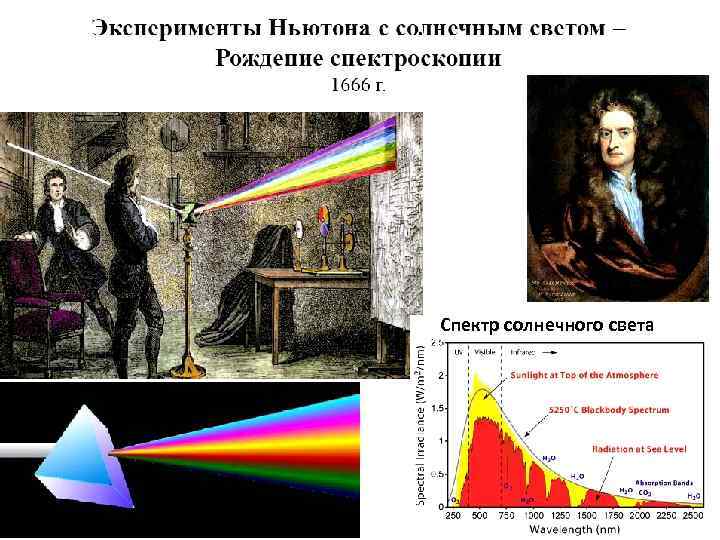 Спектр солнечного света
Спектр солнечного света
 История атомного спектрального анализа началась с опытов Исаака Ньютона (1666 г) по разложению света в спектр. Первые атомные спектры наблюдали в начале XIX века в ходе астрономических исследований. Возникновение спектрального анализа как метода определения химичес-кого состава вещества относят к 1859 г. , когда немецкие ученые Г. Кирхгоф и Р. Бунзен, исследуя поведение солей металлов в пламени, наблюдали появление линий в спектрах элементов. Густав Кирхгоф (слева) и Роберт Бунзен (справа) Спектроскоп Кирхгофа и Бунзена
История атомного спектрального анализа началась с опытов Исаака Ньютона (1666 г) по разложению света в спектр. Первые атомные спектры наблюдали в начале XIX века в ходе астрономических исследований. Возникновение спектрального анализа как метода определения химичес-кого состава вещества относят к 1859 г. , когда немецкие ученые Г. Кирхгоф и Р. Бунзен, исследуя поведение солей металлов в пламени, наблюдали появление линий в спектрах элементов. Густав Кирхгоф (слева) и Роберт Бунзен (справа) Спектроскоп Кирхгофа и Бунзена
 Окрашивание пламени горелки при внесении соли металла
Окрашивание пламени горелки при внесении соли металла
 Эксперимент Бунзена-Кирхгофа А – сигарный ящик, B – часть подзорной трубы, С – подзорная труба, D – газовая горелка Бунзена, E – штатив с солью натрия, F – призма из стекла с CS 2, G – зеркало, H – поворотное устройство
Эксперимент Бунзена-Кирхгофа А – сигарный ящик, B – часть подзорной трубы, С – подзорная труба, D – газовая горелка Бунзена, E – штатив с солью натрия, F – призма из стекла с CS 2, G – зеркало, H – поворотное устройство
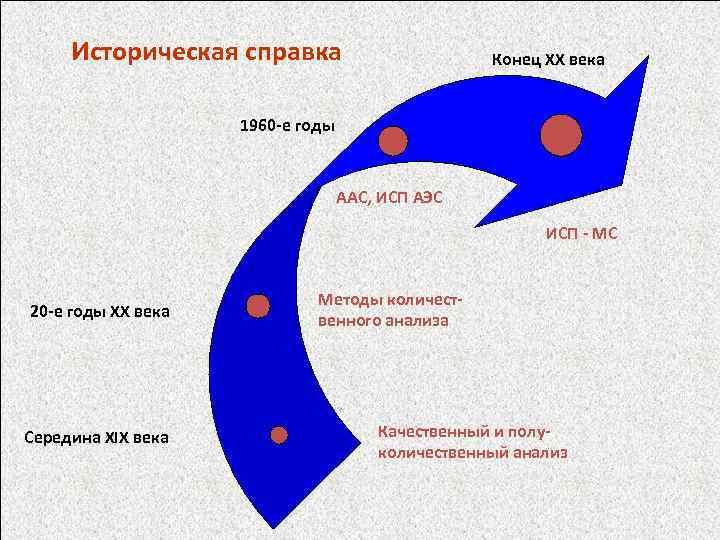 Историческая справка Конец XX века 1960 -е годы ААС, ИСП АЭС ИСП - МС 20 -е годы XX века Середина XIX века Методы количественного анализа Качественный и полуколичественный анализ
Историческая справка Конец XX века 1960 -е годы ААС, ИСП АЭС ИСП - МС 20 -е годы XX века Середина XIX века Методы количественного анализа Качественный и полуколичественный анализ
 Спектры атомов Атомы химических элементов имеют строго определённые частоты, на которых они излучают или поглощают свет. При этом на спектрах элементов наблюдаются светлые или темные линии в определённых местах, характерные для каждого элемента. Атомарные спектры получают переведением веществ в парообраз-ное состояние путём нагревания до 1000— 10000 °C. В качестве источни-ков возбуждения атомов применяют искру, дугу переменного тока, пламя или плазму различных газов, лазеры и др. Спектры поглощения и испускания атомов натрия
Спектры атомов Атомы химических элементов имеют строго определённые частоты, на которых они излучают или поглощают свет. При этом на спектрах элементов наблюдаются светлые или темные линии в определённых местах, характерные для каждого элемента. Атомарные спектры получают переведением веществ в парообраз-ное состояние путём нагревания до 1000— 10000 °C. В качестве источни-ков возбуждения атомов применяют искру, дугу переменного тока, пламя или плазму различных газов, лазеры и др. Спектры поглощения и испускания атомов натрия
 Сплошной спектр Спектр испускания (эмиссионный) Спектр поглощения (абсорбционный)
Сплошной спектр Спектр испускания (эмиссионный) Спектр поглощения (абсорбционный)

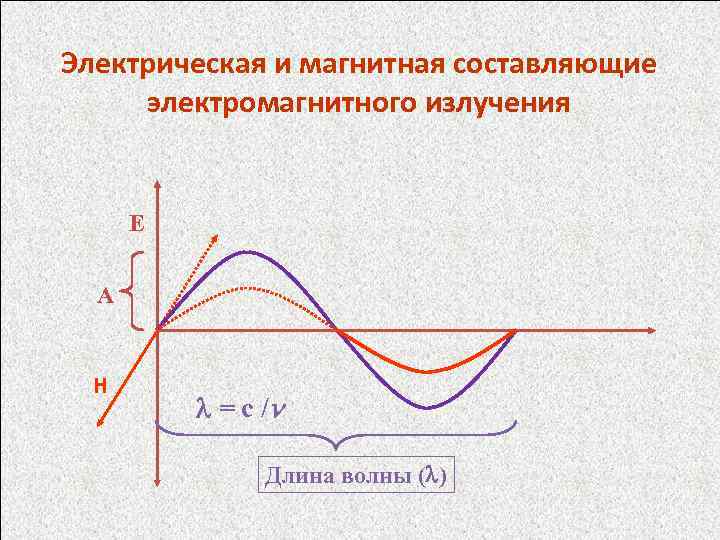 Электрическая и магнитная составляющие электромагнитного излучения E A H = с / Длина волны ( )
Электрическая и магнитная составляющие электромагнитного излучения E A H = с / Длина волны ( )
 Спектральные линии характеризуют частотой излучения , которая соответствует квантовому переходу между уровнями энергии Еi и Еk атома согласно соотношению h = Еi - Еk , где h – постоянная Планка, а также длиной волны = с / (с – скорость света), волновым числом ’ = 1/ и энергией фотона h. Частоты спектральных линий выражают в обратных секундах (с-1), длины волн – в нм, мкм и ангстремах, волновые числа – в обратных сантиметрах (см-1), энергию фотонов в электронвольтах (э. В). Спектры испускания (эмиссионные) получают при возбуждении атомов различными способами. Время жизни возбужденного состояния 10 -7 – 10 -8 с. В течение этого времени атом испускает квант электро-магнитного излучения и переходит в состояние с более низкой энергией. Спектры поглощения (абсорбционные) наблюдаются при прохож-дении электромагнитного излучения, имеющего непрерывный спектр, через пары или газы атомов. Возникновение оптических спектров и их характер определяет система электронов атома, которые характеризуются четыремя квантовыми числами: главным квантовым числом (уровни K, L, M, N…Q), орбитальным квантовым числом (подуровни s, p, d, f…), магнитным и спиновым квантовыми числами.
Спектральные линии характеризуют частотой излучения , которая соответствует квантовому переходу между уровнями энергии Еi и Еk атома согласно соотношению h = Еi - Еk , где h – постоянная Планка, а также длиной волны = с / (с – скорость света), волновым числом ’ = 1/ и энергией фотона h. Частоты спектральных линий выражают в обратных секундах (с-1), длины волн – в нм, мкм и ангстремах, волновые числа – в обратных сантиметрах (см-1), энергию фотонов в электронвольтах (э. В). Спектры испускания (эмиссионные) получают при возбуждении атомов различными способами. Время жизни возбужденного состояния 10 -7 – 10 -8 с. В течение этого времени атом испускает квант электро-магнитного излучения и переходит в состояние с более низкой энергией. Спектры поглощения (абсорбционные) наблюдаются при прохож-дении электромагнитного излучения, имеющего непрерывный спектр, через пары или газы атомов. Возникновение оптических спектров и их характер определяет система электронов атома, которые характеризуются четыремя квантовыми числами: главным квантовым числом (уровни K, L, M, N…Q), орбитальным квантовым числом (подуровни s, p, d, f…), магнитным и спиновым квантовыми числами.
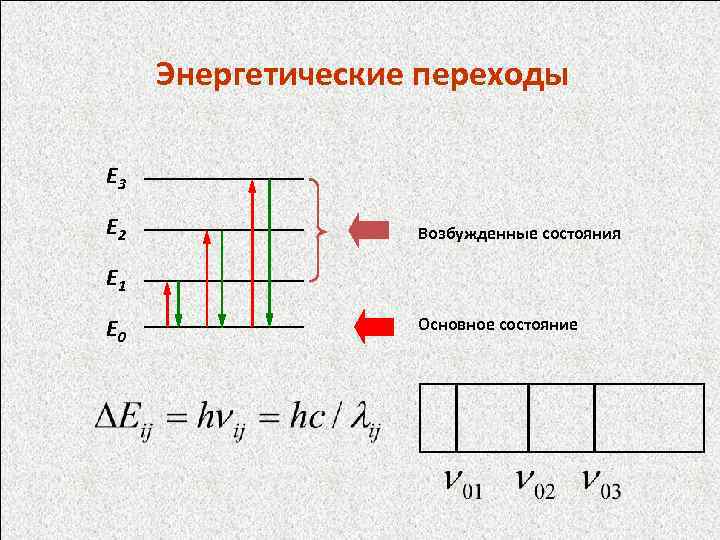 Энергетические переходы Е 3 Е 2 Возбужденные состояния Е 1 Е 0 Основное состояние
Энергетические переходы Е 3 Е 2 Возбужденные состояния Е 1 Е 0 Основное состояние
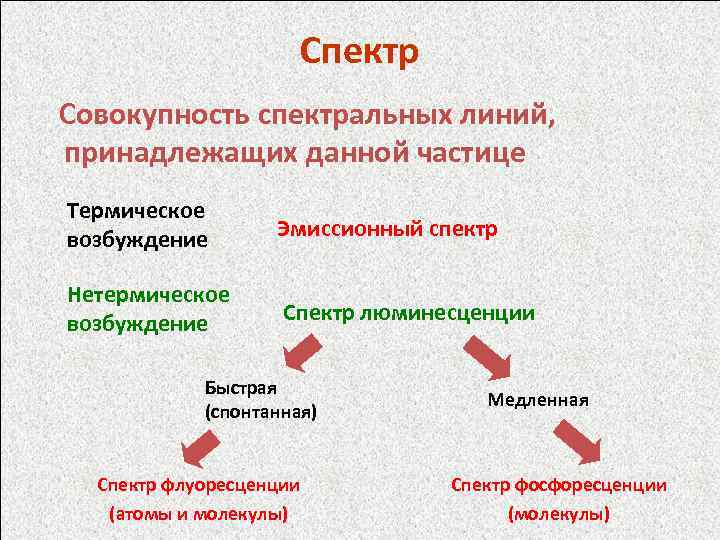 Спектр Совокупность спектральных линий, принадлежащих данной частице Термическое возбуждение Эмиссионный спектр Нетермическое возбуждение Спектр люминесценции Быстрая (спонтанная) Спектр флуоресценции (атомы и молекулы) Медленная Спектр фосфоресценции (молекулы)
Спектр Совокупность спектральных линий, принадлежащих данной частице Термическое возбуждение Эмиссионный спектр Нетермическое возбуждение Спектр люминесценции Быстрая (спонтанная) Спектр флуоресценции (атомы и молекулы) Медленная Спектр фосфоресценции (молекулы)
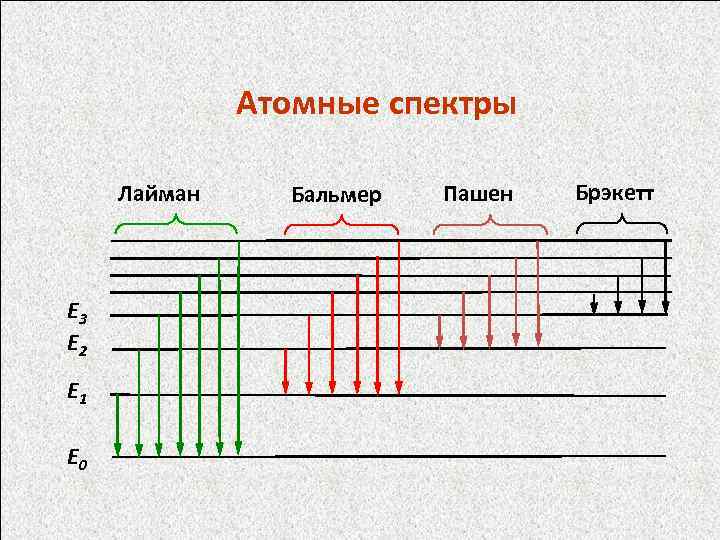 Атомные спектры Лайман Е 3 Е 2 Е 1 Е 0 Бальмер Пашен Брэкетт
Атомные спектры Лайман Е 3 Е 2 Е 1 Е 0 Бальмер Пашен Брэкетт
 Спектры атомов с малым числом валентных электронов (щелочные металлы, водород) имеют относительно мало линий (менее 100) в диапазоне 200 - 800 нм. Атомы с более сложными электронными оболочками (элементы побочных групп) имеют спектры с большим числом линий ( Cu – более 500, Fe – более 3000, U – несколько тысяч). Линии, обусловленные переходом электронов на основной энергетический уровень, называются резонансными. Вследствие высокой интенсивности они обеспечивают наибольшую чувствитель-ность определений и используются для аналитических целей. Для возбуждения резонансных линий щелочных металлов необхо-дима небольшая энергия, тогда как для неметаллов она высокая и спектры из видимой области смещаются в труднодоступную ультра-фиолетовую область: для Na – 589 нм, Mg – 285 нм, Si – 251 нм, P – 176 нм. Основная область применения атомной спектроскопии – опреде-ление элементов с металлическими и полуметаллическими свойствами. Для получения количественной информации измеряют интенсив-ность одной из спектральных линий определяемого элемента. Процессы, происходящие с атомом при поглощении или испускании фотона, описывают с помощью спектральных термов, характеризующих энергетическое состояние поглощающего или испускающего атома. Спектральные термы получают путем векторного сложения орбитальных моментов и спинов всех электронов атома.
Спектры атомов с малым числом валентных электронов (щелочные металлы, водород) имеют относительно мало линий (менее 100) в диапазоне 200 - 800 нм. Атомы с более сложными электронными оболочками (элементы побочных групп) имеют спектры с большим числом линий ( Cu – более 500, Fe – более 3000, U – несколько тысяч). Линии, обусловленные переходом электронов на основной энергетический уровень, называются резонансными. Вследствие высокой интенсивности они обеспечивают наибольшую чувствитель-ность определений и используются для аналитических целей. Для возбуждения резонансных линий щелочных металлов необхо-дима небольшая энергия, тогда как для неметаллов она высокая и спектры из видимой области смещаются в труднодоступную ультра-фиолетовую область: для Na – 589 нм, Mg – 285 нм, Si – 251 нм, P – 176 нм. Основная область применения атомной спектроскопии – опреде-ление элементов с металлическими и полуметаллическими свойствами. Для получения количественной информации измеряют интенсив-ность одной из спектральных линий определяемого элемента. Процессы, происходящие с атомом при поглощении или испускании фотона, описывают с помощью спектральных термов, характеризующих энергетическое состояние поглощающего или испускающего атома. Спектральные термы получают путем векторного сложения орбитальных моментов и спинов всех электронов атома.
 Спектральные термы Формула Бальмера (m > n) Серия Лаймана n = 1 Серия Бальмера: n = 2 Серия Пашена: n = 3 Серия Брэкетта: n = 4 Терм: Спектральный терм: R = 109 677 см− 1 – постоянная Ридберга, m – целые числа.
Спектральные термы Формула Бальмера (m > n) Серия Лаймана n = 1 Серия Бальмера: n = 2 Серия Пашена: n = 3 Серия Брэкетта: n = 4 Терм: Спектральный терм: R = 109 677 см− 1 – постоянная Ридберга, m – целые числа.
 Эмиссионный спектр атома водорода ИК vis УФ
Эмиссионный спектр атома водорода ИК vis УФ
 Спектральные термы многоэлектронных атомов Учет заряда ядра: He+, Li 2+, Be 3+ Учет суммарного орбитального момента и суммарного спина
Спектральные термы многоэлектронных атомов Учет заряда ядра: He+, Li 2+, Be 3+ Учет суммарного орбитального момента и суммарного спина
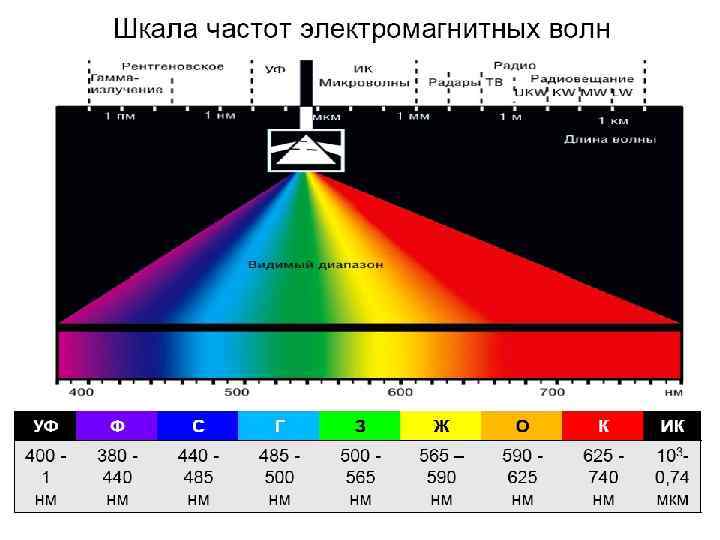
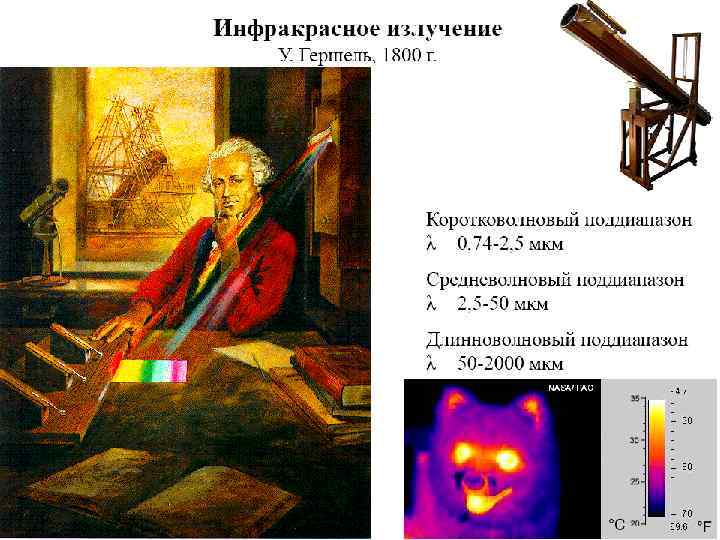
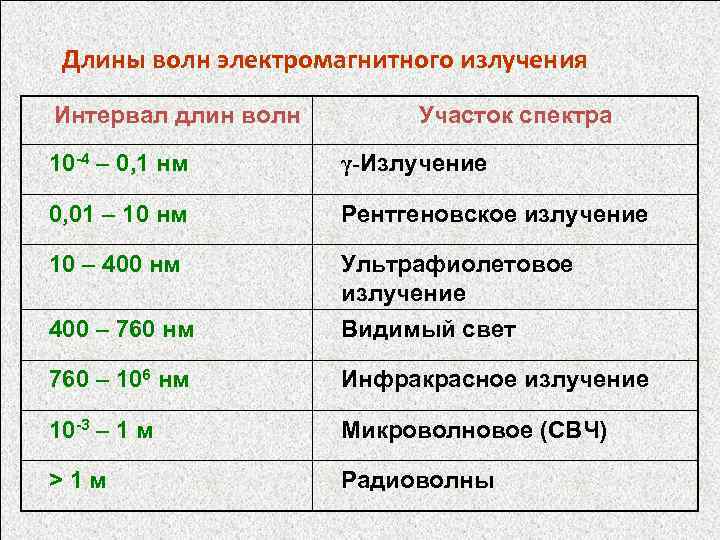 Длины волн электромагнитного излучения Интервал длин волн Участок спектра 10 -4 – 0, 1 нм γ-Излучение 0, 01 – 10 нм Рентгеновское излучение 10 – 400 нм Ультрафиолетовое излучение 400 – 760 нм Видимый свет 760 – 106 нм Инфракрасное излучение 10 -3 – 1 м Микроволновое (СВЧ) >1 м Радиоволны
Длины волн электромагнитного излучения Интервал длин волн Участок спектра 10 -4 – 0, 1 нм γ-Излучение 0, 01 – 10 нм Рентгеновское излучение 10 – 400 нм Ультрафиолетовое излучение 400 – 760 нм Видимый свет 760 – 106 нм Инфракрасное излучение 10 -3 – 1 м Микроволновое (СВЧ) >1 м Радиоволны
 Интенсивность спектральных линий Энергия, поглощаемая, излучаемая или рассеиваемая в единицу времени Спектр испускания: Рентгеновская спектроскопия, АЭС, АФС Спектр поглощения: ААС, UV-Vis, ИК, микроволновая и радиочастотная спектроскопия
Интенсивность спектральных линий Энергия, поглощаемая, излучаемая или рассеиваемая в единицу времени Спектр испускания: Рентгеновская спектроскопия, АЭС, АФС Спектр поглощения: ААС, UV-Vis, ИК, микроволновая и радиочастотная спектроскопия
 Ширина спектральных линий естественная УФ: 10 -5 нм тепловое движение (допплеровское уширение) УФ: 10 -3 -10 -2 нм соударение частиц (лоренцево уширение) расщепление энергетических уровней в магнитном поле (эффект Зеемана)
Ширина спектральных линий естественная УФ: 10 -5 нм тепловое движение (допплеровское уширение) УФ: 10 -3 -10 -2 нм соударение частиц (лоренцево уширение) расщепление энергетических уровней в магнитном поле (эффект Зеемана)
 МОЛЕКУЛЯРНЫЕ СПЕКТРЫ - спектры поглощения, испускания или рассеяния, возникающие при квантовых переходах молекул из одного энергетического состояния в другое. Молекулярные спектры определяются составом молекул, их структурой, характером химических связей и взаимодействием с окружающими атомами и молекулами. Наиболее характерными являются молекулярные спектры молекул разреженных газов, которые состоят из узких линий. Молекулярные спектры состоят из электронных, колебательных и вращательных спектров и лежат в диапазоне электромагнитных волн от радиочастот до рентгеновской области спектра. Частоты переходов между вращательными уровнями энергии обычно попадают в микроволновую область, частоты переходов между колебательными уровнями - в ИК-область, а частоты переходов между электронными уровнями - в видимую и УФ-области спектра. Часто вращательные переходы попадают в ИК-область, колебательные - в видимую область, электронные - в ИК-область. Электронные переходы сопровождаются изменением колебательной энергии молекул, а при колебательных переходах изменяется вращательная энергия. Поэтому электронные спектры обычно представляют собой электронно-колебательные полосы. При высоком разрешении обнаруживается и вращательная структура.
МОЛЕКУЛЯРНЫЕ СПЕКТРЫ - спектры поглощения, испускания или рассеяния, возникающие при квантовых переходах молекул из одного энергетического состояния в другое. Молекулярные спектры определяются составом молекул, их структурой, характером химических связей и взаимодействием с окружающими атомами и молекулами. Наиболее характерными являются молекулярные спектры молекул разреженных газов, которые состоят из узких линий. Молекулярные спектры состоят из электронных, колебательных и вращательных спектров и лежат в диапазоне электромагнитных волн от радиочастот до рентгеновской области спектра. Частоты переходов между вращательными уровнями энергии обычно попадают в микроволновую область, частоты переходов между колебательными уровнями - в ИК-область, а частоты переходов между электронными уровнями - в видимую и УФ-области спектра. Часто вращательные переходы попадают в ИК-область, колебательные - в видимую область, электронные - в ИК-область. Электронные переходы сопровождаются изменением колебательной энергии молекул, а при колебательных переходах изменяется вращательная энергия. Поэтому электронные спектры обычно представляют собой электронно-колебательные полосы. При высоком разрешении обнаруживается и вращательная структура.
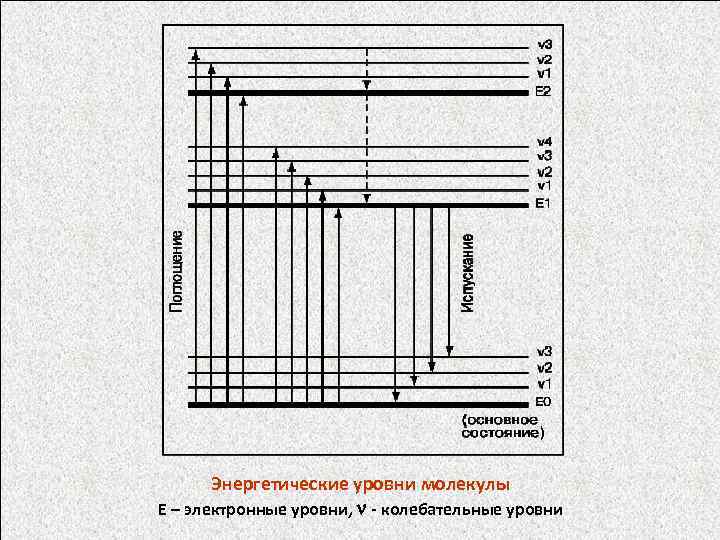 Энергетические уровни молекулы Е – электронные уровни, - колебательные уровни
Энергетические уровни молекулы Е – электронные уровни, - колебательные уровни
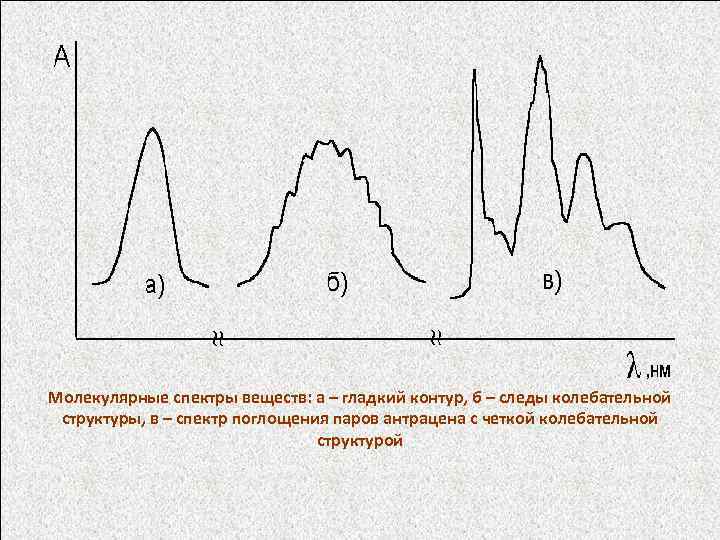 Молекулярные спектры веществ: а – гладкий контур, б – следы колебательной структуры, в – спектр поглощения паров антрацена с четкой колебательной структурой
Молекулярные спектры веществ: а – гладкий контур, б – следы колебательной структуры, в – спектр поглощения паров антрацена с четкой колебательной структурой
 Электронные спектры молекул • Электронные спектры обусловлены переходами между электронными энергетическими уровнями. • Чем определяются электронные спектры? • Для атомов электронной конфигурацией атомов • Для молекул электронной конфигурацией молекул Электронные переходы в молекулах, как правило, имеют энергию, соответствующую УФ- и видимой областям электромагнитного спектра.
Электронные спектры молекул • Электронные спектры обусловлены переходами между электронными энергетическими уровнями. • Чем определяются электронные спектры? • Для атомов электронной конфигурацией атомов • Для молекул электронной конфигурацией молекул Электронные переходы в молекулах, как правило, имеют энергию, соответствующую УФ- и видимой областям электромагнитного спектра.
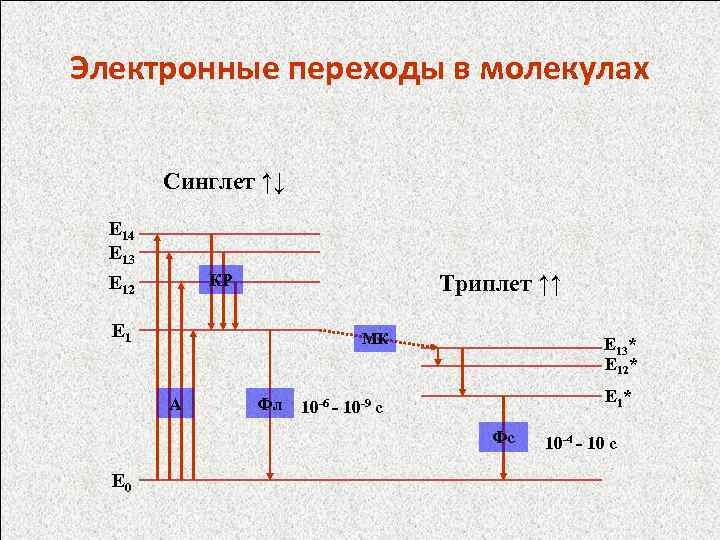 Электронные переходы в молекулах Синглет ↑↓ E 14 E 13 Триплет ↑↑ КР E 12 E 1 МК А Фл Е 13* Е 12* Е 1 * 10 -6 - 10 -9 с Фс E 0 10 -4 - 10 c
Электронные переходы в молекулах Синглет ↑↓ E 14 E 13 Триплет ↑↑ КР E 12 E 1 МК А Фл Е 13* Е 12* Е 1 * 10 -6 - 10 -9 с Фс E 0 10 -4 - 10 c
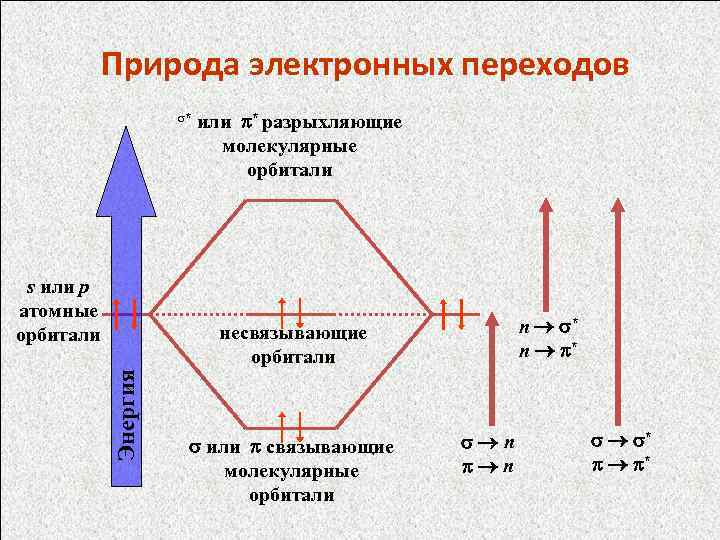 Природа электронных переходов s* s или p атомные орбитали или * разрыхляющие молекулярные орбитали n * Энергия несвязывающие орбитали или связывающие молекулярные орбитали n n * *
Природа электронных переходов s* s или p атомные орбитали или * разрыхляющие молекулярные орбитали n * Энергия несвязывающие орбитали или связывающие молекулярные орбитали n n * *
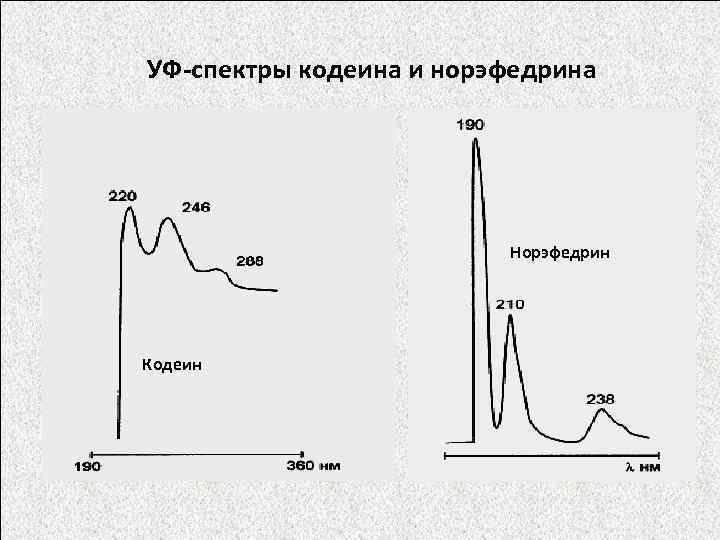 УФ-спектры кодеина и норэфедрина Норэфедрин Кодеин
УФ-спектры кодеина и норэфедрина Норэфедрин Кодеин
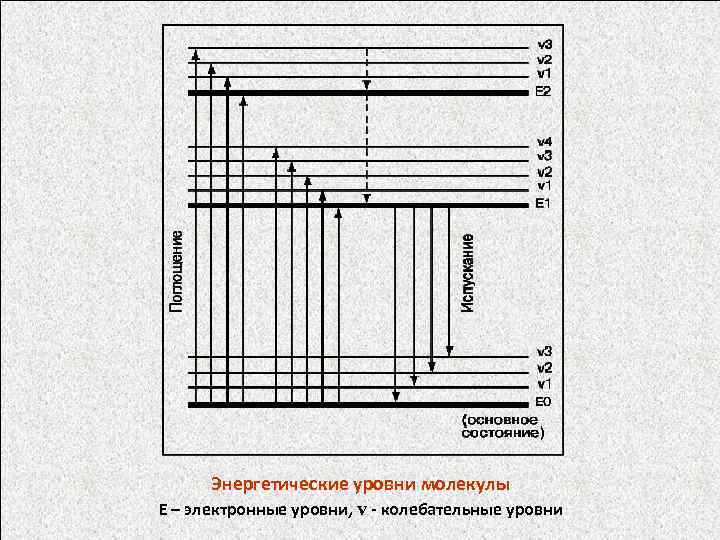 Энергетические уровни молекулы Е – электронные уровни, v - колебательные уровни
Энергетические уровни молекулы Е – электронные уровни, v - колебательные уровни
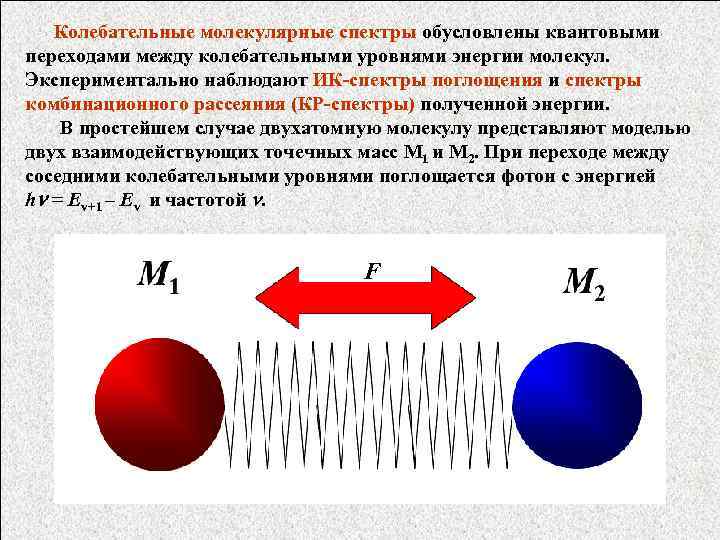 Колебательные молекулярные спектры обусловлены квантовыми переходами между колебательными уровнями энергии молекул. Экспериментально наблюдают ИК-спектры поглощения и спектры комбинационного рассеяния (КР-спектры) полученной энергии. В простейшем случае двухатомную молекулу представляют моделью двух взаимодействующих точечных масс M 1 и M 2. При переходе между соседними колебательными уровнями поглощается фотон с энергией h = Ev+1 – Ev и частотой . F
Колебательные молекулярные спектры обусловлены квантовыми переходами между колебательными уровнями энергии молекул. Экспериментально наблюдают ИК-спектры поглощения и спектры комбинационного рассеяния (КР-спектры) полученной энергии. В простейшем случае двухатомную молекулу представляют моделью двух взаимодействующих точечных масс M 1 и M 2. При переходе между соседними колебательными уровнями поглощается фотон с энергией h = Ev+1 – Ev и частотой . F
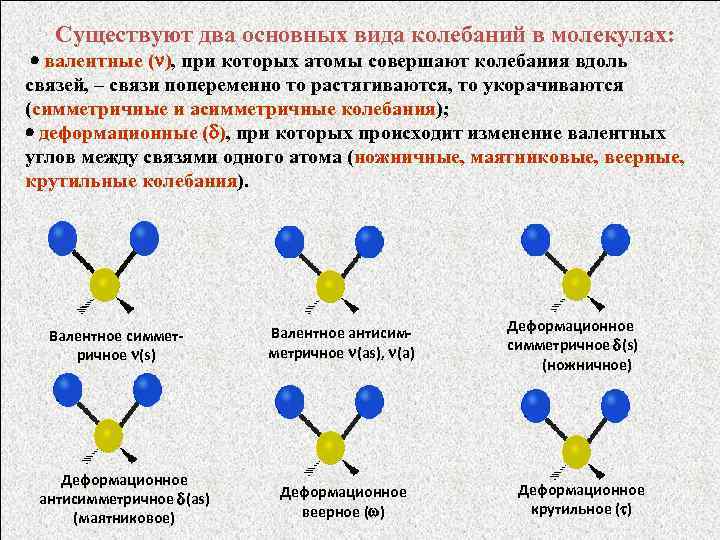 Существуют два основных вида колебаний в молекулах: валентные ( ), при которых атомы совершают колебания вдоль связей, – связи попеременно то растягиваются, то укорачиваются (симметричные и асимметричные колебания); деформационные ( ), при которых происходит изменение валентных углов между связями одного атома (ножничные, маятниковые, веерные, крутильные колебания). Валентное симметричное (s) Деформационное антисимметричное (аs) (маятниковое) Валентное антисимметричное (as), (a) Деформационное веерное ( ) Деформационное симметричное (s) (ножничное) Деформационное крутильное ( )
Существуют два основных вида колебаний в молекулах: валентные ( ), при которых атомы совершают колебания вдоль связей, – связи попеременно то растягиваются, то укорачиваются (симметричные и асимметричные колебания); деформационные ( ), при которых происходит изменение валентных углов между связями одного атома (ножничные, маятниковые, веерные, крутильные колебания). Валентное симметричное (s) Деформационное антисимметричное (аs) (маятниковое) Валентное антисимметричное (as), (a) Деформационное веерное ( ) Деформационное симметричное (s) (ножничное) Деформационное крутильное ( )
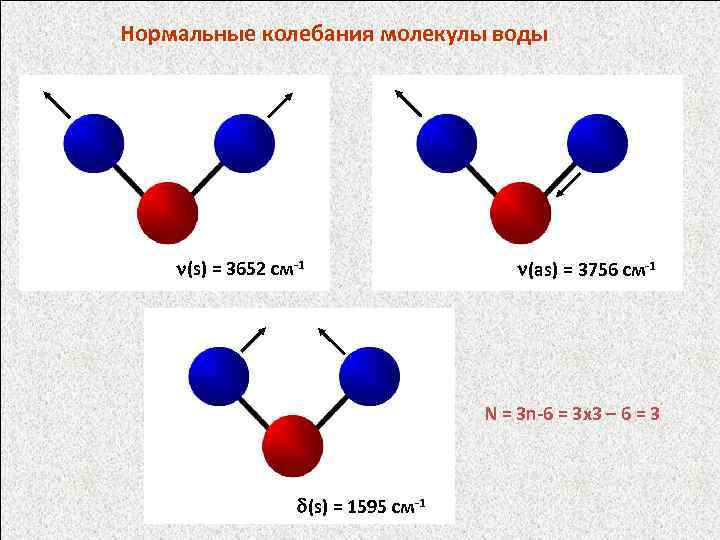 Нормальные колебания молекулы воды (s) = 3652 см-1 (as) = 3756 см-1 N = 3 n-6 = 3 x 3 – 6 = 3 (s) = 1595 см-1
Нормальные колебания молекулы воды (s) = 3652 см-1 (as) = 3756 см-1 N = 3 n-6 = 3 x 3 – 6 = 3 (s) = 1595 см-1
 Частота колебаний зависит от массы атомов (легче атом – выше частота) C – H 3000 см-1 C – D 2200 см-1 C – O 1100 см-1 C – Cl 700 см-1 Частота колебаний зависит от энергии связи (связь прочнее – выше частота) C С 2143 см-1 C = O 1715 см-1 C – O 1100 см-1
Частота колебаний зависит от массы атомов (легче атом – выше частота) C – H 3000 см-1 C – D 2200 см-1 C – O 1100 см-1 C – Cl 700 см-1 Частота колебаний зависит от энергии связи (связь прочнее – выше частота) C С 2143 см-1 C = O 1715 см-1 C – O 1100 см-1
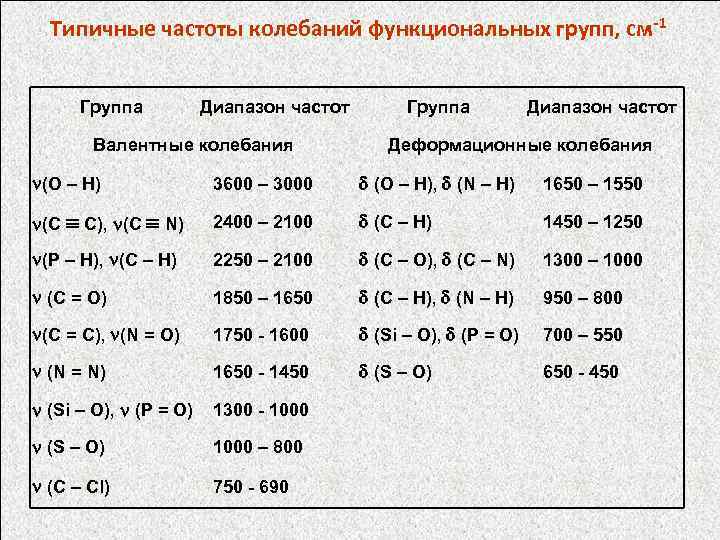 Типичные частоты колебаний функциональных групп, см-1 Группа Диапазон частот Валентные колебания Группа Диапазон частот Деформационные колебания (O – H) 3600 – 3000 (O – H), (N – H) 1650 – 1550 (C C), (C N) 2400 – 2100 (C – H) 1450 – 1250 (P – H), (C – H) 2250 – 2100 (C – O), (C – N) 1300 – 1000 (C = O) 1850 – 1650 (C – H), (N – H) 950 – 800 (C = C), (N = O) 1750 - 1600 (Si – O), (P = O) 700 – 550 (N = N) 1650 - 1450 (S – O) 650 - 450 (Si – O), (P = O) 1300 - 1000 (S – O) 1000 – 800 (C – Cl) 750 - 690
Типичные частоты колебаний функциональных групп, см-1 Группа Диапазон частот Валентные колебания Группа Диапазон частот Деформационные колебания (O – H) 3600 – 3000 (O – H), (N – H) 1650 – 1550 (C C), (C N) 2400 – 2100 (C – H) 1450 – 1250 (P – H), (C – H) 2250 – 2100 (C – O), (C – N) 1300 – 1000 (C = O) 1850 – 1650 (C – H), (N – H) 950 – 800 (C = C), (N = O) 1750 - 1600 (Si – O), (P = O) 700 – 550 (N = N) 1650 - 1450 (S – O) 650 - 450 (Si – O), (P = O) 1300 - 1000 (S – O) 1000 – 800 (C – Cl) 750 - 690
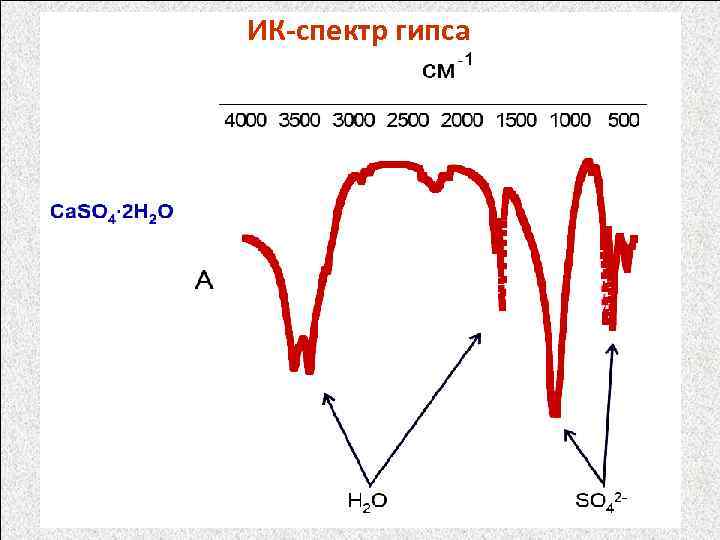 ИК-спектр гипса
ИК-спектр гипса
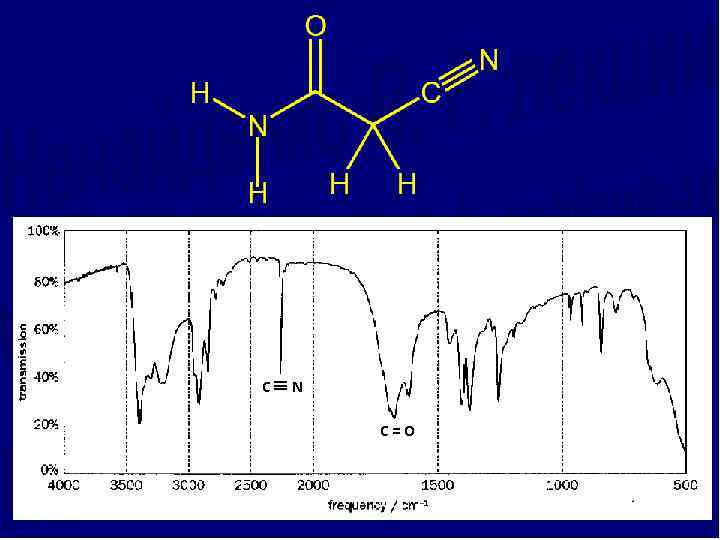 C N C = O
C N C = O
 Литература 1. Основы аналитической химии. Кн. 2. Методы химического анализа. / Под ред. Ю. А. Золотова. 2 -е изд. М. : Высшая школа, 2004. 2. Аналитическая химия. Физические и физико-химические методы анализа. Под ред. О. М. Петрухина. М. : Химия, 2001. 3. Васильев В. П. Аналитическая химия. Кн. 2. Физико-химические методы анализа. М. : Дрофа, 2004. Дополнительная литература 1. Кристиан Г. Аналитическая химия. В 2 -х т. М. : БИНОМ, 2009. 2. Аналитическая химия. Проблемы и подходы: В 2 т. / Под ред. Р. Кельнера, Ж-М. Мерме, М. Отто, Н. Видмера. М. : Мир, 2004. 3. Отто М. Современные методы аналитической химии. В 2 т. М. : Техносфера, 2003. 4. Кузяков Ю. Я. , Семененко К. А. , Зоров Н. Б. Методы спектрального анализа. М. : МГУ, 1990. 5. Казицына Л. А. , Куплетская Н. Б. Применение УФ-, ИК- и ЯМР- спектроскопии в органической химии. М. : Высшая школа, 1971.
Литература 1. Основы аналитической химии. Кн. 2. Методы химического анализа. / Под ред. Ю. А. Золотова. 2 -е изд. М. : Высшая школа, 2004. 2. Аналитическая химия. Физические и физико-химические методы анализа. Под ред. О. М. Петрухина. М. : Химия, 2001. 3. Васильев В. П. Аналитическая химия. Кн. 2. Физико-химические методы анализа. М. : Дрофа, 2004. Дополнительная литература 1. Кристиан Г. Аналитическая химия. В 2 -х т. М. : БИНОМ, 2009. 2. Аналитическая химия. Проблемы и подходы: В 2 т. / Под ред. Р. Кельнера, Ж-М. Мерме, М. Отто, Н. Видмера. М. : Мир, 2004. 3. Отто М. Современные методы аналитической химии. В 2 т. М. : Техносфера, 2003. 4. Кузяков Ю. Я. , Семененко К. А. , Зоров Н. Б. Методы спектрального анализа. М. : МГУ, 1990. 5. Казицына Л. А. , Куплетская Н. Б. Применение УФ-, ИК- и ЯМР- спектроскопии в органической химии. М. : Высшая школа, 1971.
 Спасибо!
Спасибо!


