Обзорная лекция.ppt
- Количество слайдов: 63

АНАЛИТИЧЕСКАЯ ХИМИЯ

Аналитическая химия – наука об определении химического состава веществ и отчасти их химического строения. (Ю. А. Золотов)

Методы аналитической химии: Пробоотбора Разложения проб Обнаружения Разделения Определения
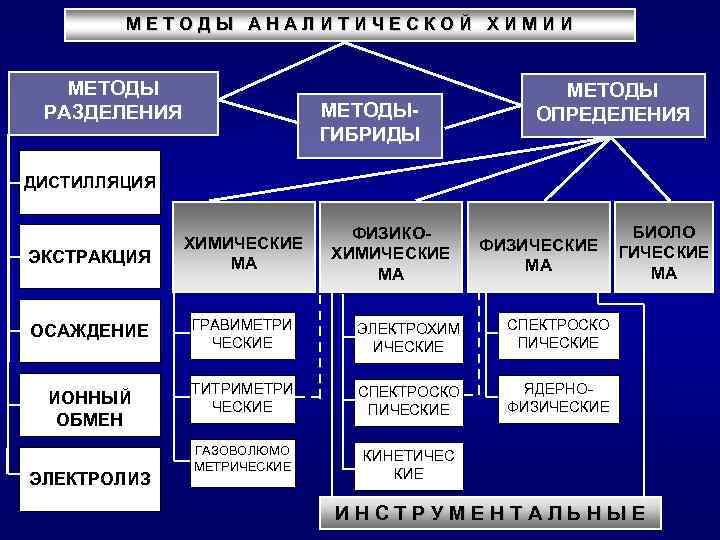
М Е Т О Д Ы А Н А Л И Т И Ч Е С К О Й Х И М И И МЕТОДЫ РАЗДЕЛЕНИЯ МЕТОДЫГИБРИДЫ МЕТОДЫ ОПРЕДЕЛЕНИЯ ДИСТИЛЛЯЦИЯ ФИЗИКОХИМИЧЕСКИЕ МА БИОЛО ФИЗИЧЕСКИЕ ГИЧЕСКИЕ МА МА ЭКСТРАКЦИЯ ХИМИЧЕСКИЕ МА ОСАЖДЕНИЕ ГРАВИМЕТРИ ЧЕСКИЕ ЭЛЕКТРОХИМ ИЧЕСКИЕ СПЕКТРОСКО ПИЧЕСКИЕ ТИТРИМЕТРИ ЧЕСКИЕ СПЕКТРОСКО ПИЧЕСКИЕ ЯДЕРНОФИЗИЧЕСКИЕ ГАЗОВОЛЮМО МЕТРИЧЕСКИЕ КИНЕТИЧЕС КИЕ ИОННЫЙ ОБМЕН ЭЛЕКТРОЛИЗ И Н С Т Р У М Е Н Т А Л Ь Н Ы Е

Метод анализа – достаточно универсальный и теоретически обоснованный способ определения состава вещества. Методика – подробное описание анализа данного объекта с использованием выбранного метода.

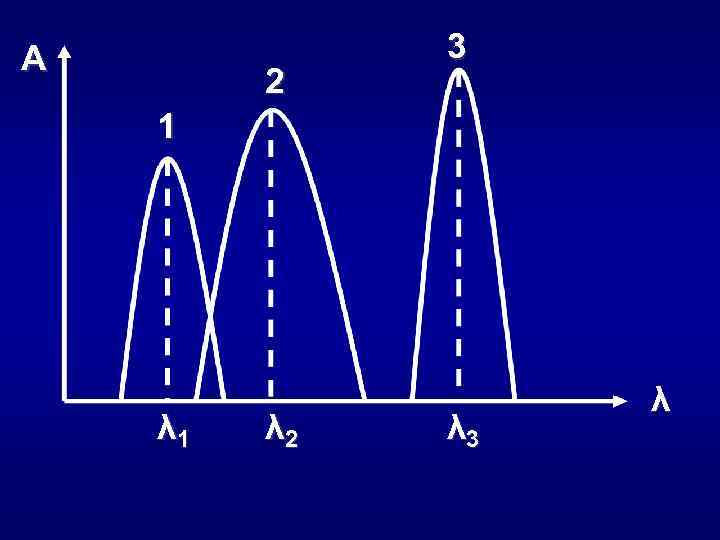
Аналитический сигнал – это среднее результатов измерения физической величины в заключительной стадии анализа, функционально связанное с содержанием определяемых компонентов.
А 2 3 1 λ 2 λ 3 λ

Химические методы анализа – методы анализа, в основе которых лежит химическая реакция и аналитический сигнал появляется в результате ее протекания. M + R = MR

Гравиметрический метод анализа Основан на осаждении компонента из раствора в виде малорастворимого соединения и определения массы осадка Ag+ + Cl− = Ag. Cl↓ осаждаемая форма гравиметрическая форма

Ca 2+ + C 2 O 42− = Ca. C 2 O 4↓ осажд. форма Ca. C 2 O 4 → Ca. O + CO 2 + CO грав. форма mопр. в = mгр. ф F F = Mопр. в / Mгр. в (F – фактор пересчета) ω(%) = (mопр. в / mнав) • 100%

Титриметрический анализ Основан на измерении объема раствора реагента, затраченного на химическую реакцию с определяемым веществом A + T = C + D CA = CT • VT / VA

Газоволюмометрический анализ Основан на измерении объема газообразных продуктов реакции V 1 (CO 2, C 2 H 4, N 2) → KOH → V 2 конц. (O 2, C 2 H 4, N 2) → Br 2 → V 3 (O 2, N 2) → водн. пирогаллол → V 4 (N 2) щел. раствор

ОСНОВНЫЕ ТИПЫ ХИМИЧЕСКИХ РЕАКЦИЙ, ПРИМЕНЯЕМЫХ В ХИМИЧЕСКОМ АНАЛИЗЕ 1. С переносом протона – кислотноосновные реакции. 2. С переносом электрона – окислительно-восстановительные реакции. 3. С переносом электронных пар с образованием донорно-акцепторных связей – реакции комплексообразования.

Знание константы равновесия химической реакции позволяет: − Предсказать направление ее протекания: К > 1 - равновесие сдвинуто вправо, К < 1 – равновесие сдвинуто влево, К = 1 - система находится в состоянии равновесия;

− Рассчитать степень протекания (выход) реакции; − Рассчитать концентрацию каждого из участников реакции в условиях равновесия; − Оценить влияние изменения концентрации каждого из реагирующих веществ на направление сдвига равновесия; − Оценить применимость химической реакции для целей количественного анализа (К > 106 – 108).

Физико-химические методы анализа – методы, в которых аналитический сигнал возникает в результате протекания химической реакции и измеряется с помощью прибора (потенциал электрода, электропроводность, оптическая плотность и т. д. ).

1. Электрохимические методы анализа. Основаны на явлениях, протекающих на электродах или в межэлектродном пространстве.

2. Спектроскопические методы анализа. Основаны на взаимодействии молекул вещества с электромагнитным излучением.

3. Кинетические методы анализа. Основаны на зависимости скорости химической реакции от концентрации определяемых веществ.

Физические методы анализа – методы, основанные на физических явлениях и процессах (испускание света веществом, ядерный и парамагнитный резонанс и т. д. ).

1. Спектроскопические методы анализа. Основаны на поглощении или испускании света атомами.

2. Ядерно-физические методы анализа. Основаны на явлении радиоактивности.

Биологические методы анализа – методы, основанные на применении живых организмов в качестве аналитических индикаторов

КЛАССИФИКАЦИЯ МЕТОДОВ АНАЛИЗА 1. Электрохимические методы анализа Измеряемая физическая Второстепенные № Название МА величина факторы (анал. сигнал) 1 Равновесный I Потенциометрия вн. цепи = 0 потенциал E = f(lg C) электрода Е, В Используются ИСЭ E = f (Vт) Прямая потенциметрия Ионометрия Потенциометрическое титрование

2 Сила тока I = f (Евн. ) Вольтамперометрия I, мк. А, А Используется р. к. э. Полярография I = f (с) Прямая вольтамперометрия Электрорастворение Инверсионная предварительно сконцентрирован ного на электроде определяемого вещества I = f (Vт) вольтамперометрия Амперометрическое титрование

3 Электропровод- I~(1000 Гц) ность W, Ом-1 W = f(C ) W = f (V т ) 4 Количество электричества Q, Кл Прямая Кондуктометрическое титрование I = const, Кулонометрия y = f (t) Кулонометрическое титрование Прямая кулонометрия E = const 5 Масса, г Кондуктометрия Электрогравиметрия

Спектроскопические методы анализа (Физико-химические методы анализа) № Измеряемая физическая величина (анал. сигнал) Второстепенные факторы Название метода Абсорбционная 1 Поглощение молекулярная спектроскопия молекулами (фотометрия – старое бл. УФ и название) видимого а) измерение идет Колориметрия излучения с помощью глаза б) с помощью Фотометрия Оптическая фотоэлемента плотность А (монохроматическ Спектрофотометрия ий свет)

2 Рассеяние света веществом 3 Поглощение света веществом с последующим испусканием др. фотонов а) измерение интенсивности прошедшего света б) измерение интенсивности рассеянного света Турбидиметрия Нефелометрия Люминесценция

Спектроскопические методы анализа (Физические методы анализа) № Измеряемая физическая величина (анал. сигнал) Второстепенные факторы 1 Излучение а) измерение УФ-и видимого излучения при света веществом возбуждении атомов в дуге или искре б) измерение УФ-и видимого излучения при возбуждении атомов в пламени в) рентгеновское излучение атомов после облучения рентгеновскими лучами Название метода Эмиссионный спектральный анализ Пламенная фотометрия (эмис. фотом. пламени) Рентгенофлуорес центный анализ

2 Поглощение света а) поглощение УФ -и видимого света атомами б) поглощение молекулами ИК излучения в) поглощение атомами рн излучения Атомноабсорбционный анализ ИК-спектроскопия рн-спектроскопия
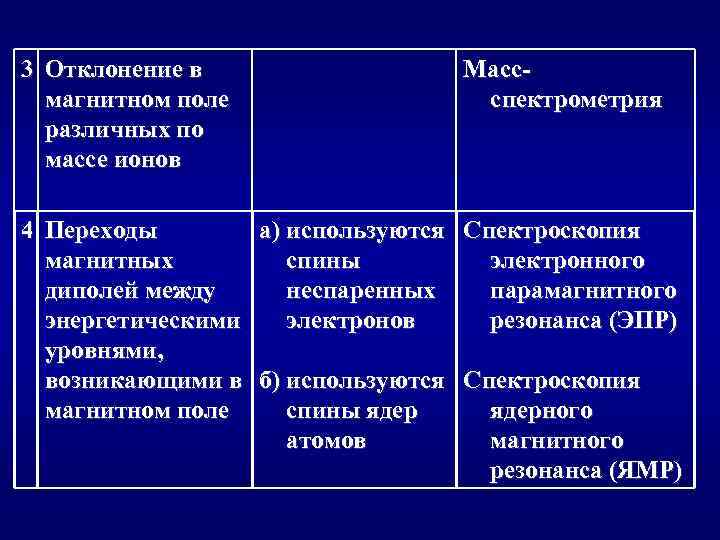
3 Отклонение в магнитном поле различных по массе ионов Массспектрометрия 4 Переходы а) используются Спектроскопия магнитных спины электронного диполей между неспаренных парамагнитного энергетическими электронов резонанса (ЭПР) уровнями, возникающими в б) используются Спектроскопия магнитном поле спины ядерного атомов магнитного резонанса (ЯМР)

Сопоставление методов анализа При выборе и сравнении методов анализа используют метрологические и аналитические характеристики – показатели качества анализа. Метрология – наука об измерениях. С позиции метрологии химический анализ есть измерение химического состава вещества.

АНАЛИТИЧЕСКИЕ ХАРАКТЕРИСТИКИ Характеристики качества результатов анализа Экономические характеристики Правильность Воспроизводимость Продолжительность анализа Особые меры безопасности Погрешность Стоимость Точность - оборудования Чувствительность - обучения персонала Диапазон определяемых содержаний Избирательность (селективность) - реактивов - капитальных затрат
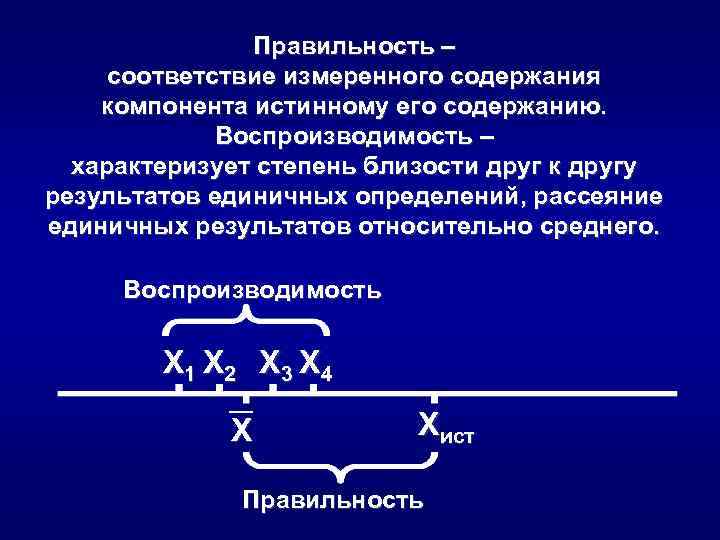
Правильность – соответствие измеренного содержания компонента истинному его содержанию. Воспроизводимость – характеризует степень близости друг к другу результатов единичных определений, рассеяние единичных результатов относительно среднего. Воспроизводимость Х 1 Х 2 Х 3 Х 4 Х Хист Правильность

Результаты правильные и хорошо воспроизводимые Результаты хорошо воспроизводимые, но неправильные Результаты правильные, но плохо воспроизводимые Результаты неправильные и плохо воспроизводимые

Погрешность – отклонение результатов анализа от истинного содержания определяемого компонента. Точность – понятие собирательное, качественное, характеризующее метод и включающее правильность и воспроизводимость.
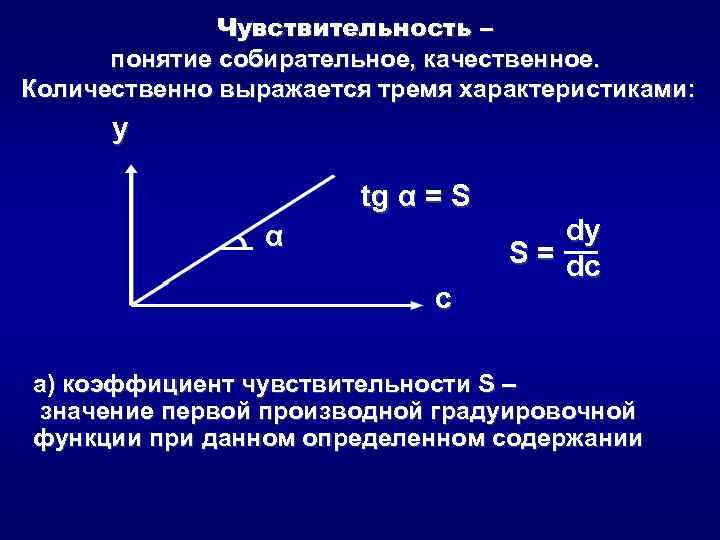
Чувствительность – понятие собирательное, качественное. Количественно выражается тремя характеристиками: y tg α = S α c dy S = dc а) коэффициент чувствительности S – значение первой производной градуировочной функции при данном определенном содержании

б) предел обнаружения Сmin, p – наименьшее содержание, при котором по данной методике можно обнаружить присутствие компонента с заданной доверительной вероятностью в) нижняя граница определяемых содержаний Сн – наименьшее значение содержания компонента, определяемое по данной методике

Диапазон определяемых содержаний Сн –Св. Сн – нижняя граница, характеризует чувствительность метода, Св – верхняя граница, определяется собенностью данного метода. Избирательность (селективность) – возможность обнаружения или определения данным методом нужных компонентов без помех со стороны других. Если метод позволяет определить один компонент позволяет в присутствии других, то это специфический метод анализа.

Экспрессность – время, необходимое для выполнения анализа. Стоимость – стоимость выполнения анализа, включая затраты на реактивы, оборудование, содержание персонала и т. д.

Сравнение методов анализа 1. Чувствительность, Сн, г ФМА до 10 -16 радиофизические, масс-спектрометрия, атомно-абсорбционный анализ ФХМА до 10 -13 кинетические МА, газовая хроматография, инверсионная вольтамперометрия ХМА до 10 -9 гравиметрия, титриметрия (в отд. случаях) 2. Точность, относительная погрешность, % ФХМА кулонометрический – 0, 001 – 0, 1 ХМА гравиметрический – 0, 05 – 0, 2 титриметрический – 0, 1 – 0, 5 ФМА рентгенофлуоресцентный – 0, 1

3. Избирательность ФХМА ионометрия ФМА атомно-абсорбционный анализ БМА 4. Экспрессность Недеструктивные МА – ФМА эмиссионный спектральный анализ рентгеноспектральный ФХМА ионометрия (раствор) ХМА титриметрия (раствор) 5. Стоимость анализа Низкая – ХМА титриметрия, гравиметрия Умеренная – ФХМА потенциометрия, кулонометрия, кондуктометрия Средняя – ФХМА спектрофотометрия, вольтамперометрия ФМА эмиссионный спектральный анализ, ААА Высокая – ФМА

Абсолютные (безэталонные) и относительные (эталонные) методы анализа МА абс ФХМА отн прям y = f(c) косв y = f(v)

МЕТОДЫ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ: 1. Метод градуировочного графика 2. Метод стандартов 3. Метод добавок. y=SC
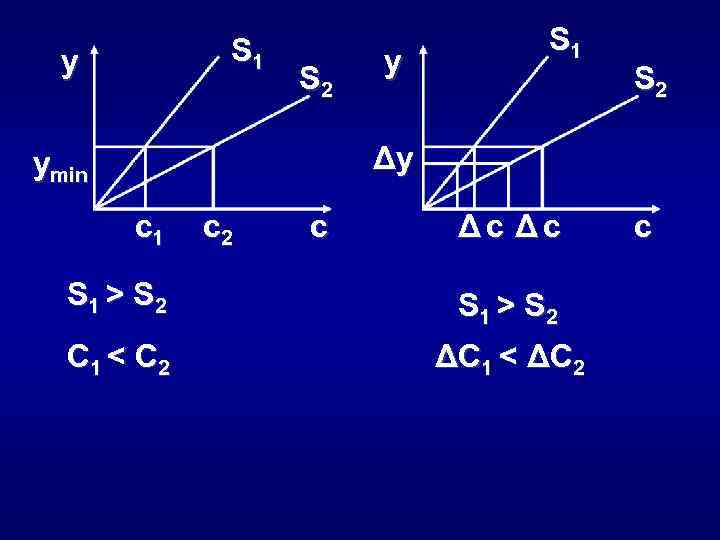
S 1 y S 2 y S 1 S 2 Δy ymin c 1 c 2 c Δc Δc S 1 > S 2 C 1 < C 2 ΔC 1 < ΔC 2 c
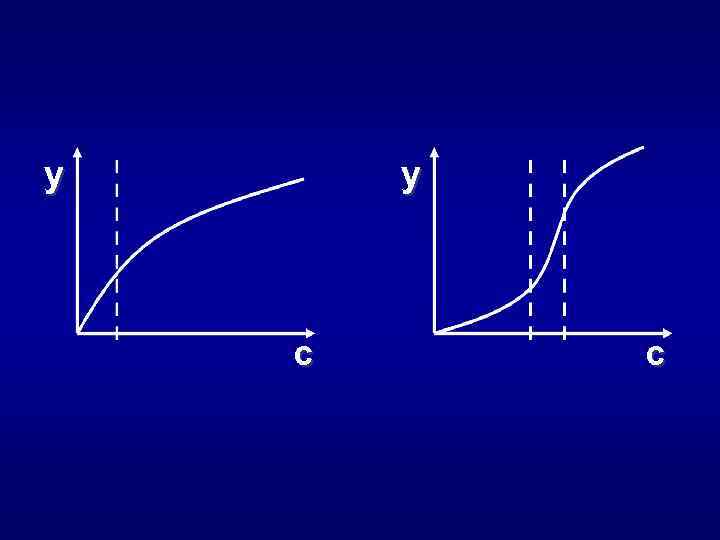
y y c c
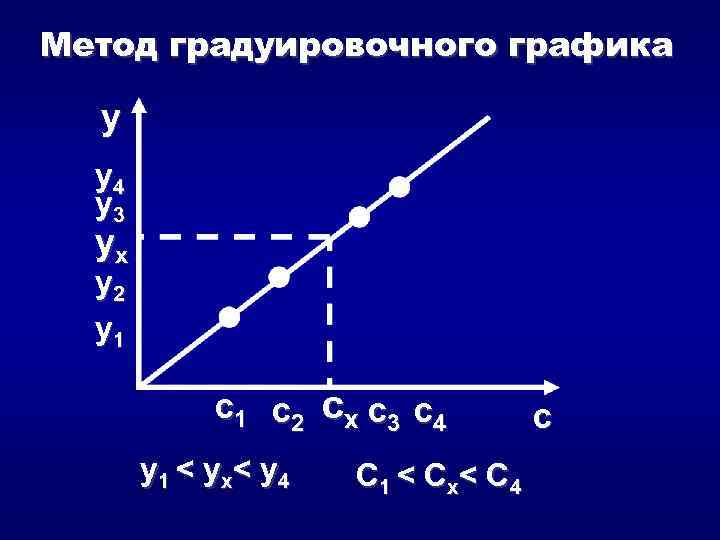
Метод градуировочного графика y y 4 y 3 yx y 2 y 1 c 2 cx c 3 c 4 y 1 < yx< y 4 C 1 < Cx< C 4 c

Метод стандартов yx = S Cx (1) yx Сx = yст Сст yст = S Cст (2) (S = const) yx Cст Cx = yст

Метод двух стандартов y = a + S C y 2 = a + S C 2 y 1 = a + S C 1 yx = a + S Cx C 1 < Cx < C 2 (yx – y 1) + C 1 (y 2 – yx) Cx = y 2 – y 1

Метод добавок yx = S Cx (3) yx+доб = S (Cx+ Сдоб) (4) yx+доб Cx+ Сдоб = yх Cx yх Сдоб Cx = yx+доб - yх
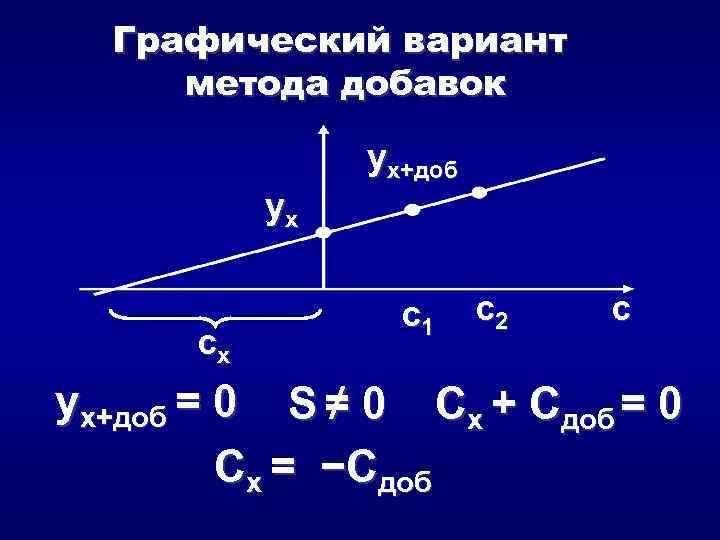
Графический вариант метода добавок yx+доб yx cx c 1 c 2 c yx+доб = 0 S ≠ 0 Cx + Сдоб = 0 Cx = −Сдоб

ТЕНДЕНЦИИ РАЗВИТИЯ АНАЛИТИЧЕСКОЙ ХИМИИ 1. Перемещение анализа из лабораторий к тем местам, где находится анализируемый объект

2. Миниатюризация анализа и его средств

3. Переход от покомпонентного анализа к распознаванию образа анализируемого объекта

4. Вещественный анализ

5. Автоматизация и компьютеризация анализа

6. Интенсификация процессов, используемых в анализе

7. Обеспечение и контроль качества анализа

8. Повышение точности и чувствительности аналитических методов

9. Гибридные методы

10. Микроанализ и нанотехнологии
11. Интеллектуальные сенсорные системы

Обзорная лекция.ppt