 Аммиак
Аммиак
 Строение молекулы Ковалентная связь по донорно-акцепторному механизму NH 3
Строение молекулы Ковалентная связь по донорно-акцепторному механизму NH 3
 Открытие аммиака Аммиак был открыт Дж. Пристли в 1774 г. и назван им щелочным воздухом или газом.
Открытие аммиака Аммиак был открыт Дж. Пристли в 1774 г. и назван им щелочным воздухом или газом.
 Физические свойства Аммиак (NH 3) представляет собой бесцветный газ, который легче воздуха. Аммиак обладает резко выраженным запахом нашатырного спирта. Этот газ очень ядовит и вреден для человека. Аммиак может находиться в сжиженном, жидком и твердом состоянии. Жидкий аммиак требует очень тщательного хранения в специальных емкостях, так как является сильнейшим растворителем веществ. В твердом состоянии аммиак выглядит как бесцветные кристаллы в виде кубиков. Облака Юпитера состоят из аммиака.
Физические свойства Аммиак (NH 3) представляет собой бесцветный газ, который легче воздуха. Аммиак обладает резко выраженным запахом нашатырного спирта. Этот газ очень ядовит и вреден для человека. Аммиак может находиться в сжиженном, жидком и твердом состоянии. Жидкий аммиак требует очень тщательного хранения в специальных емкостях, так как является сильнейшим растворителем веществ. В твердом состоянии аммиак выглядит как бесцветные кристаллы в виде кубиков. Облака Юпитера состоят из аммиака.
 Химические свойства 1. Разлагается при нагревании 2 NH 3 + 3 O 2 -> 2 N 2 + 6 H 2 O 2. Реагирует с водой NH 3 + H 2 O -> NH 4 + OH 3. Горит в кислороде 4 NH 3 + 3 O 2 -> 2 N 2 + 6 H 2 O Некоторые цветы, не имеющие запаха от природы, после обработки аммиаком начинают благоухать.
Химические свойства 1. Разлагается при нагревании 2 NH 3 + 3 O 2 -> 2 N 2 + 6 H 2 O 2. Реагирует с водой NH 3 + H 2 O -> NH 4 + OH 3. Горит в кислороде 4 NH 3 + 3 O 2 -> 2 N 2 + 6 H 2 O Некоторые цветы, не имеющие запаха от природы, после обработки аммиаком начинают благоухать.
 Химические свойства 4. Реагирует с кислотами NH 3 + HCl -> NH 4 Cl 5. В присутствии катализатора окисляется с образованием оксида азота(II) 4 NH 3 + 5 O 2 ->(в присутствии катал. ) 4 NO + 6 H 2 O Пары нашатырного спирта способны изменять окраску цветов. Например, голубые и синие лепестки становятся зелеными, ярко красные — черными
Химические свойства 4. Реагирует с кислотами NH 3 + HCl -> NH 4 Cl 5. В присутствии катализатора окисляется с образованием оксида азота(II) 4 NH 3 + 5 O 2 ->(в присутствии катал. ) 4 NO + 6 H 2 O Пары нашатырного спирта способны изменять окраску цветов. Например, голубые и синие лепестки становятся зелеными, ярко красные — черными
 Получение аммиака В лабораториях аммиак получают следующей реакцией Крупнейшие производители аммиака в России: ОАО «Тальяттиазот» ОАО НАК «Азот» ОАО «Акрон»
Получение аммиака В лабораториях аммиак получают следующей реакцией Крупнейшие производители аммиака в России: ОАО «Тальяттиазот» ОАО НАК «Азот» ОАО «Акрон»
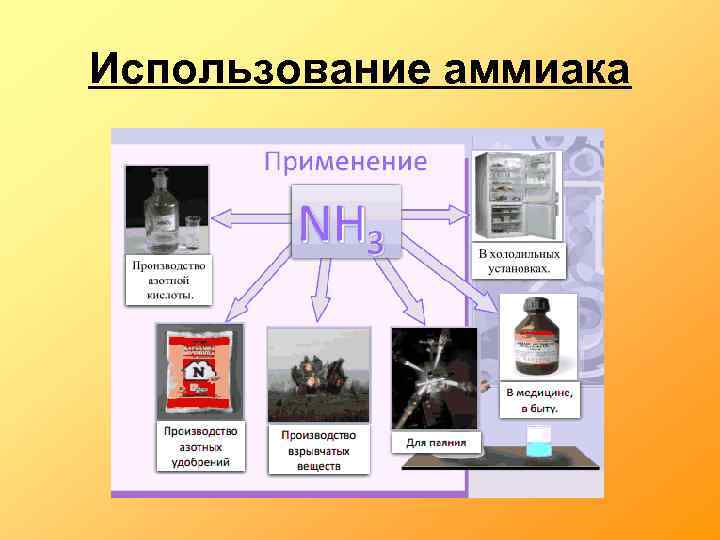 Использование аммиака
Использование аммиака
 Значение аммиака Сегодня аммиак — исключительной важности сырье для производства азотсодержащих веществ, применяемых в сельском хозяйстве, химии, медицине, военном деле. И что не менее важно, он является одним из продуктов белкового обмена в организме.
Значение аммиака Сегодня аммиак — исключительной важности сырье для производства азотсодержащих веществ, применяемых в сельском хозяйстве, химии, медицине, военном деле. И что не менее важно, он является одним из продуктов белкового обмена в организме.
 Конец презентации Спасибо за просмотр!! Автор презентации: Журавлев Владимир
Конец презентации Спасибо за просмотр!! Автор презентации: Журавлев Владимир