Аммиак 1.Строение, химическая связь H-N-H ( структурная формула)












![+ Соли аммония состоят из катиона [NH4] и аниона кислотного остатка. Пример: NH4Cl + Соли аммония состоят из катиона [NH4] и аниона кислотного остатка. Пример: NH4Cl](https://present5.com/presentacii-2/20171213\36500-47_au_.ppt\36500-47_au__14.jpg)





36500-47_au_.ppt
- Количество слайдов: 21
 Аммиак
Аммиак
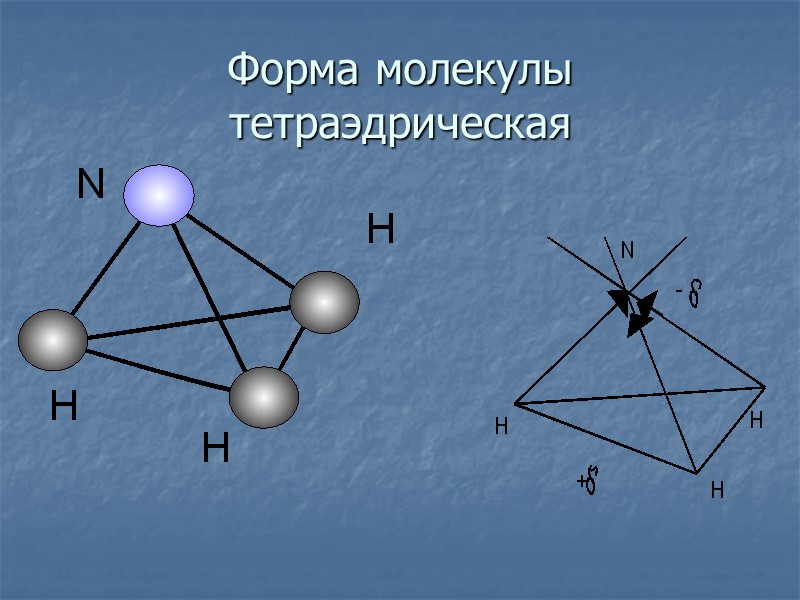
 1.Строение, химическая связь H-N-H ( структурная формула) | H Связь ковалентная полярная. Молекула полярная.
1.Строение, химическая связь H-N-H ( структурная формула) | H Связь ковалентная полярная. Молекула полярная.
 Форма молекулы тетраэдрическая
Форма молекулы тетраэдрическая
 Это особый вид химической межмолекулярной связи и называется эта связи - водородной Водородная связь-это химическая связь между атомами водорода одной молекулы и атомами очень электроотрицательных элементов (фтора, кислорода, азота), имеющих неподелённые электронные пары. Подобную связь образуют молекулы воды, спирта, фтороводорода.
Это особый вид химической межмолекулярной связи и называется эта связи - водородной Водородная связь-это химическая связь между атомами водорода одной молекулы и атомами очень электроотрицательных элементов (фтора, кислорода, азота), имеющих неподелённые электронные пары. Подобную связь образуют молекулы воды, спирта, фтороводорода.
 2.Получение. а) Промышленный способ: P=30МПа, t=450C, k N2 +3H2=2NH3 +Q где k-катализатор, в качестве которого используют Fe c Al2O3 или Pt
2.Получение. а) Промышленный способ: P=30МПа, t=450C, k N2 +3H2=2NH3 +Q где k-катализатор, в качестве которого используют Fe c Al2O3 или Pt
 б) Лабораторный способ: 2NH4Cl + Ca(OH)2=CaCl2 + 2NH3 +2H2O хлорид аммония
б) Лабораторный способ: 2NH4Cl + Ca(OH)2=CaCl2 + 2NH3 +2H2O хлорид аммония
 3.Физические свойства: а) газ б) без цвета в) с резким запахом г) очень хорошо растворим в воде ( в 1 объёме воды растворяется 700 объёмов NH3 д)tкип= -33.410С е) при повышенном давлении легко сжижается. ё) при испарении жидкого аммиака из окружающей среды поглощается много тепла.
3.Физические свойства: а) газ б) без цвета в) с резким запахом г) очень хорошо растворим в воде ( в 1 объёме воды растворяется 700 объёмов NH3 д)tкип= -33.410С е) при повышенном давлении легко сжижается. ё) при испарении жидкого аммиака из окружающей среды поглощается много тепла.
 4.Химические свойства: Реакции с изменением степени окисления азота а) Разложение при нагревании t 2 NH3= 3N2 +3H2 б) Реакции окислении аммиака 1.Горение 4NH3 + 3O2 = 2N20 +6 H2O 2.каталитическое окисление Pt,Rh 4NH3 + 5O2 = 4 NO + 6H2O
4.Химические свойства: Реакции с изменением степени окисления азота а) Разложение при нагревании t 2 NH3= 3N2 +3H2 б) Реакции окислении аммиака 1.Горение 4NH3 + 3O2 = 2N20 +6 H2O 2.каталитическое окисление Pt,Rh 4NH3 + 5O2 = 4 NO + 6H2O
 Донорно-акцепторная связь Такой механизм образования ковалентной связи, которая возникает не в результате обобществления непарных электронов, а благодаря свободной электронной паре, имеющейся у одного из атомов, называется донорно-акцепторным. донор- азот, акцептор – водород.
Донорно-акцепторная связь Такой механизм образования ковалентной связи, которая возникает не в результате обобществления непарных электронов, а благодаря свободной электронной паре, имеющейся у одного из атомов, называется донорно-акцепторным. донор- азот, акцептор – водород.
 гидрооксид аммония (раствор называется нашатырным спиртом) + _ NH3 +H2O NH4OHNH4 +OH гидроксид аммония проявляет все свойства щелочей !!!
гидрооксид аммония (раствор называется нашатырным спиртом) + _ NH3 +H2O NH4OHNH4 +OH гидроксид аммония проявляет все свойства щелочей !!!
 г) Реакции с кислотами Аммиак слабое основание и водные растворы его обладают щелочной реакцией. NH3 образует соли аммония (кислые и средние) почти со всеми известными кислотами:
г) Реакции с кислотами Аммиак слабое основание и водные растворы его обладают щелочной реакцией. NH3 образует соли аммония (кислые и средние) почти со всеми известными кислотами:
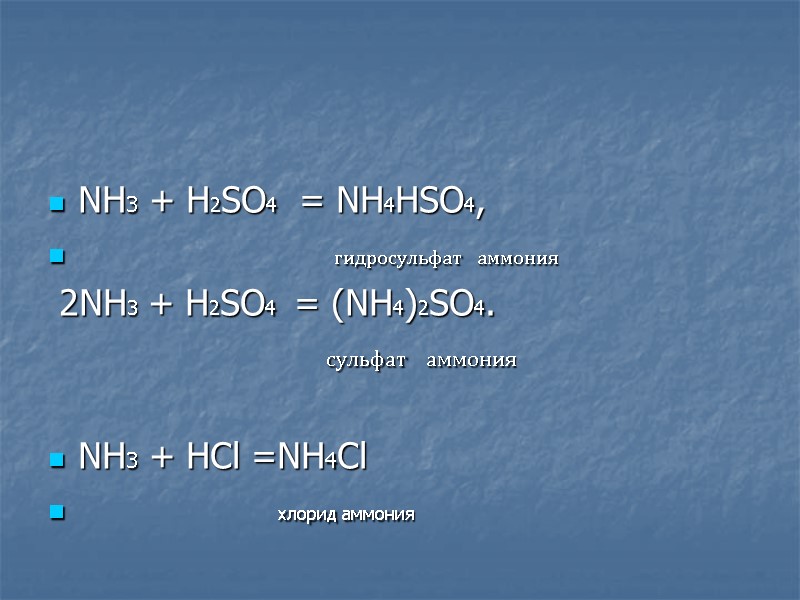
 NH3 + H2SO4 = NH4HSO4, гидросульфат аммония 2NH3 + H2SO4 = (NH4)2SO4. сульфат аммония NH3 + HCl =NH4Cl хлорид аммония
NH3 + H2SO4 = NH4HSO4, гидросульфат аммония 2NH3 + H2SO4 = (NH4)2SO4. сульфат аммония NH3 + HCl =NH4Cl хлорид аммония
 5.Применение. а) производство азотной кислоты б) производство удобрений в) нашатырный спирт г) взрывчатые вещества д) в быту е) в холодильных установках
5.Применение. а) производство азотной кислоты б) производство удобрений в) нашатырный спирт г) взрывчатые вещества д) в быту е) в холодильных установках
![>+ Соли аммония состоят из катиона [NH4] и аниона кислотного остатка. Пример: NH4Cl >+ Соли аммония состоят из катиона [NH4] и аниона кислотного остатка. Пример: NH4Cl](https://present5.com/presentacii-2/20171213\36500-47_au_.ppt\36500-47_au__14.jpg) + Соли аммония состоят из катиона [NH4] и аниона кислотного остатка. Пример: NH4Cl , NH4NO3 NH4HSO4 , ( NH4)2SO4 NH4H2PO4 (NH4)2HPO4 (NH4)3PO3 Соли аммония
+ Соли аммония состоят из катиона [NH4] и аниона кислотного остатка. Пример: NH4Cl , NH4NO3 NH4HSO4 , ( NH4)2SO4 NH4H2PO4 (NH4)2HPO4 (NH4)3PO3 Соли аммония
 2.Физические свойства: а) твёрдые вещества б) кристаллического строения- ионные кр. решётки в) хорошо растворимые в воде.
2.Физические свойства: а) твёрдые вещества б) кристаллического строения- ионные кр. решётки в) хорошо растворимые в воде.
 3 .Химические свойства: Общие с другими солями + - а)NH4Cl=NH4 +Cl б)2 NH4Cl +H2SO4= ( NH4)2SO4 +2HCl сухая соль в) NH4Cl +AgNO=3AgCl+ NH4NO3 р-р р-р р-р Специфические г)реакция с щелочами - качественная реакция NH4Cl +NaOH=NH4OH+NaCl /\ NH3 H2O Появляется резкий запах аммиака д) при нагревании разлагаются t NH4CI=NH3 +HCl
3 .Химические свойства: Общие с другими солями + - а)NH4Cl=NH4 +Cl б)2 NH4Cl +H2SO4= ( NH4)2SO4 +2HCl сухая соль в) NH4Cl +AgNO=3AgCl+ NH4NO3 р-р р-р р-р Специфические г)реакция с щелочами - качественная реакция NH4Cl +NaOH=NH4OH+NaCl /\ NH3 H2O Появляется резкий запах аммиака д) при нагревании разлагаются t NH4CI=NH3 +HCl
 4. Применение солей аммония: NH4NO3- минеральное удобрение NH4Cl- используют при паянии, так как он очищает поверхность металла от оксидной пленки NH4HCO3 - используют в кондитерском деле (NH4HCO3=NH3+ H2O+CO2) (NH4)2CO3- используют в кондитерском деле NH4NO3 +C(уголь) +Al (пудра)-используют в качестве взрывчатого вещества.
4. Применение солей аммония: NH4NO3- минеральное удобрение NH4Cl- используют при паянии, так как он очищает поверхность металла от оксидной пленки NH4HCO3 - используют в кондитерском деле (NH4HCO3=NH3+ H2O+CO2) (NH4)2CO3- используют в кондитерском деле NH4NO3 +C(уголь) +Al (пудра)-используют в качестве взрывчатого вещества.
 Биологическая роль. Аммиак является конечным продуктом азотистого обмена в организме человека и животных. Аммиак может также использоваться печенью для обратного процесса — ресинтеза аминокислот из аммиака и кетоаналогов аминокислот.
Биологическая роль. Аммиак является конечным продуктом азотистого обмена в организме человека и животных. Аммиак может также использоваться печенью для обратного процесса — ресинтеза аминокислот из аммиака и кетоаналогов аминокислот.
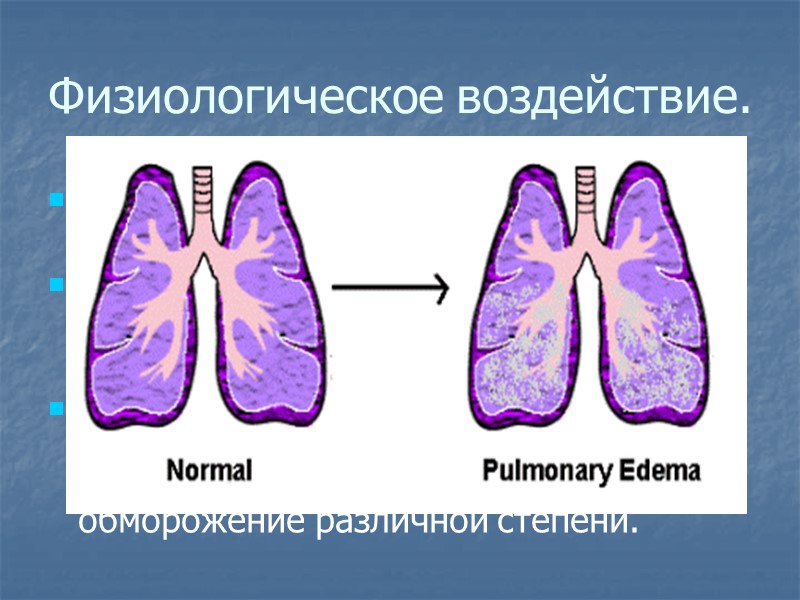
 Физиологическое воздействие. Вызывает токсический отёк лёгких и тяжёлое поражение нервной системы. Раздражает слизистые оболочки глаз и органов дыхания, а также кожные покровы. Кроме того, сжиженный аммиак при испарении поглощает тепло, и при соприкосновении с кожей возникает обморожение различной степени.
Физиологическое воздействие. Вызывает токсический отёк лёгких и тяжёлое поражение нервной системы. Раздражает слизистые оболочки глаз и органов дыхания, а также кожные покровы. Кроме того, сжиженный аммиак при испарении поглощает тепло, и при соприкосновении с кожей возникает обморожение различной степени.
 Интересные факты: Пары нашатырного спирта способны изменять окраску цветов. Например, голубые и синие лепестки становятся зелеными, ярко красные — черными. Облака Юпитера состоят из аммиака. Некоторые цветы, не имеющие запаха от природы, после обработки аммиаком начинают благоухать. Например, приятный аромат приобретают астры
Интересные факты: Пары нашатырного спирта способны изменять окраску цветов. Например, голубые и синие лепестки становятся зелеными, ярко красные — черными. Облака Юпитера состоят из аммиака. Некоторые цветы, не имеющие запаха от природы, после обработки аммиаком начинают благоухать. Например, приятный аромат приобретают астры
 Вывод: Аммиак- это химическое вещество, которая является одним из ключевых составляющим во всех сферах применения. Он так же является веществом, без которого наш организм не сможет функционировать.
Вывод: Аммиак- это химическое вещество, которая является одним из ключевых составляющим во всех сферах применения. Он так же является веществом, без которого наш организм не сможет функционировать.

