аммиак.ppt
- Количество слайдов: 18

Аммиак өндірісі

Оқу мақсаттары: Ú -аммиак өндірісінің үрдісін білу Ú - аммиакты өндіру тепе-теңдік процесс деп түсініп, сыртқы жағдайлардың өзгеруін мақсатты өнім шығымына әсерін болжай алу. Ú - аммиактың тұтынушы негізгі өндірістік аймақтарын білу Ú - аммиак өндірісінің экологиялық салдарын және зауыттар қалдықтарының көлемін азайту тәсілдерін түсіну

Жетістік критерийлері: -Аммиак өндірісін сипаттай алады; -Өнім шығымын қалай арттыруға болатын ұсына алады; -Аммиактың негізгі қолданылу аясын біледі; -Аммиак өндірісінің экологиялық салдарын түсіндіре алады;

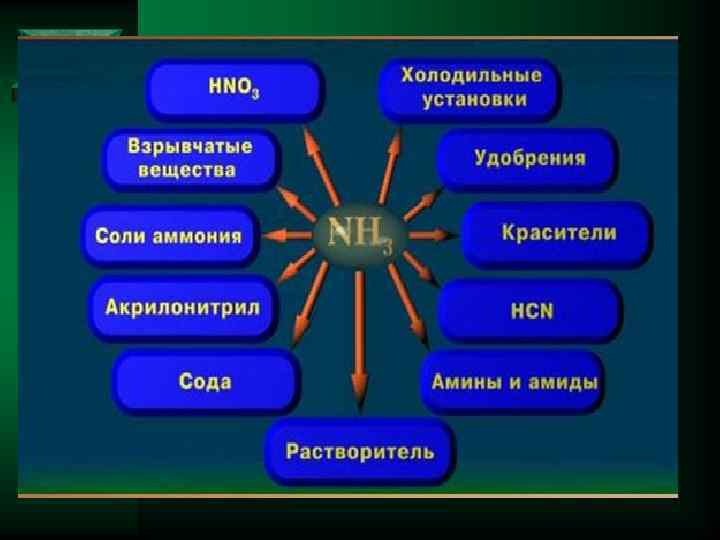
Аммиак қандай зат? ? ? Лабораторияда аммиак қалай алынады? Структура молекулы NH 3


Есеп № 1 Азот пен сутек әрекеттескен кезде 35% шығыммен массасы 95 г аммиак алынды. Осы реакцияны жүргізу үшін қажетті сутек пен азот газының көлемін есептеңдер.

N 2 + 3 H 2 → 2 NH 3 + Q. Өнімнің шығымын қалай арттыруға болады?
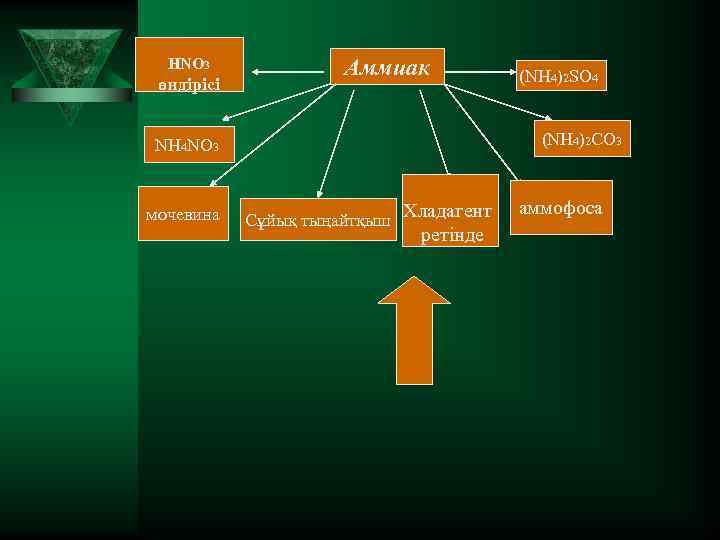
HNO 3 өндірісі Аммиак (NH 4)2 CO 3 NH 4 NO 3 мочевина (NH 4)2 SO 4 Сұйық тыңайтқыш Хладагент ретінде аммофоса

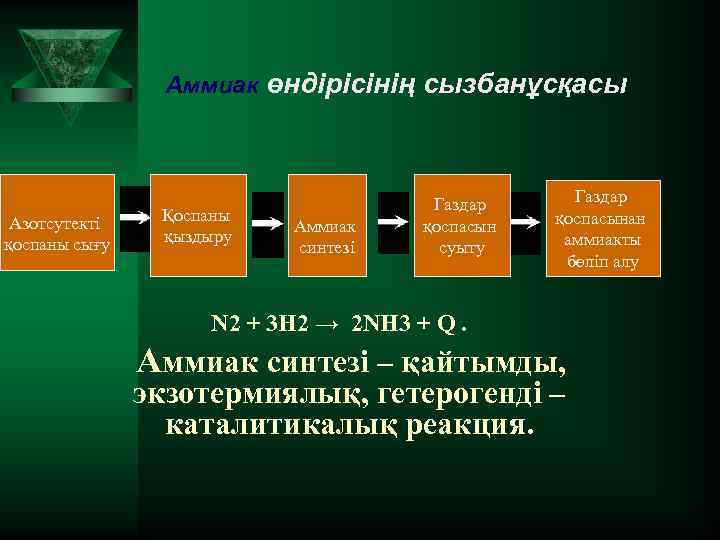
Аммиак өндірісінің сызбанұсқасы Азотсутекті қоспаны сығу Қоспаны қыздыру Аммиак синтезі Газдар қоспасын суыту Газдар қоспасынан аммиакты бөліп алу N 2 + 3 H 2 → 2 NH 3 + Q. Аммиак синтезі – қайтымды, экзотермиялық, гетерогенді – каталитикалық реакция.

Аммиак өндіріс жағдайлары: Қысым - 300 -350 МПа шығым жоғары болады Проблема: үрдіс жоғары қысымда және температурада жүруі қажет. Мұндай жағдайда азот пен сутек қондырғы материалымен реакцияға түсіп кетеді. Сондықтан қондырғы өте берік және инертті материалдан жасалуы қажет. Мұндай материал өте қымбат. 300 МПа қысымда аммиак синтезін жүзеге асыру қымбат әрі қауіпті өндіріске жатады.

Үй жұмысы 1 -есеп Өндірісте аммиакты Габер процесі арқылы алады. 67, 2 л (қ. ж. ) сутек азотпен әрекеттескен кезде 17 г аммиак алынды. Теориялық мүмкіндікпен салыстырғанда пайыз түріндегі реакция өнімінің шығымы нешеге тең болады? 2 -есеп Аммиактың тотығу реакциясының теңдеуін жазыңыздар. Азотты тыңайтқыштар жайында хабарлама дайындап келу.

Нахождение в природе Небольшие количества аммиака находятся в воздухе в виде углекислой и азотнокислой соли аммония, откуда они уносятся атмосферными осадками, как например дождем, росой, снегом и достигают таким образом поверхности земли уже в более концентрированном состоянии; поглощенный почвою аммиак является важным питательным материалом для растительных организмов и преобразуется ими в белки и прочие необходимые составные части растении.

Действие на организм При содержании в воздухе 0, 5% по объему аммиак сильно раздражает слизистые оболочки. При остром отравлении поражаются глаза и дыхательных пути, при хронических отравлениях наблюдаются расстройство пищеварения, ослабление слуха. Жидкий аммиак вызывает сильные ожоги кожи. Смесь аммиака с воздухом взрывоопасна

Аммиак был открыт Дж. Пристли в 1774 г. и назван им щелочным воздухом или газом. Твердый аммиак - бесцветные кристаллы с кубической решеткой (а = =0, 515 нм, 2 = 4, пространств, группа Р 213). Жидкий аммиак растворяет щелочные и щел. -зем. металлы, Al, Eu, Yb, P, S, I, мн. интерметаллиды.
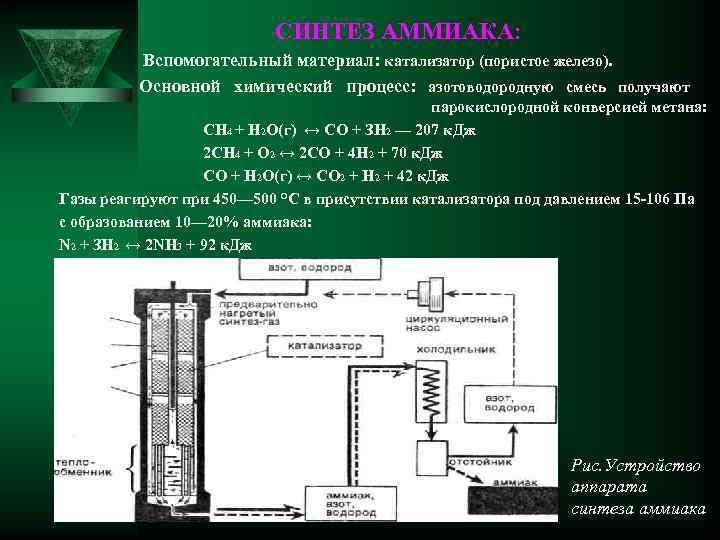
СИНТЕЗ АММИАКА: Вспомогательный материал: катализатор (пористое железо). Основной химический процесс: азотоводородную смесь получают парокислородной конверсией метана: СН 4 + Н 2 O(г) ↔ СО + ЗН 2 — 207 к. Дж 2 СН 4 + O 2 ↔ 2 СО + 4 Н 2 + 70 к. Дж СО + Н 2 O(г) ↔ СO 2 + Н 2 + 42 к. Дж Газы реагируют при 450— 500 °С в присутствии катализатора под давлением 15 -106 Па с образованием 10— 20% аммиака: N 2 + ЗН 2 ↔ 2 NН 3 + 92 к. Дж Рис. Устройство аппарата синтеза аммиака
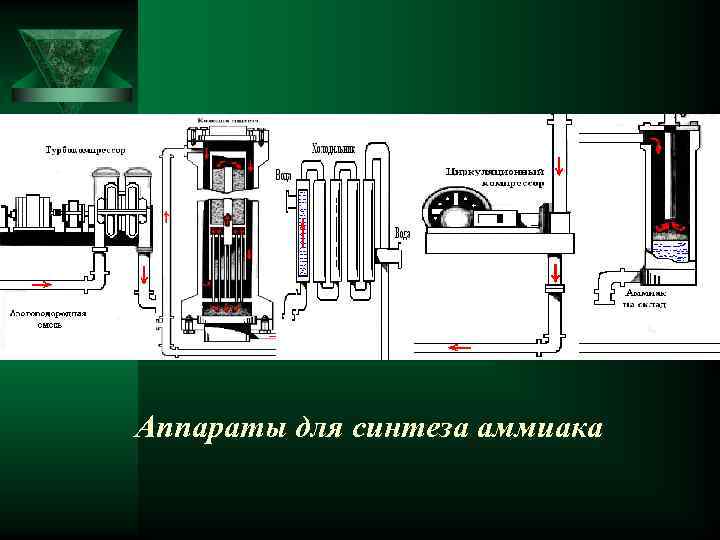
Аппараты для синтеза аммиака
аммиак.ppt