 Амины. Анилин.
Амины. Анилин.
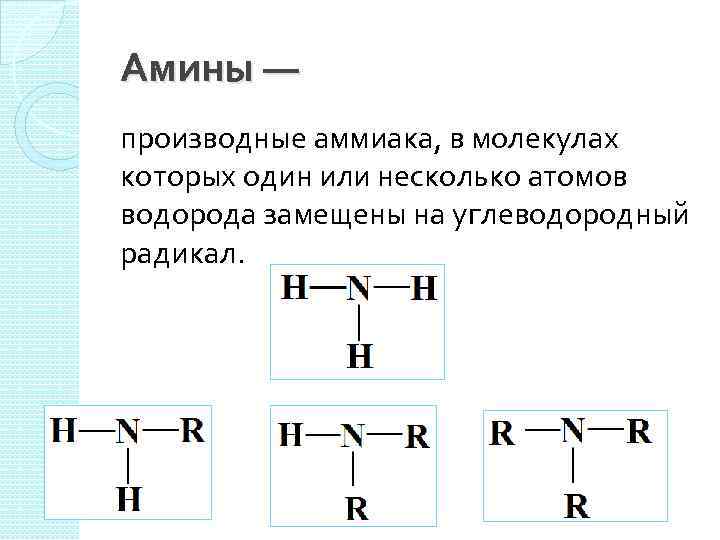 Амины — производные аммиака, в молекулах которых один или несколько атомов водорода замещены на углеводородный радикал.
Амины — производные аммиака, в молекулах которых один или несколько атомов водорода замещены на углеводородный радикал.
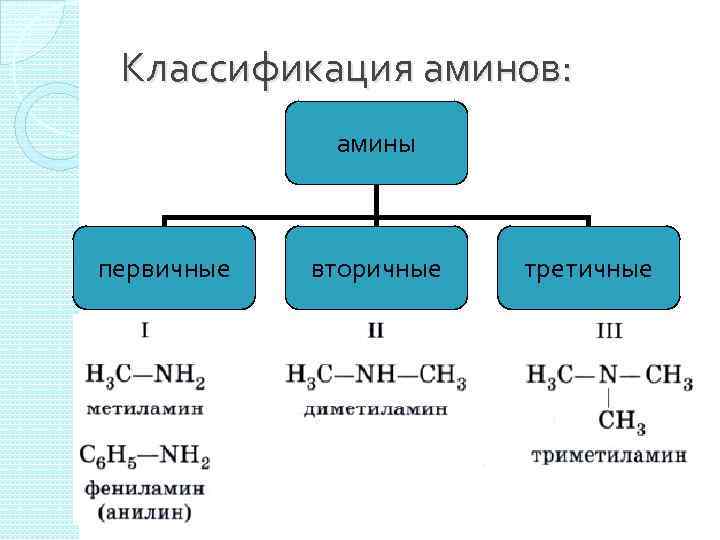 Классификация аминов: амины первичные вторичные третичные
Классификация аминов: амины первичные вторичные третичные
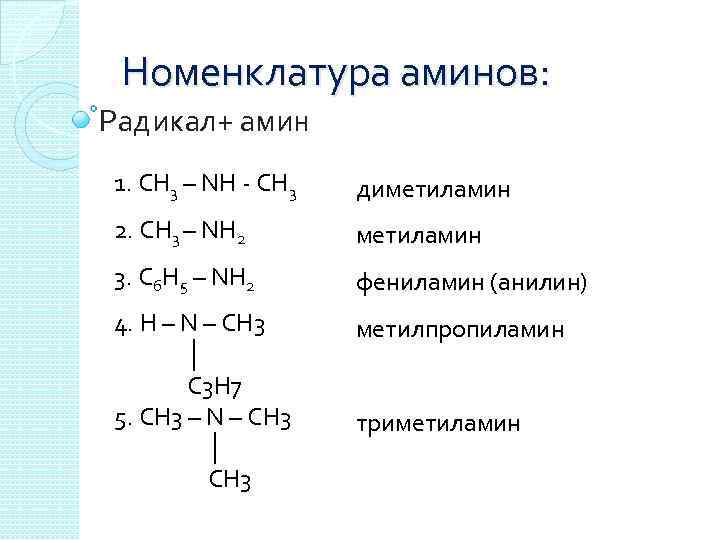 Номенклатура аминов: Радикал+ амин 1. СН 3 – NН - СН 3 диметиламин 2. СН 3 – NН 2 метиламин 3. С 6 Н 5 – NН 2 фениламин (анилин) 4. H – N – CH 3 │ С 3 Н 7 5. CH 3 – N – CH 3 │ СН 3 метилпропиламин триметиламин
Номенклатура аминов: Радикал+ амин 1. СН 3 – NН - СН 3 диметиламин 2. СН 3 – NН 2 метиламин 3. С 6 Н 5 – NН 2 фениламин (анилин) 4. H – N – CH 3 │ С 3 Н 7 5. CH 3 – N – CH 3 │ СН 3 метилпропиламин триметиламин
 Строение и свойства Аммиак NH 3 Строение атома азота 1 s 22 p 3 Строение атома водорода 1 s 1 Атом азота имеет неподеленную электронную пару Аммиак проявляет основный характер Амин CH 3 NH 2 Амины органические основания C 6 H 5←NH 2 Основный характер выражен слабее, чем у аммиака CH 3→NH 2 Основный характер выражен сильнее, чем у аммиака
Строение и свойства Аммиак NH 3 Строение атома азота 1 s 22 p 3 Строение атома водорода 1 s 1 Атом азота имеет неподеленную электронную пару Аммиак проявляет основный характер Амин CH 3 NH 2 Амины органические основания C 6 H 5←NH 2 Основный характер выражен слабее, чем у аммиака CH 3→NH 2 Основный характер выражен сильнее, чем у аммиака
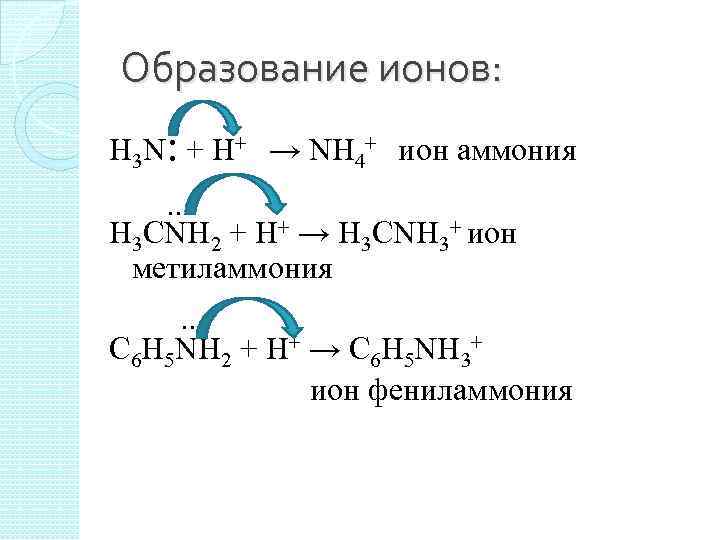 Образование ионов: H 3 N: + H+ → NH 4+ ион аммония. . H 3 CNH 2 + H+ → H 3 CNH 3+ ион метиламмония. . C 6 H 5 NH 2 + H+ → C 6 H 5 NH 3+ ион фениламмония
Образование ионов: H 3 N: + H+ → NH 4+ ион аммония. . H 3 CNH 2 + H+ → H 3 CNH 3+ ион метиламмония. . C 6 H 5 NH 2 + H+ → C 6 H 5 NH 3+ ион фениламмония
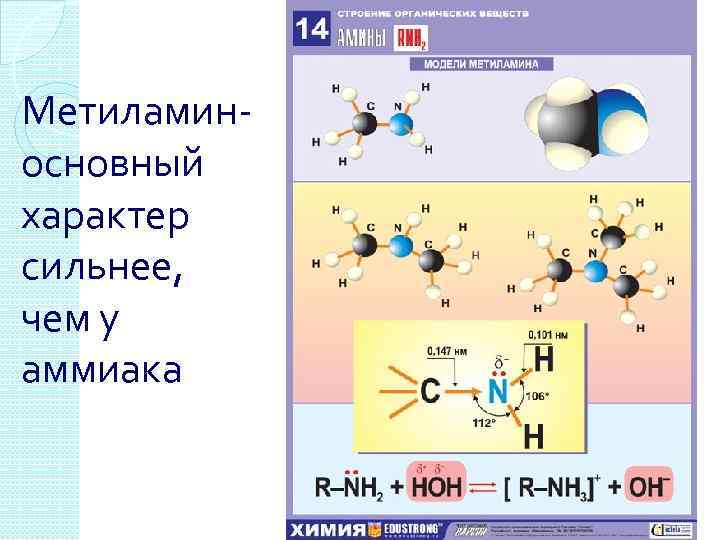 Метиламиносновный характер сильнее, чем у аммиака
Метиламиносновный характер сильнее, чем у аммиака
![Химические свойства CH 3 NH 2+HOH→[CH 3 NH 3]OH Гидроксид метиламмония C 6 H Химические свойства CH 3 NH 2+HOH→[CH 3 NH 3]OH Гидроксид метиламмония C 6 H](https://present5.com/presentation/276359328_381424385/image-8.jpg) Химические свойства CH 3 NH 2+HOH→[CH 3 NH 3]OH Гидроксид метиламмония C 6 H 5 NH 2+HOH → не взаимодействует CH 3 NH 2+HCl → [CH 3 NH 3]Cl Хлорид метиламмония C 6 H 5 NH 2+HCl → [C 6 H 5 NH 3]Cl Хлорид фениламмония (хлористый анилин) 9 CH 3 NH 2+9 O 2 → 4 CO 2+2 N 2+10 H 2 O
Химические свойства CH 3 NH 2+HOH→[CH 3 NH 3]OH Гидроксид метиламмония C 6 H 5 NH 2+HOH → не взаимодействует CH 3 NH 2+HCl → [CH 3 NH 3]Cl Хлорид метиламмония C 6 H 5 NH 2+HCl → [C 6 H 5 NH 3]Cl Хлорид фениламмония (хлористый анилин) 9 CH 3 NH 2+9 O 2 → 4 CO 2+2 N 2+10 H 2 O
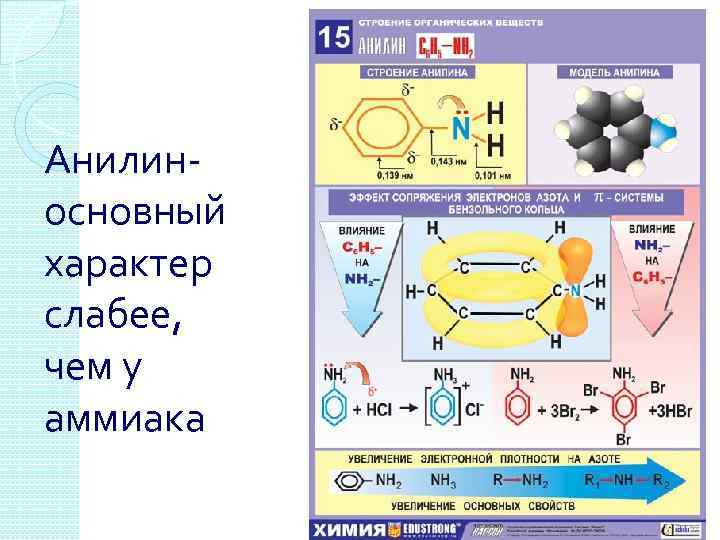 Анилиносновный характер слабее, чем у аммиака
Анилиносновный характер слабее, чем у аммиака
 Реакции замещения ароматических аминов Увеличивая электронную плотность в кольце, аминогруппа облегчает протекание реакций электрофильного замещения, то есть является активирующим заместителем. C 6 H 5 NH 2+3 Br 2→C 6 H 2 Br 3 NH 2+3 HBr
Реакции замещения ароматических аминов Увеличивая электронную плотность в кольце, аминогруппа облегчает протекание реакций электрофильного замещения, то есть является активирующим заместителем. C 6 H 5 NH 2+3 Br 2→C 6 H 2 Br 3 NH 2+3 HBr
 Получение аминов 1. Взаимодействие аммиака с галогенпроизводными углеводородов CH 3 Cl+2 NH 3→ →CH 3 NH 2+NH 4 Cl 2. Восстановление нитросоединений C 6 H 5 NO 2+3 H 2 → →C 6 H 5 NH 2+2 H 2 O
Получение аминов 1. Взаимодействие аммиака с галогенпроизводными углеводородов CH 3 Cl+2 NH 3→ →CH 3 NH 2+NH 4 Cl 2. Восстановление нитросоединений C 6 H 5 NO 2+3 H 2 → →C 6 H 5 NH 2+2 H 2 O
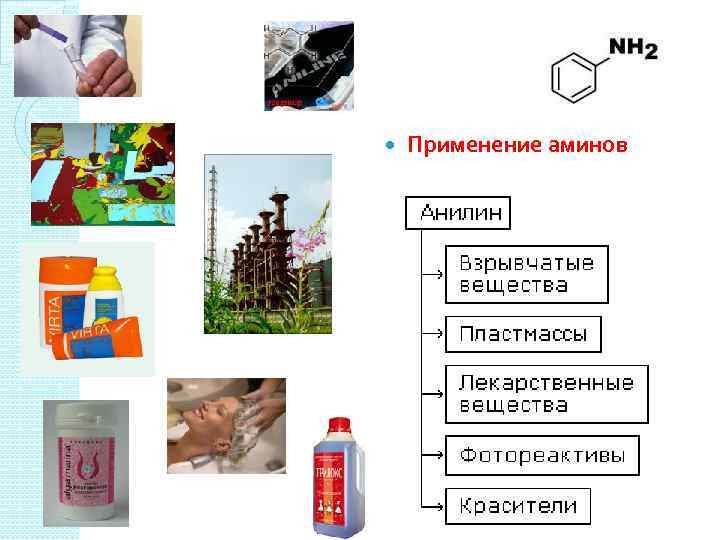 Применение аминов
Применение аминов
 Открытие анилина: Ф. Ф. Рунге кианол 1840 г. Ю. Ф. Фрицше анилин Унфердорбе н кристаллин 1841 г. Н. Н. Зинин бензидам 1843 г. Гофман доказал, что это одно вещество
Открытие анилина: Ф. Ф. Рунге кианол 1840 г. Ю. Ф. Фрицше анилин Унфердорбе н кристаллин 1841 г. Н. Н. Зинин бензидам 1843 г. Гофман доказал, что это одно вещество
 Домашнее задание: § 16, № 4, 5, с. 121
Домашнее задание: § 16, № 4, 5, с. 121