Амины.ppt
- Количество слайдов: 33
 Амины Алифатические амины Ароматические амины Алкилароматические амины 1
Амины Алифатические амины Ароматические амины Алкилароматические амины 1
 Способы получения Восстановление азотсодержащих соединений 2
Способы получения Восстановление азотсодержащих соединений 2
 Алкилирование аммиака и аминов Реакция переалкилирования Аминолиз (алкилирование аммиака и аминов спиртами) Процесс неселективный 3
Алкилирование аммиака и аминов Реакция переалкилирования Аминолиз (алкилирование аммиака и аминов спиртами) Процесс неселективный 3
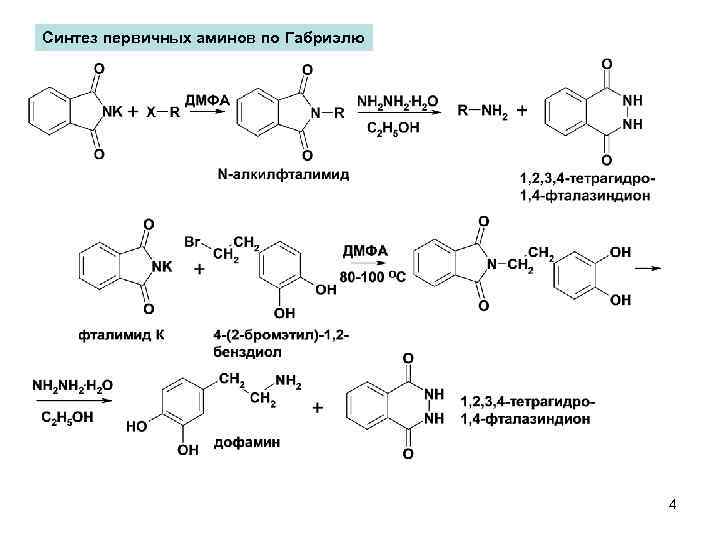 Синтез первичных аминов по Габриэлю 4
Синтез первичных аминов по Габриэлю 4
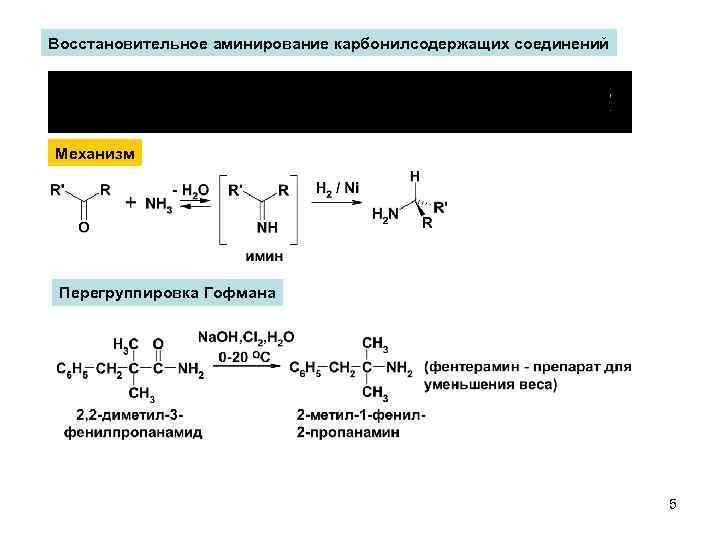 Восстановительное аминирование карбонилсодержащих соединений Механизм Перегруппировка Гофмана 5
Восстановительное аминирование карбонилсодержащих соединений Механизм Перегруппировка Гофмана 5
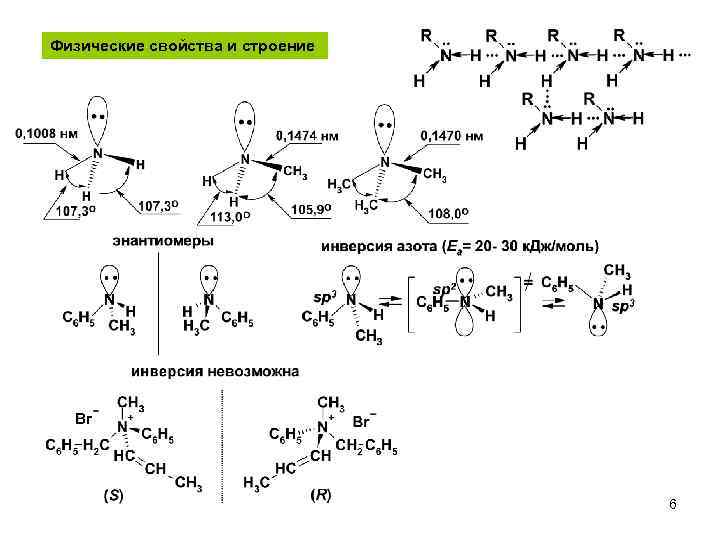 Физические свойства и строение 6
Физические свойства и строение 6
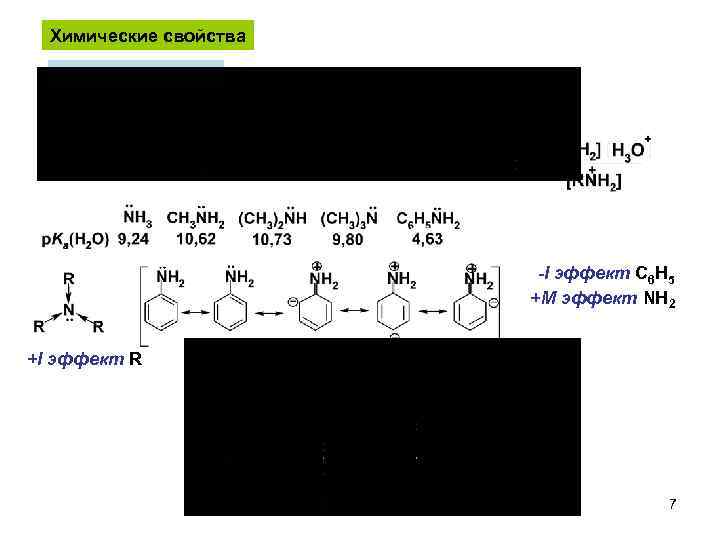 Химические свойства Основность аминов -I эффект C 6 H 5 +M эффект NH 2 +I эффект R 7
Химические свойства Основность аминов -I эффект C 6 H 5 +M эффект NH 2 +I эффект R 7
 Образование солей 8
Образование солей 8
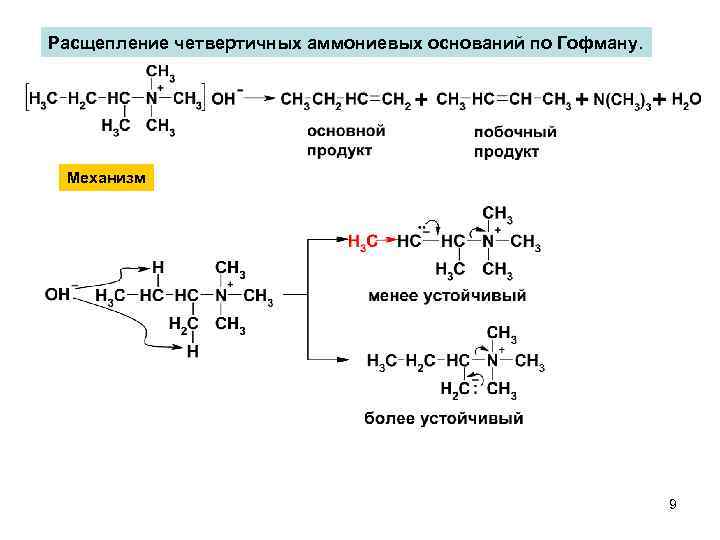 Расщепление четвертичных аммониевых оснований по Гофману. Механизм 9
Расщепление четвертичных аммониевых оснований по Гофману. Механизм 9
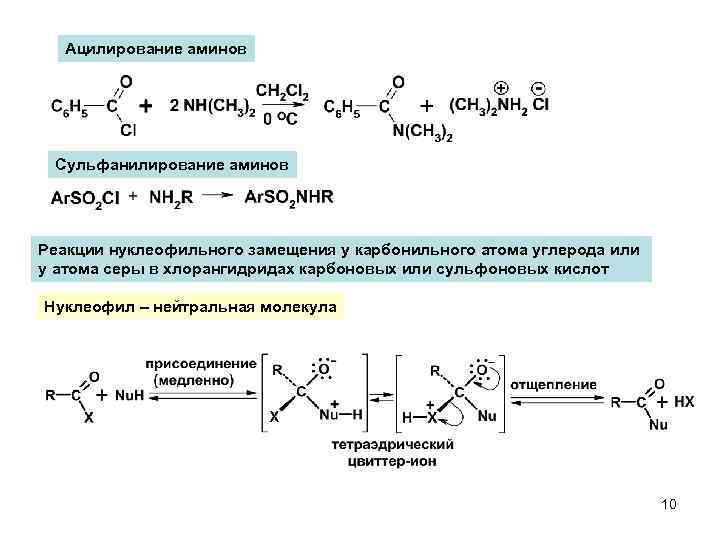 Ацилирование аминов Сульфанилирование аминов Реакции нуклеофильного замещения у карбонильного атома углерода или у атома серы в хлорангидридах карбоновых или сульфоновых кислот Нуклеофил – нейтральная молекула 10
Ацилирование аминов Сульфанилирование аминов Реакции нуклеофильного замещения у карбонильного атома углерода или у атома серы в хлорангидридах карбоновых или сульфоновых кислот Нуклеофил – нейтральная молекула 10
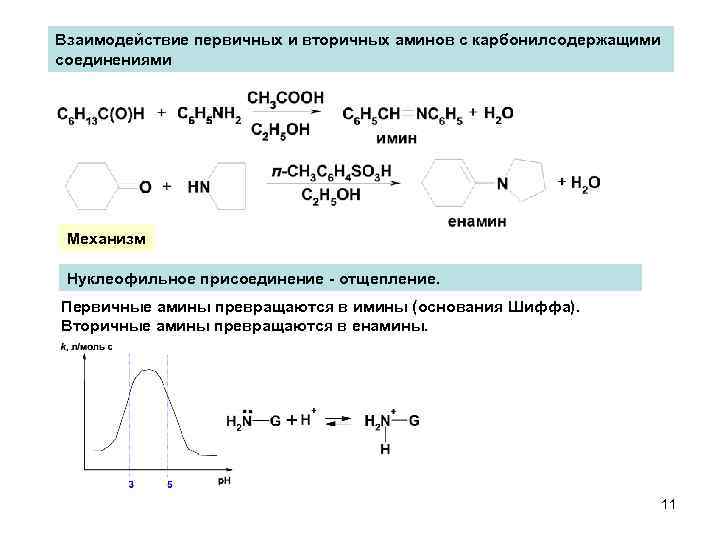 Взаимодействие первичных и вторичных аминов с карбонилсодержащими соединениями Механизм Нуклеофильное присоединение - отщепление. Первичные амины превращаются в имины (основания Шиффа). Вторичные амины превращаются в енамины. 11
Взаимодействие первичных и вторичных аминов с карбонилсодержащими соединениями Механизм Нуклеофильное присоединение - отщепление. Первичные амины превращаются в имины (основания Шиффа). Вторичные амины превращаются в енамины. 11
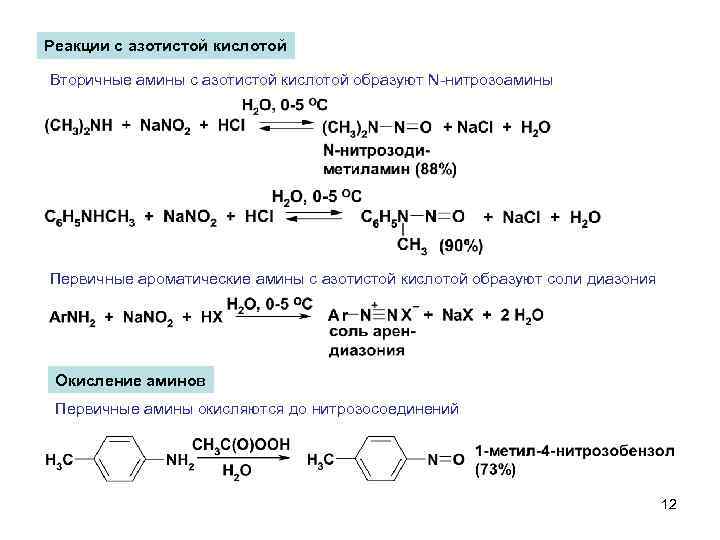 Реакции с азотистой кислотой Вторичные амины с азотистой кислотой образуют N-нитрозоамины Первичные ароматические амины с азотистой кислотой образуют соли диазония Окисление аминов Первичные амины окисляются до нитрозосоединений 12
Реакции с азотистой кислотой Вторичные амины с азотистой кислотой образуют N-нитрозоамины Первичные ароматические амины с азотистой кислотой образуют соли диазония Окисление аминов Первичные амины окисляются до нитрозосоединений 12
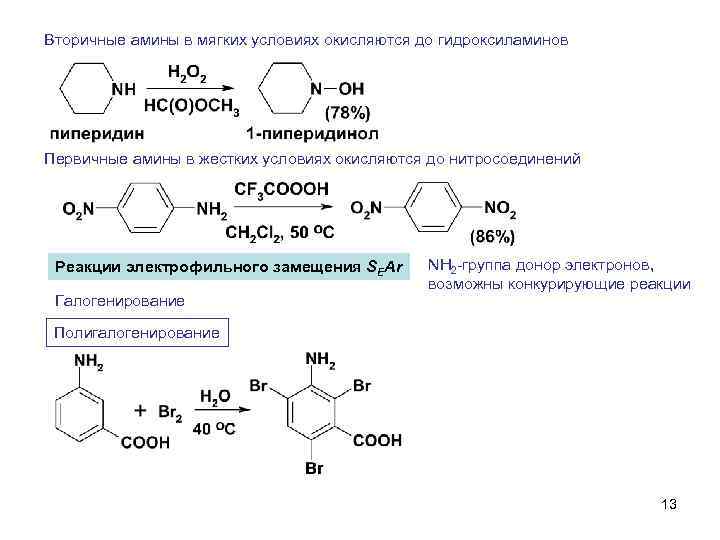 Вторичные амины в мягких условиях окисляются до гидроксиламинов Первичные амины в жестких условиях окисляются до нитросоединений Реакции электрофильного замещения SEAr Галогенирование NH 2 -группа донор электронов, возможны конкурирующие реакции Полигалогенирование 13
Вторичные амины в мягких условиях окисляются до гидроксиламинов Первичные амины в жестких условиях окисляются до нитросоединений Реакции электрофильного замещения SEAr Галогенирование NH 2 -группа донор электронов, возможны конкурирующие реакции Полигалогенирование 13
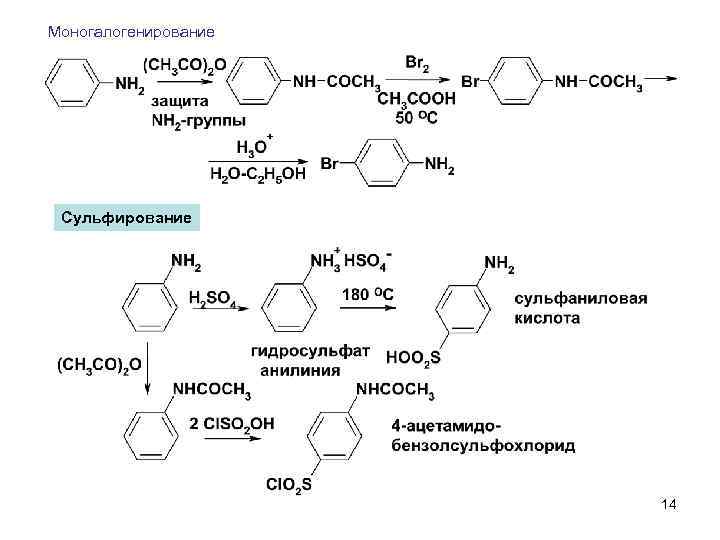 Моногалогенирование Сульфирование 14
Моногалогенирование Сульфирование 14
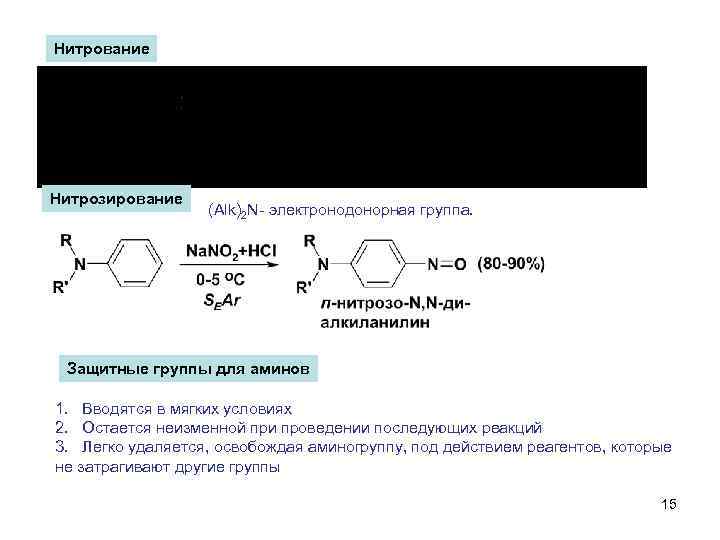 Нитрование Нитрозирование (Alk)2 N- электронодонорная группа. Защитные группы для аминов 1. Вводятся в мягких условиях 2. Остается неизменной при проведении последующих реакций 3. Легко удаляется, освобождая аминогруппу, под действием реагентов, которые не затрагивают другие группы 15
Нитрование Нитрозирование (Alk)2 N- электронодонорная группа. Защитные группы для аминов 1. Вводятся в мягких условиях 2. Остается неизменной при проведении последующих реакций 3. Легко удаляется, освобождая аминогруппу, под действием реагентов, которые не затрагивают другие группы 15
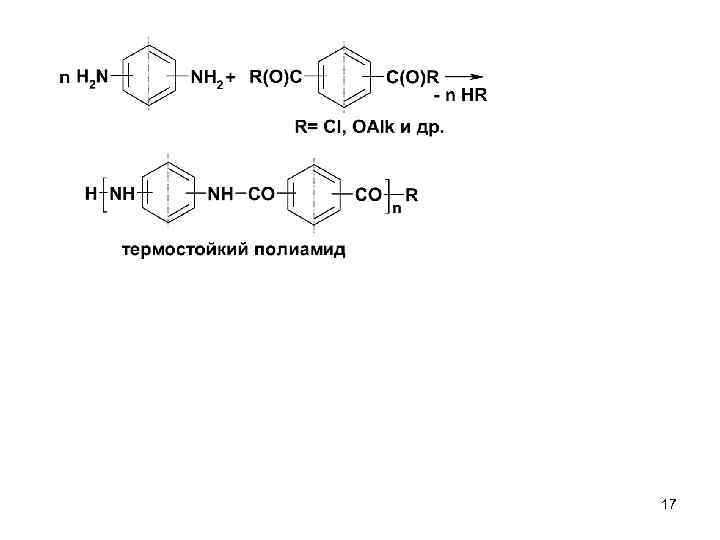
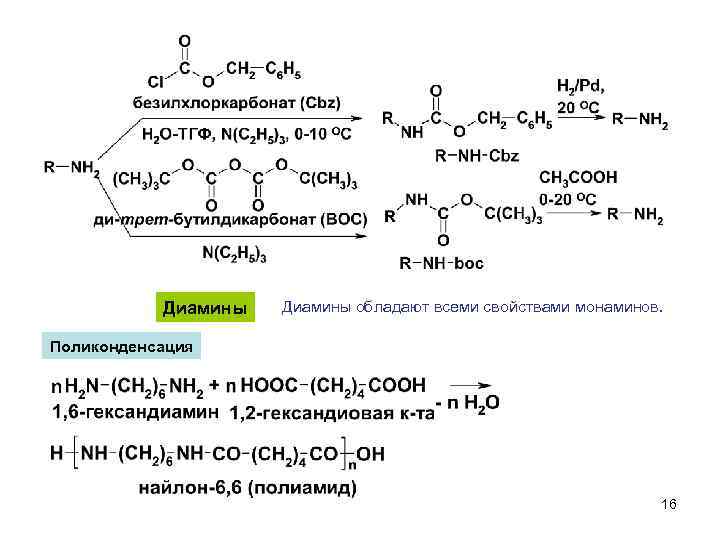 Диамины обладают всеми свойствами монаминов. Поликонденсация 16
Диамины обладают всеми свойствами монаминов. Поликонденсация 16
 17
17
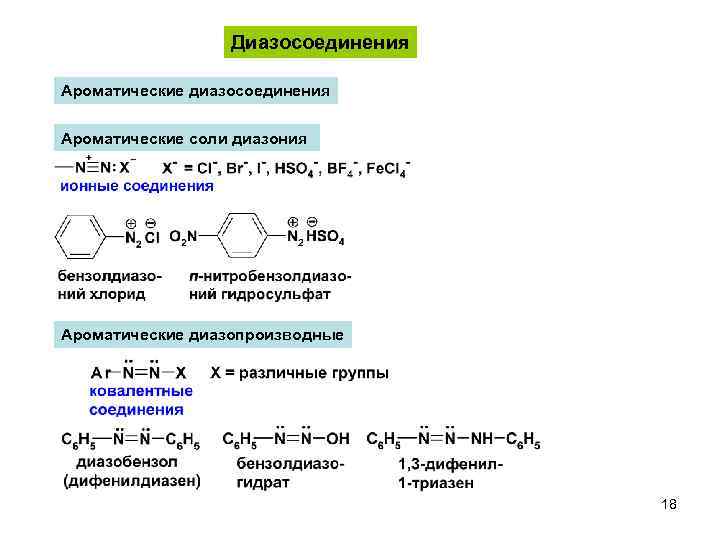 Диазосоединения Ароматические диазосоединения Ароматические соли диазония Ароматические диазопроизводные 18
Диазосоединения Ароматические диазосоединения Ароматические соли диазония Ароматические диазопроизводные 18
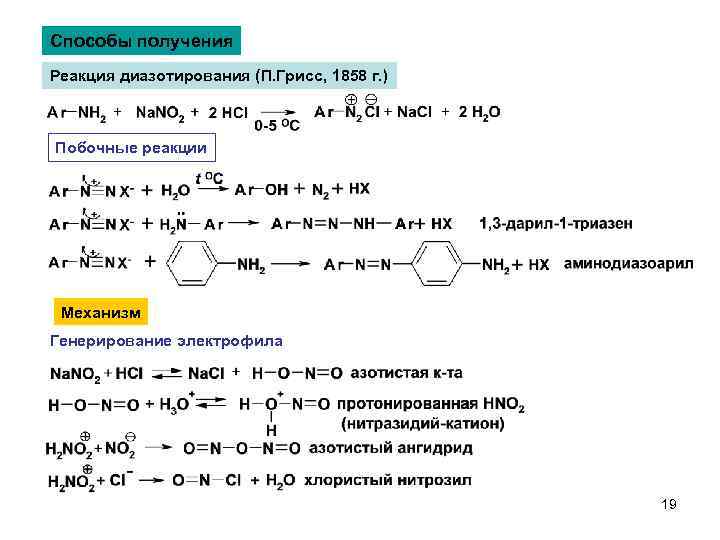 Способы получения Реакция диазотирования (П. Грисс, 1858 г. ) Побочные реакции Механизм Генерирование электрофила 19
Способы получения Реакция диазотирования (П. Грисс, 1858 г. ) Побочные реакции Механизм Генерирование электрофила 19
 Ряд активности электрофилов в реакции диазотирования NO+ >> H 2 NO 2+ > NOBr > NOCl > N 2 O 3 >> HNO 2 20
Ряд активности электрофилов в реакции диазотирования NO+ >> H 2 NO 2+ > NOBr > NOCl > N 2 O 3 >> HNO 2 20
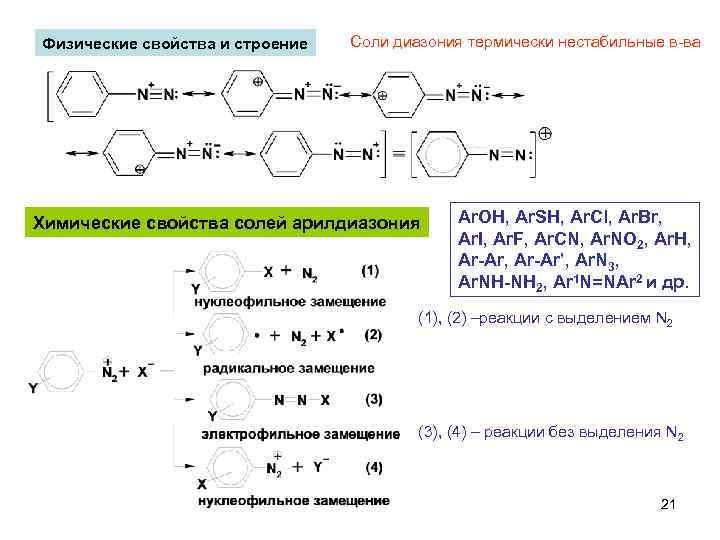 Физические свойства и строение Соли диазония термически нестабильные в-ва Химические свойства солей арилдиазония Ar. OH, Ar. SH, Ar. Cl, Ar. Br, Ar. I, Ar. F, Ar. CN, Ar. NO 2, Ar. H, Ar-Ar’, Ar. N 3, Ar. NH-NH 2, Ar 1 N=NAr 2 и др. (1), (2) –реакции с выделением N 2 (3), (4) – реакции без выделения N 2 21
Физические свойства и строение Соли диазония термически нестабильные в-ва Химические свойства солей арилдиазония Ar. OH, Ar. SH, Ar. Cl, Ar. Br, Ar. I, Ar. F, Ar. CN, Ar. NO 2, Ar. H, Ar-Ar’, Ar. N 3, Ar. NH-NH 2, Ar 1 N=NAr 2 и др. (1), (2) –реакции с выделением N 2 (3), (4) – реакции без выделения N 2 21
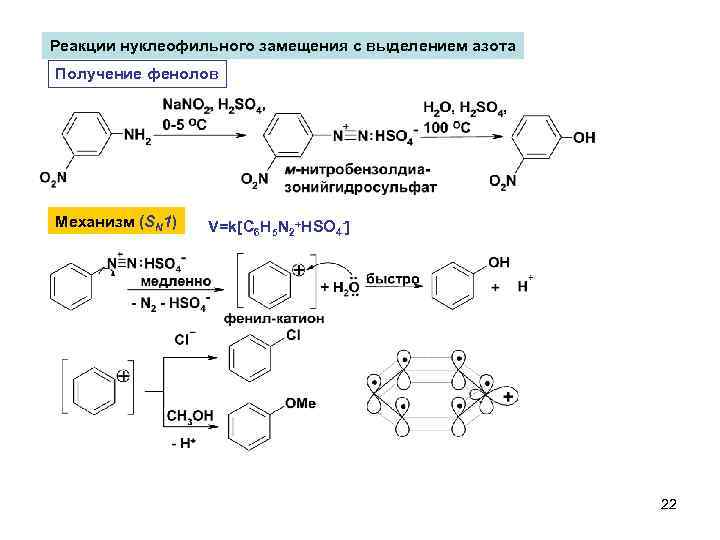 Реакции нуклеофильного замещения с выделением азота Получение фенолов Механизм (SN 1) V=k[C 6 H 5 N 2+HSO 4 -] 22
Реакции нуклеофильного замещения с выделением азота Получение фенолов Механизм (SN 1) V=k[C 6 H 5 N 2+HSO 4 -] 22
 Получение иод- и тиоцианатаренов I-, SCN- более сильные нуклеофилы, чем Cl- Механизм SRN 1 Инициирование цепи Развитие цепи 23
Получение иод- и тиоцианатаренов I-, SCN- более сильные нуклеофилы, чем Cl- Механизм SRN 1 Инициирование цепи Развитие цепи 23
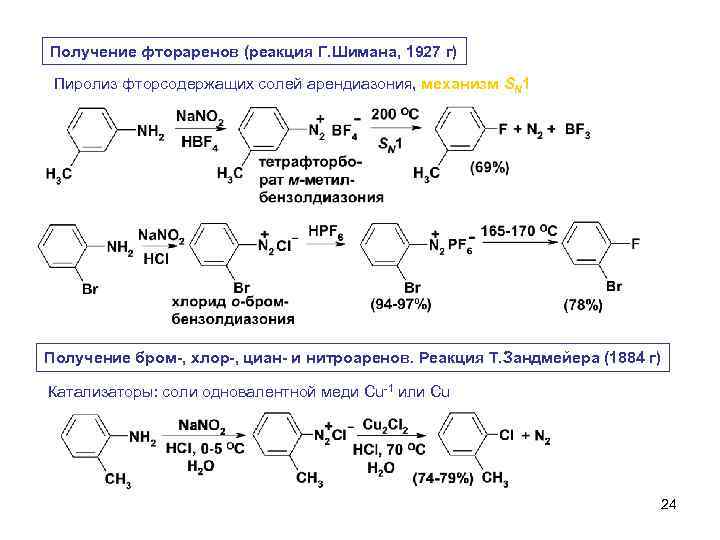 Получение фтораренов (реакция Г. Шимана, 1927 г) Пиролиз фторсодержащих солей арендиазония, механизм SN 1 Получение бром-, хлор-, циан- и нитроаренов. Реакция Т. Зандмейера (1884 г) Катализаторы: соли одновалентной меди Cu-1 или Cu 24
Получение фтораренов (реакция Г. Шимана, 1927 г) Пиролиз фторсодержащих солей арендиазония, механизм SN 1 Получение бром-, хлор-, циан- и нитроаренов. Реакция Т. Зандмейера (1884 г) Катализаторы: соли одновалентной меди Cu-1 или Cu 24
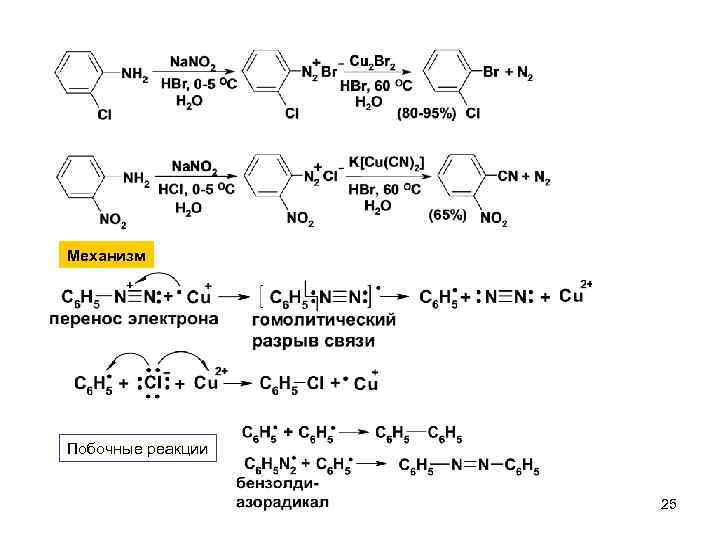 Механизм Побочные реакции 25
Механизм Побочные реакции 25
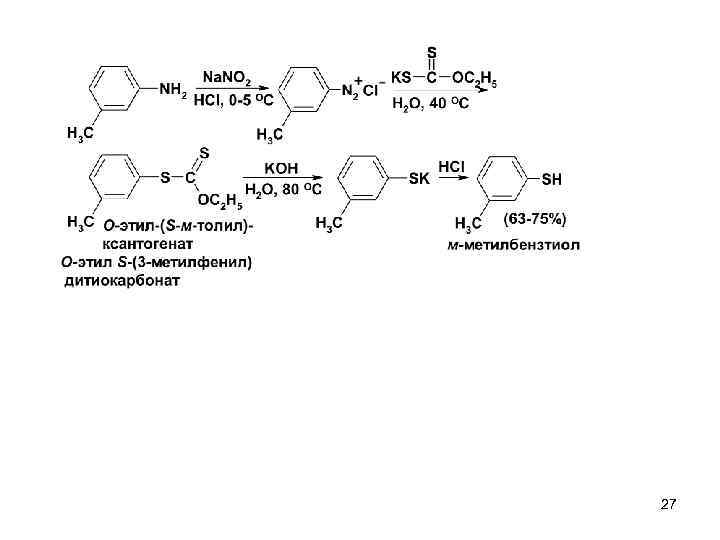
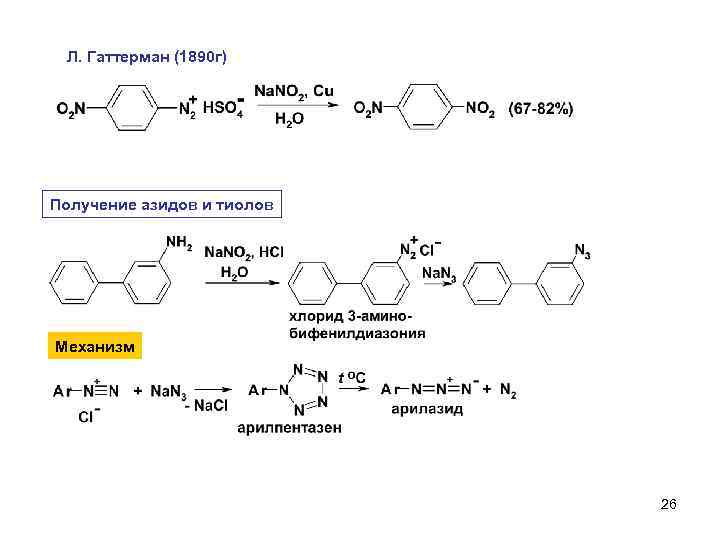 Л. Гаттерман (1890 г) Получение азидов и тиолов Механизм 26
Л. Гаттерман (1890 г) Получение азидов и тиолов Механизм 26
 27
27
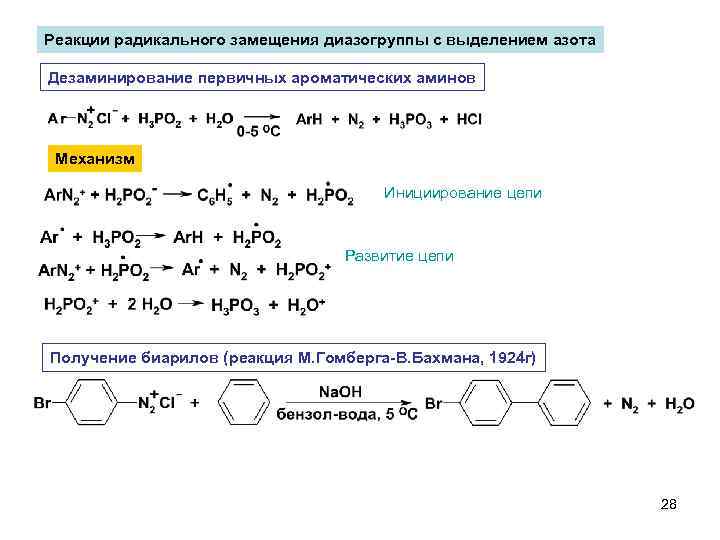 Реакции радикального замещения диазогруппы с выделением азота Дезаминирование первичных ароматических аминов Механизм Инициирование цепи Развитие цепи Получение биарилов (реакция М. Гомберга-В. Бахмана, 1924 г) 28
Реакции радикального замещения диазогруппы с выделением азота Дезаминирование первичных ароматических аминов Механизм Инициирование цепи Развитие цепи Получение биарилов (реакция М. Гомберга-В. Бахмана, 1924 г) 28
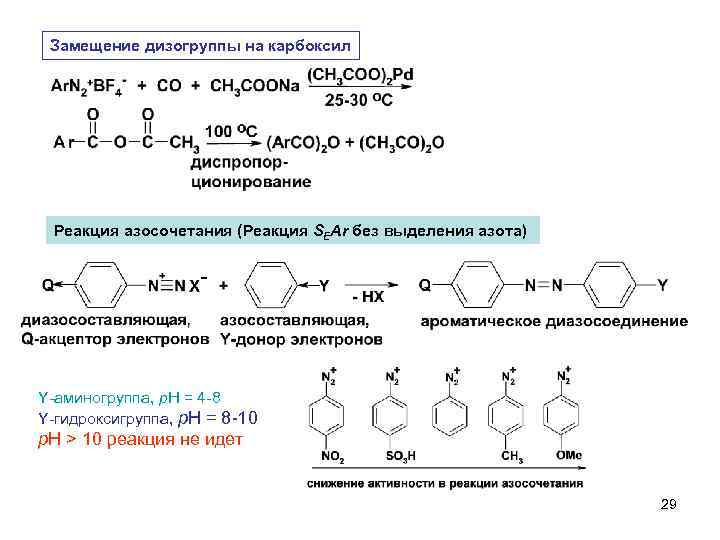 Замещение дизогруппы на карбоксил Реакция азосочетания (Реакция SEAr без выделения азота) Y-аминогруппа, p. H = 4 -8 Y-гидроксигруппа, p. H = 8 -10 p. H > 10 реакция не идет 29
Замещение дизогруппы на карбоксил Реакция азосочетания (Реакция SEAr без выделения азота) Y-аминогруппа, p. H = 4 -8 Y-гидроксигруппа, p. H = 8 -10 p. H > 10 реакция не идет 29
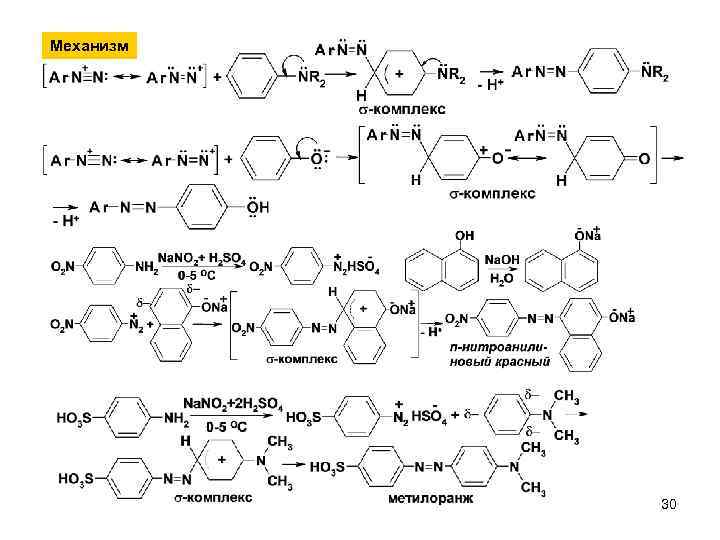 Механизм 30
Механизм 30
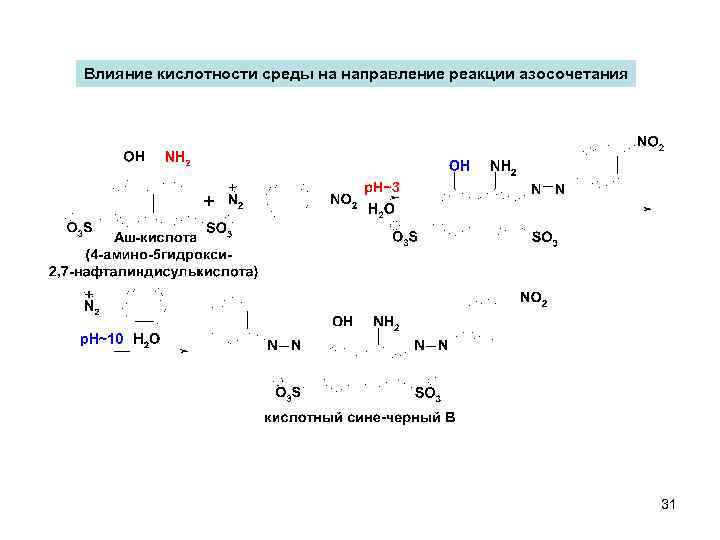 Влияние кислотности среды на направление реакции азосочетания 31
Влияние кислотности среды на направление реакции азосочетания 31
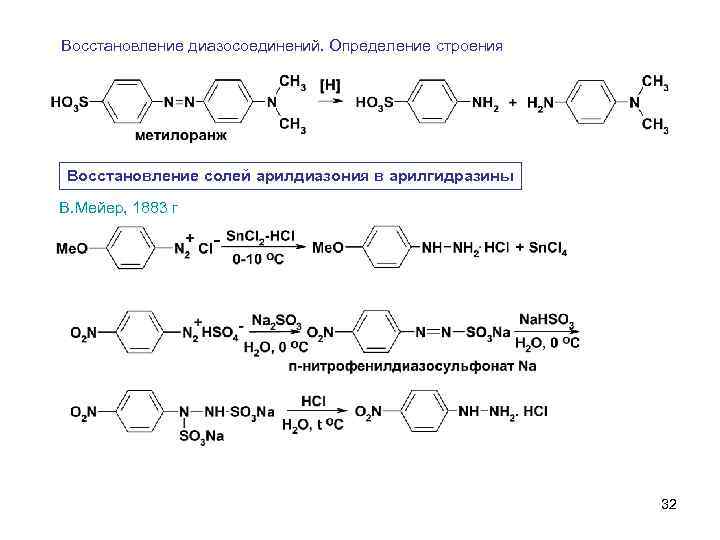 Восстановление диазосоединений. Определение строения Восстановление солей арилдиазония в арилгидразины В. Мейер, 1883 г 32
Восстановление диазосоединений. Определение строения Восстановление солей арилдиазония в арилгидразины В. Мейер, 1883 г 32
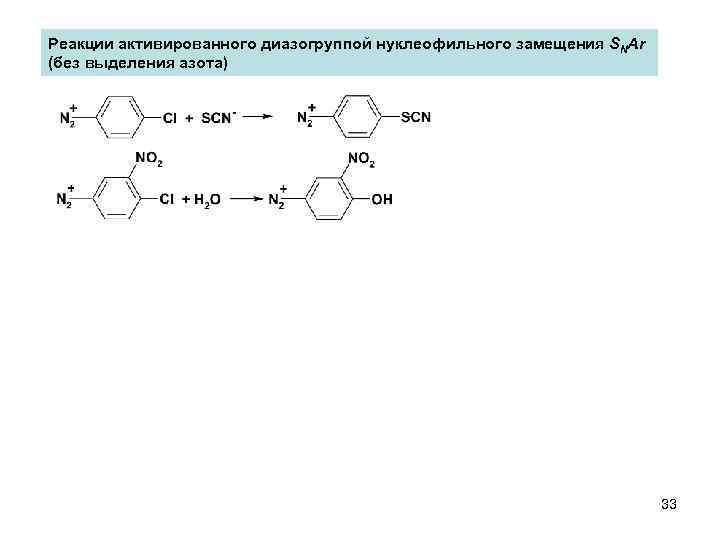 Реакции активированного диазогруппой нуклеофильного замещения SNAr (без выделения азота) 33
Реакции активированного диазогруппой нуклеофильного замещения SNAr (без выделения азота) 33


