Аминокислоты.ppt
- Количество слайдов: 24
 Аминокислоты – соединения, в молекулах которых одновременно присутствуют амино- и карбоксильные группы
Аминокислоты – соединения, в молекулах которых одновременно присутствуют амино- и карбоксильные группы
 НОМЕНКЛАТУРА АМИНОКИСЛОТ
НОМЕНКЛАТУРА АМИНОКИСЛОТ
 γ-аминомаслянная кислота
γ-аминомаслянная кислота

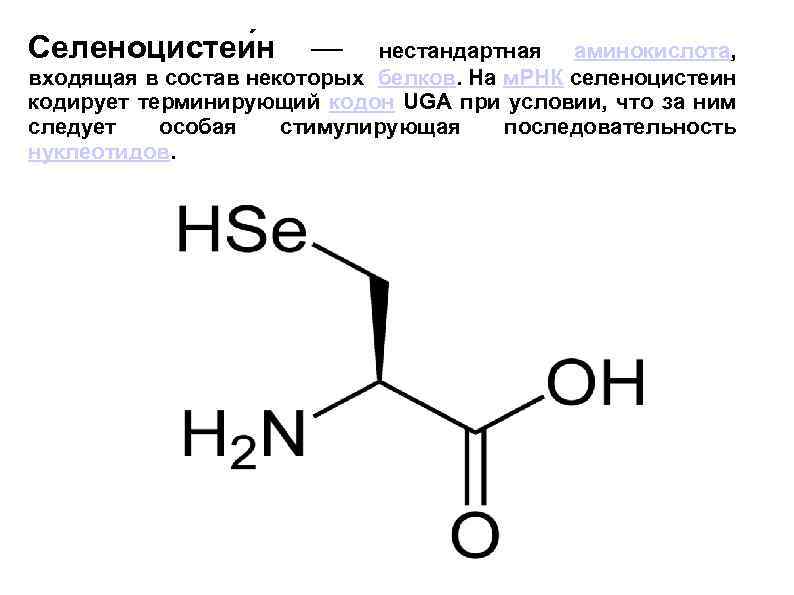 Селеноцистеи н — нестандартная аминокиcлота, входящая в состав некоторых белков. На м. РНК селеноцистеин кодирует терминирующий кодон UGA при условии, что за ним следует особая стимулирующая последовательность нуклеотидов.
Селеноцистеи н — нестандартная аминокиcлота, входящая в состав некоторых белков. На м. РНК селеноцистеин кодирует терминирующий кодон UGA при условии, что за ним следует особая стимулирующая последовательность нуклеотидов.
 Происхождение тривиальных названий От названия сырья из которого они были выделены Аспарагин и аспарагиновая кислота (от латинского asparagus — спаржа) Глутамин и глутаминовая кислота (от немецкого das Gluten — клейковина) Тирозин (от греческого tyros — сыр) Названия связанные с методом выделения Аргинин (от латинского argentum — серебро) был получен в виде серебряной соли Триптофан выделен при расщеплении белка трипсином Структурные связи с другими природными соединениями Валин назван как производное валериановой кислоты Треонин структурно похож на моносахарид треозу
Происхождение тривиальных названий От названия сырья из которого они были выделены Аспарагин и аспарагиновая кислота (от латинского asparagus — спаржа) Глутамин и глутаминовая кислота (от немецкого das Gluten — клейковина) Тирозин (от греческого tyros — сыр) Названия связанные с методом выделения Аргинин (от латинского argentum — серебро) был получен в виде серебряной соли Триптофан выделен при расщеплении белка трипсином Структурные связи с другими природными соединениями Валин назван как производное валериановой кислоты Треонин структурно похож на моносахарид треозу
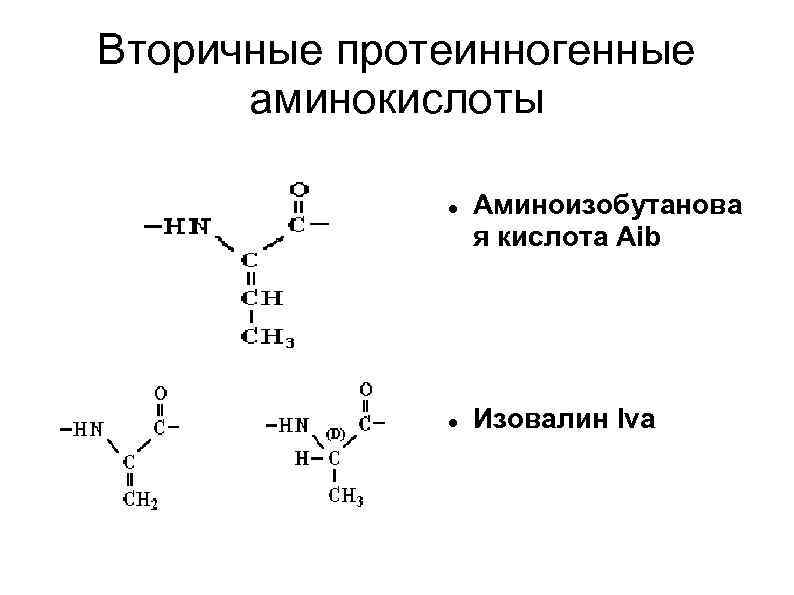 Вторичные протеинногенные аминокислоты Аминоизобутанова я кислота Aib Изовалин Iva
Вторичные протеинногенные аминокислоты Аминоизобутанова я кислота Aib Изовалин Iva
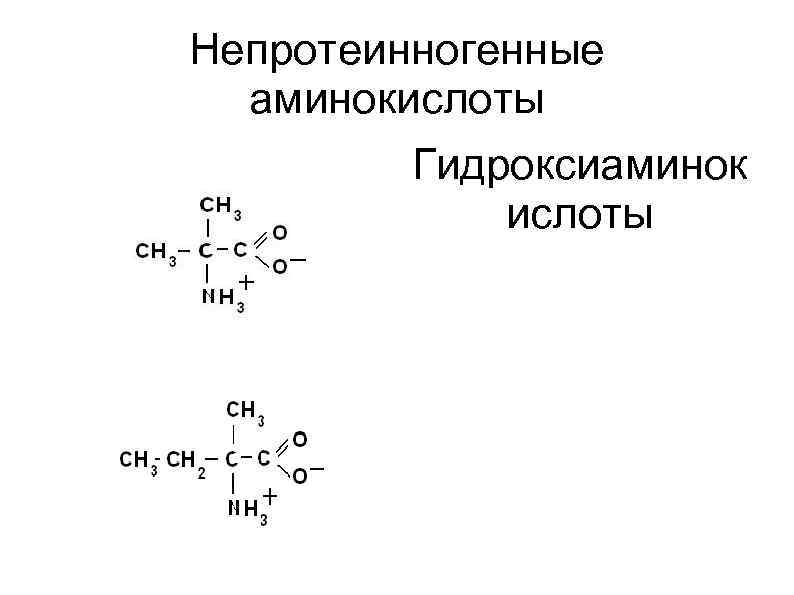 Непротеинногенные аминокислоты Гидроксиаминок ислоты
Непротеинногенные аминокислоты Гидроксиаминок ислоты
 ГОМОСЕРИН - Hse Приставка гомо — обозначает, что боковая цепь данной аминокислоты содержит дополнительную метиленовую группу - СН 2 -
ГОМОСЕРИН - Hse Приставка гомо — обозначает, что боковая цепь данной аминокислоты содержит дополнительную метиленовую группу - СН 2 -
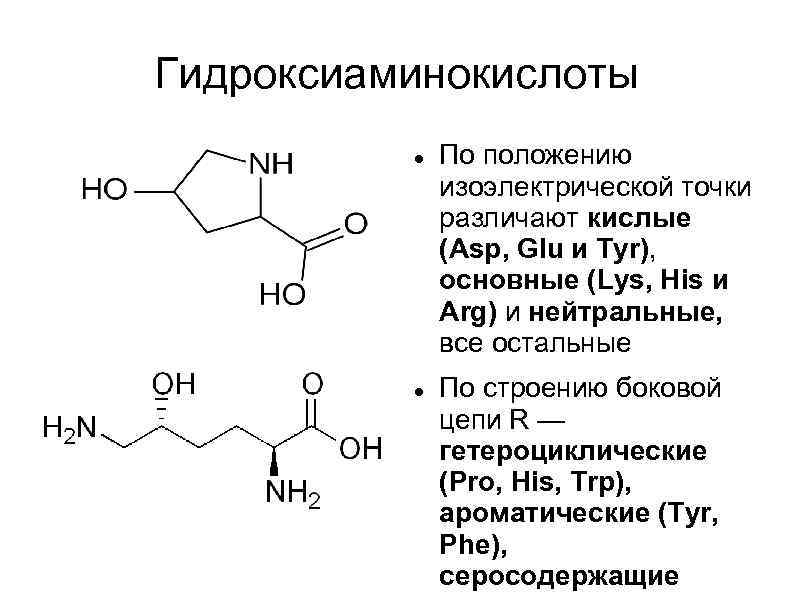 Гидроксиаминокислоты По положению изоэлектрической точки различают кислые (Asp, Glu и Tyr), основные (Lys, His и Arg) и нейтральные, все остальные По строению боковой цепи R — гетероциклические (Pro, His, Trp), ароматические (Tyr, Phe), серосодержащие
Гидроксиаминокислоты По положению изоэлектрической точки различают кислые (Asp, Glu и Tyr), основные (Lys, His и Arg) и нейтральные, все остальные По строению боковой цепи R — гетероциклические (Pro, His, Trp), ароматические (Tyr, Phe), серосодержащие
 Другие классификации генетически кодируемых аминокислот По положению изоэлектрической точки различают кислые (Asp, Glu и Tyr), основные (Lys, His и Arg) и нейтральные, все остальные По строению боковой цепи R — гетероциклические (Pro, His, Trp), ароматические (Tyr, Phe), серосодержащие аминокислоты (Cys, Met) имеют в боковой цепи тиольную или тиоэфирную группы и алифатические (Ala, Val, Leu и т. д. ) Самостоятельные группы образуют иминокислота Pro и селеноцистеин Sec
Другие классификации генетически кодируемых аминокислот По положению изоэлектрической точки различают кислые (Asp, Glu и Tyr), основные (Lys, His и Arg) и нейтральные, все остальные По строению боковой цепи R — гетероциклические (Pro, His, Trp), ароматические (Tyr, Phe), серосодержащие аминокислоты (Cys, Met) имеют в боковой цепи тиольную или тиоэфирную группы и алифатические (Ala, Val, Leu и т. д. ) Самостоятельные группы образуют иминокислота Pro и селеноцистеин Sec
 Другие классификации генетически кодируемых аминокислот По полярности боковой цепи R различают полярные и неполярные аминокислоты Неполярные аминокислоты (гидрофобные) — Val, Leu, Ile, Pro, Met, и Phe, а так же Gly и Ala Полярные (нейтральные) аминокислоты — Ser, Thr, Cys, Sec, Asn, Gln и Trp Кислые гидрофильные аминокислоты — Asp, Glu и Tyr Основные гидрофильные аминокислоты — Lys, Hys и Arg
Другие классификации генетически кодируемых аминокислот По полярности боковой цепи R различают полярные и неполярные аминокислоты Неполярные аминокислоты (гидрофобные) — Val, Leu, Ile, Pro, Met, и Phe, а так же Gly и Ala Полярные (нейтральные) аминокислоты — Ser, Thr, Cys, Sec, Asn, Gln и Trp Кислые гидрофильные аминокислоты — Asp, Glu и Tyr Основные гидрофильные аминокислоты — Lys, Hys и Arg
 Заменимые и незаменимые аминокислоты Незаменимые аминокислоты (НАК) для организма человека — Arg, His, Lys, Val, Leu, Ile, Met, Thr, Phe, Trp Cys и Tyr так же можно отнести к незаменимым, поскольку они синтезируются из Met и Phe, соответственно.
Заменимые и незаменимые аминокислоты Незаменимые аминокислоты (НАК) для организма человека — Arg, His, Lys, Val, Leu, Ile, Met, Thr, Phe, Trp Cys и Tyr так же можно отнести к незаменимым, поскольку они синтезируются из Met и Phe, соответственно.
 Кислотно-основные свойства аминокислот Вода является слабым электролитом; она слабо диссоциирует по уравнению H 2 O = H+ + OH- Понятие p. H При 25 °С в 1 л воды распадается на ионы 10 -7 моль H 2 O. Концентрация ионов H+ и OH- (в моль/л) будет равна [H+]=[OH-]=10 -7 p. H= -lg[H+] p. K= -lg[Ka]
Кислотно-основные свойства аминокислот Вода является слабым электролитом; она слабо диссоциирует по уравнению H 2 O = H+ + OH- Понятие p. H При 25 °С в 1 л воды распадается на ионы 10 -7 моль H 2 O. Концентрация ионов H+ и OH- (в моль/л) будет равна [H+]=[OH-]=10 -7 p. H= -lg[H+] p. K= -lg[Ka]
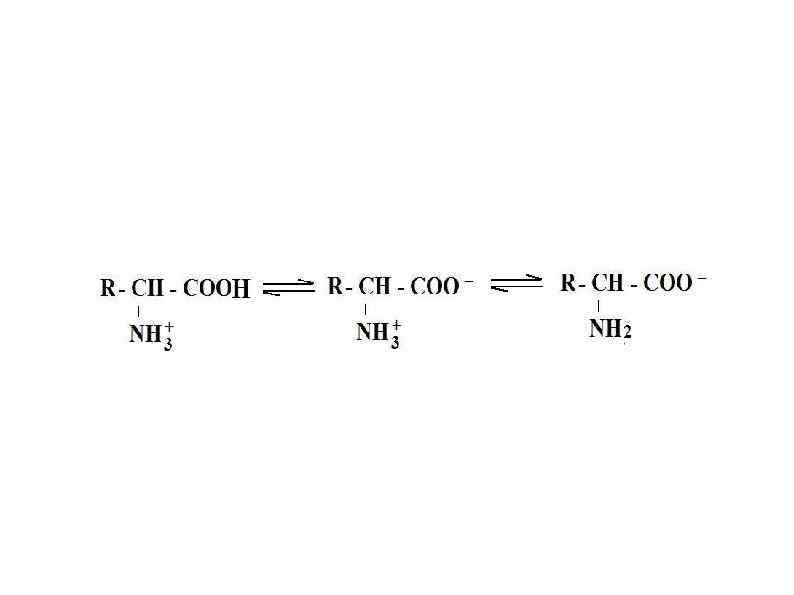
 p. Ka кислоты или кислотной группы — это значение р. Н раствора, при котором данная кислота или кислотная группа диссоциирована на 50%
p. Ka кислоты или кислотной группы — это значение р. Н раствора, при котором данная кислота или кислотная группа диссоциирована на 50%
 Буферные растворы представляют собой чаще всего смеси слабых кислот с солями этих кислот или смеси слабых оснований с солями этих же оснований. Если, например, в ацетатный буферный раствор, состоящий из уксусной кислоты CH 3 COOH и ацетата натрия CH 3 COONa добавить некоторое количество такой сильной кислоты, как HCl, она будет реагировать с ацетат-ионами с образованием малодиссоциирующей CH 3 COOH: CH 3 COO- + H+ = CH 3 COOH Таким образом, добавленные в раствор ионы H+ не останутся свободными, а будут связаны ионами CH 3 COO-, и поэтому p. H раствора почти не изменится. При добавлении раствора щелочи к ацетатному буферному раствору ионы OH будут связаны недиссоциированными молекулами уксусной кислоты CO 3 COOH: OH- + CH 3 COOH = H 2 O + CH 3 COO- Следовательно, p. H раствора и в этом случае также почти не изменится.
Буферные растворы представляют собой чаще всего смеси слабых кислот с солями этих кислот или смеси слабых оснований с солями этих же оснований. Если, например, в ацетатный буферный раствор, состоящий из уксусной кислоты CH 3 COOH и ацетата натрия CH 3 COONa добавить некоторое количество такой сильной кислоты, как HCl, она будет реагировать с ацетат-ионами с образованием малодиссоциирующей CH 3 COOH: CH 3 COO- + H+ = CH 3 COOH Таким образом, добавленные в раствор ионы H+ не останутся свободными, а будут связаны ионами CH 3 COO-, и поэтому p. H раствора почти не изменится. При добавлении раствора щелочи к ацетатному буферному раствору ионы OH будут связаны недиссоциированными молекулами уксусной кислоты CO 3 COOH: OH- + CH 3 COOH = H 2 O + CH 3 COO- Следовательно, p. H раствора и в этом случае также почти не изменится.
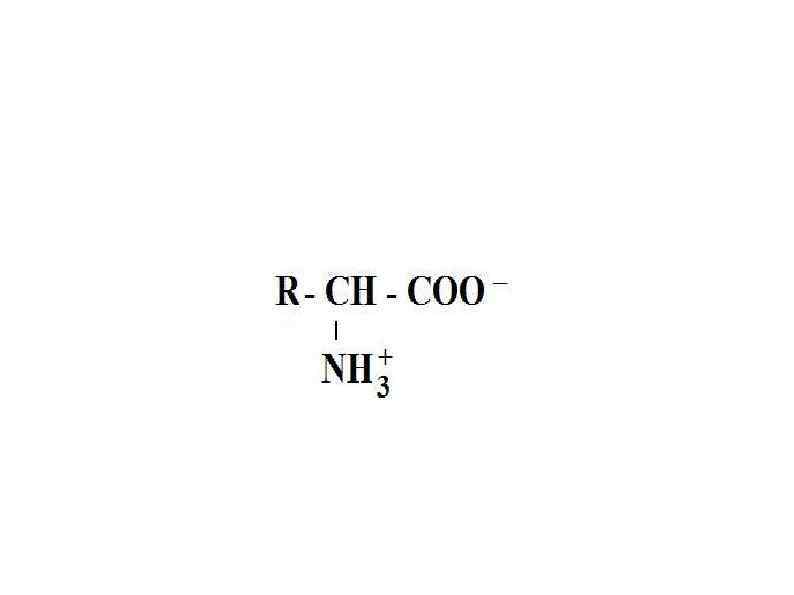
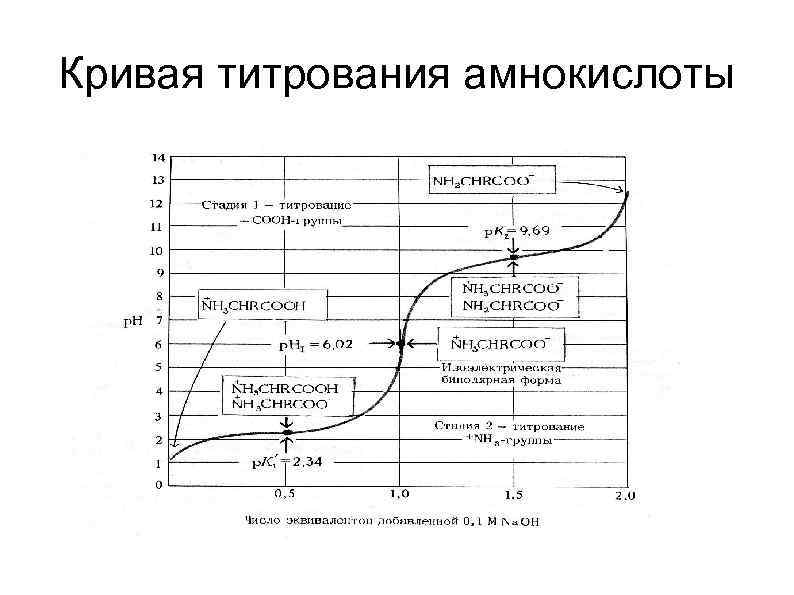 Кривая титрования амнокислоты
Кривая титрования амнокислоты
 Аминокислоты, имеющие диссоциирующие группы в боковой цепи Asp, Glu, Lys, Arg, His, Cys, Sec, Tyr Кривые титрования имеют три перегиба, то есть три р. К.
Аминокислоты, имеющие диссоциирующие группы в боковой цепи Asp, Glu, Lys, Arg, His, Cys, Sec, Tyr Кривые титрования имеют три перегиба, то есть три р. К.
 Все аминокислоты в растворе ведут себя как сильные электролиты Изоэлектрическая точка p. I аминокислоты определяется значением констант диссоциации её кислотных групп. Для всех аминокислот p. I=p. K 1+p. K 2/2, кроме основных аминокислот Lys, Arg и His, для них p. I равно среднеарифметическому значений p. K 2 и p. K 3 Водные растворы всех аминокислот обладают буферными свойствами
Все аминокислоты в растворе ведут себя как сильные электролиты Изоэлектрическая точка p. I аминокислоты определяется значением констант диссоциации её кислотных групп. Для всех аминокислот p. I=p. K 1+p. K 2/2, кроме основных аминокислот Lys, Arg и His, для них p. I равно среднеарифметическому значений p. K 2 и p. K 3 Водные растворы всех аминокислот обладают буферными свойствами
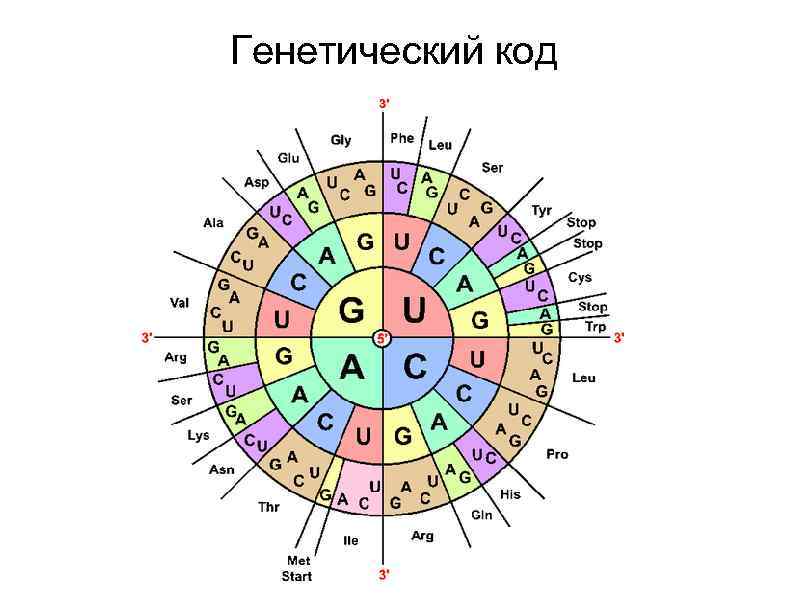 Генетический код
Генетический код
 Свойства генетического кода Триплетность ― значащей единицей кода является сочетание трёх нуклеотидов (триплет, или кодон). Непрерывность ― между триплетами нет знаков препинания, то есть информация считывается непрерывно. Неперекрываемость ― один и тот же нуклеотид не может входить одновременно в состав двух или более триплетов. (Не соблюдается для некоторых перекрывающихся генов вирусов, митохондрий и бактерий, которые кодируют несколько белков, считывающихся со сдвигом рамки). Однозначность ― определённый кодон соответствует только одной аминокислоте. (Свойство не является универсальным. Кодон UGA у Euplotes crassus кодирует две аминокислоты - цистеин и селеноцистеин) Вырожденность (избыточность) ― одной и той же аминокислоте может соответствовать несколько кодонов. Универсальность ― генетический код работает одинаково в организмах разного уровня сложности ― от вирусов до человека (на этом основаны методы генной инженерии)
Свойства генетического кода Триплетность ― значащей единицей кода является сочетание трёх нуклеотидов (триплет, или кодон). Непрерывность ― между триплетами нет знаков препинания, то есть информация считывается непрерывно. Неперекрываемость ― один и тот же нуклеотид не может входить одновременно в состав двух или более триплетов. (Не соблюдается для некоторых перекрывающихся генов вирусов, митохондрий и бактерий, которые кодируют несколько белков, считывающихся со сдвигом рамки). Однозначность ― определённый кодон соответствует только одной аминокислоте. (Свойство не является универсальным. Кодон UGA у Euplotes crassus кодирует две аминокислоты - цистеин и селеноцистеин) Вырожденность (избыточность) ― одной и той же аминокислоте может соответствовать несколько кодонов. Универсальность ― генетический код работает одинаково в организмах разного уровня сложности ― от вирусов до человека (на этом основаны методы генной инженерии)
 Обратная таблица (указаны кодоны для каждой аминокислоты, а также стоп-кодоны) Ala/A - GCU, GCC, GCA, GCG Arg/R - CGU, CGC, CGA, CGG, AGA, AGG Lys/K - AAA, AAG Asn/N - AAU, AAC Phe/F - UUU, UUC Asp/D - GAU, GAC Pro/P - CCU, CCC, CCA, CCG Cys/C - UGU, UGC Gln/Q - CAA, CAG Glu/E - GAA, GAG Gly/G - GGU, GGC, GGA, GGG His/H - CAU, CAC Ile/I - AUU, AUC, AUA Met/M - AUG START - AUG Leu/L - UUA, UUG, CUU, CUC, CUA, CUG Ser/S - UCU, UCC, UCA, UCG, AGU, AGC Thr/T - ACU, ACC, ACA, ACG Trp/W - UGG Tyr/Y - UAU, UAC Val/V - GUU, GUC, GUA, GUG STOP - UAG, UGA, UAA
Обратная таблица (указаны кодоны для каждой аминокислоты, а также стоп-кодоны) Ala/A - GCU, GCC, GCA, GCG Arg/R - CGU, CGC, CGA, CGG, AGA, AGG Lys/K - AAA, AAG Asn/N - AAU, AAC Phe/F - UUU, UUC Asp/D - GAU, GAC Pro/P - CCU, CCC, CCA, CCG Cys/C - UGU, UGC Gln/Q - CAA, CAG Glu/E - GAA, GAG Gly/G - GGU, GGC, GGA, GGG His/H - CAU, CAC Ile/I - AUU, AUC, AUA Met/M - AUG START - AUG Leu/L - UUA, UUG, CUU, CUC, CUA, CUG Ser/S - UCU, UCC, UCA, UCG, AGU, AGC Thr/T - ACU, ACC, ACA, ACG Trp/W - UGG Tyr/Y - UAU, UAC Val/V - GUU, GUC, GUA, GUG STOP - UAG, UGA, UAA


