Лекция 3 Аминокислоты белки.pptx
- Количество слайдов: 31

Аминокислоты, пептиды и белки
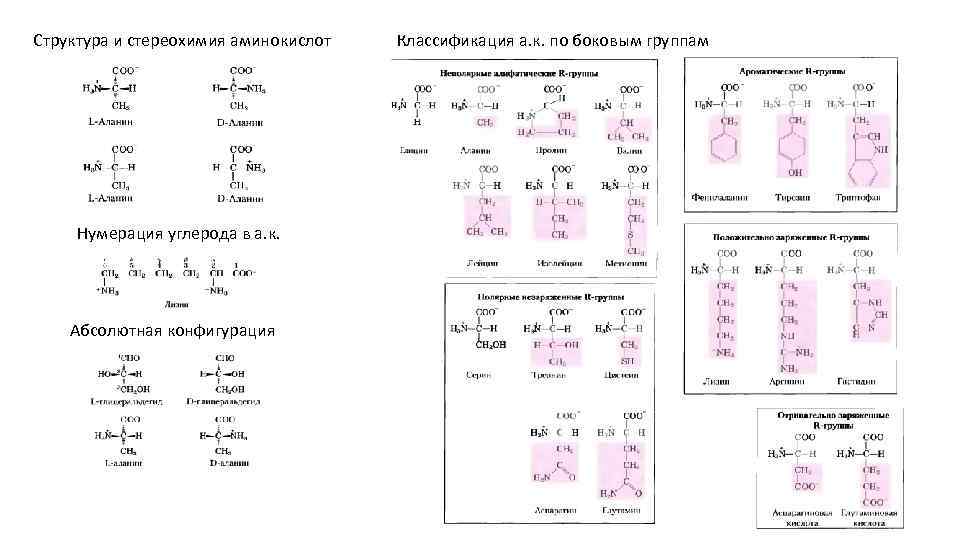
Структура и стереохимия аминокислот Нумерация углерода в а. к. Абсолютная конфигурация Классификация а. к. по боковым группам
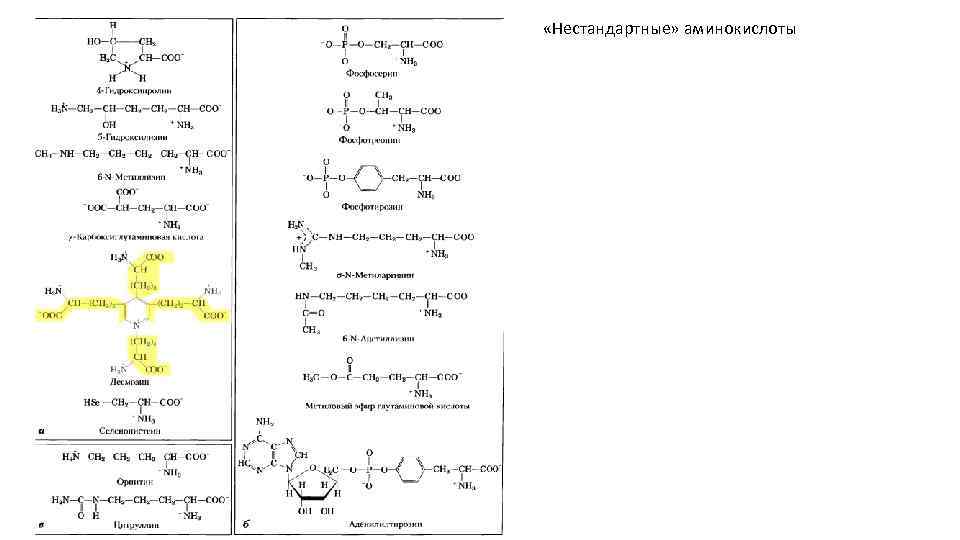
«Нестандартные» аминокислоты
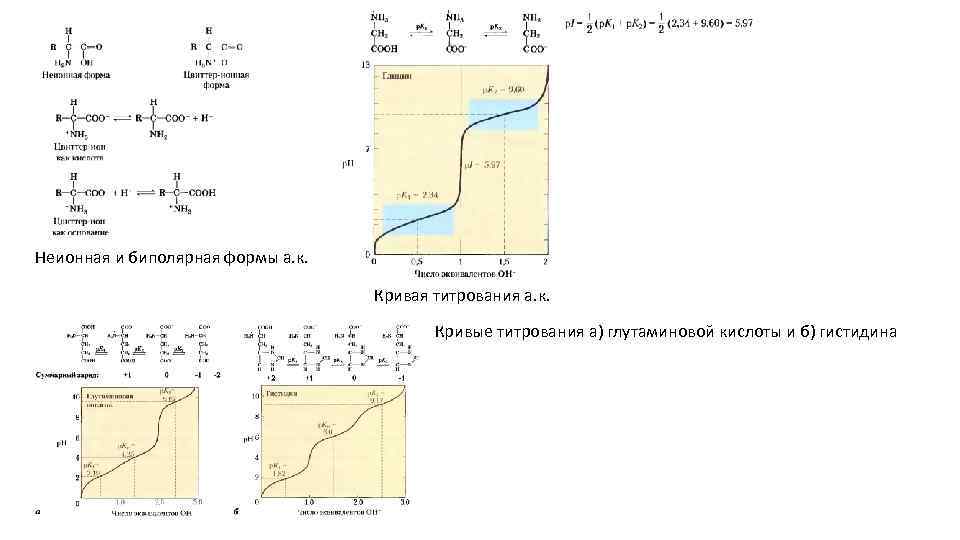
Неионная и биполярная формы а. к. Кривая титрования а. к. Кривые титрования а) глутаминовой кислоты и б) гистидина
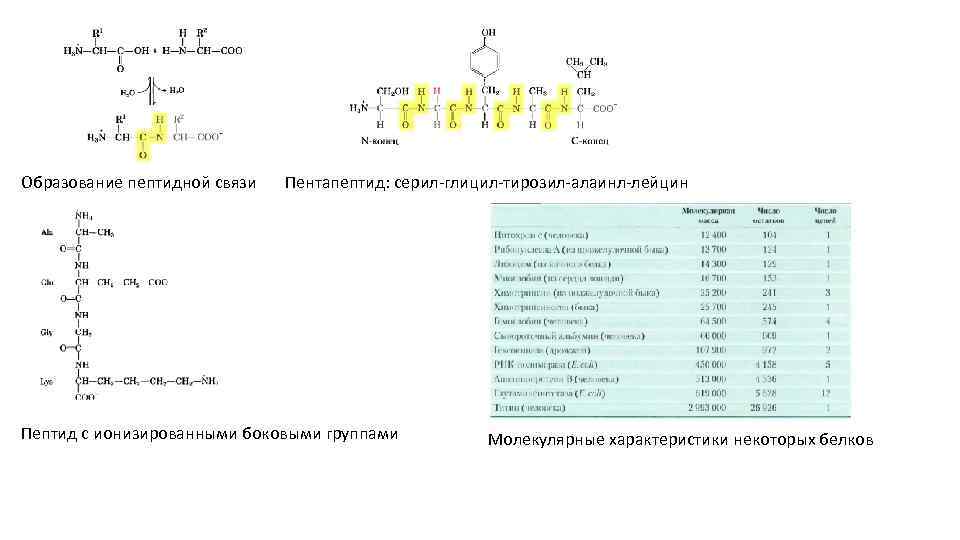
Образование пептидной связи Пентапептид: серил-глицил-тирозил-алаинл-лейцин Пептид с ионизированными боковыми группами Молекулярные характеристики некоторых белков

Классификация белков
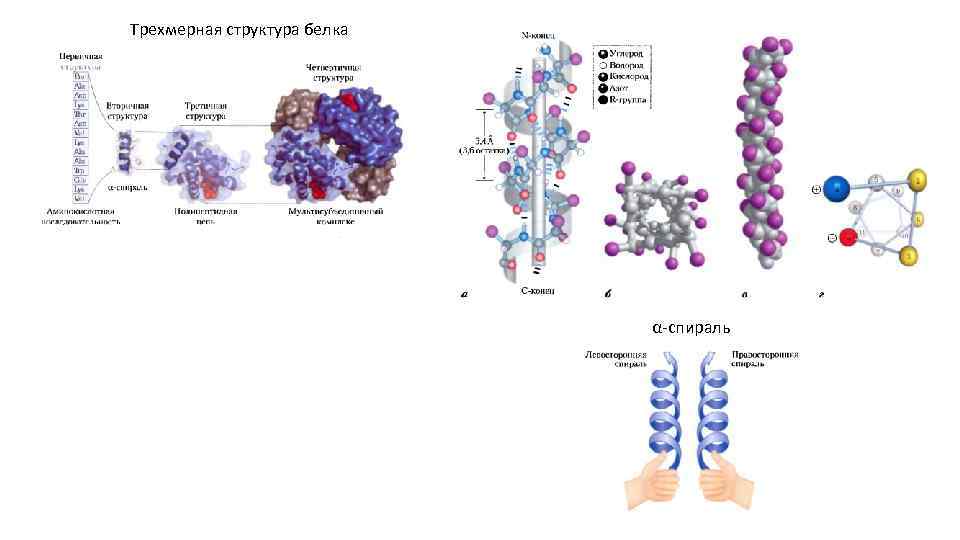
Трехмерная структура белка α-спираль
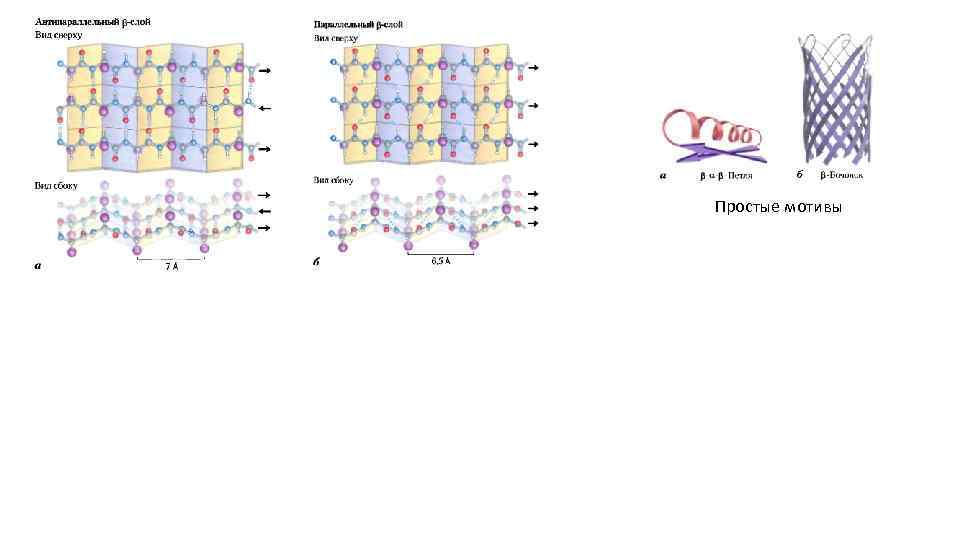
Простые мотивы
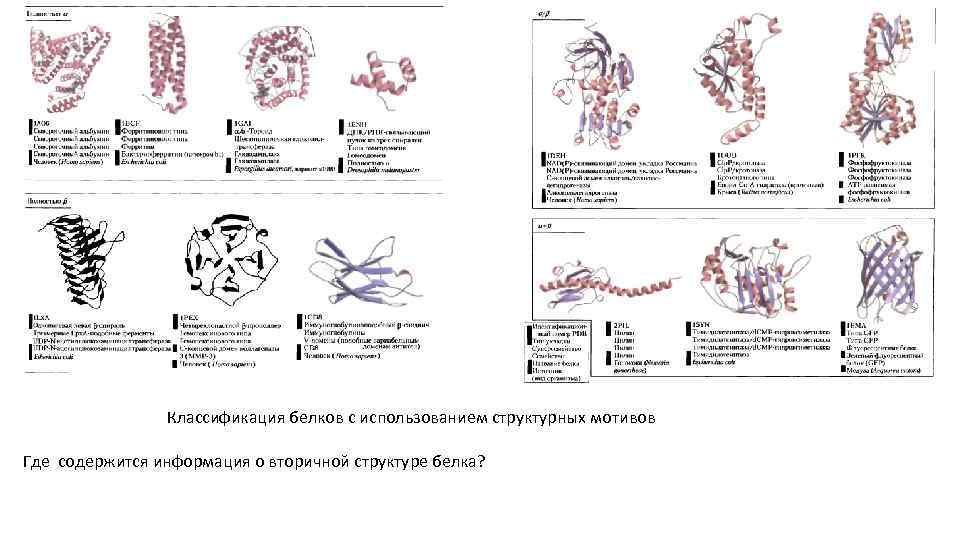
Классификация белков с использованием структурных мотивов Где содержится информация о вторичной структуре белка?
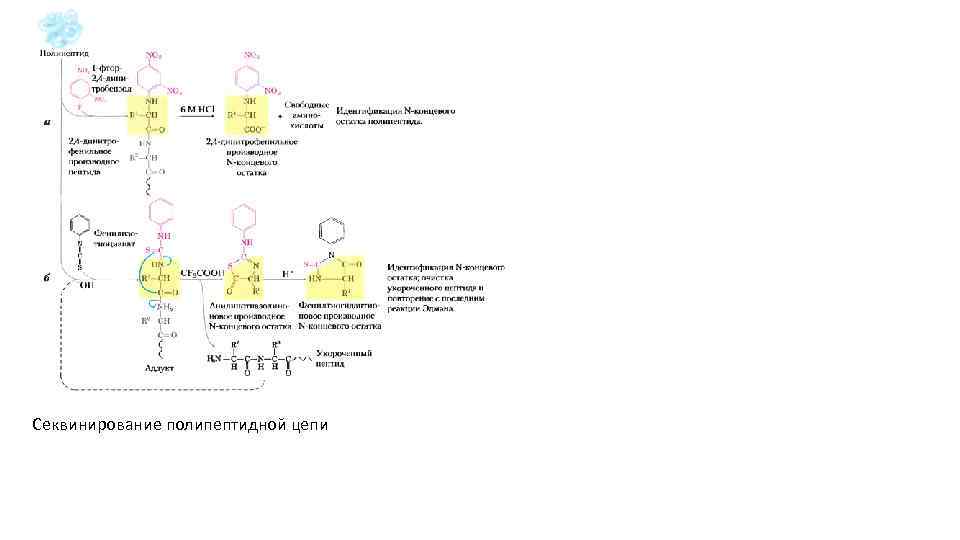
Секвинирование полипептидной цепи

Специфичность ферментов к расщепляемой пептидной связи
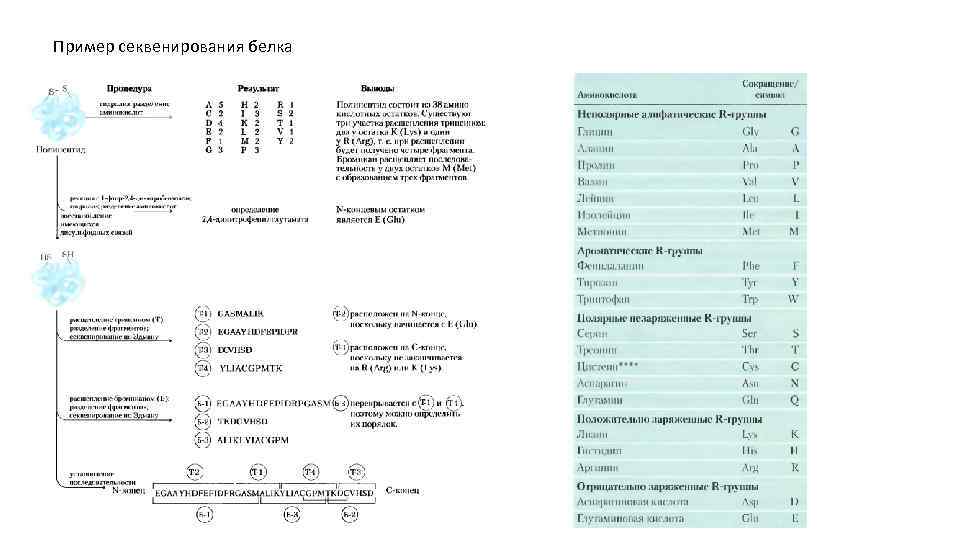
Пример секвенирования белка
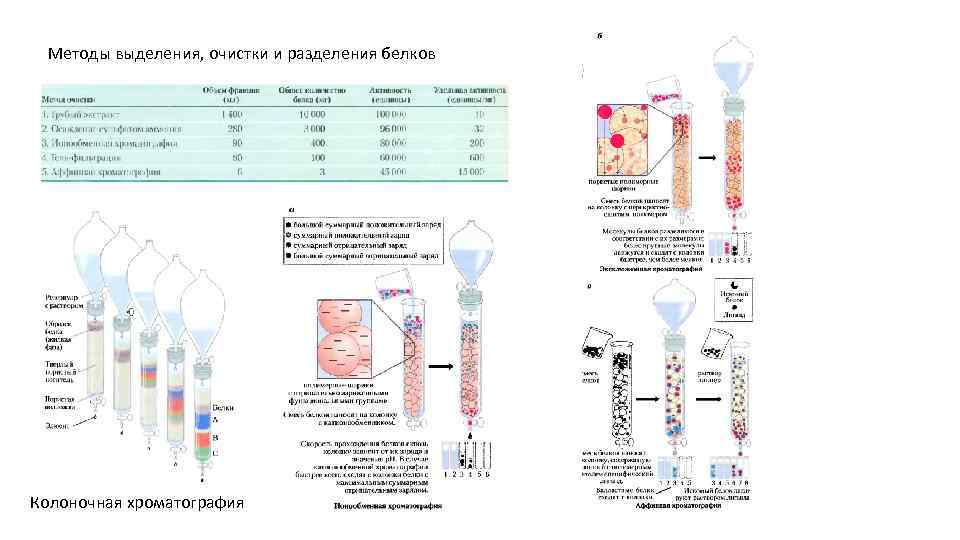
Методы выделения, очистки и разделения белков Колоночная хроматография
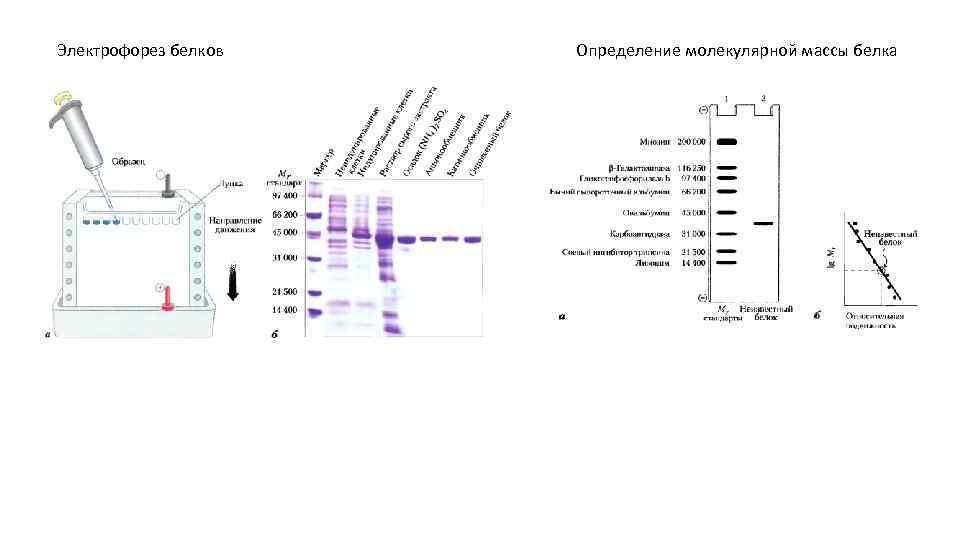
Электрофорез белков Определение молекулярной массы белка
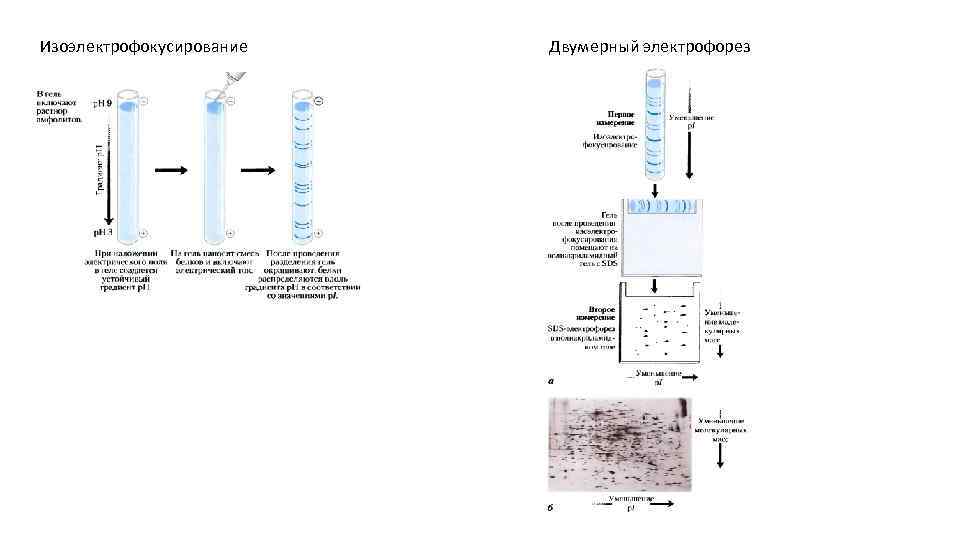
Изоэлектрофокусирование Двумерный электрофорез
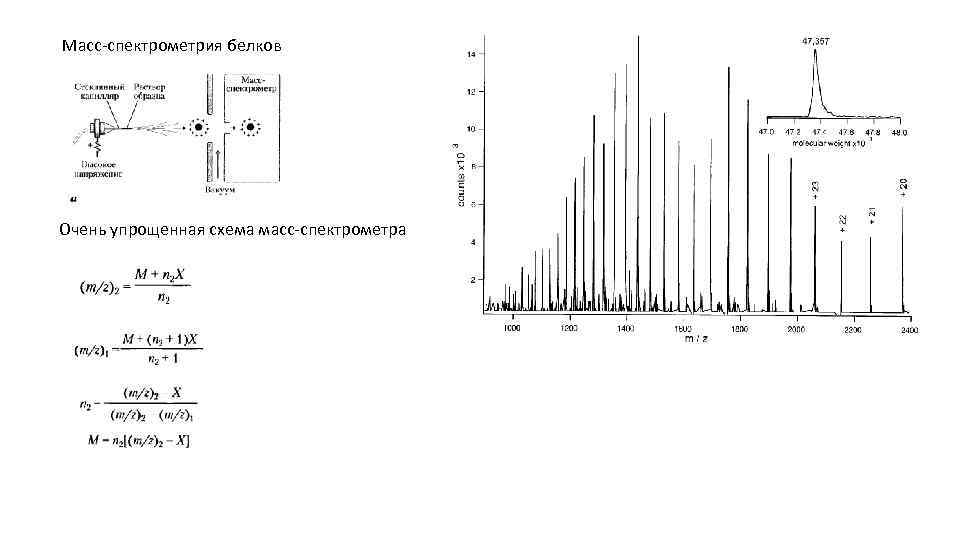
Масс-спектрометрия белков Очень упрощенная схема масс-спектрометра
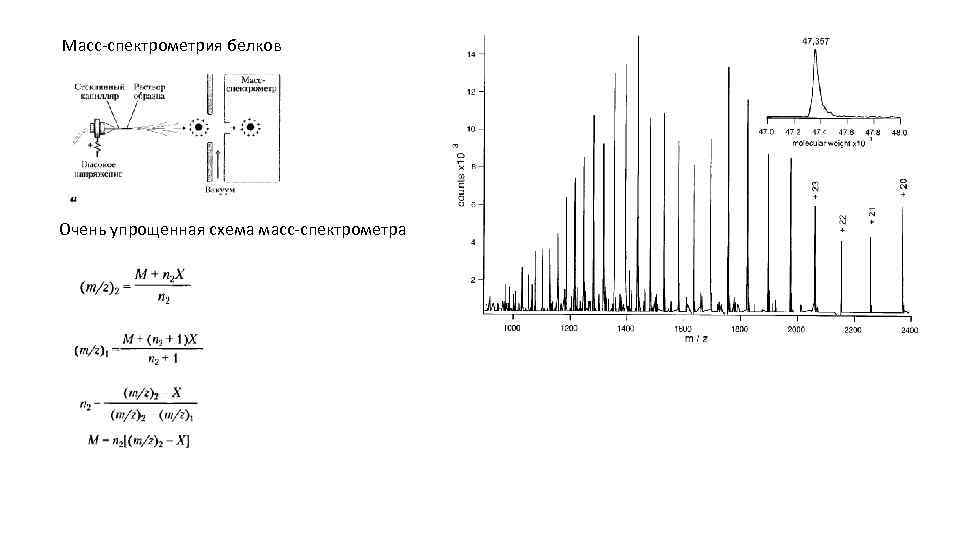
Масс-спектрометрия белков Очень упрощенная схема масс-спектрометра
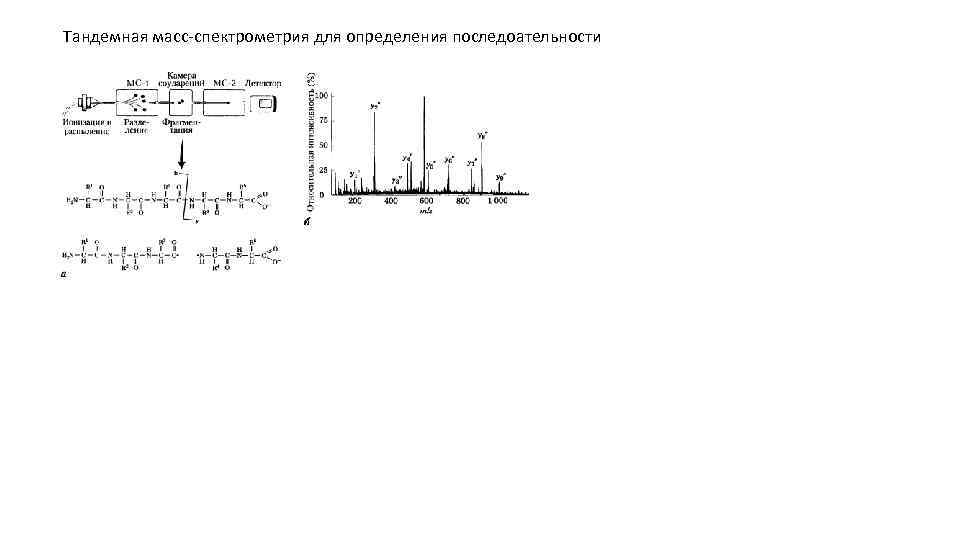
Тандемная масс-спектрометрия для определения последоательности
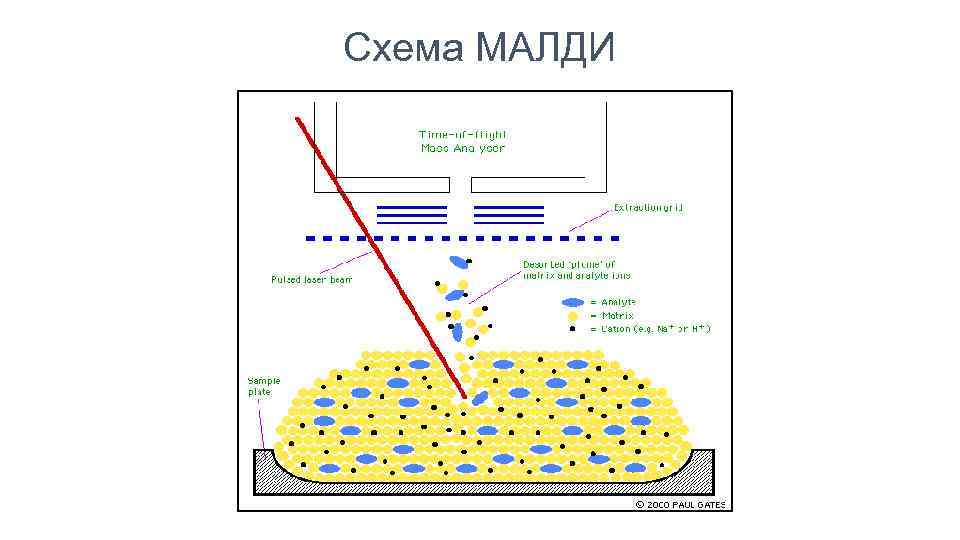
Схема МАЛДИ
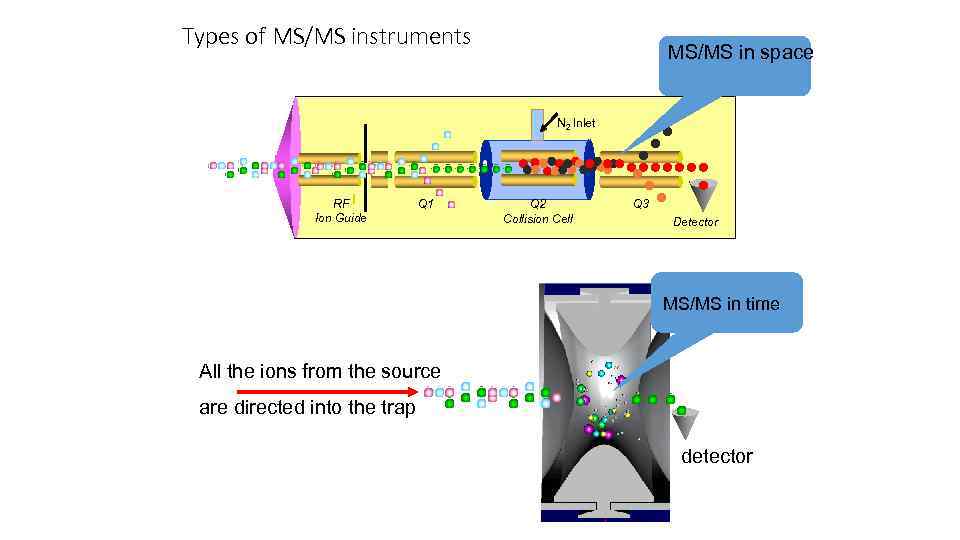
Types of MS/MS instruments MS/MS in space N 2 Inlet RF Ion Guide Q 1 Q 2 Collision Cell Q 3 Detector MS/MS in time All the ions from the source are directed into the trap detector
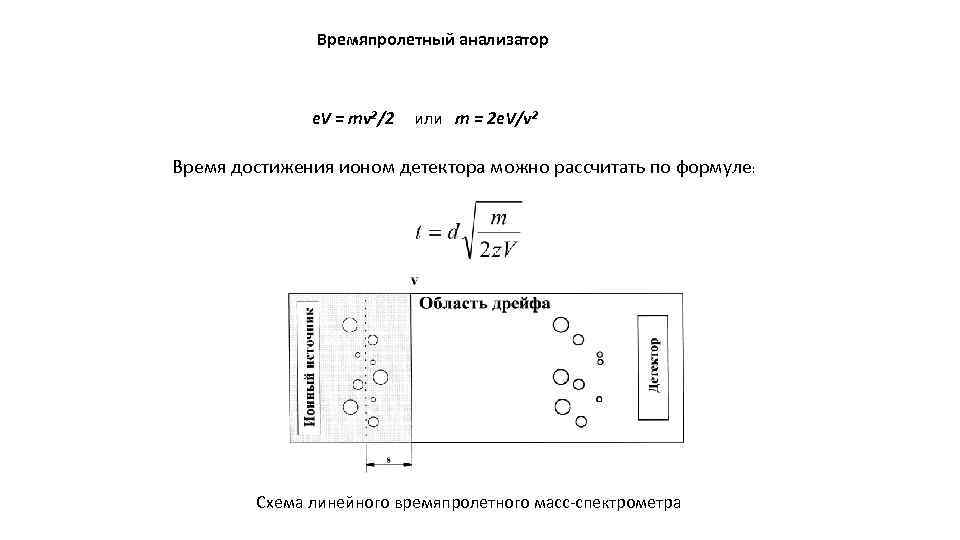
Времяпролетный анализатор e. V = mv 2/2 или m = 2 e. V/v 2 Время достижения ионом детектора можно рассчитать по формуле: Схема линейного времяпролетного масс-спектрометра
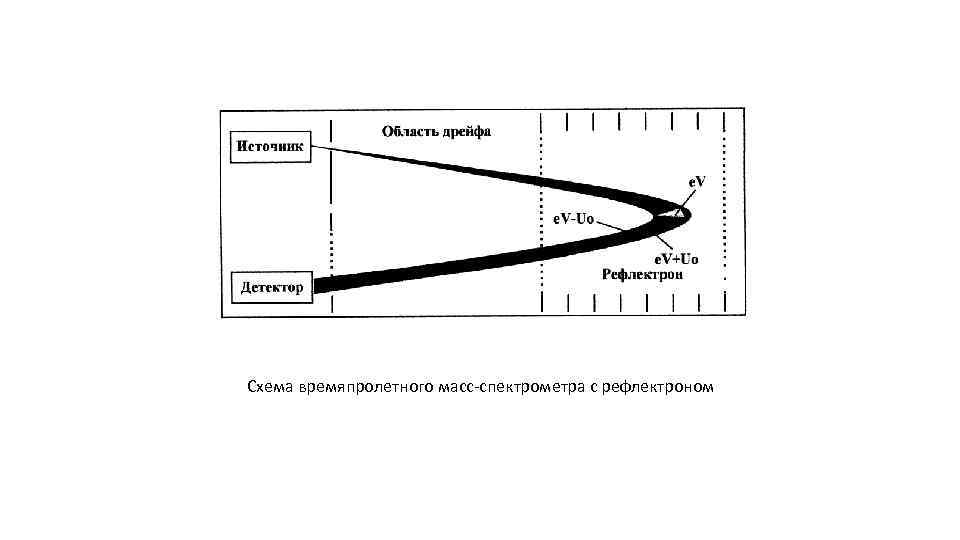
Схема времяпролетного масс-спектрометра с рефлектроном
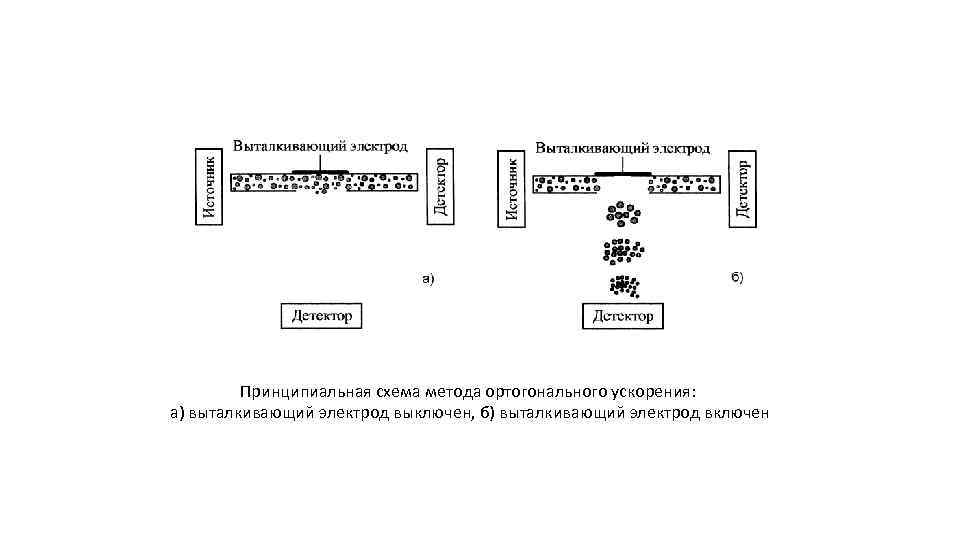
Принципиальная схема метода ортогонального ускорения: а) выталкивающий электрод выключен, б) выталкивающий электрод включен
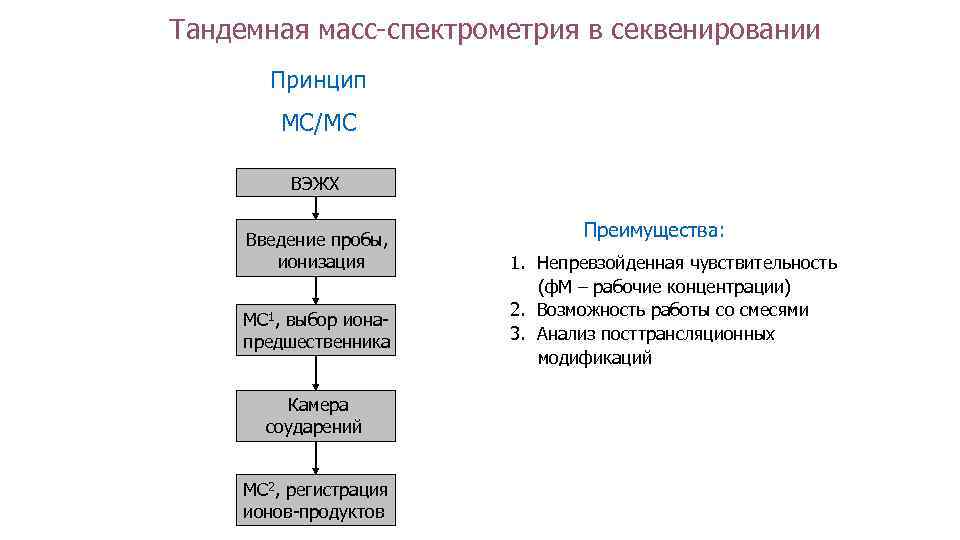
Тандемная масс-спектрометрия в секвенировании Принцип МС/МС ВЭЖХ Введение пробы, ионизация МС 1, выбор ионапредшественника Камера соударений МС 2, регистрация ионов-продуктов Преимущества: 1. Непревзойденная чувствительность (ф. М – рабочие концентрации) 2. Возможность работы со смесями 3. Анализ посттрансляционных модификаций
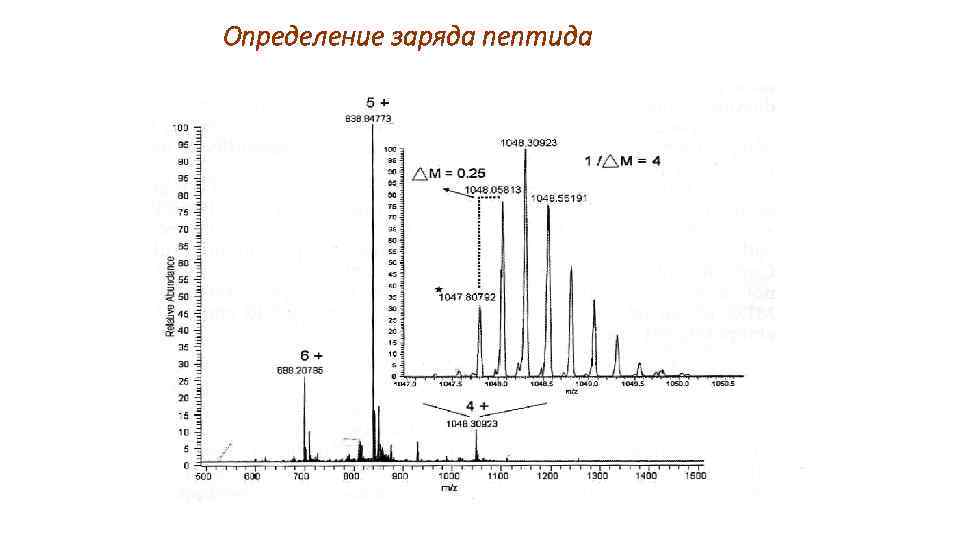
Определение заряда пептида
![Кластер октапротонированной молекулы пептида [M + 8 H]8+ с моноизотопной молекулярной массой 4813, 6974 Кластер октапротонированной молекулы пептида [M + 8 H]8+ с моноизотопной молекулярной массой 4813, 6974](https://present5.com/presentation/-90933273_378534262/image-26.jpg)
Кластер октапротонированной молекулы пептида [M + 8 H]8+ с моноизотопной молекулярной массой 4813, 6974 единиц

Типы разрывов пептидной цепи и обозначение ионов, образующихся при фрагментации протонированных молекул пептидов

Стратегия de novo секвенирования пептидов в ручном режиме Найти иммониевые ионы в области низких значений m/z Найти пару ионов b 2 -a 2 в области низких значений m/z Найти y 1 -ион в области низких значений m/z Идентифицировать ион у n-1 в области высоких значений m/z Максимально расширить серии у-ионов в область низких значений m/z и b-ионов в область высоких значений m/z • Рассчитать массу пептида • Сверить полученный аминокислотный состав пептида с его спектром (соответствие иммониевых ионов и заряда пептида с установленной структурой) • Идентифицировать все ионы в спектре, т. е. увязать все интенсивные пики спектра с полученной структурой пептида. Обратить внимание на нейтральные потери в виде Н 2 О, NH 3, HSOCH 3. ; на присутствие двухзарядных ионов и другие возможные разрывы • • •
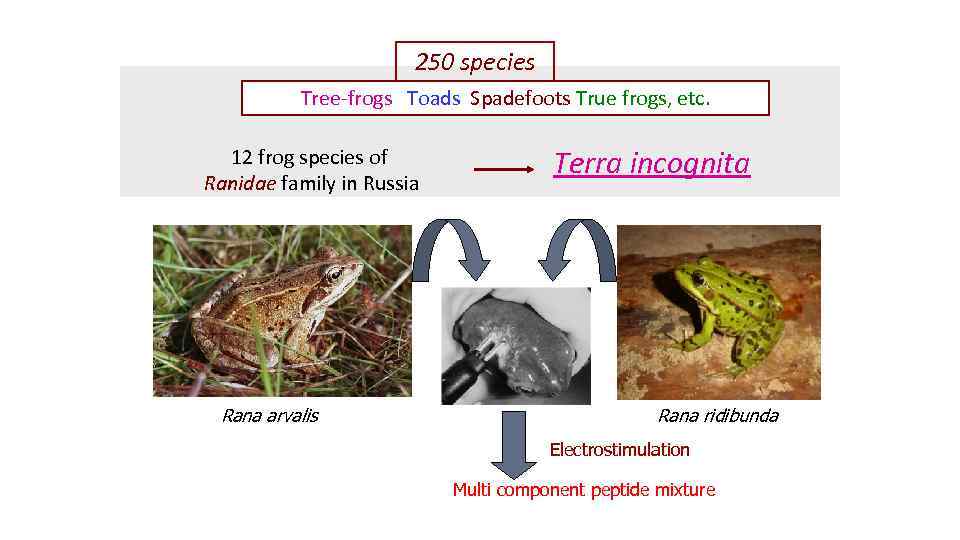
250 species Tree-frogs Toads Spadefoots True frogs, etc. 12 frog species of Ranidae family in Russia Rana arvalis Terra incognita Rana ridibunda Electrostimulation Multi component peptide mixture
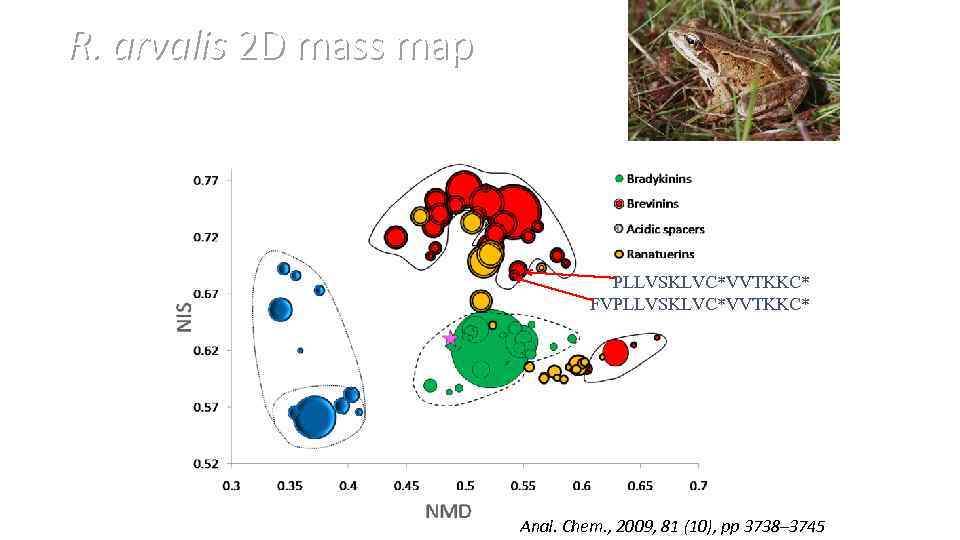
R. arvalis 2 D mass map PLLVSKLVC*VVTKKC* FVPLLVSKLVC*VVTKKC* Anal. Chem. , 2009, 81 (10), pp 3738– 3745

Лекция 3 Аминокислоты белки.pptx