_Sem_03_Aminoacids & Proteins.pptx
- Количество слайдов: 48

АМИНОКИСЛОТЫ Общее строение и структура всех АМК Физико-химические свойства Классификация Взаимодействие радикалов Спектральные свойства Модификации радикалов
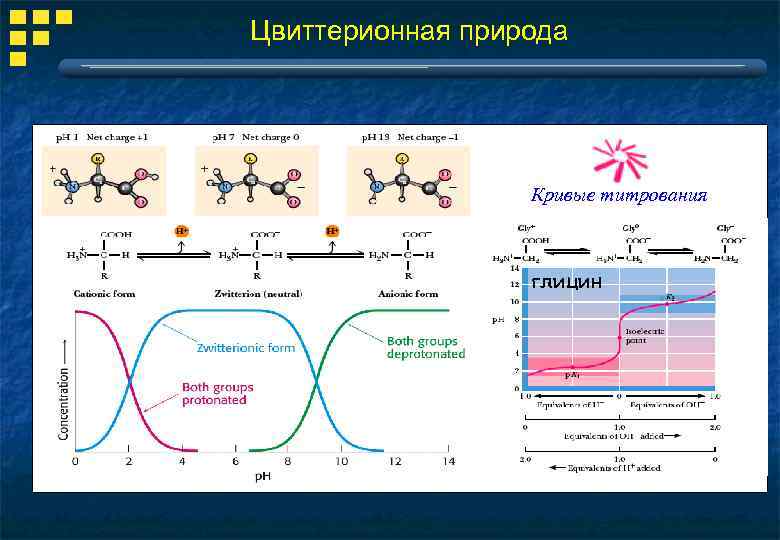
Цвиттерионная природа Кривые титрования глицин
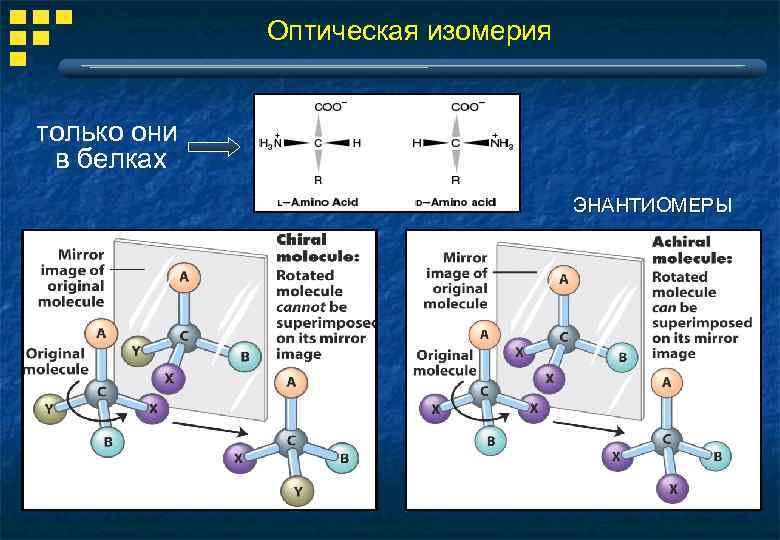
Оптическая изомерия только они в белках ЭНАНТИОМЕРЫ

Оптическое вращение 1815 - оптическое вращение кварца (J. -B. Biot) 1848 - кристаллы Na-NH 4 -тартрата оптически активны (L. Pasteur) 1847 - тетраэдрическая структура связей углерода (van’t Hoff) 1888 -1891 - относительная конфигурация (+)-глюкозы (Emil Fisher Нобелевская премия 1902 г) 1951 - подтверждение догадки Фишера с помощью рентгеновской дифракции (J. M. Bijvoet) (+)-глюкоза 1906 - правило Розанова (M. A. Rosanoff), согласно которому + = D. Отвергнуто Фишером, но часто употребляется именно как правило Фишера
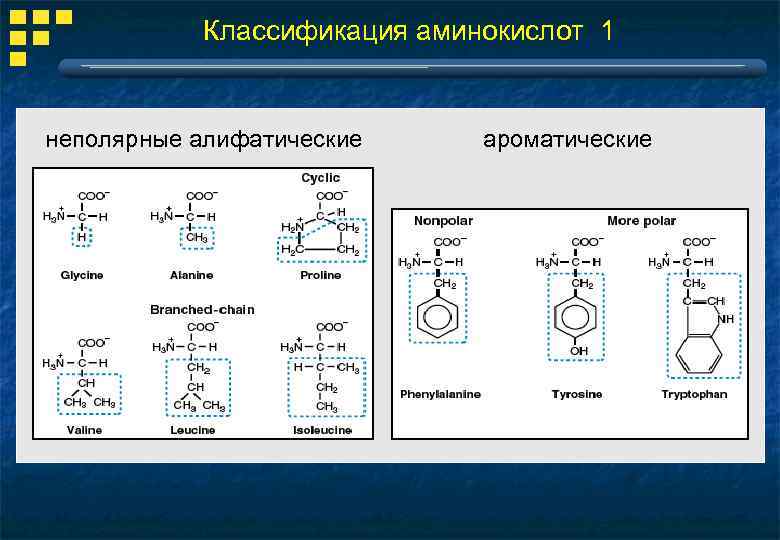
Классификация аминокислот 1 неполярные алифатические ароматические
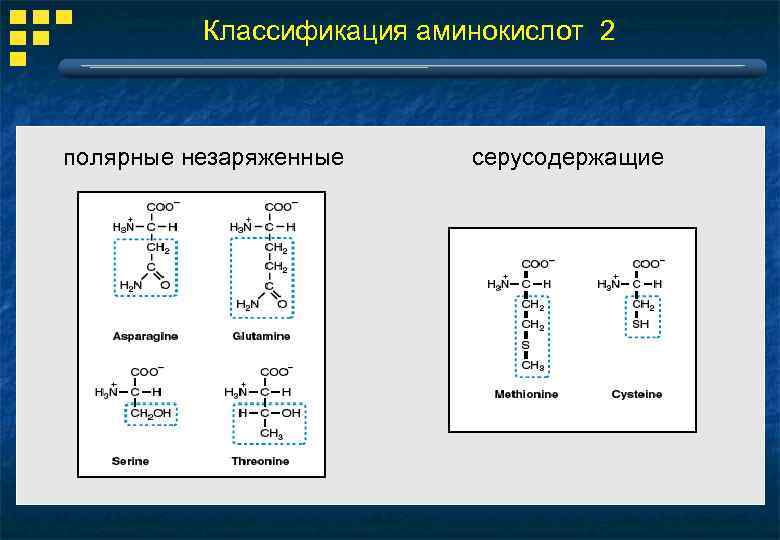
Классификация аминокислот 2 полярные незаряженные серусодержащие

Классификация аминокислот 3 заряженные положительно отрицательно
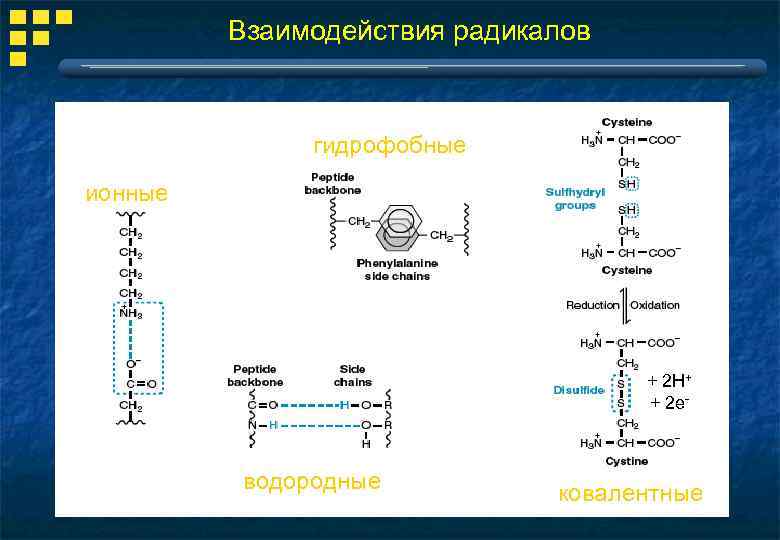
Взаимодействия радикалов гидрофобные ионные + 2 Н+ + 2 е- водородные ковалентные
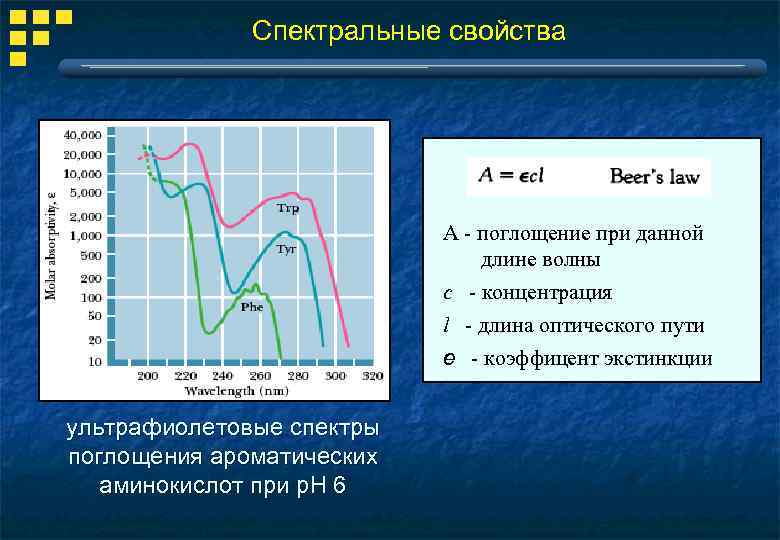
Спектральные свойства А - поглощение при данной длине волны с - концентрация l - длина оптического пути e - коэффицент экстинкции ультрафиолетовые спектры поглощения ароматических аминокислот при р. Н 6
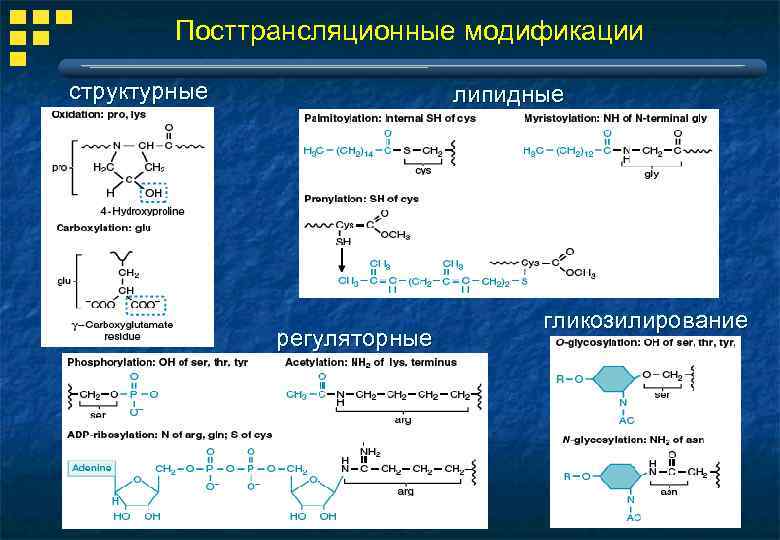
Посттрансляционные модификации структурные липидные регуляторные гликозилирование

ПЕРВИЧНАЯ СТРУКТУРА БЕЛКОВ Четыре уровня структурной организации белков Образование, строение и геометрия пептидной связи Способы определения первичной структуры белков
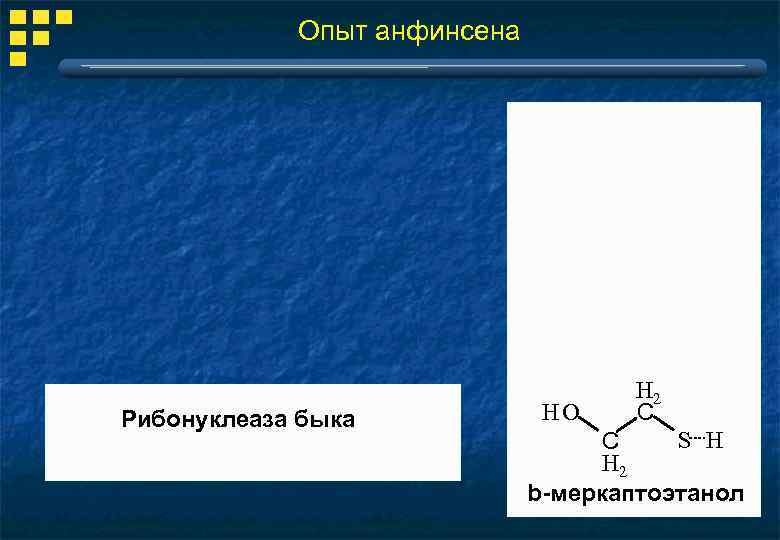
Опыт анфинсена Рибонуклеаза быка HO H 2 С S H С H 2 b-меркаптоэтанол
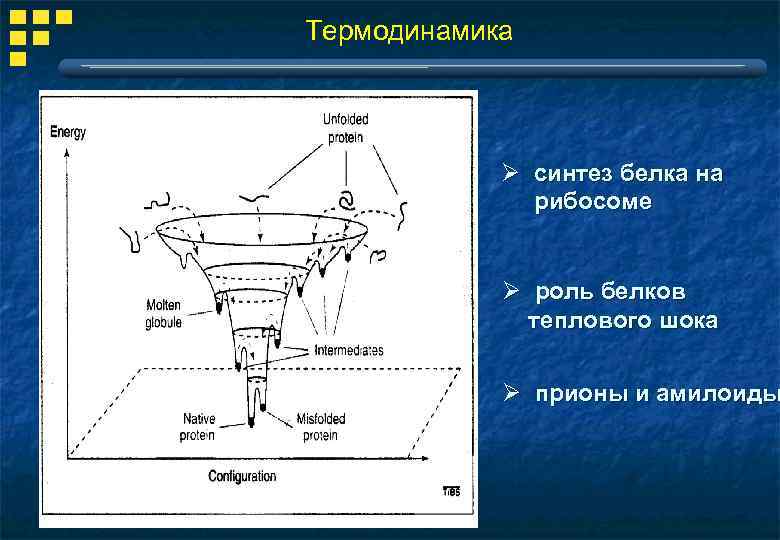
Термодинамика Ø синтез белка на рибосоме Ø роль белков теплового шока Ø прионы и амилоиды
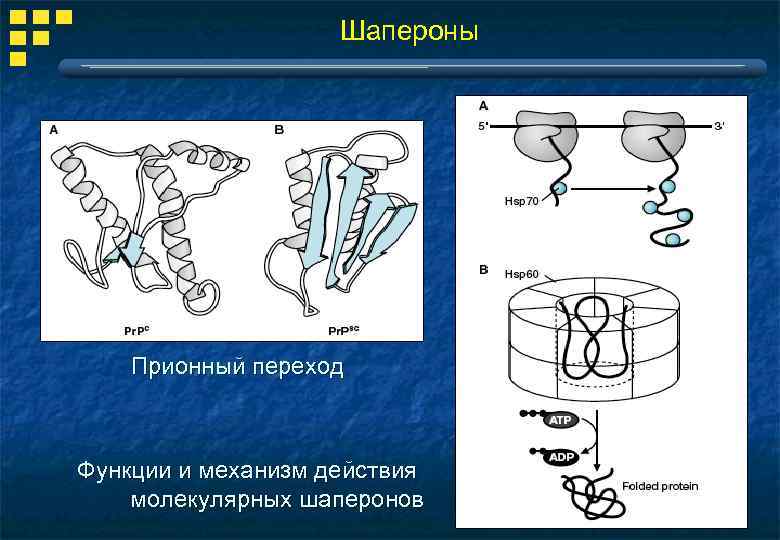
Шапероны Прионный переход Функции и механизм действия молекулярных шаперонов
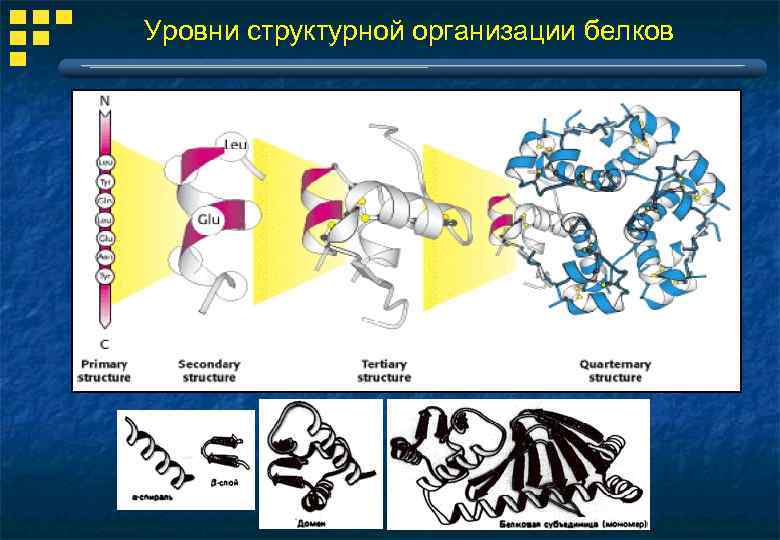
Уровни структурной организации белков
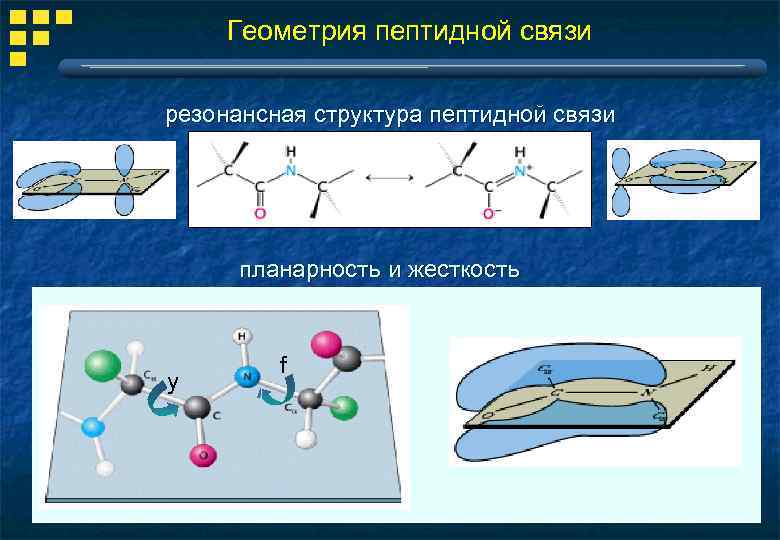
Геометрия пептидной связи резонансная структура пептидной связи планарность и жесткость y f
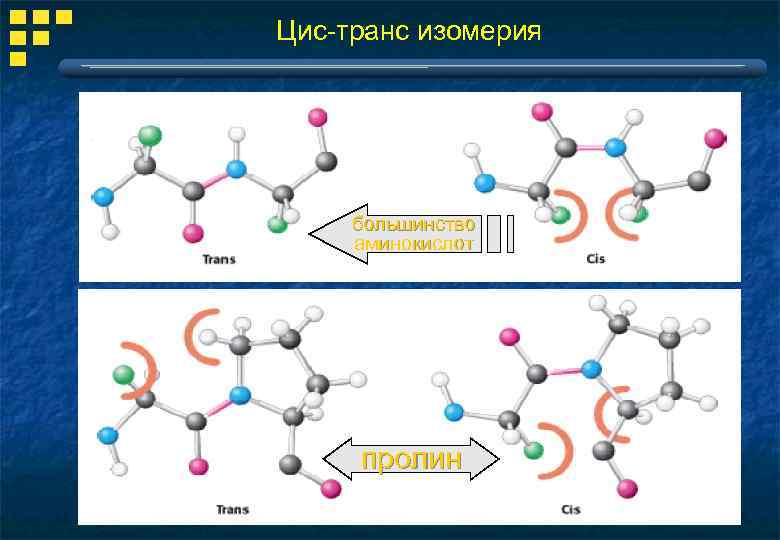
Цис-транс изомерия большинство аминокислот пролин

ВТОРИЧНАЯ СТРУКТУРА БЕЛКОВ Элементы вторичной структуры (αспираль, β-складка, поворот) Конформация полипептидной цепии вращение связей Карты Рамачандрана
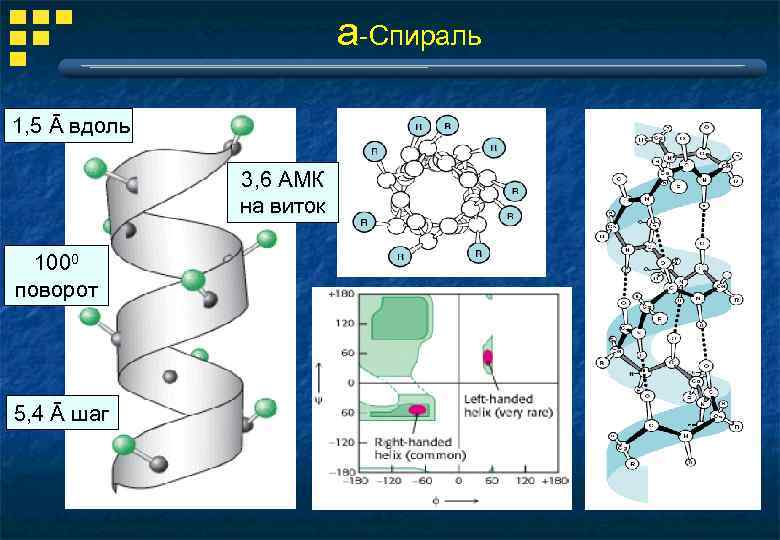
a-Спираль 1, 5 Ā вдоль 3, 6 АМК на виток 1000 поворот 5, 4 Ā шаг
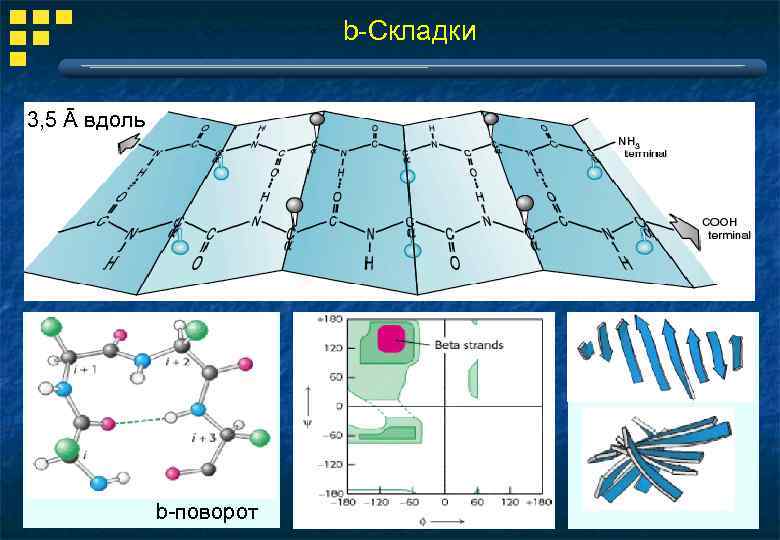
b-Складки 3, 5 Ā вдоль b-поворот
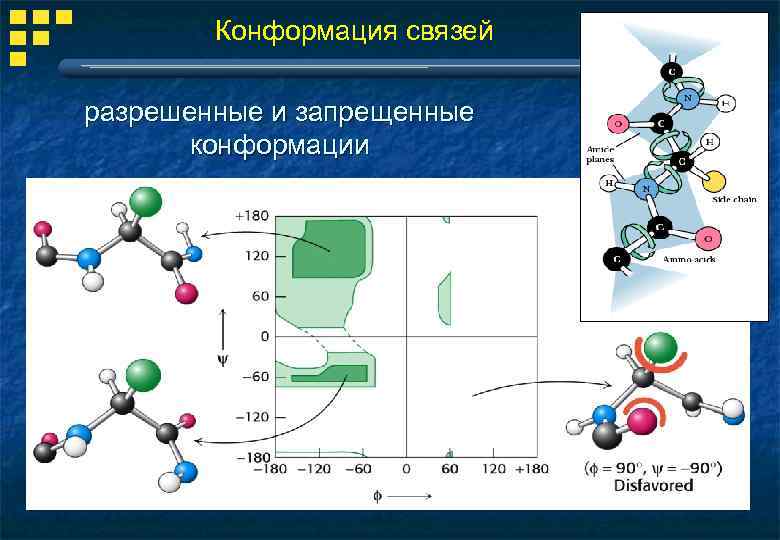
Конформация связей разрешенные и запрещенные конформации
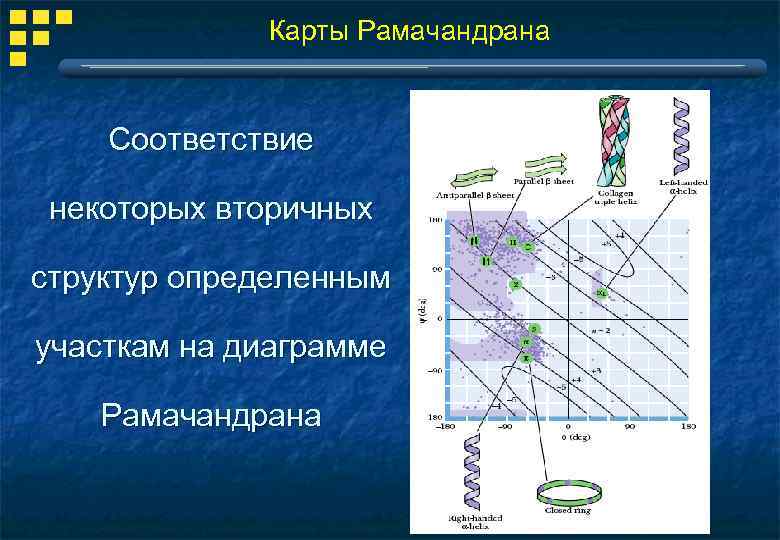
Карты Рамачандрана Соответствие некоторых вторичных структур определенным участкам на диаграмме Рамачандрана
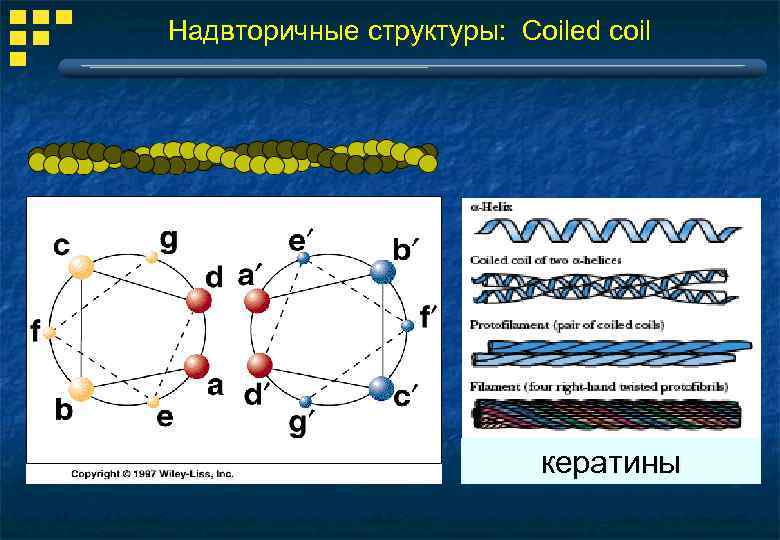
Надвторичные структуры: Coiled coil кератины
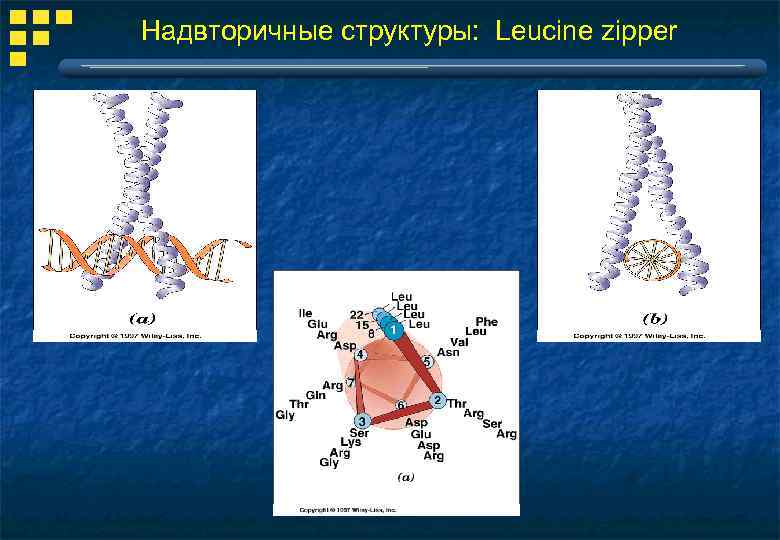
Надвторичные структуры: Leucine zipper
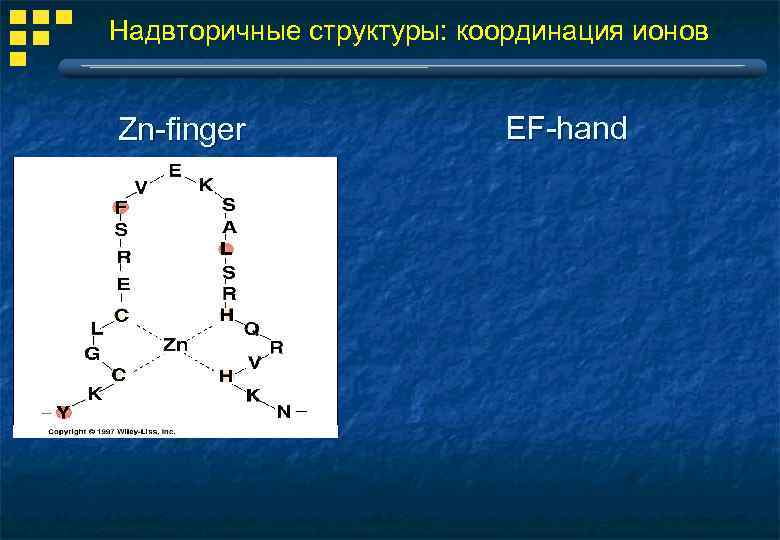
Надвторичные структуры: координация ионов Zn-finger EF-hand

ТРЕТИЧНАЯ СТРУКТУРА БЕЛКОВ Домены Модульные белки Киназы и фосфатазы Зеленый флуоресцентный белок
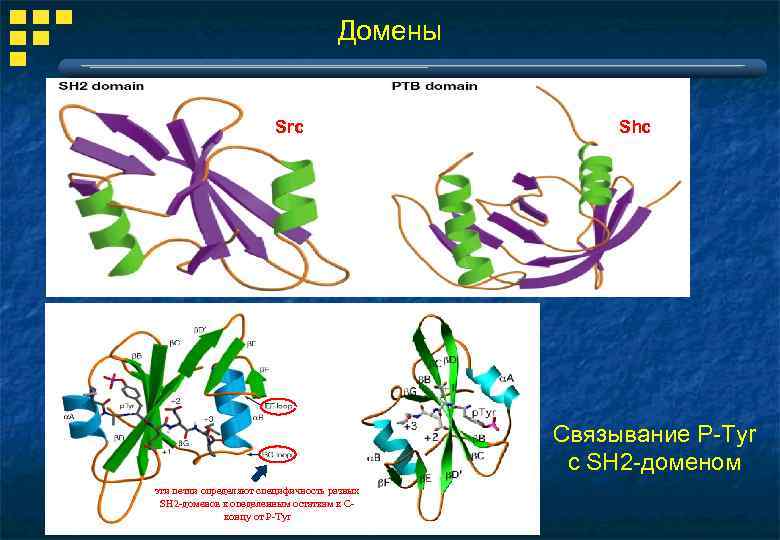
Домены Src Shc Cвязывание P-Tyr с SH 2 -доменом эти петли определяют специфичность разных SH 2 -доменов к опеделенным остаткам к Сконцу от P-Tyr
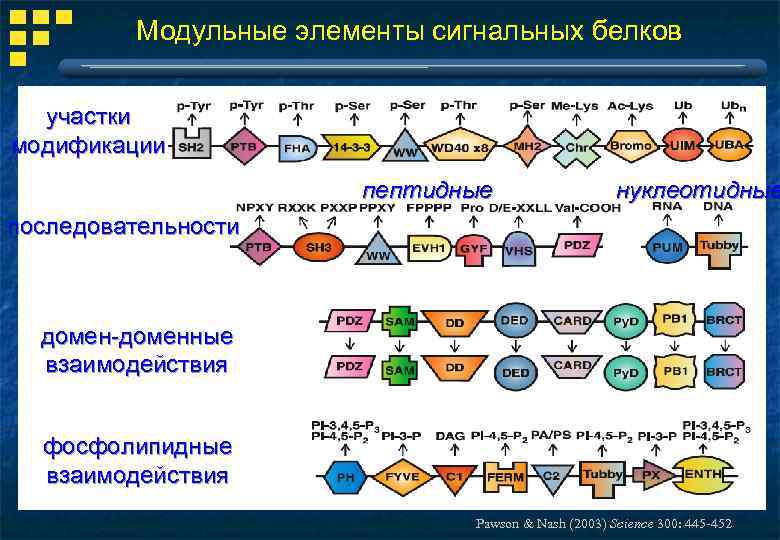
Модульные элементы сигнальных белков участки модификации пептидные нуклеотидные последовательности домен-доменные взаимодействия фосфолипидные взаимодействия Pawson & Nash (2003) Science 300: 445 -452
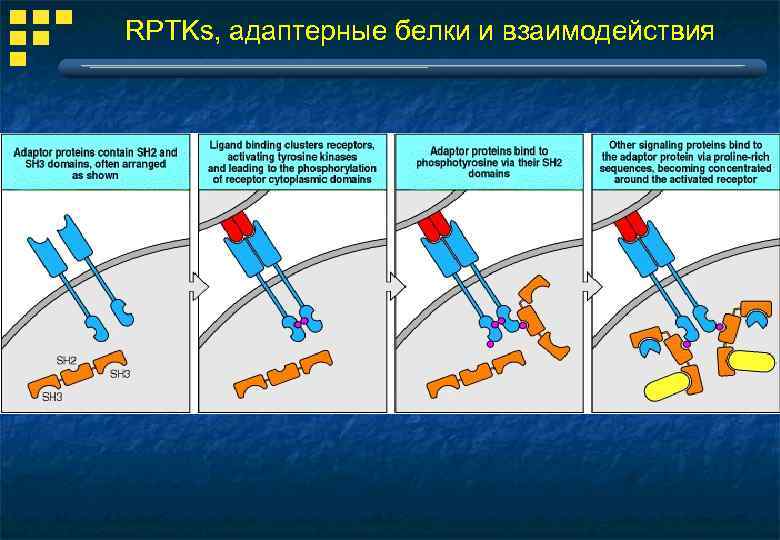
RPTKs, адаптерные белки и взаимодействия
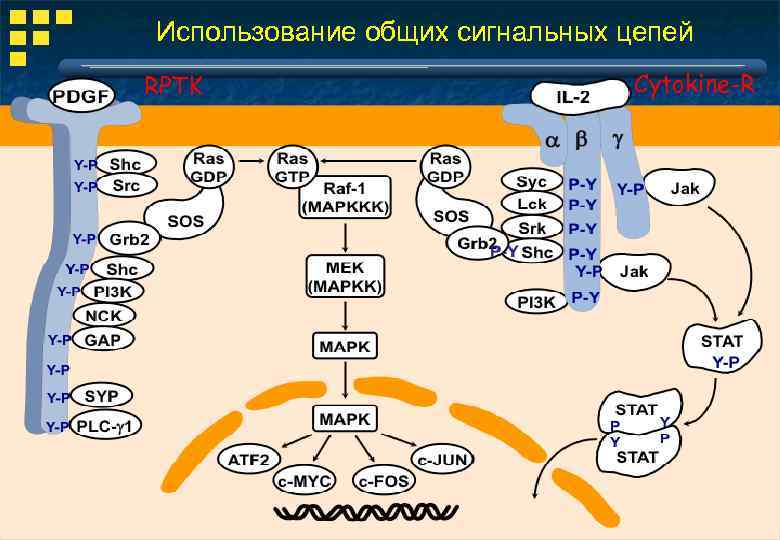
Использование общих сигнальных цепей RPTK Cytokine-R
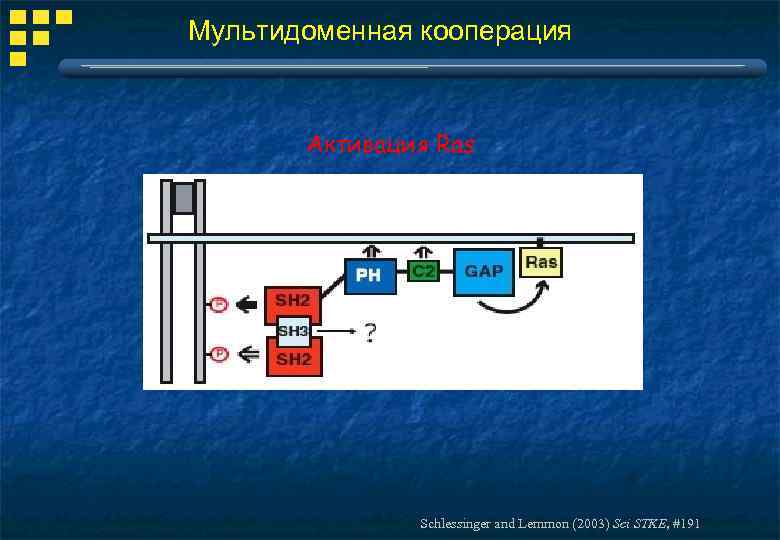
Мультидоменная кооперация Активация Ras Schlessinger and Lemmon (2003) Sci STKE, #191
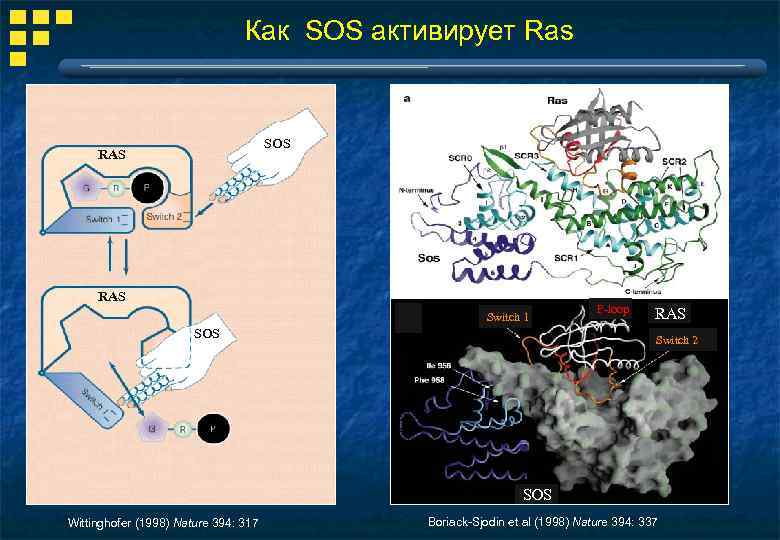
Как SOS активирует Ras SOS RAS Switch 1 SOS P-loop RAS Switch 2 SOS Wittinghofer (1998) Nature 394: 317 Boriack-Sjodin et al (1998) Nature 394: 337
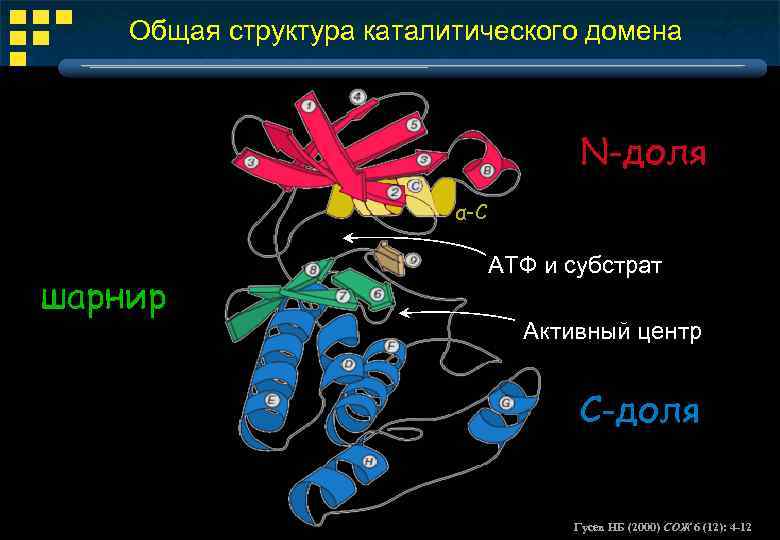
Общая структура каталитического домена N-доля α-С шарнир АТФ и субстрат Активный центр C-доля Гусев НБ (2000) СОЖ 6 (12): 4 -12
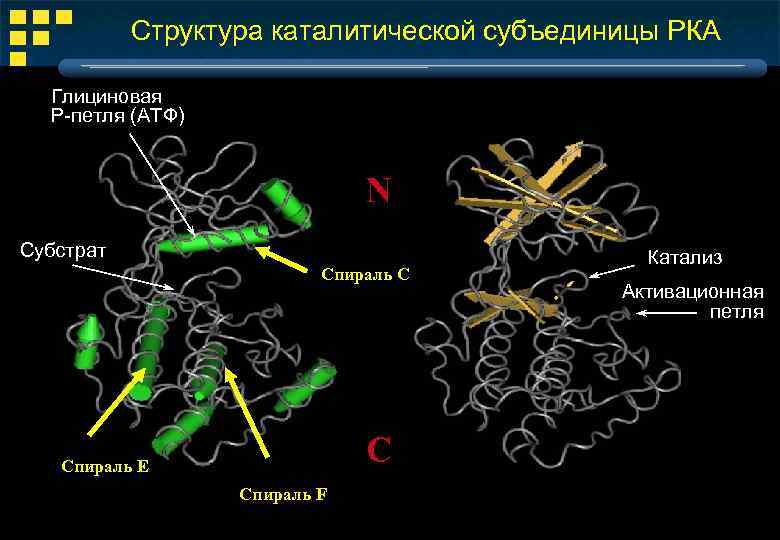
Структура каталитической субъединицы РКА Глициновая P-петля (ATФ) N Субстрат Спираль C C Спираль E Спираль F Катализ Активационная петля
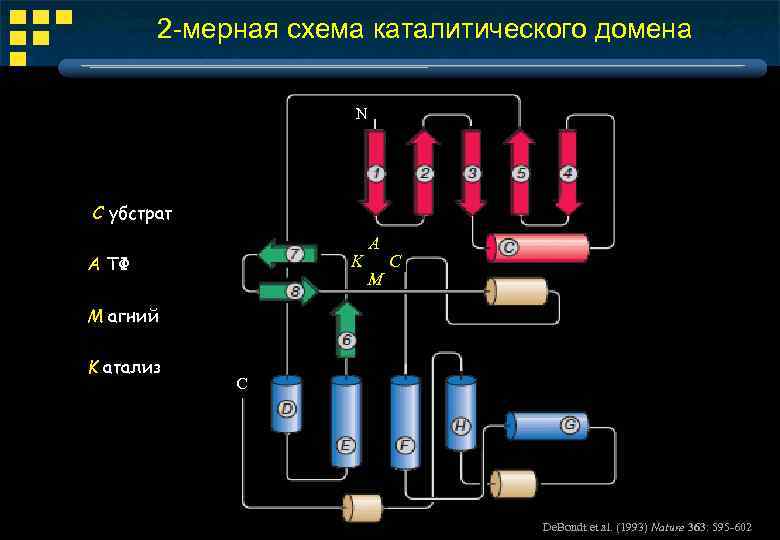
2 -мерная схема каталитического домена Ν С убстрат А ТФ K А M С М агний K атализ C De. Bondt et al. (1993) Nature 363: 595 -602
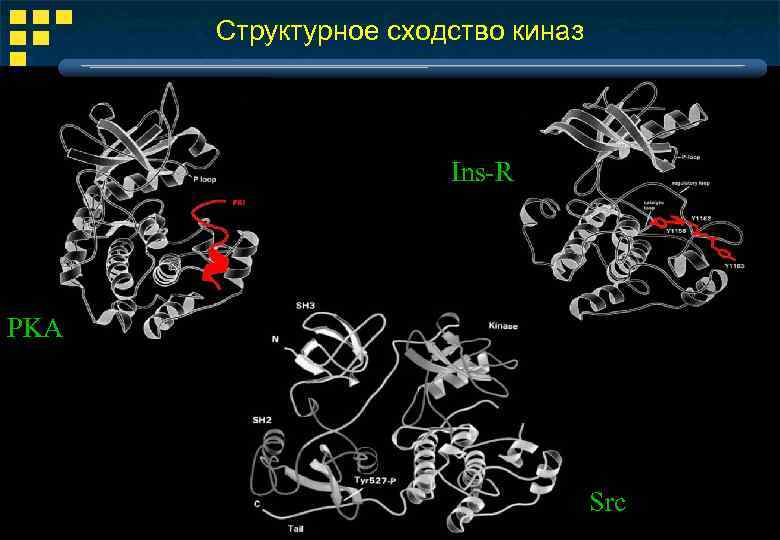
Структурное сходство киназ Ins-R PKA Src
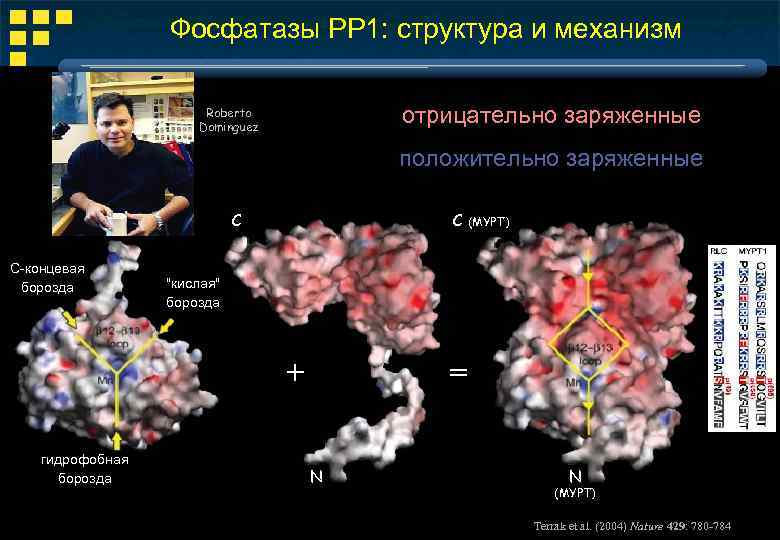
Фосфатазы РР 1: структура и механизм отрицательно заряженные Roberto Dominguez положительно заряженные C С-концевая борозда С (MYPT) "кислая" борозда + гидрофобная борозда = N N (MYPT) Terrak et al. (2004) Nature 429: 780 -784
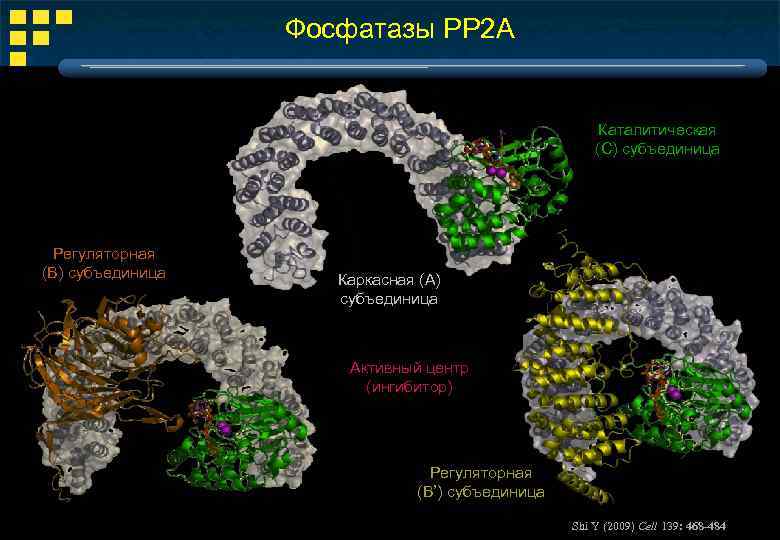
Фосфатазы РР 2 А Каталитическая (С) субъединица Регуляторная (В) субъединица Каркасная (А) субъединица Активный центр (ингибитор) Регуляторная (В’) субъединица Shi Y (2009) Cell 139: 468 -484
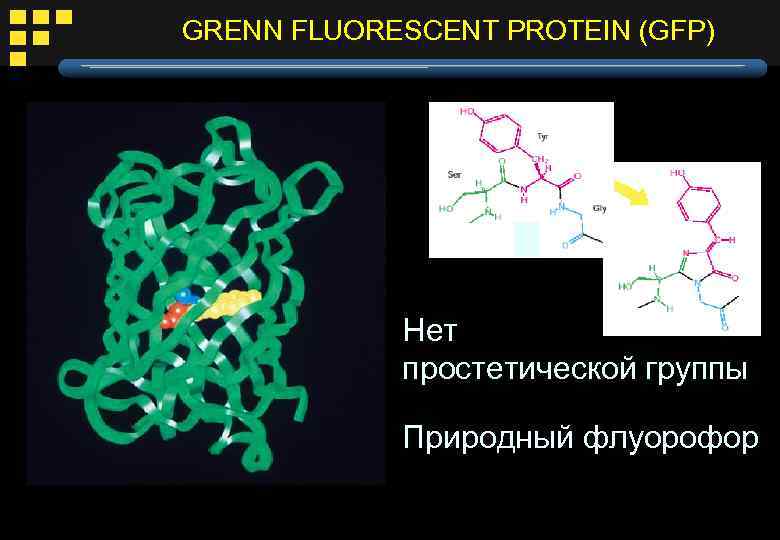
GRENN FLUORESCENT PROTEIN (GFP) Нет простетической группы Природный флуорофор
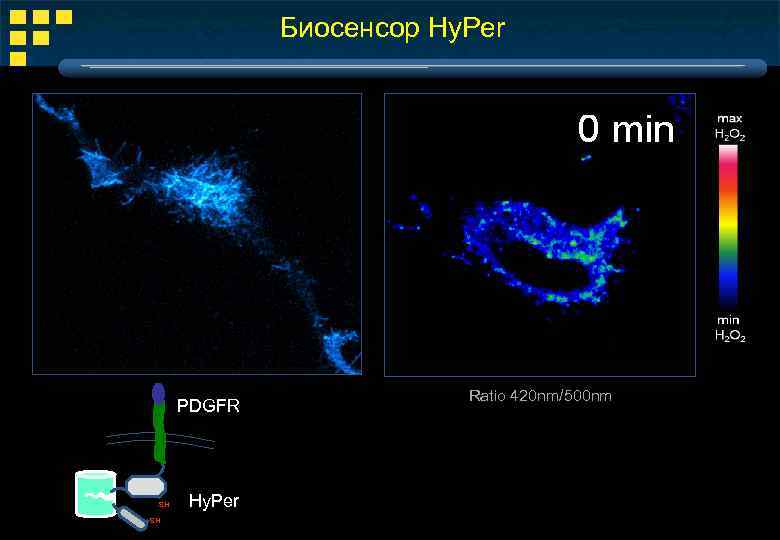
Биосенсор Hy. Per PDGFR SH SH Hy. Per Ratio 420 nm/500 nm
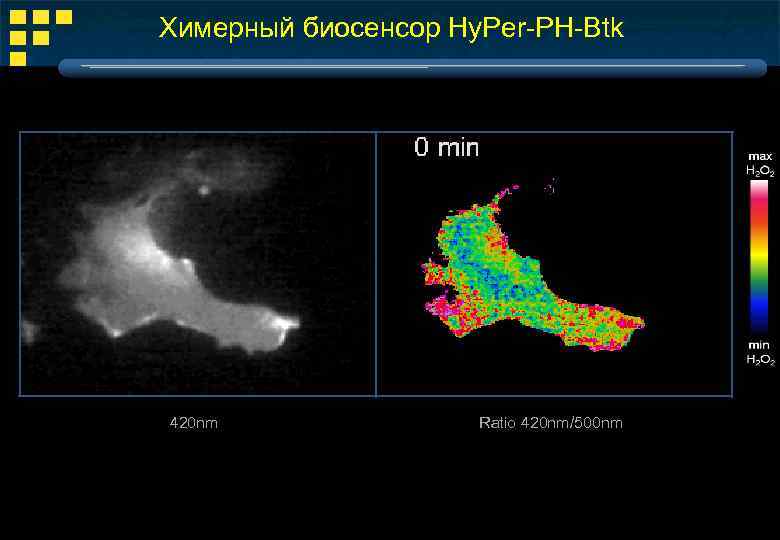
Xимерный биосенсор Hy. Per-PH-Btk 420 nm Ratio 420 nm/500 nm

ЧЕТВЕРТИЧНАЯ СТРУКТУРА БЕЛКОВ
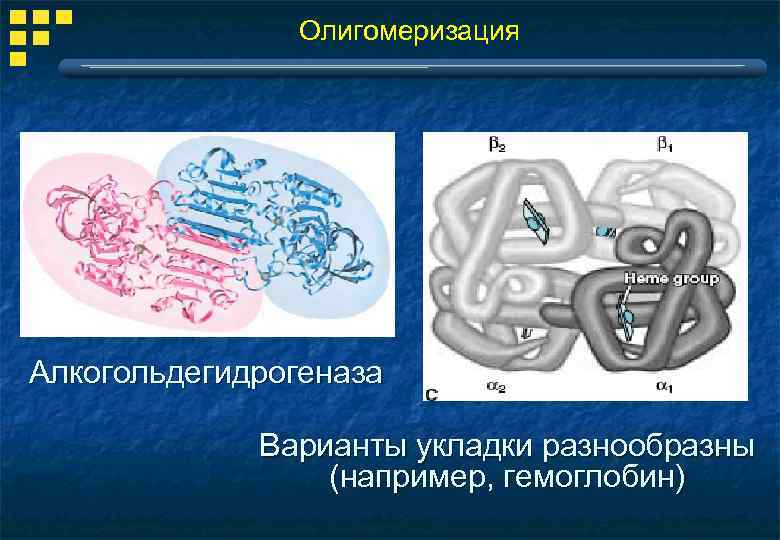
Олигомеризация Алкогольдегидрогеназа Варианты укладки разнообразны (например, гемоглобин)

Виды надмолекулярных структур Олигомеризация из мономеров (гемоглобин) Сборка комплексов из разных субъединиц Модификация: - гликопротеиды - протеогликаны - гликолипиды Образование функциональных комплексов с другими типами соединений (липопротеиды, каналы, холоферменты)
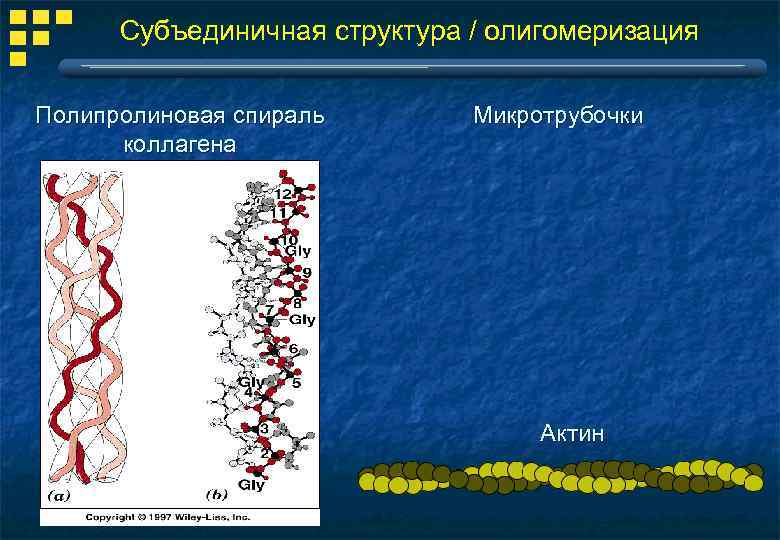
Субъединичная структура / олигомеризация Полипролиновая спираль коллагена Микротрубочки Актин
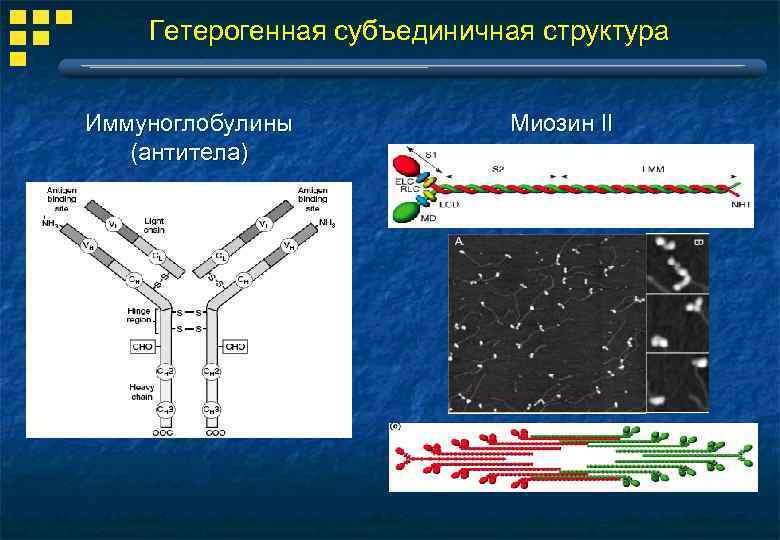
Гетерогенная субъединичная структура Иммуноглобулины (антитела) Миозин II
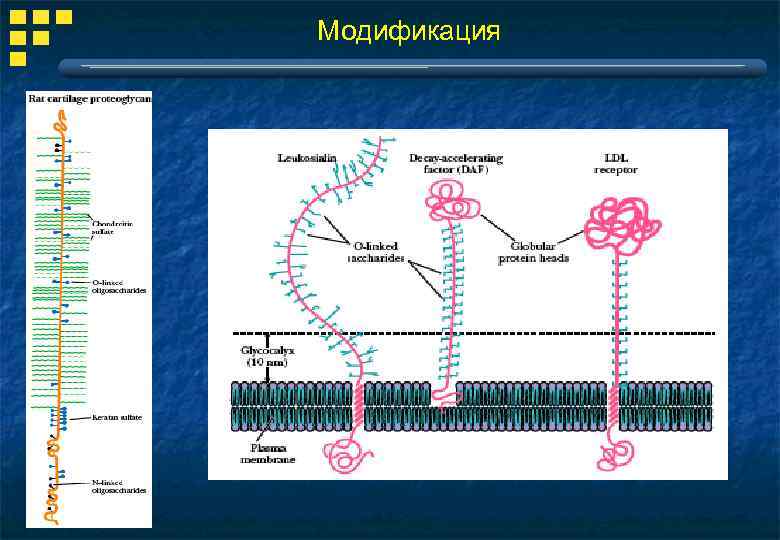
Модификация
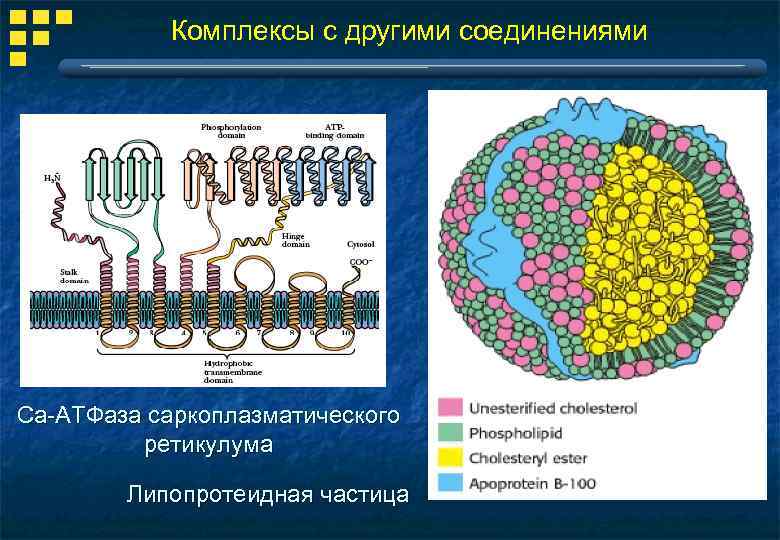
Комплексы с другими соединениями Cа-АТФаза саркоплазматического ретикулума Липопротеидная частица
_Sem_03_Aminoacids & Proteins.pptx