Аминокислоты.ppt
- Количество слайдов: 33
 Аминокислоты и пептиды План лекции 1. Структура и классификация аминокислот. 2. Стереохимия аминокислот 3. Физико-химические свойства аминокислот: амфотерность, реакционная способность аминокислот. 4. Принципы организации и биологическая роль важнейших природных пептидов.
Аминокислоты и пептиды План лекции 1. Структура и классификация аминокислот. 2. Стереохимия аминокислот 3. Физико-химические свойства аминокислот: амфотерность, реакционная способность аминокислот. 4. Принципы организации и биологическая роль важнейших природных пептидов.
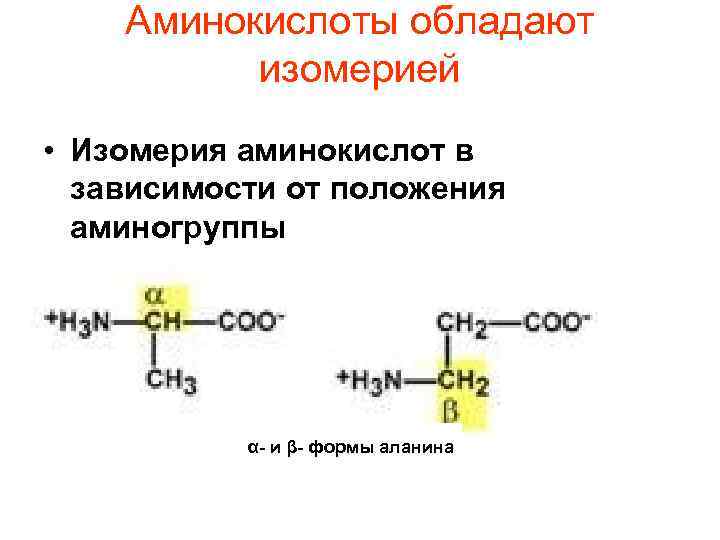 Аминокислоты обладают изомерией • Изомерия аминокислот в зависимости от положения аминогруппы α- и β- формы аланина
Аминокислоты обладают изомерией • Изомерия аминокислот в зависимости от положения аминогруппы α- и β- формы аланина
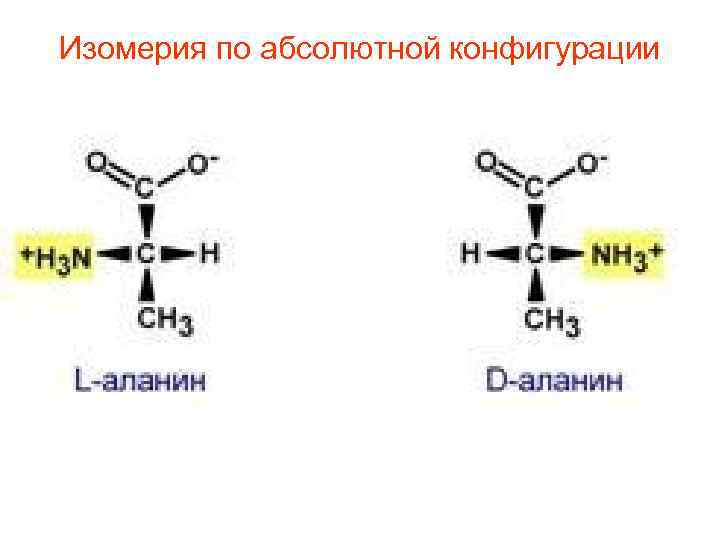 Изомерия по абсолютной конфигурации
Изомерия по абсолютной конфигурации
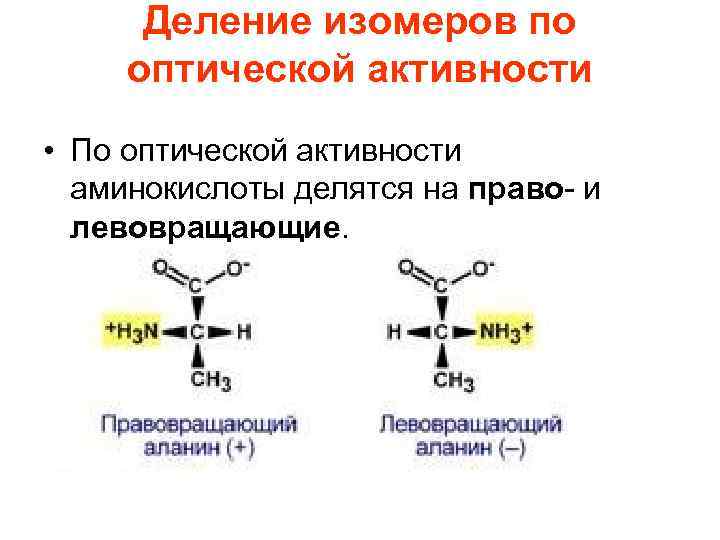 Деление изомеров по оптической активности • По оптической активности аминокислоты делятся на право- и левовращающие.
Деление изомеров по оптической активности • По оптической активности аминокислоты делятся на право- и левовращающие.
 • Деление на L- и D-формы не соответствует делению на право- и левовращающие. Для одних аминокислот L-формы (или D-формы) являются правовращающими, для других – левовращающими. Например, L-аланин – правовращающий, а L-фенилаланин – левовращающий. При смешивании L- и Dформ одной аминокислоты образуется рацемическая смесь, не обладающая оптической активностью.
• Деление на L- и D-формы не соответствует делению на право- и левовращающие. Для одних аминокислот L-формы (или D-формы) являются правовращающими, для других – левовращающими. Например, L-аланин – правовращающий, а L-фенилаланин – левовращающий. При смешивании L- и Dформ одной аминокислоты образуется рацемическая смесь, не обладающая оптической активностью.
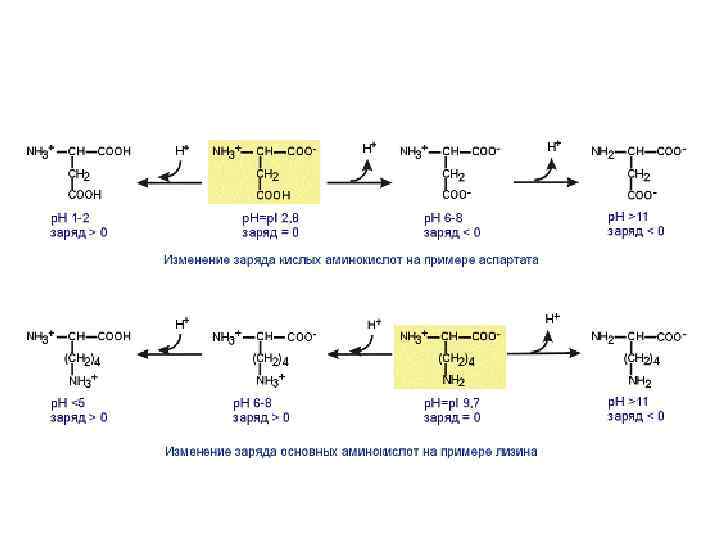
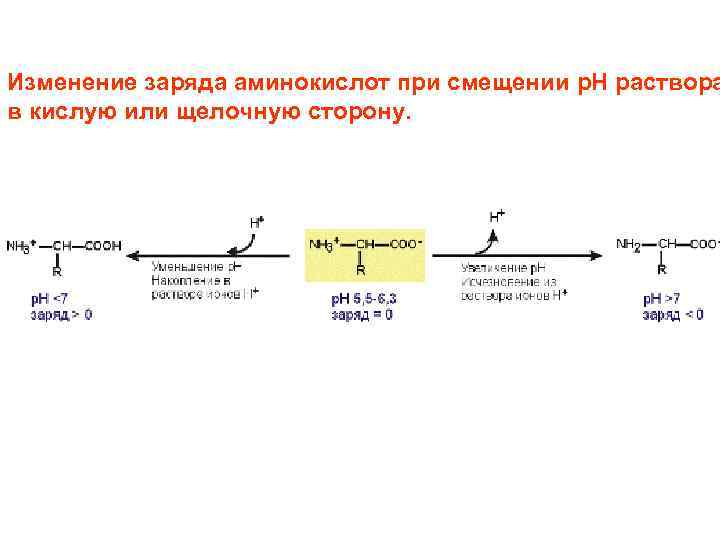 Изменение заряда аминокислот при смещении р. Н раствора в кислую или щелочную сторону.
Изменение заряда аминокислот при смещении р. Н раствора в кислую или щелочную сторону.
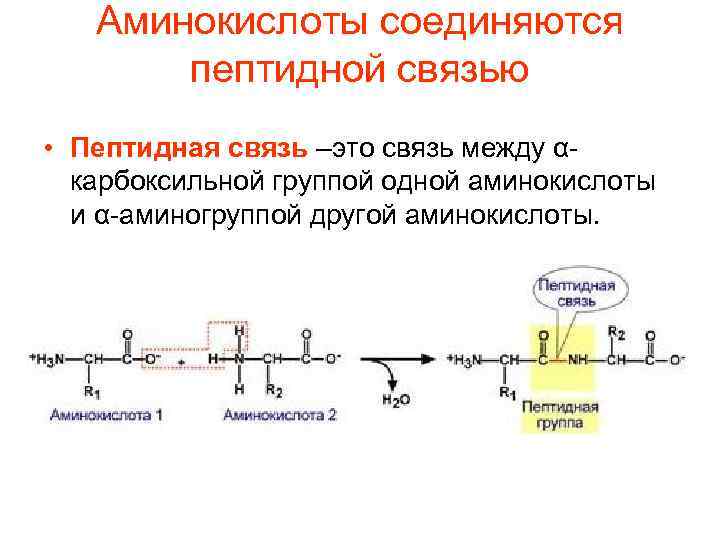 Аминокислоты соединяются пептидной связью • Пептидная связь –это связь между αкарбоксильной группой одной аминокислоты и α-аминогруппой другой аминокислоты.
Аминокислоты соединяются пептидной связью • Пептидная связь –это связь между αкарбоксильной группой одной аминокислоты и α-аминогруппой другой аминокислоты.
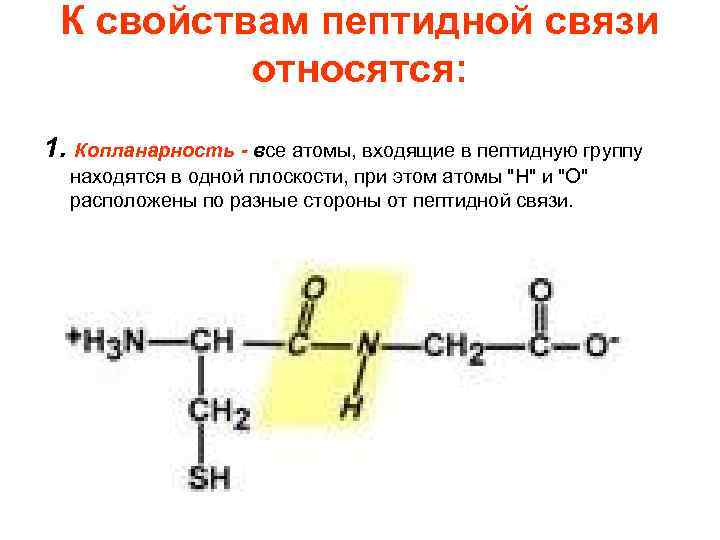 К свойствам пептидной связи относятся: 1. Копланарность - все атомы, входящие в пептидную группу находятся в одной плоскости, при этом атомы "Н" и "О" расположены по разные стороны от пептидной связи.
К свойствам пептидной связи относятся: 1. Копланарность - все атомы, входящие в пептидную группу находятся в одной плоскости, при этом атомы "Н" и "О" расположены по разные стороны от пептидной связи.
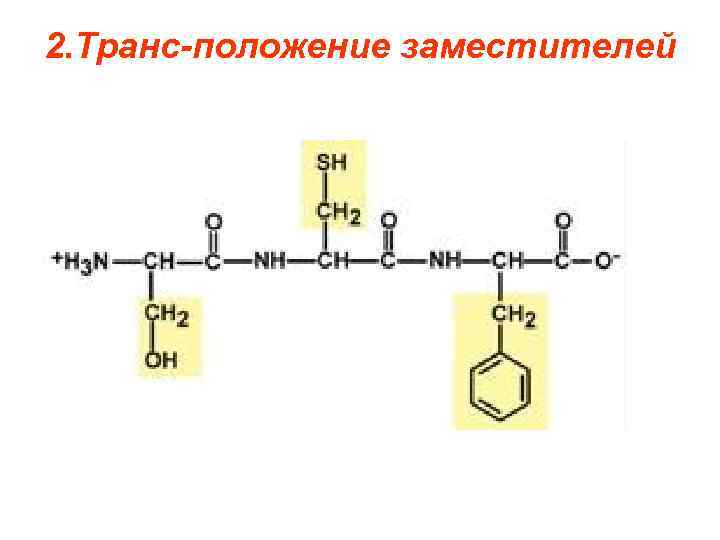 2. Транс-положение заместителей
2. Транс-положение заместителей
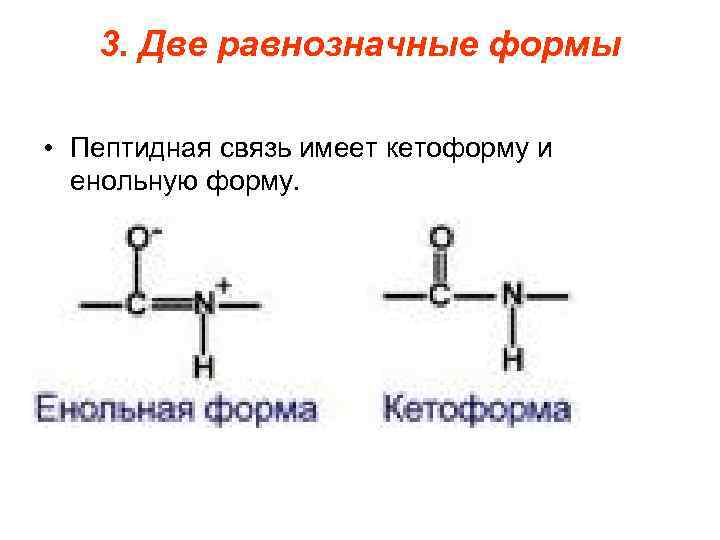 3. Две равнозначные формы • Пептидная связь имеет кетоформу и енольную форму.
3. Две равнозначные формы • Пептидная связь имеет кетоформу и енольную форму.
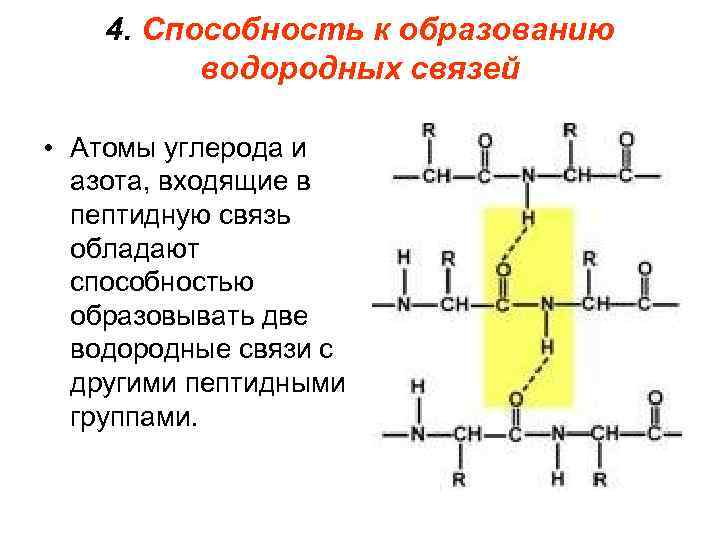 4. Способность к образованию водородных связей • Атомы углерода и азота, входящие в пептидную связь обладают способностью образовывать две водородные связи с другими пептидными группами.
4. Способность к образованию водородных связей • Атомы углерода и азота, входящие в пептидную связь обладают способностью образовывать две водородные связи с другими пептидными группами.
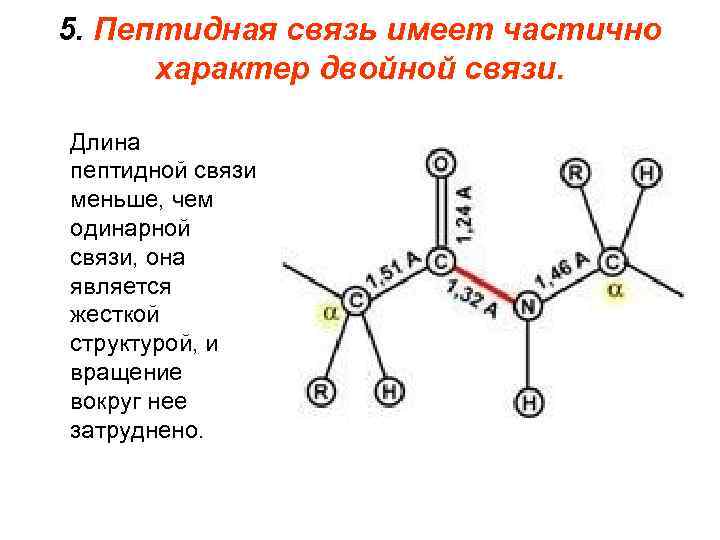 5. Пептидная связь имеет частично характер двойной связи. Длина пептидной связи меньше, чем одинарной связи, она является жесткой структурой, и вращение вокруг нее затруднено.
5. Пептидная связь имеет частично характер двойной связи. Длина пептидной связи меньше, чем одинарной связи, она является жесткой структурой, и вращение вокруг нее затруднено.
 Биохимически важные свойства аминокислот • Реакции трансаминирования (переаминирования) • Реакции дезаминирования • Реакции декарбоксилирования
Биохимически важные свойства аминокислот • Реакции трансаминирования (переаминирования) • Реакции дезаминирования • Реакции декарбоксилирования
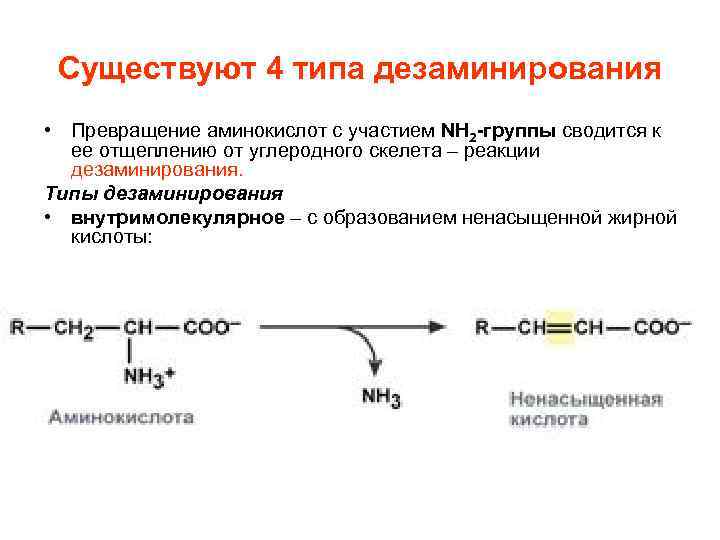 Существуют 4 типа дезаминирования • Превращение аминокислот с участием NH 2 -группы сводится к ее отщеплению от углеродного скелета – реакции дезаминирования. Типы дезаминирования • внутримолекулярное – с образованием ненасыщенной жирной кислоты:
Существуют 4 типа дезаминирования • Превращение аминокислот с участием NH 2 -группы сводится к ее отщеплению от углеродного скелета – реакции дезаминирования. Типы дезаминирования • внутримолекулярное – с образованием ненасыщенной жирной кислоты:
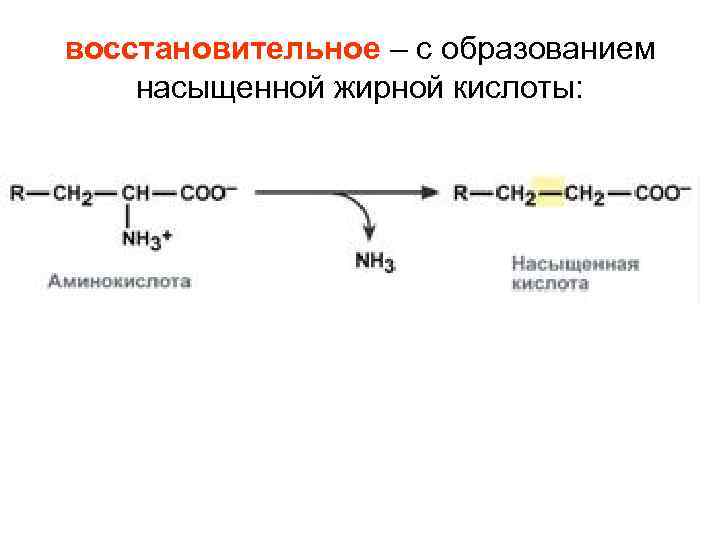 восстановительное – с образованием насыщенной жирной кислоты:
восстановительное – с образованием насыщенной жирной кислоты:
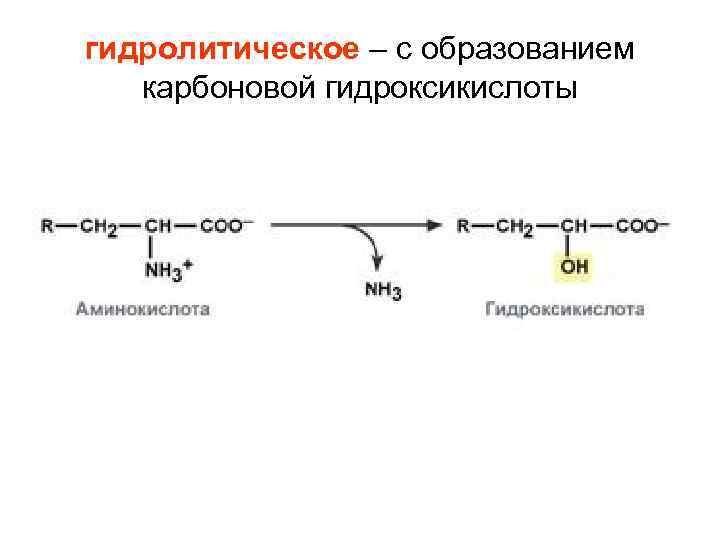 гидролитическое – с образованием карбоновой гидроксикислоты
гидролитическое – с образованием карбоновой гидроксикислоты
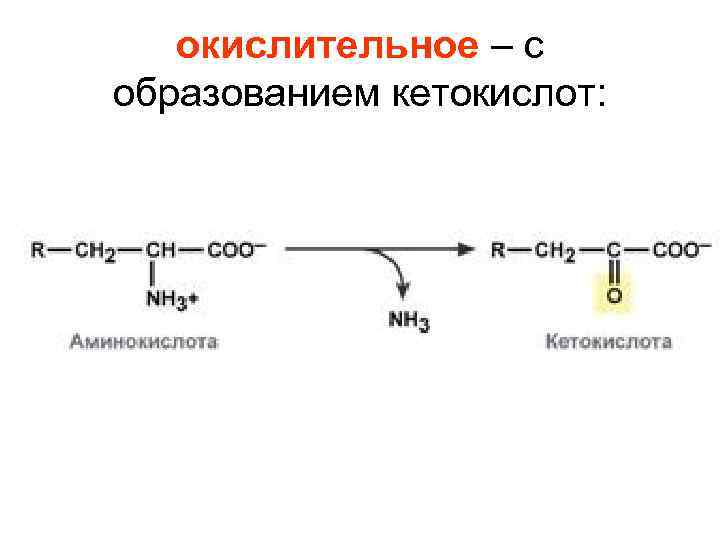 окислительное – с образованием кетокислот:
окислительное – с образованием кетокислот:
 У человека окислительное дезаминирование является основным путем катаболизма аминокислот. Однако такие аминокислоты как серин и гистидин могут терять аминогруппу с использованием других типов дезаминирования, а треонин сразу подвергается прямому расщеплению до глицина и ацетальдегида.
У человека окислительное дезаминирование является основным путем катаболизма аминокислот. Однако такие аминокислоты как серин и гистидин могут терять аминогруппу с использованием других типов дезаминирования, а треонин сразу подвергается прямому расщеплению до глицина и ацетальдегида.
 • Выделяют два варианта окислительного дезаминирования: прямое и непрямое. • Прямое окислительное дезаминирование катализируется одним ферментом, в результате образуется NH 3 и кетокислота. Прямое окислительное дезаминирование может идти в присутствии кислорода (аэробное) и не нуждаться в кислороде (анаэробное).
• Выделяют два варианта окислительного дезаминирования: прямое и непрямое. • Прямое окислительное дезаминирование катализируется одним ферментом, в результате образуется NH 3 и кетокислота. Прямое окислительное дезаминирование может идти в присутствии кислорода (аэробное) и не нуждаться в кислороде (анаэробное).
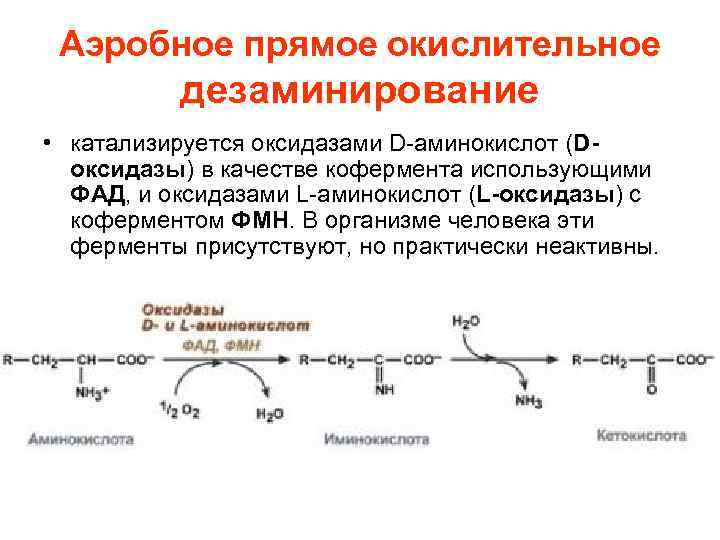 Аэробное прямое окислительное дезаминирование • катализируется оксидазами D-аминокислот (Dоксидазы) в качестве кофермента использующими ФАД, и оксидазами L-аминокислот (L-оксидазы) с коферментом ФМН. В организме человека эти ферменты присутствуют, но практически неактивны.
Аэробное прямое окислительное дезаминирование • катализируется оксидазами D-аминокислот (Dоксидазы) в качестве кофермента использующими ФАД, и оксидазами L-аминокислот (L-оксидазы) с коферментом ФМН. В организме человека эти ферменты присутствуют, но практически неактивны.
 Анаэробное прямое окислительное дезаминирование • существует только для глутаминовой кислоты, катализируется только глутаматдегидрогеназой, превращающей глутамат в α-кетоглутарат. • Фермент глутаматдегидрогеназа имеется в митохондриях всех клеток организма (кроме мышечных). • Этот тип дезаминирования теснейшим образом связан с трансаминированием аминокислот и формирует с ним процесс трансдезаминирования
Анаэробное прямое окислительное дезаминирование • существует только для глутаминовой кислоты, катализируется только глутаматдегидрогеназой, превращающей глутамат в α-кетоглутарат. • Фермент глутаматдегидрогеназа имеется в митохондриях всех клеток организма (кроме мышечных). • Этот тип дезаминирования теснейшим образом связан с трансаминированием аминокислот и формирует с ним процесс трансдезаминирования
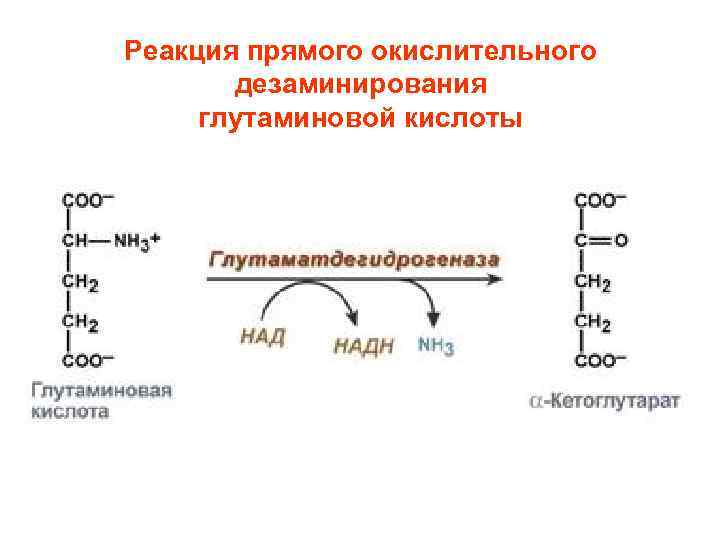 Реакция прямого окислительного дезаминирования глутаминовой кислоты
Реакция прямого окислительного дезаминирования глутаминовой кислоты
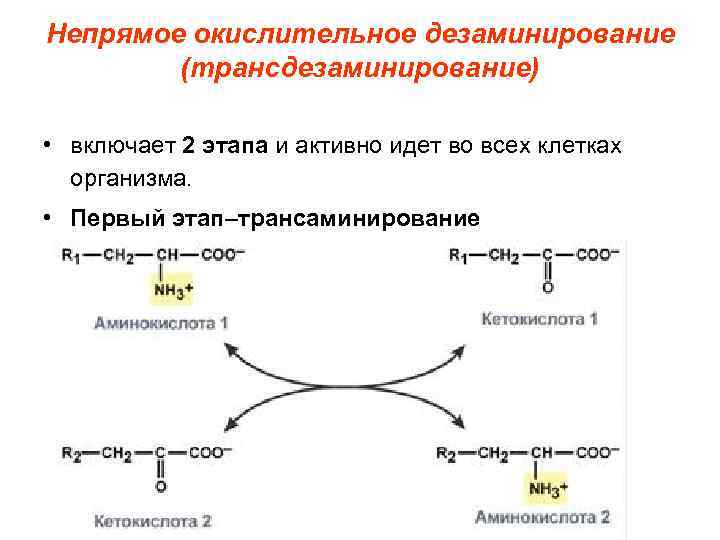 Непрямое окислительное дезаминирование (трансдезаминирование) • включает 2 этапа и активно идет во всех клетках организма. • Первый этап–трансаминирование
Непрямое окислительное дезаминирование (трансдезаминирование) • включает 2 этапа и активно идет во всех клетках организма. • Первый этап–трансаминирование
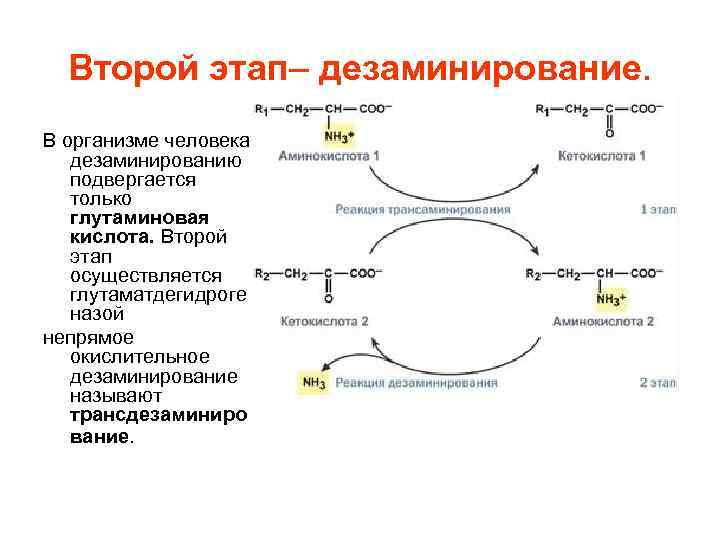 Второй этап– дезаминирование. В организме человека дезаминированию подвергается только глутаминовая кислота. Второй этап осуществляется глутаматдегидроге назой непрямое окислительное дезаминирование называют трансдезаминиро вание.
Второй этап– дезаминирование. В организме человека дезаминированию подвергается только глутаминовая кислота. Второй этап осуществляется глутаматдегидроге назой непрямое окислительное дезаминирование называют трансдезаминиро вание.
 Роль трансаминирования и трансдезаминирования Реакции трансаминирования: • активируются в печени, мышцах и других органах при поступлении в клетку избыточного количества тех или иных аминокислот – с целью оптимизации их соотношения, • обеспечивают синтез заменимых аминокислот в клетке при наличии их углеродного скелета (кетоаналога), • начинаются при прекращении использования аминокислот на синтез азотсодержащих соединений (белков, креатина, фосфолипидов, пуриновых и пиримидиновых оснований) – с целью дальнейшего катаболизма их безазотистого остатка и выработки энергии, • необходимы при внутриклеточном голодании, например, при гипогликемиях различного генеза – для использования безазотистого остатка аминокислот в печени для кетогенеза и глюконеогенеза, в других органах – для его прямого вовлечения в реакции цикла трикарбоновых кислот. • при патологиях (сахарный диабет, гиперкортицизм) обуславливают наличие субстратов для глюконеогенеза и способствуют патологической гипергликемии.
Роль трансаминирования и трансдезаминирования Реакции трансаминирования: • активируются в печени, мышцах и других органах при поступлении в клетку избыточного количества тех или иных аминокислот – с целью оптимизации их соотношения, • обеспечивают синтез заменимых аминокислот в клетке при наличии их углеродного скелета (кетоаналога), • начинаются при прекращении использования аминокислот на синтез азотсодержащих соединений (белков, креатина, фосфолипидов, пуриновых и пиримидиновых оснований) – с целью дальнейшего катаболизма их безазотистого остатка и выработки энергии, • необходимы при внутриклеточном голодании, например, при гипогликемиях различного генеза – для использования безазотистого остатка аминокислот в печени для кетогенеза и глюконеогенеза, в других органах – для его прямого вовлечения в реакции цикла трикарбоновых кислот. • при патологиях (сахарный диабет, гиперкортицизм) обуславливают наличие субстратов для глюконеогенеза и способствуют патологической гипергликемии.
 • Процесс трансдезаминирования идет в организме непрерывно, потому что: • сопряженные реакции трансаминирования и дезаминирования создают поток лишнего аминного азота из периферических клеток в печень для синтеза мочевины и в почки для синтеза аммонийных солей. • Трансаминирование нуждается в витамине В 6
• Процесс трансдезаминирования идет в организме непрерывно, потому что: • сопряженные реакции трансаминирования и дезаминирования создают поток лишнего аминного азота из периферических клеток в печень для синтеза мочевины и в почки для синтеза аммонийных солей. • Трансаминирование нуждается в витамине В 6
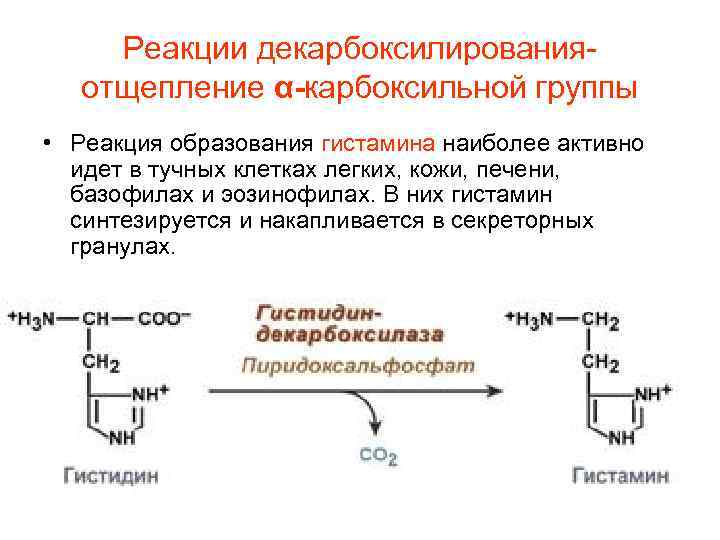 Реакции декарбоксилирования- отщепление α-карбоксильной группы • Реакция образования гистамина наиболее активно идет в тучных клетках легких, кожи, печени, базофилах и эозинофилах. В них гистамин синтезируется и накапливается в секреторных гранулах.
Реакции декарбоксилирования- отщепление α-карбоксильной группы • Реакция образования гистамина наиболее активно идет в тучных клетках легких, кожи, печени, базофилах и эозинофилах. В них гистамин синтезируется и накапливается в секреторных гранулах.
 Физиологические эффекты гистамина • расширение артериол и капилляров и, как следствие, покраснение кожи, снижение артериального давления; • повышение проницаемости стенки капилляров и, как следствие, выход жидкости в межклеточное пространство (отечность), снижение артериального давления; • если предыдущие пункты имеют место в головном мозге – повышение внутричерепного давления; • увеличивает тонус гладких мышц бронхов, как следствие – спазм и удушье; • слабо повышает тонус мышц желудочно-кишечного тракта; • стимулирует секрецию слюны и желудочного сока.
Физиологические эффекты гистамина • расширение артериол и капилляров и, как следствие, покраснение кожи, снижение артериального давления; • повышение проницаемости стенки капилляров и, как следствие, выход жидкости в межклеточное пространство (отечность), снижение артериального давления; • если предыдущие пункты имеют место в головном мозге – повышение внутричерепного давления; • увеличивает тонус гладких мышц бронхов, как следствие – спазм и удушье; • слабо повышает тонус мышц желудочно-кишечного тракта; • стимулирует секрецию слюны и желудочного сока.
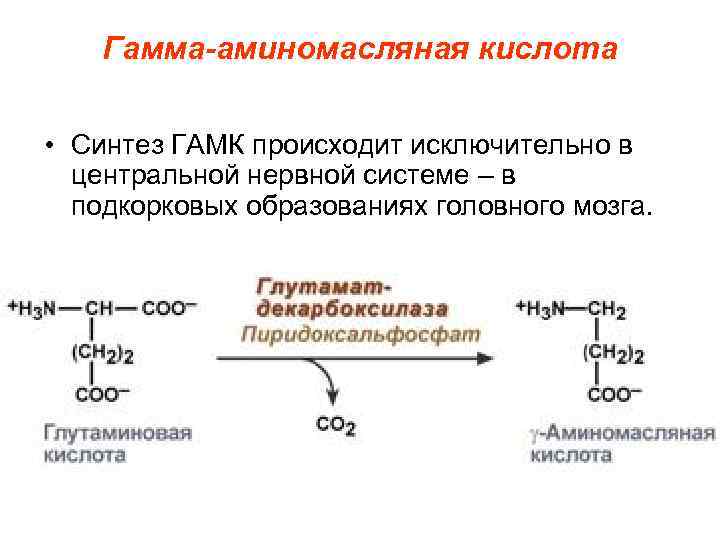 Гамма-аминомасляная кислота • Синтез ГАМК происходит исключительно в центральной нервной системе – в подкорковых образованиях головного мозга.
Гамма-аминомасляная кислота • Синтез ГАМК происходит исключительно в центральной нервной системе – в подкорковых образованиях головного мозга.
 Физиологические эффекты ГАМК • В центральной нервной системе ГАМК (наряду с глутаминовой кислотой) является тормозным медиатором. Наиболее высока ее роль в височной и лобной коре, гиппокампе, миндалевидных и гипоталамических ядрах, черной субстанции, ядрах мозжечка.
Физиологические эффекты ГАМК • В центральной нервной системе ГАМК (наряду с глутаминовой кислотой) является тормозным медиатором. Наиболее высока ее роль в височной и лобной коре, гиппокампе, миндалевидных и гипоталамических ядрах, черной субстанции, ядрах мозжечка.
 Дофамин • Синтез дофамина происходит в основном в нейронах промежуточного и среднего мозга.
Дофамин • Синтез дофамина происходит в основном в нейронах промежуточного и среднего мозга.
 Физиологические эффекты дофамина • Является медиатором дофаминовых рецепторов в подкорковых образованиях ЦНС, в больших дозах расширяет сосуды сердца, стимулирует частоту и силу сердечных сокращений, расширяет сосуды почек, увеличивая диурез.
Физиологические эффекты дофамина • Является медиатором дофаминовых рецепторов в подкорковых образованиях ЦНС, в больших дозах расширяет сосуды сердца, стимулирует частоту и силу сердечных сокращений, расширяет сосуды почек, увеличивая диурез.


