Аминокислоты и белки.pptx
- Количество слайдов: 28

Аминокислоты и белки. Клеточный транспорт Жизнь – есть форма существования белковых тел Ф. Энгельс Шлахтер М. Харьков - 2016
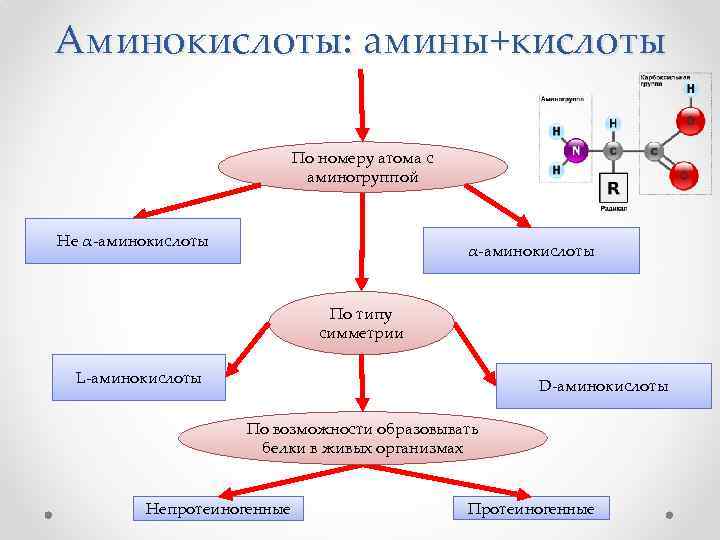
Аминокислоты: амины+кислоты По номеру атома с аминогруппой Не α-аминокислоты По типу симметрии L-аминокислоты D-аминокислоты По возможности образовывать белки в живых организмах Непротеиногенные Протеиногенные

L- и D-аминокислоты D-аминокислота L-аминокислота В живых организмах встречаются только L-аминокислоты (кроме бактерии Rhizobium tumefaciens)

Что могут аминокислоты • Диссоциировать в воде как и все кислоты • Могут вступать в реакции эстерификации • Могут лишаться своих функциональных групп (дезаминирование и декарбоксилирование) • Могут образовывать пептидную связь Диссоциация аминокислот в растворах
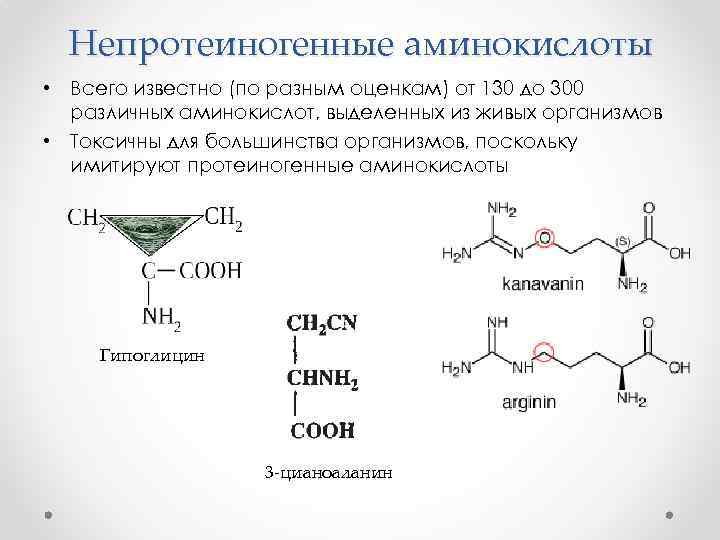
Непротеиногенные аминокислоты • Всего известно (по разным оценкам) от 130 до 300 различных аминокислот, выделенных из живых организмов • Токсичны для большинства организмов, поскольку имитируют протеиногенные аминокислоты Гипоглицин 3 -цианоаланин
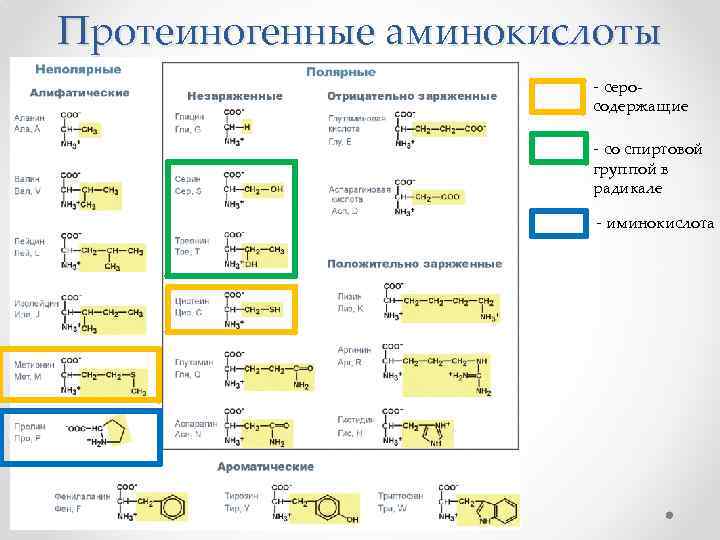
Протеиногенные аминокислоты - серо- содержащие - со спиртовой группой в радикале - иминокислота
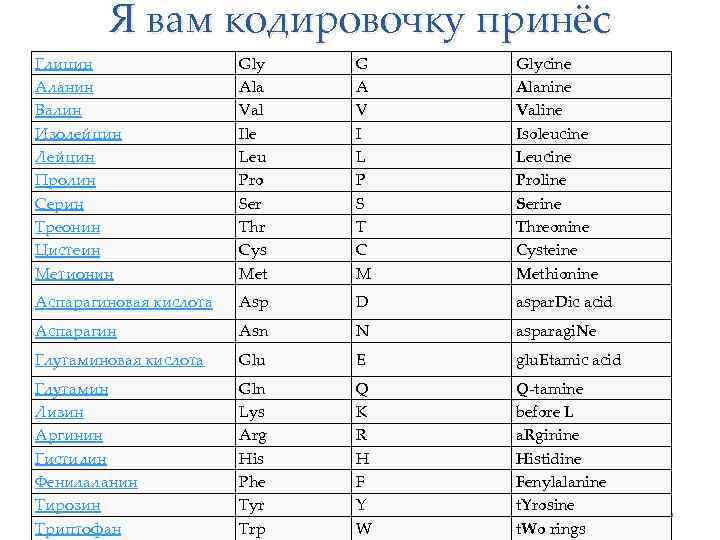
Я вам кодировочку принёс Глицин Аланин Валин Изолейцин Лейцин Пролин Серин Треонин Цистеин Метионин Gly Ala Val Ile Leu Pro Ser Thr Cys Met G A V I L P S T C M Glycine Alanine Valine Isoleucine Leucine Proline Serine Threonine Cysteine Methionine Аспарагиновая кислота Asp D aspar. Dic acid Аспарагин Asn N asparagi. Ne Глутаминовая кислота Glu E glu. Etamic acid Глутамин Лизин Аргинин Гистидин Фенилаланин Тирозин Триптофан Gln Lys Arg His Phe Tyr Trp Q K R H F Y W Q-tamine before L a. Rginine Histidine Fenylalanine t. Yrosine t. Wo rings
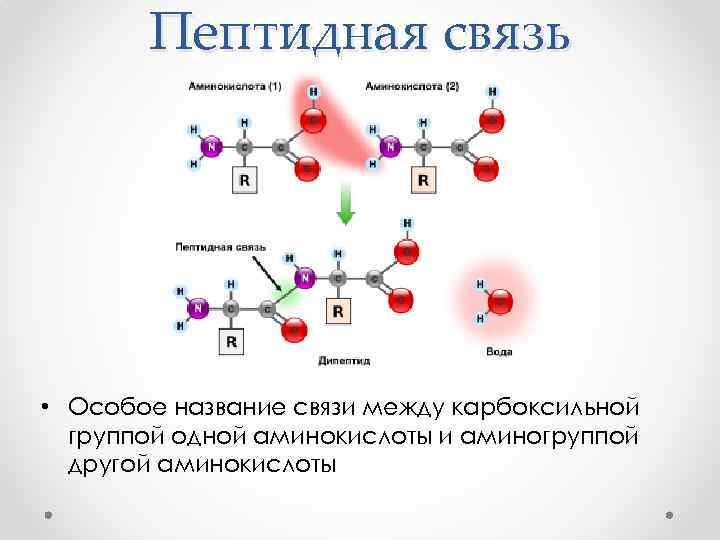
Пептидная связь • Особое название связи между карбоксильной группой одной аминокислоты и аминогруппой другой аминокислоты

? Пептид=белок • Белок – это пептид a) длиной больше 50 аминокислот b) Который состоит не только из аминокислот, а и из углеводов/ионов металлов и т. д.
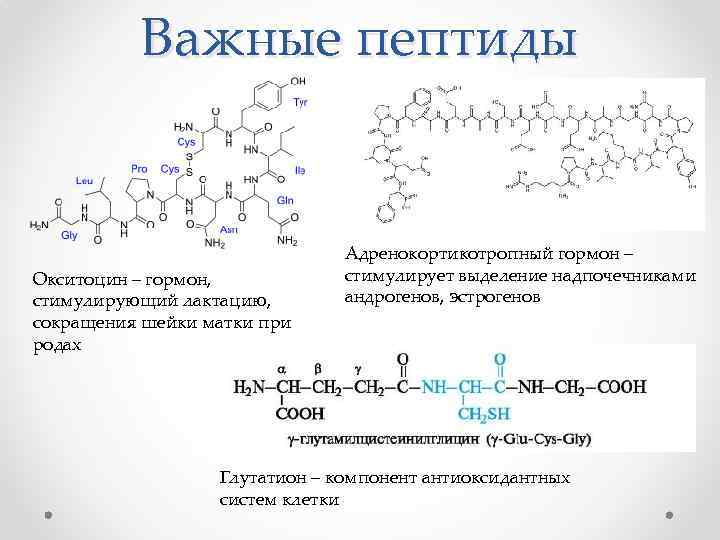
Важные пептиды Окситоцин – гормон, стимулирующий лактацию, сокращения шейки матки при родах Адренокортикотропный гормон – стимулирует выделение надпочечниками андрогенов, эстрогенов Глутатион – компонент антиоксидантных систем клетки
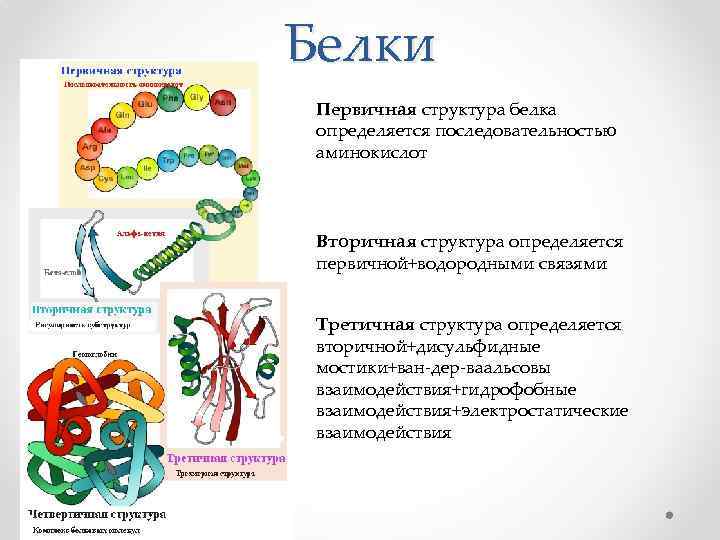
Белки Первичная структура белка определяется последовательностью аминокислот Вторичная структура определяется первичной+водородными связями Третичная структура определяется вторичной+дисульфидные мостики+ван-дер-ваальсовы взаимодействия+гидрофобные взаимодействия+электростатические взаимодействия
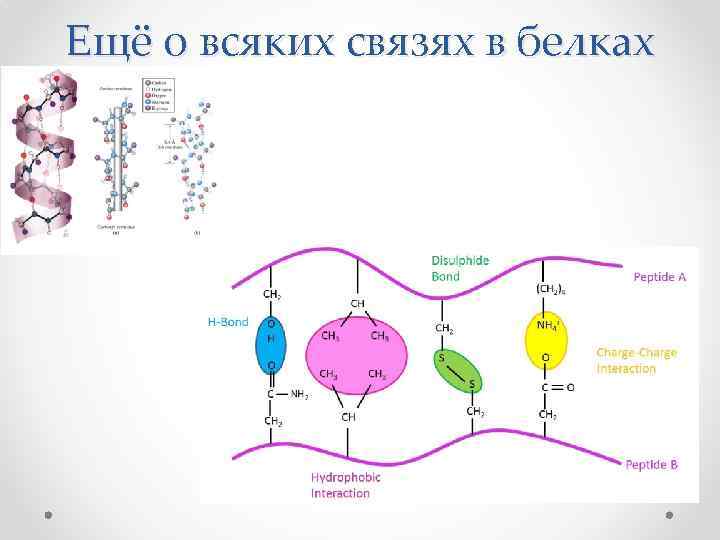
Ещё о всяких связях в белках
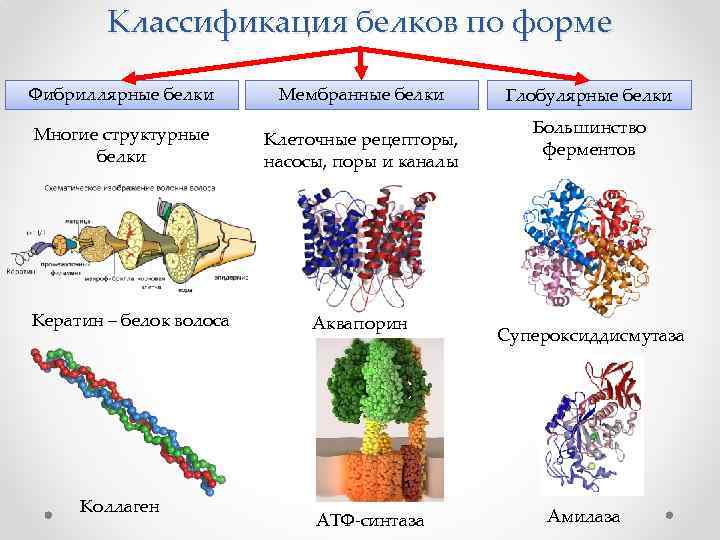
Классификация белков по форме Фибриллярные белки Мембранные белки Многие структурные белки Клеточные рецепторы, насосы, поры и каналы Кератин – белок волоса Коллаген Аквапорин АТФ-синтаза Глобулярные белки Большинство ферментов Супероксиддисмутаза Амилаза
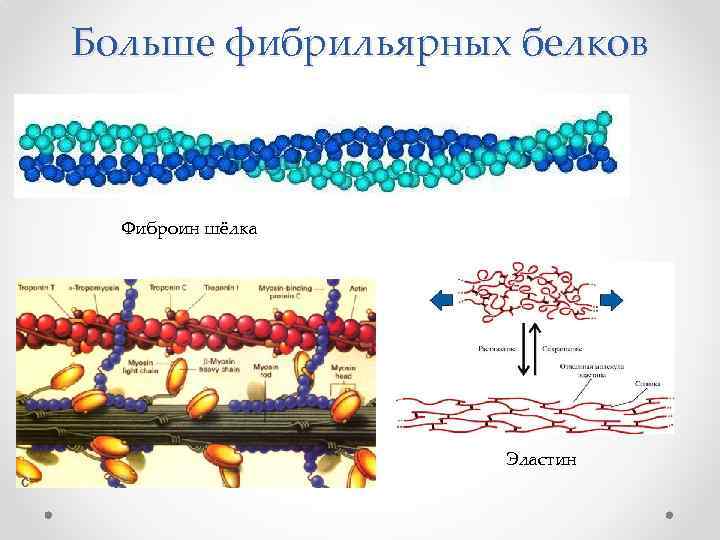
Больше фибрильярных белков Фиброин шёлка Эластин
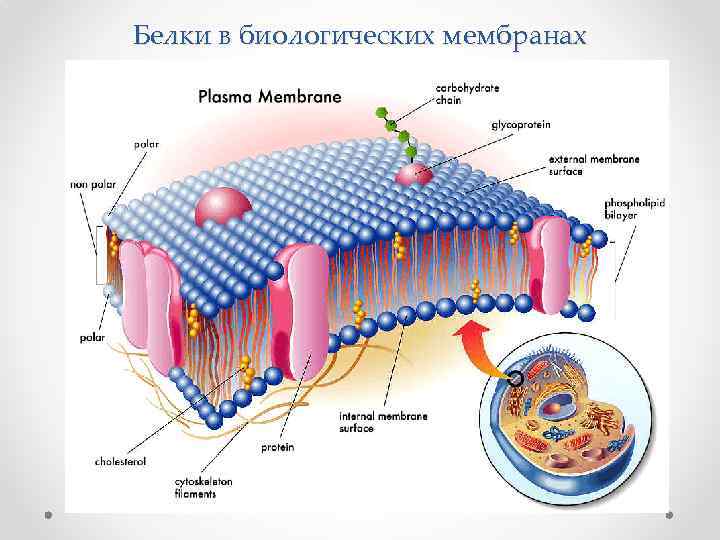
Белки в биологических мембранах
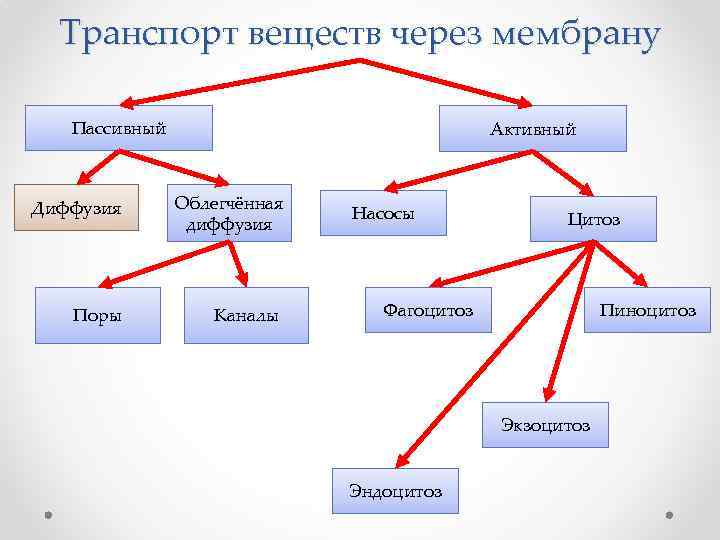
Транспорт веществ через мембрану Пассивный Диффузия Поры Активный Облегчённая диффузия Каналы Насосы Цитоз Фагоцитоз Пиноцитоз Экзоцитоз Эндоцитоз
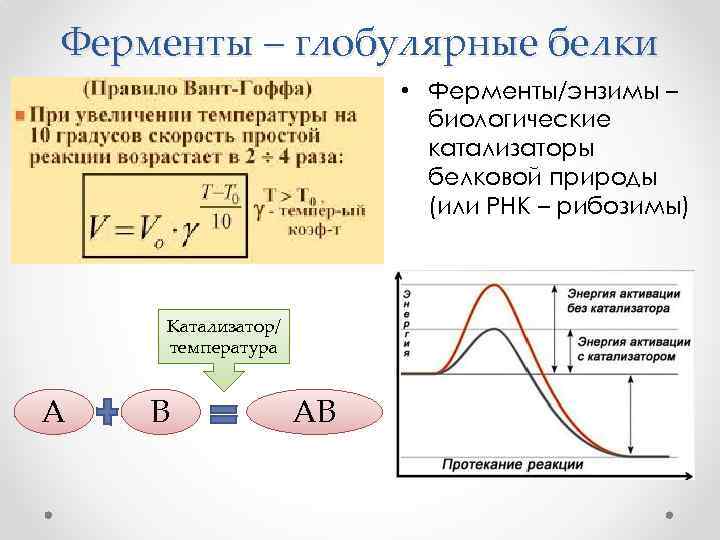
Ферменты – глобулярные белки • Ферменты/энзимы – биологические катализаторы белковой природы (или РНК – рибозимы) Катализатор/ температура А В АВ

Ещё немного о катализаторах
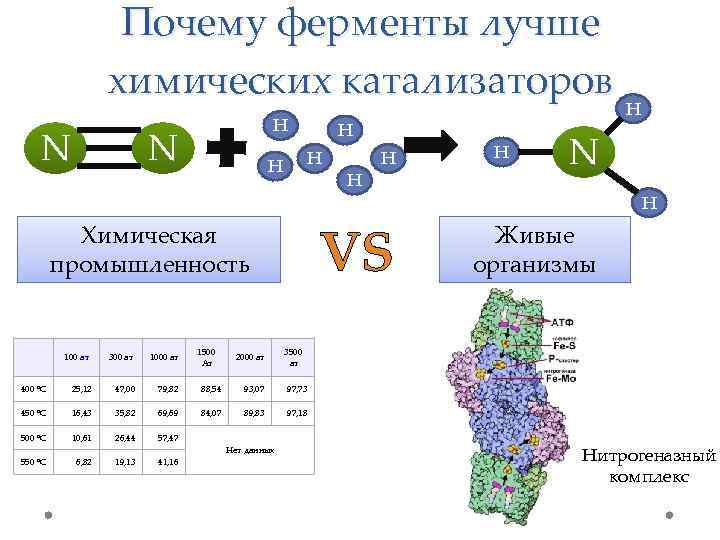
Почему ферменты лучше химических катализаторов N H H H VS Химическая промышленность 100 ат H H 300 ат 1000 ат 1500 Ат 2000 ат H H N H Живые организмы 3500 ат 400 °C 25, 12 47, 00 79, 82 88, 54 93, 07 97, 73 450 °C 16, 43 35, 82 69, 69 84, 07 89, 83 97, 18 500 °C 10, 61 26, 44 57, 47 550 °C 6, 82 19, 13 41, 16 Нет данных Нитрогеназный комплекс
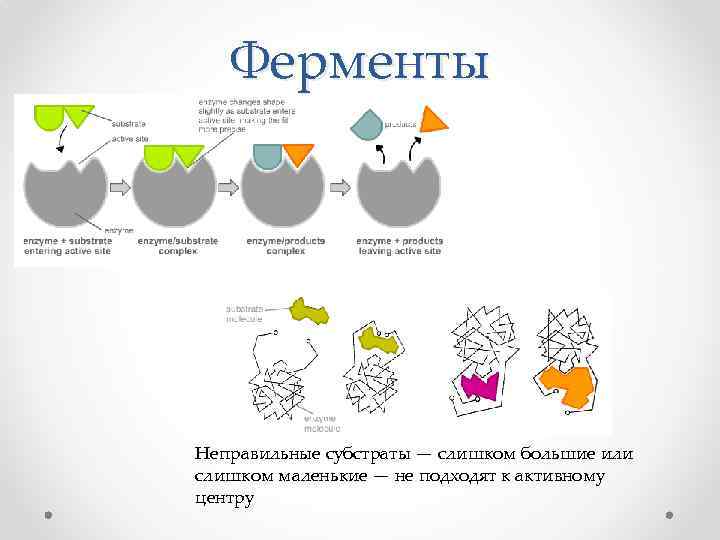
Ферменты Неправильные субстраты — слишком большие или слишком маленькие — не подходят к активному центру
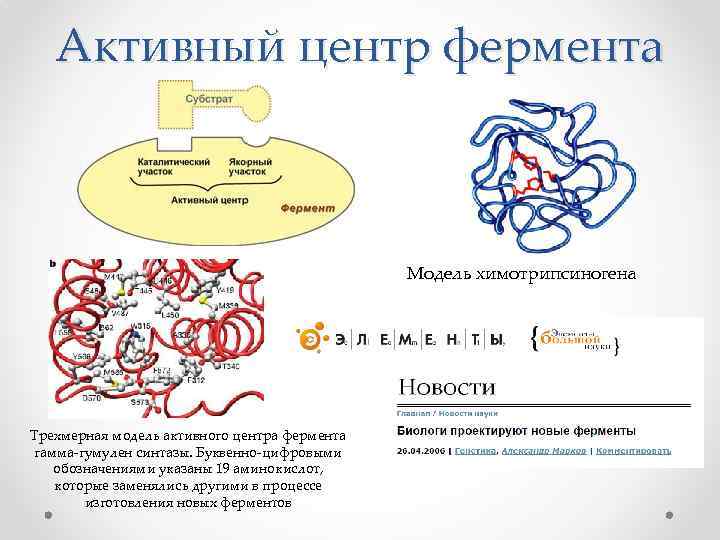
Активный центр фермента Модель химотрипсиногена Трехмерная модель активного центра фермента гамма-гумулен синтазы. Буквенно-цифровыми обозначениями указаны 19 аминокислот, которые заменялись другими в процессе изготовления новых ферментов

Как называть ферменты? • Субстрат+ «аза» : лактоза- дисахарид; лактаза – фермент, расщепляющий лактозу • С учётом p. H среды – щелочная фосфатаза • С учётом локализации в клетке – мембранная АТФ-аза • Тривиальные (традиционные названия – трипсин, пепсин)

Как классифицировать ферменты – КФ *. *. / ЕС *. *. 1. КФ 1. *. *. *. – Оксидоредуктазы: перенос электронов/водородов/кислородов 2. КФ 2. *. *. *. – Трансферазы: перенос функциональных групп 3. КФ 3. *. *. *. - Гидролазы: расщепление веществ с добавлением по месту разрыва ОН и Н 4. КФ 4. *. *. *. – Лиазы/синтазы: негидролитическое добавление или удаление функциональной группы 5. КФ 5. *. *. *. – Изомеразы: внутримолекулярная перестановка 6. КФ 6. *. *. *. – Лигазы/синтетазы: соединение двух молекул в одну с использованием энергии АТФ

Пример о КФ. Или биологи тоже шутят • КФ 1. 1 – алкогольдегидрогеназа (алкоголь: НАД-оксидоредуктаза) - Coprinus comatus
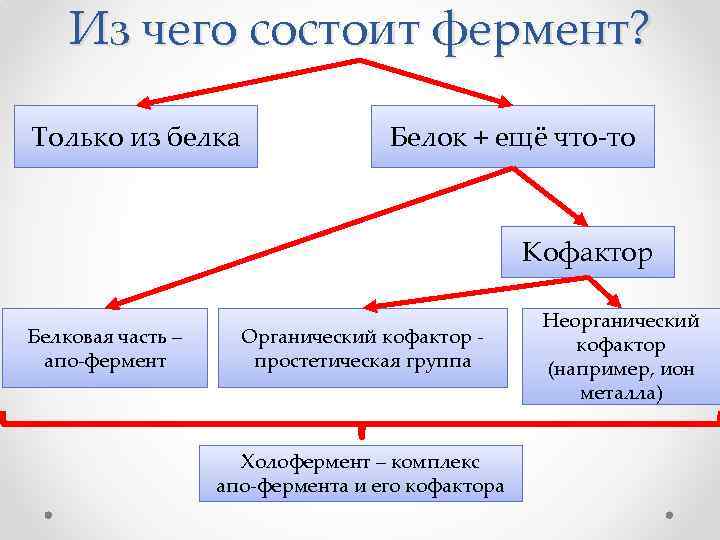
Из чего состоит фермент? Только из белка Белок + ещё что-то Кофактор Белковая часть – апо-фермент Органический кофактор - простетическая группа Холофермент – комплекс апо-фермента и его кофактора Неорганический кофактор (например, ион металла)
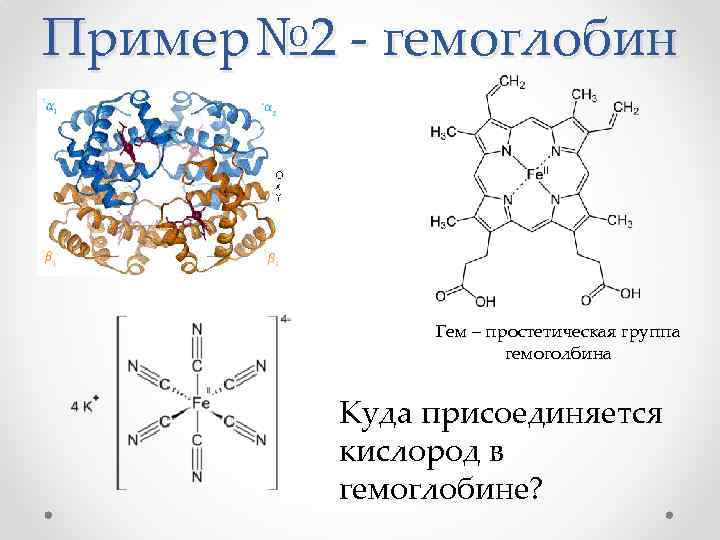
Пример№ 2 - гемоглобин Гем – простетическая группа гемоголбина Куда присоединяется кислород в гемоглобине?

Выводы • Аминокислоты выполняют в организмах много функций как в свободном виде, так и в составе белков • Белки – сложные гетерополимеры, которые могут очень много чего • Биологические катализаторы – ферменты – часто включают в себя, помимо апо-фермента ещё кофактор

Спасибо за внимание!
Аминокислоты и белки.pptx