аминокислоты и белки.ppt
- Количество слайдов: 32

Аминокислоты и белки
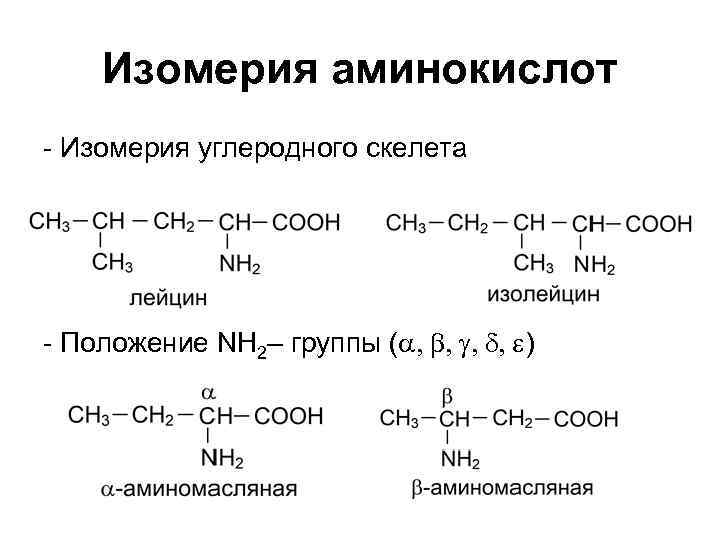
Изомерия аминокислот - Изомерия углеродного скелета - Положение NH 2– группы (a, b, g, d, e)

Общая формула a-аминокислот
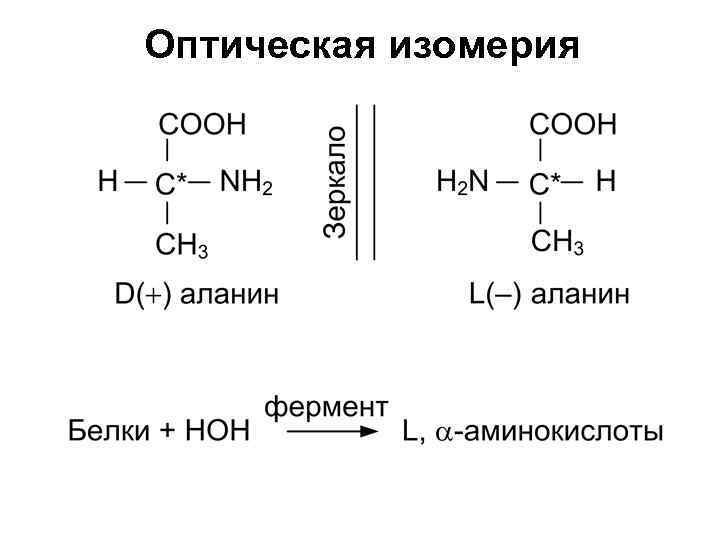
Оптическая изомерия

Незаменимые a-аминокислоты - Валин Лейцин Изолейцин Лизин Треонин Метионин Фенилаланин Триптофан

Классификация I. По химической природе радикала 1. Алифатические (гли-, ала-, вал-, лей-) по дополнительным функциональным группам: – OH (сер-, тре-) – COOH (асп-, глу-) – NH 2 CO (аспарагин, глутамин) – NH 2 (лиз-) – SH (цис-), -S- (мет-)
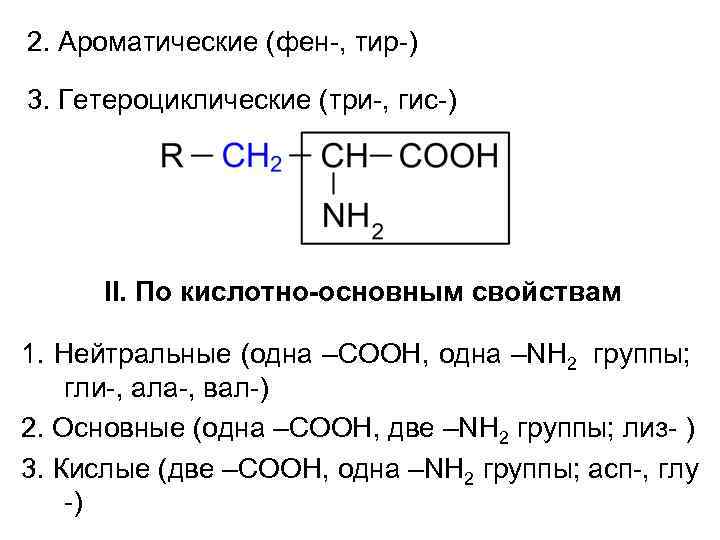
2. Ароматические (фен-, тир-) 3. Гетероциклические (три-, гис-) II. По кислотно-основным свойствам 1. Нейтральные (одна –COOH, одна –NH 2 группы; гли-, ала-, вал-) 2. Основные (одна –COOH, две –NH 2 группы; лиз- ) 3. Кислые (две –COOH, одна –NH 2 группы; асп-, глу -)
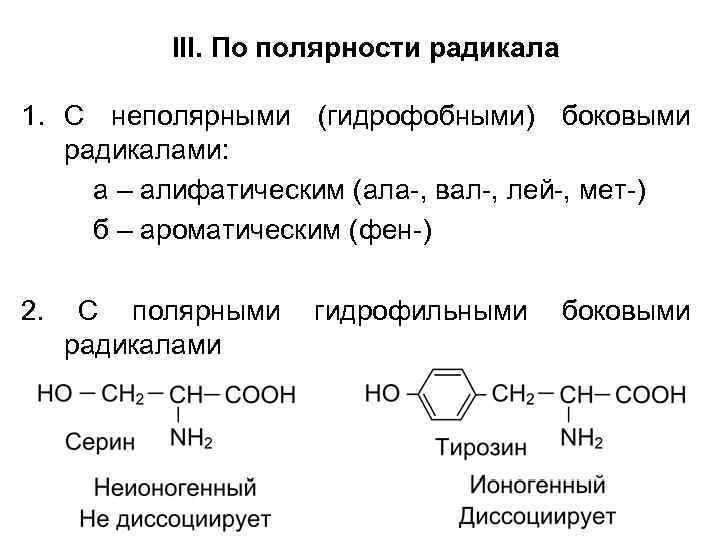
III. По полярности радикала 1. С неполярными (гидрофобными) боковыми радикалами: а – алифатическим (ала-, вал-, лей-, мет-) б – ароматическим (фен-) 2. С полярными радикалами гидрофильными боковыми

Кислотно-основные свойства Изоэлектрическое состояние (ИЭС), при котором суммарный заряд молекулы равен 0. Изоэлектрическая точка (p. I), значение p. H, при котором молекула находится в ИЭС
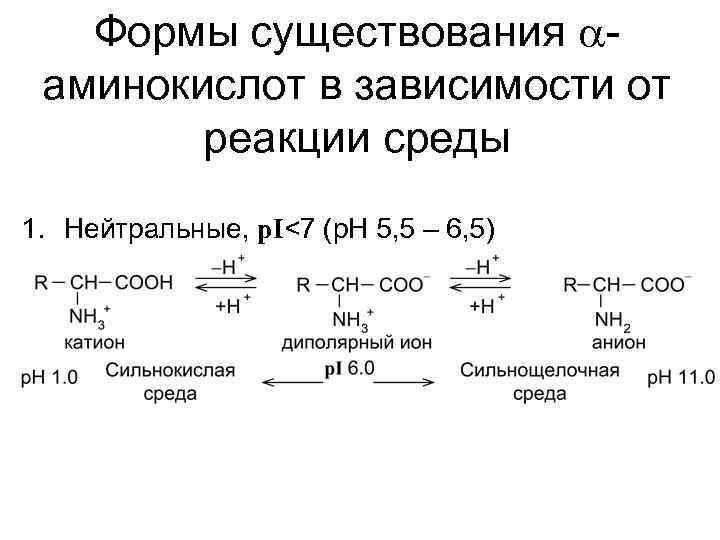
Формы существования aаминокислот в зависимости от реакции среды 1. Нейтральные, p. I<7 (p. H 5, 5 – 6, 5)
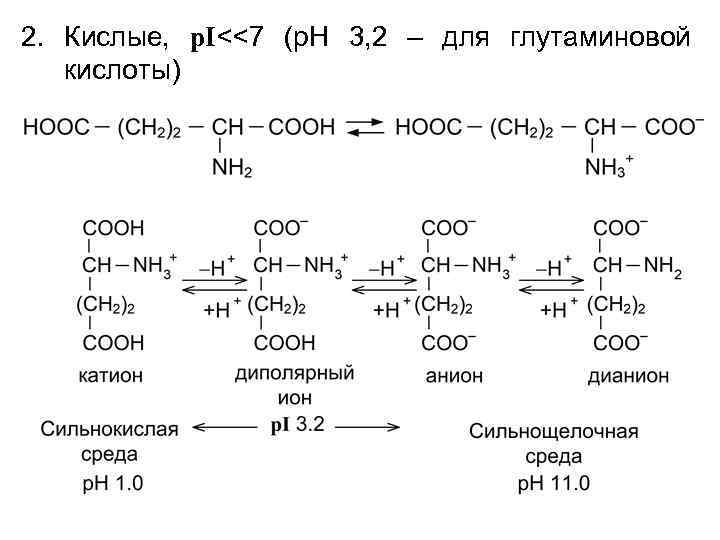
2. Кислые, p. I<<7 (p. H 3, 2 – для глутаминовой кислоты)
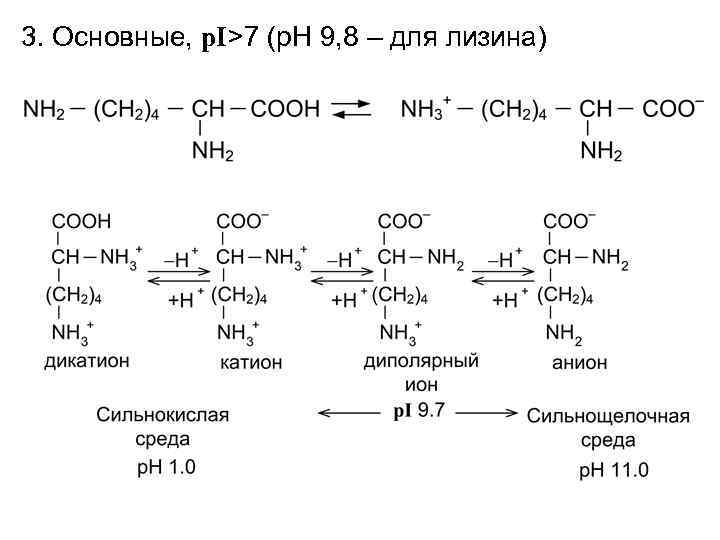
3. Основные, p. I>7 (p. H 9, 8 – для лизина)
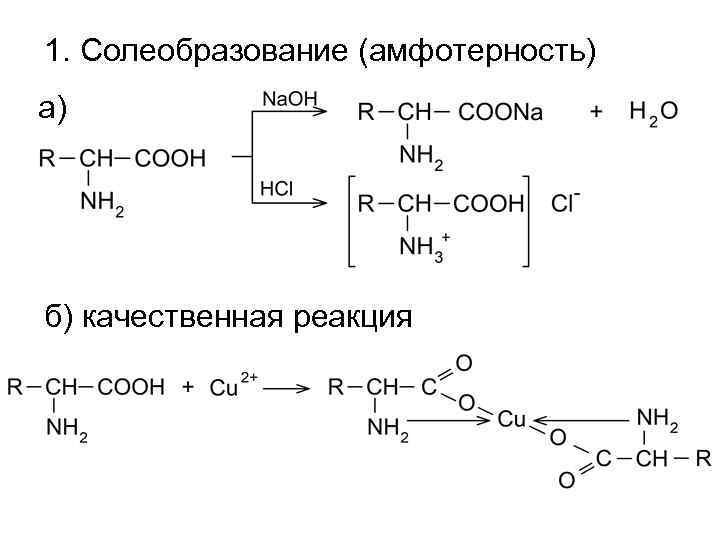
1. Солеобразование (амфотерность) а) б) качественная реакция
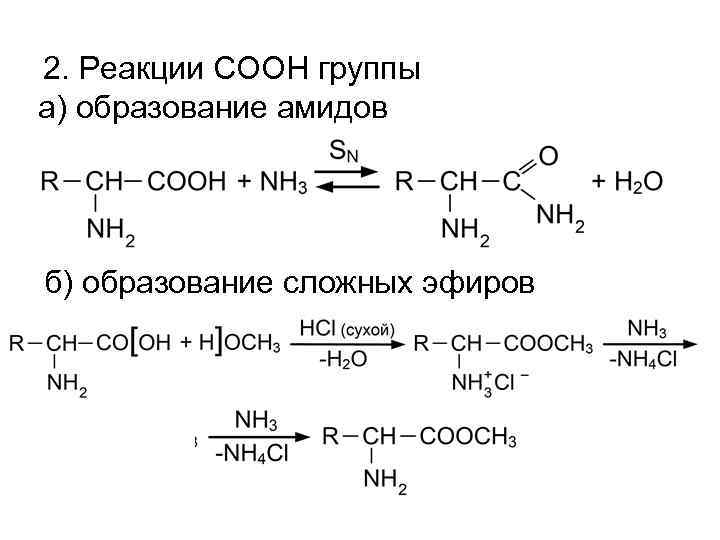
2. Реакции COOH группы а) образование амидов б) образование сложных эфиров
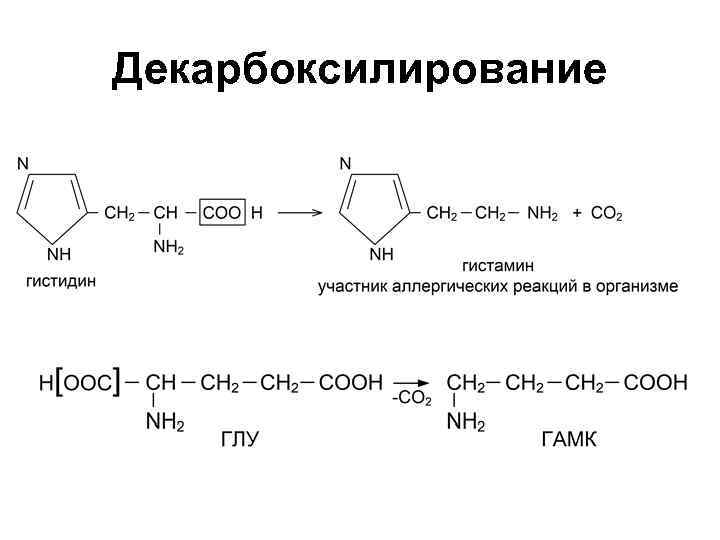
Декарбоксилирование
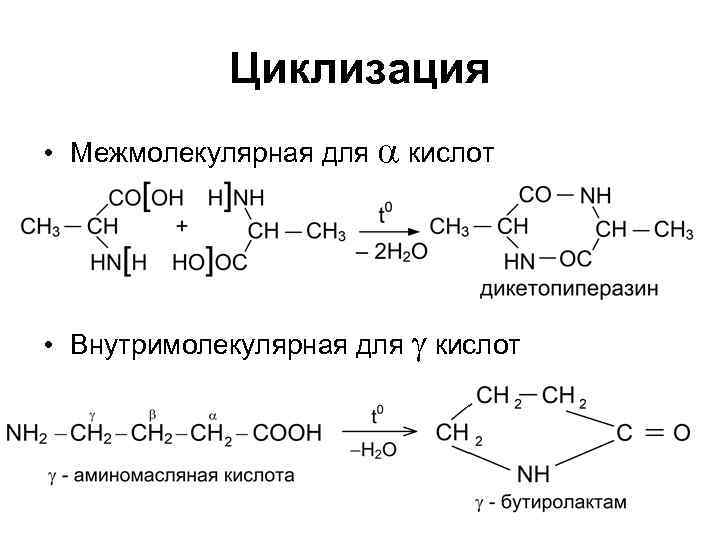
Циклизация • Межмолекулярная для a кислот • Внутримолекулярная для g кислот
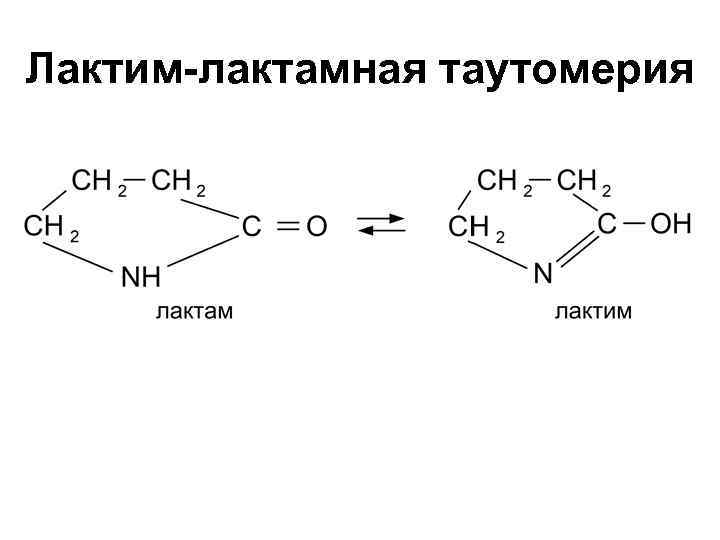
Лактим-лактамная таутомерия
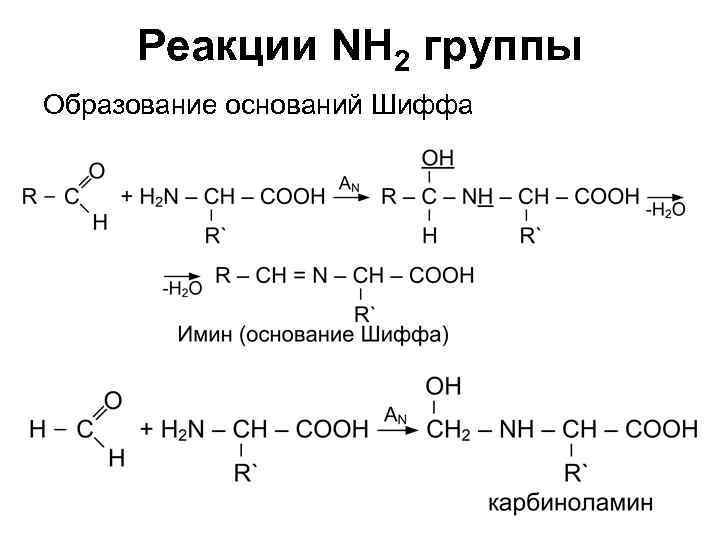
Реакции NH 2 группы Образование оснований Шиффа
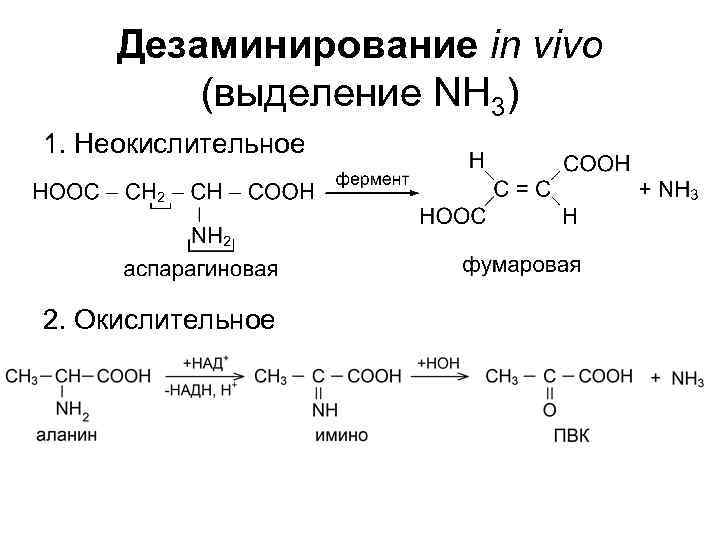
Дезаминирование in vivo (выделение NH 3) 1. Неокислительное 2. Окислительное
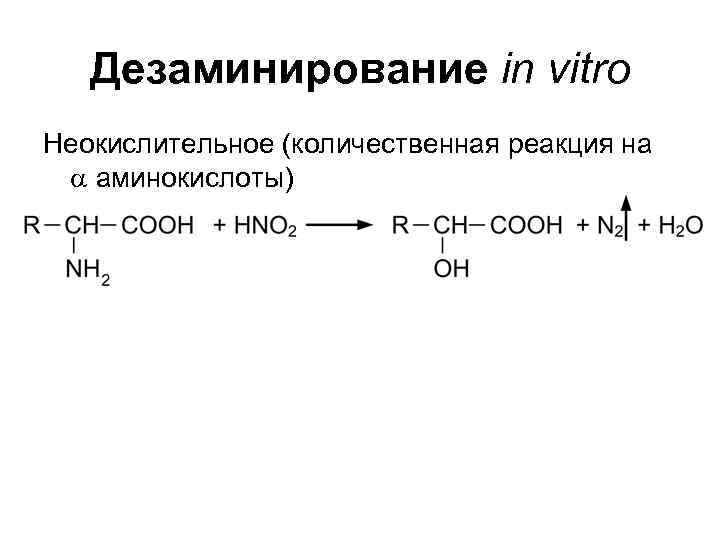
Дезаминирование in vitro Неокислительное (количественная реакция на a аминокислоты)
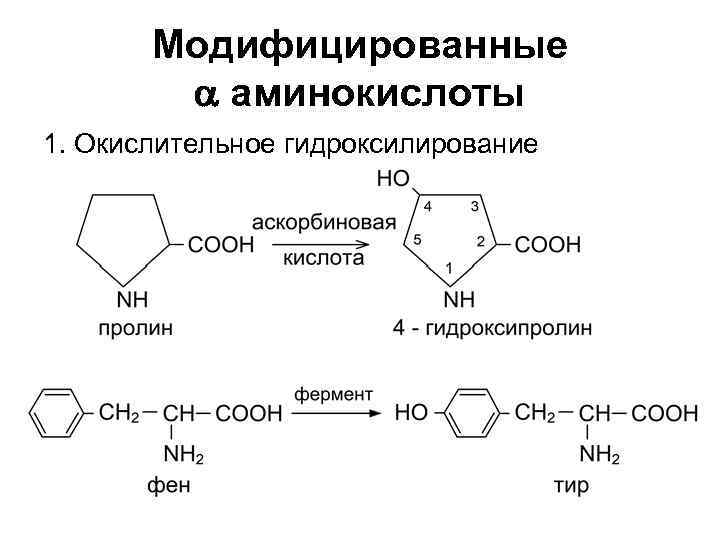
Модифицированные a аминокислоты 1. Окислительное гидроксилирование
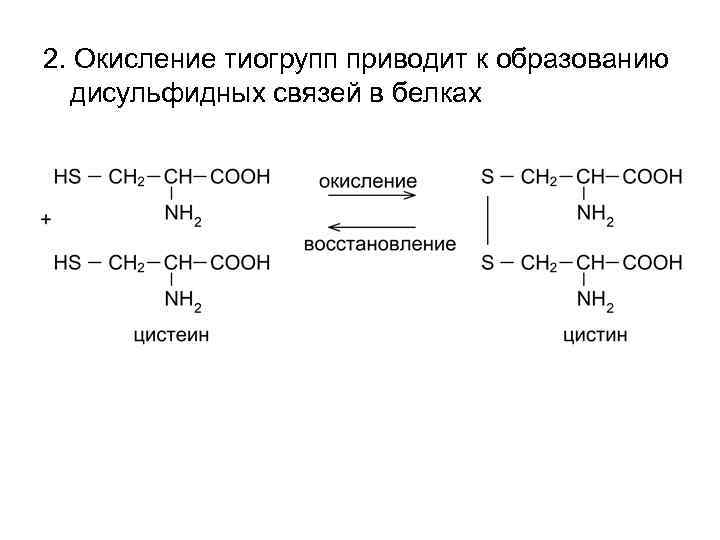
2. Окисление тиогрупп приводит к образованию дисульфидных связей в белках
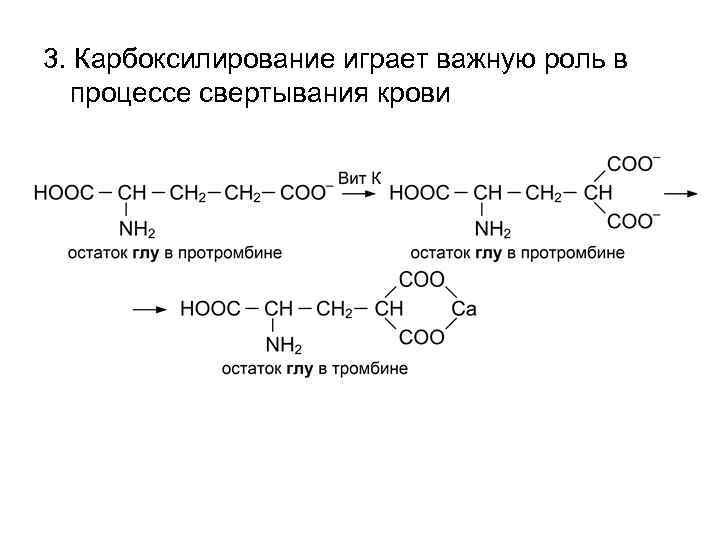
3. Карбоксилирование играет важную роль в процессе свертывания крови
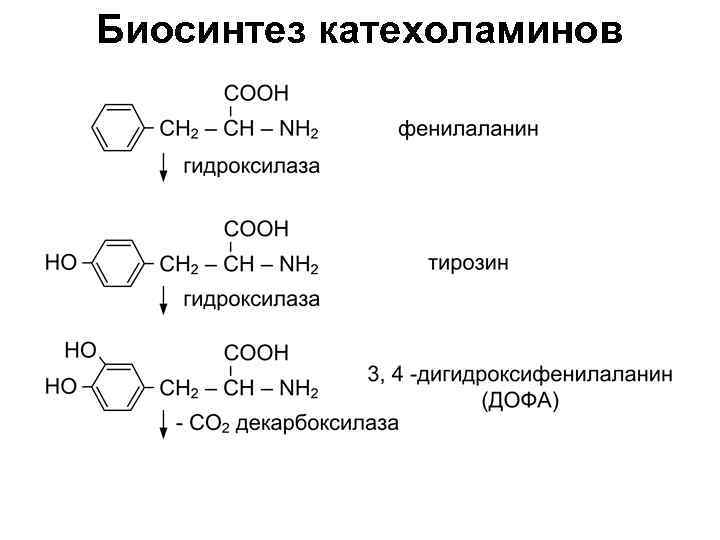
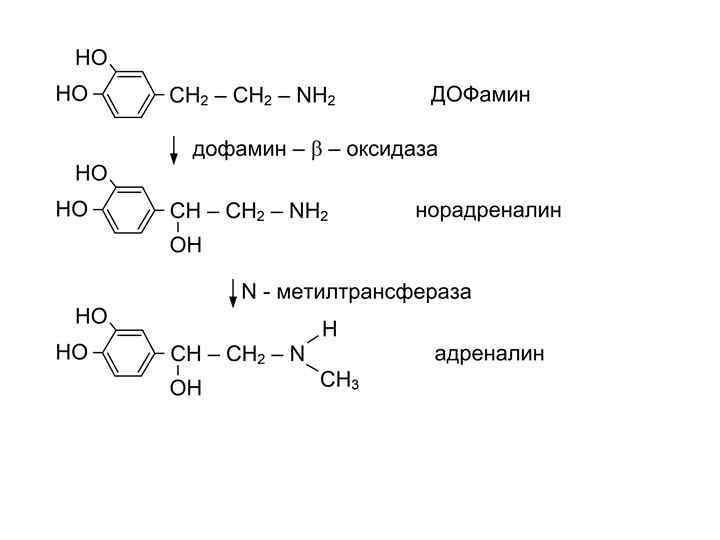
Биосинтез катехоламинов

Пептиды. Белки. Пептиды – соединения, построенные из a аминокислот и связанные между собой пептидными связями. Классификация пептидов по количеству аминокислот: 1. Олигопептиды < 10 аминокислот 2. Полипептиды от 10 – 100 аминокислот 3. Белки > 100 аминокислот

Сложные белки в зависимости от природы простетической группы подразделяются: 1. Металлопротеины (ионы металлов) 2. Фосфопротеины (остаток H 3 PO 4) 3. Гликопротеины (углеводная часть) 4. Липопротеины (липидная часть) 5. Нуклеопротеины (нуклеиновые кислоты)


Функции белков • • Структурная. Белки являются стройматериалом для всего живого. На 80% из белков состоят мышцы, 63% – кожа, 57% – печень. Транспортная. Перенос низкомолекулярных веществ в виде комплексов с белками. Двигательная. Мышечное сокращение за счет белков актина и миозина. Защитная. Иммунная защита основана на действии антител.

• • • Ферментативная. Регуляция скорости биохимических процессов с помощью ферментов. Регуляторная (гормоны). Запасные белки (казеин, яичный альбумин).
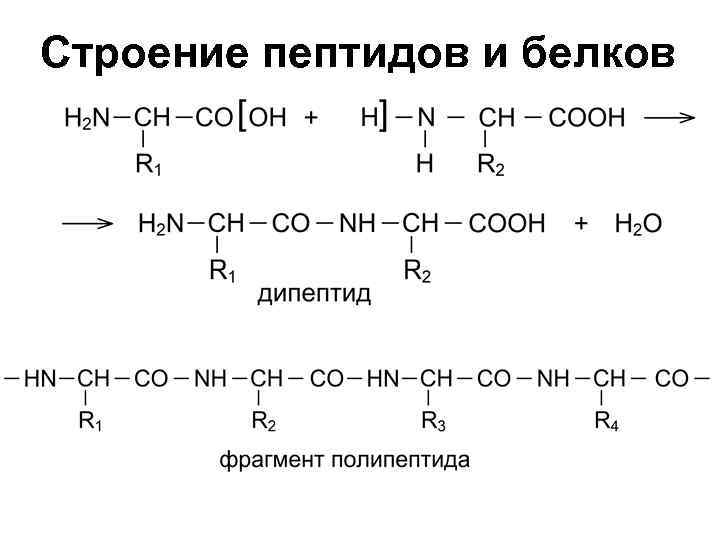
Строение пептидов и белков
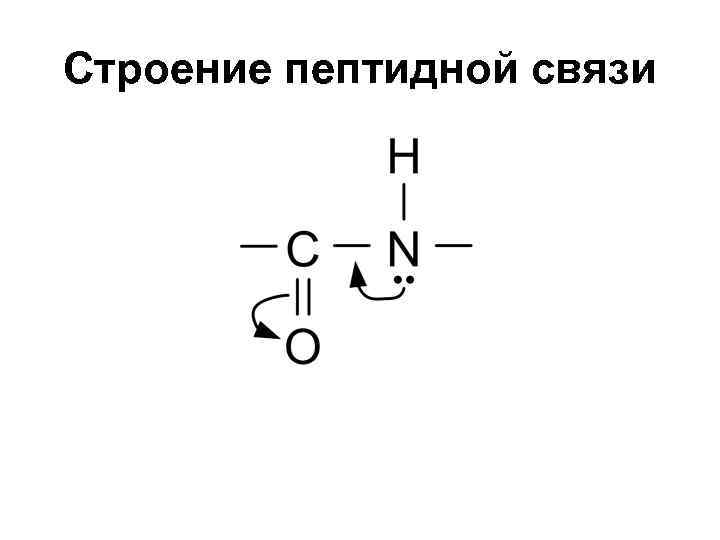
Строение пептидной связи
аминокислоты и белки.ppt