Аминокислоты.pptx
- Количество слайдов: 17

Аминокислоты. Белки.

Состав и свойства аминокислот. Если один атом водорода в метильном радикале молекулы уксусной кислоты заменить на группу –NH 2, то получится формула аминоуксусной кислоты: CH 3 COOH - уксусная кислота NH 2 COOH – аминоуксусная кислота NH 2 – функциональная группа, называемая аминогруппой.
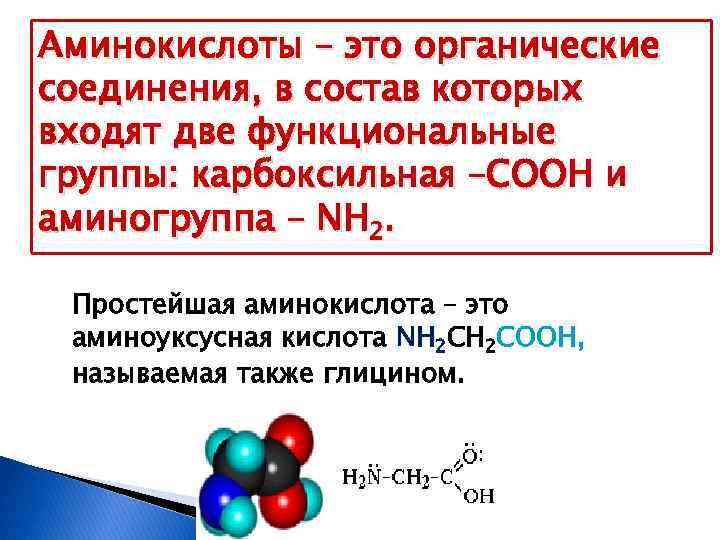
Аминокислоты – это органические соединения, в состав которых входят две функциональные группы: карбоксильная –COOH и аминогруппа – NH 2. Простейшая аминокислота – это аминоуксусная кислота NH 2 COOH, называемая также глицином.
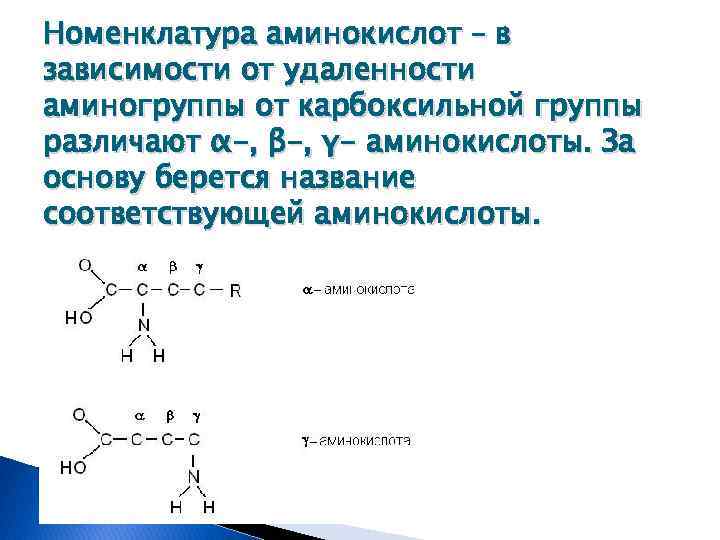
Номенклатура аминокислот – в зависимости от удаленности аминогруппы от карбоксильной группы различают α-, β-, γ- аминокислоты. За основу берется название соответствующей аминокислоты.

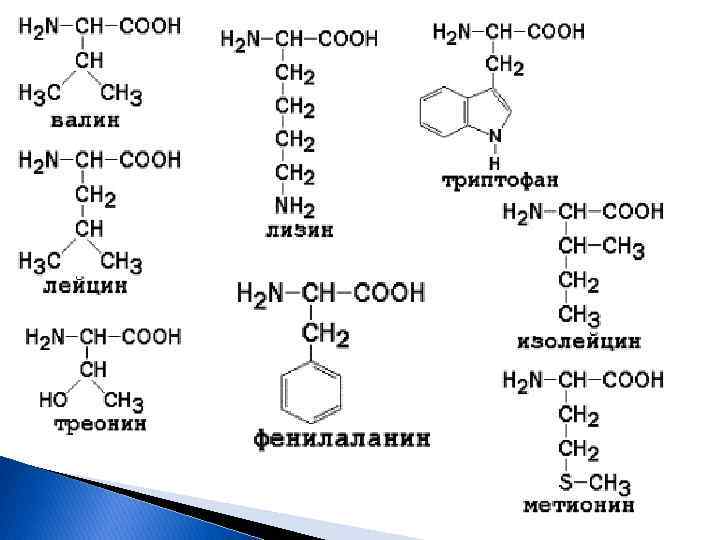
Незаменимые аминокислоты Незаменимыми называются аминокислоты, которые не могут быть синтезированы организмом из веществ, поступающих с пищей, в количествах, достаточных для того, чтобы удовлетворить физиологические потребности организма. Следующие аминокислоты принято считать незаменимыми для организма человека: изолейцин, лизин, метионин, фенилаланин, треонин, триптофан и валин. 5

Глицин – бесцветное кристаллическое вещество, хорошо растворимое в воде, сладковатого вкуса. Глицин играет большую роль в обмене веществ. Используется в качестве лекарственного средства для улучшения мозгового кровообращения.

Амфотерность аминокислот Одновременное наличие в молекулах аминокислот двух функциональных групп определяет их своеобразные химические свойства. Карбоксильная группа – СООН в аминокислотах определяет их кислотные свойства. Аминогруппа – NH 2 определяет основные свойства вещества, так как способна присоединять к себе катион водорода за счёт наличия свободной электронной пары у атома азота:

1) Кислотные свойства аминокислот: А) Взаимодействие с основаниями: H 2 N–CH 2–COOH + Na. OH H 2 N–CH 2–COONa + H 2 O Б) Взаимодействие со спиртами с образованием эфиров:

2) Основные свойства аминокислот: H 2 NCH 2 COOH + HCl [H 3 NCH 2 COOH]Cl. Хлороводородная соль глицина 3) Реакция поликонденсации, результат полипептид: Благодаря наличию кислотной и основной групп молекулы аминокислот способны взаимодействовать друг с другом и образовывать полимеры – белки. …+ HNH-CH 2 -COOH + HNH-CH 2 -COOH +… …-NH-CH 2 CO-… + n. H 2 O
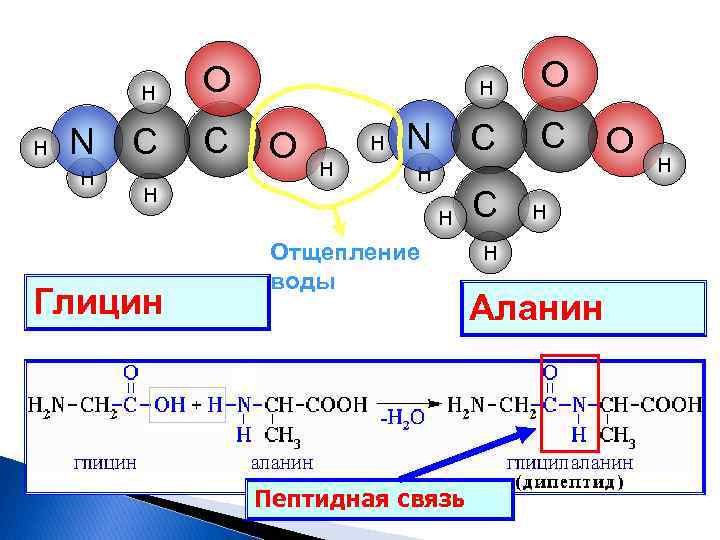
H H N H C C H H O H H N H H Глицин Отщепление воды Пептидная связь O C C H H Аланин O H
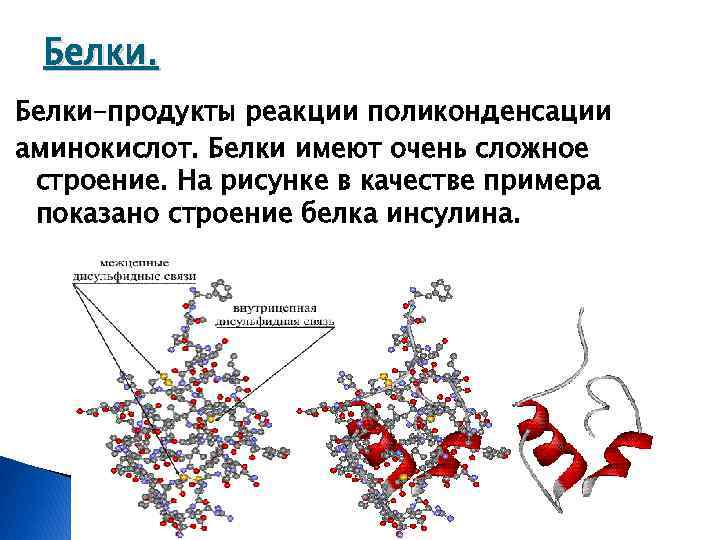
Белки–продукты реакции поликонденсации аминокислот. Белки имеют очень сложное строение. На рисунке в качестве примера показано строение белка инсулина.

Белки – важнейшая составная часть всех живых организмов. В любом живом организме содержатся тысячи белков, выполняющих разнообразные функции: 1. 2. 3. 4. 5. 6. Строительная. Каталитическая (ферментативная). Защитная. Транспортная. Запасающая (энергетическая). Сигнальная.

Белки выполняют ещё много важных функций: двигательную, сигнальную и т. д. Они могут превращаться в жиры и углеводы, но те, в свою очередь, превращаться в белки не могут. Поэтому белковое голодание особенно опасно для живого организма.

Химические свойства белков. Белки гидролизуются с образованием аминокислот. Это свойство лежит в основе процесса пищеварения. Белки денатурируются: при некоторых воздействиях разрушается структура белков. Белки горят, при этом появляется своеобразный запах жжёного пера. Для белков характерны цветные реакции, которые служат качественными на белки.

Биуретовая реакция: Р-р яичного белка + Cu(OH)2 → фиолетовое окрашивание Ксантопротеиновая реакция: Р-р яичного белка + HNO 3 → желтое окрашивание, усиливающееся при добавлении аммиака.

Домашнее задание: § 17, № 10, с. 134
Аминокислоты.pptx