Аминокислоты.ppt
- Количество слайдов: 33

Аминокислоты. Белки.

Аминокислоты (Ак) – органическая кислота, в радикале которой один или несколько атомов Н замещены на аминогруппу: H 2 N-R-COOH 2
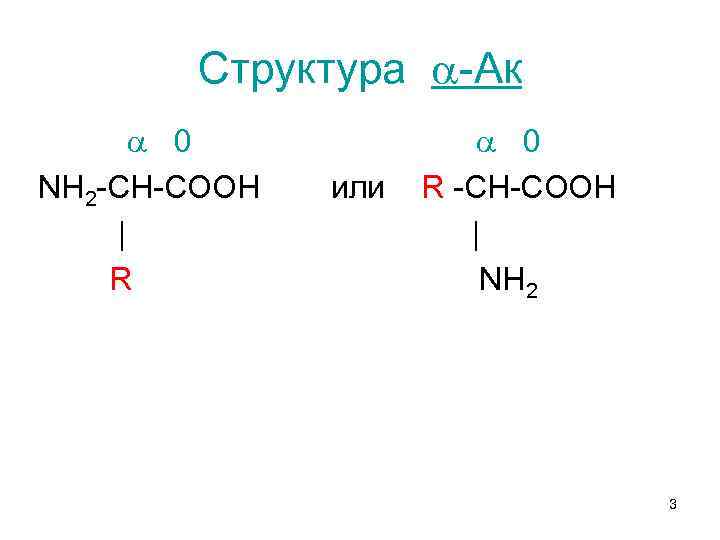
Структура -Ак 0 NH 2 -CH-COOH или R -CH-COOH | R NH 2 3

КЛАССИФИКАЦИЯ Ак I. По положению NH 2 -группы в R: 1. -Ак -Аланин (в составе белков) 2. -Ак -Аланин (БАВ) 3. -Ак -аминомасляная к-та (ГАМК) 4. -Ак орнитин (в синтезе мочевины ) II. По природе R в -Ак: 1. Алифатические: 1. 1. Моноаминомонокарбоновые (нейтральные) 1. 2. Серусодержащие 1. 3. Оксикислоты 1. 4. Моноаминодикарбоновые (кислые) 1. 5. Диаминомонокарбоновые -2 2. Ароматические 4
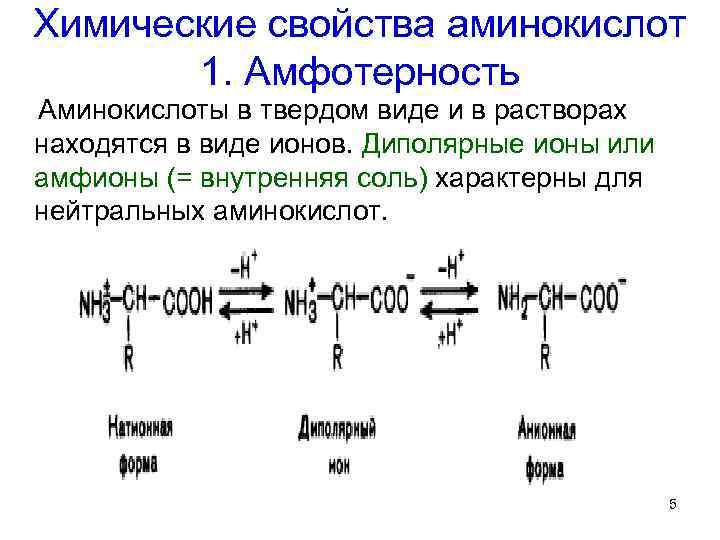
Химические свойства аминокислот 1. Амфотерность Аминокислоты в твердом виде и в растворах находятся в виде ионов. Диполярные ионы или амфионы (= внутренняя соль) характерны для нейтральных аминокислот. 5

р. I –показатель ИЭТ(изоэлектричекой точки) это величина р. Н, при котором наблюдается изоэлектрическое состояние молекулы (заряд=0 ) р. I>7 для основных аминокислот (Лиз, Арг, Гис), в R которых имеется дополнительная NH 2 - или NH–группа. р. I<7 для кислых Ак (Асп, Глу), в R которых имеется дополнительная СООН–группа. р. I~7 (около 6)для нейтральных (Остальных) Ак 6
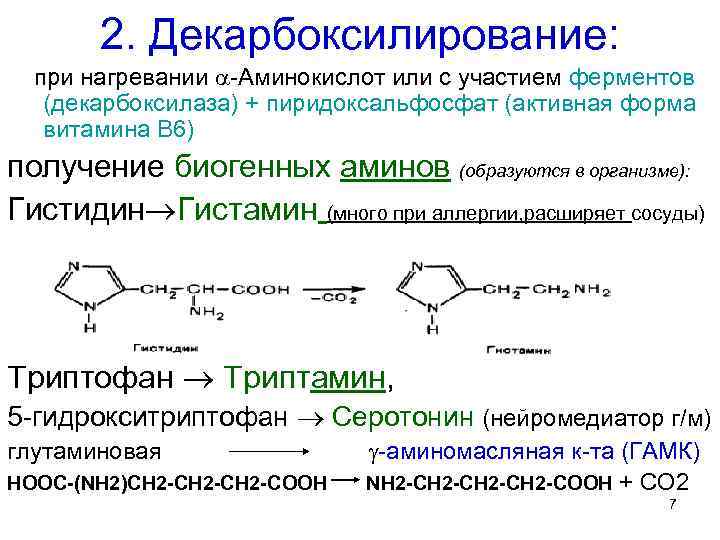
2. Декарбоксилирование: при нагревании -Аминокислот или с участием ферментов (декарбоксилаза) + пиридоксальфосфат (активная форма витамина В 6) получение биогенных аминов (образуются в организме): Гистидин Гистамин (много при аллергии, расширяет сосуды) Триптофан Триптамин, 5 -гидрокситриптофан Серотонин (нейромедиатор г/м) глутаминовая -аминомасляная к-та (ГАМК) НООС-(NН 2)СН 2 -СН 2 -СООН NН 2 -СН 2 -СООН + СО 2 7

: 4. Реакции окислительного дезаминирования 1. Окисление (дегидрирование) до иминок-ты 2. Гидролиз до кеток-ты и аммиака. В организме идет с участием ферментов и НАД Асп [O] . . . +HOH ЩУК +NH 3 8

5. Реакции трансаминирования Ферменты: Ас. Ат, Ал. Ат. Асп + -кетоглутаровая ЩУК + Глу Реакции трансаминирования играют большую роль в обмене аминокислот. Поскольку этот процесс обратим, ферменты аминотрансферазы функционируют как в процессах катаболизма, так и биосинтеза аминокислот. Трансаминирование - 471
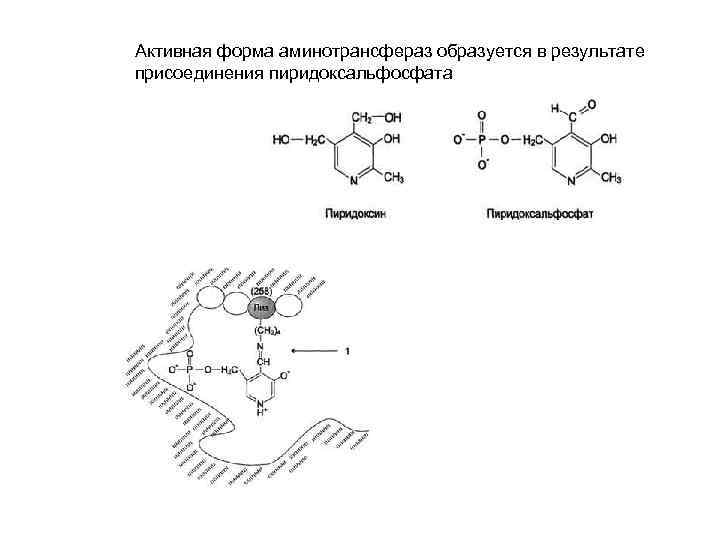
Активная форма аминотрансфераз образуется в результате присоединения пиридоксальфосфата

6. Обезвреживание аммиака. Основной реакцией связывания аммиака, протекающей во всех тканях организма, является : синтез глутамина под действием глутамин-синтетазы:

7. Образование пептидов и белков 12

Пептиды и белки 13
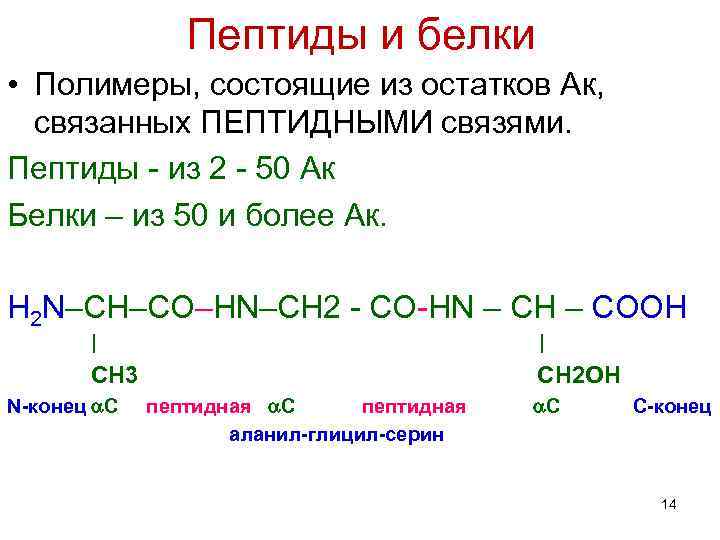
Пептиды и белки • Полимеры, состоящие из остатков Ак, связанных ПЕПТИДНЫМИ связями. Пептиды - из 2 - 50 Ак Белки – из 50 и более Ак. Н 2 N–СН–СО–НN–СН 2 - СО-НN – СН – СООН | СН 3 СН 2 ОН N-конец С пептидная С пептидная С-конец аланил-глицил-серин 14

Структура (пространственное строение) белка: • Первичная – полипептидная цепь (Ак связаны пептидной связью) • Вторичная (…+ водородные связи между группами –NH…ОС- пептидных цепей) - спираль - складчатый лист (много Гли, Про, Асп- антиспиральные Ак) • Третичная – глобулы или фибриллы(…+ слабые взаимодействия: 1)гидрофобные, 2) электростатические(ионные), 3) диполь-дипольные; прочная ковалентная (дисульфидная) связь) • Четвертичная (Hb)– несколько глобул, соединенных между собой слабыми связями (см. 15 связи третичной структуры, кроме ковалентной).
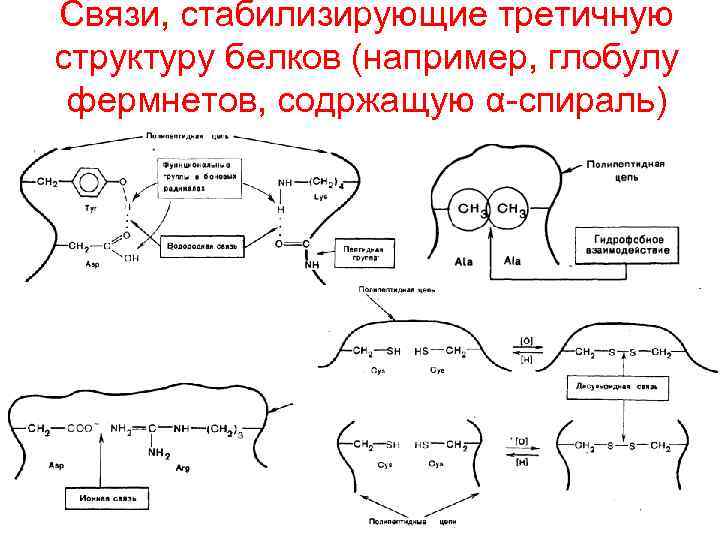
Связи, стабилизирующие третичную структуру белков (например, глобулу фермнетов, содржащую α-спираль) 17

Цветные реакции на Ак и белки (пептиды): 1. С нингидрином (для -Ак): Ак + нингидрин комплекс синефиолетового цвета 2. Биуретовая (для белков): пептидные связи белка+ Cu(OH)2 комплекс розово-фиолетового цвета 3. Реакция Фоля (на S-содерщащие Ак и белки): белок +Na. OH, t +(CH 3 COO)2 Pb Pb. S 4. Ксантопротеиновая реакция (на белки и ароматические Ак: Фен, Трп, Тир) ): белок+ НNO 3 желтый продукт 18 +Na. OH, t оранжевый продукт

Свойства растворов ВМС. Специфические свойства ВМС. • 1. ВМС набухают. Набухание сопровождается увеличением массы и объёма полимера. • 2. Растворы ВМС обладают большой вязкостью. • 3. Растворы ВМС легко желатинируются, образуя гели. • 4. ВМС лиофильны, а биополимеры гидрофильны. • 5. Растворы ВМС более устойчивы, чем растворы гидрофобных коллоидов, и поэтому могут быть получены более концентрированными.

• 6. Растворы ВМС сами не седиментируют. • 7. В растворах ВМС может иметь место коацервация. Это слияние водных оболочек частиц без объединения самих частиц. • 8. ВМС [белки] могут подвергаться денатурации. • 9. ВМС [белки] подвергаются высаливанию. • 10. ВМС дают размытый конус Тиндаля; гидрофобные золи дают чёткий конус Тиндаля.

• Гидрофильность растворов биополимеров. • Гидрофильность природных полимеров обусловлена главным образом пептидными, эфирными, двойными связями, карбоксильными, карбонильными, спиртовыми и аминными группами. • Различают ионогенные гидрофильные группы и неионогенные [полярные] группы.

• Ионогенные гидрофильные группы: R— СООН, R—СООNa, R—NН 3 ОН, R—NH 3 Cl. • полярные гидрофильные группы: R 2 C=0; R-COH • ☻Диссоциация ионогенных групп обеспечивает ВМС электрический заряд, а полярные группы притягивают диполи воды, образующие гидратную оболочку. Устойчивость растворов ВМС определяется двумя факторами: • - наличием заряда • - наличием гидратной оболочки

• • Амфотерность белков В кислой среде будет подавляться диссоциация карбоксильных групп и белки будут заряжаться положительно, в щелочной среде белки будут заряжены отрицательно: • • • Заряд белковой молекулы будет зависеть от следующих факторов: 1. От реакции среды. 2. От соотношения свободных карбоксильных и аминных групп, которое у каждого белка будет индивидуальным. 3. От степени диссоциации ионогенных групп белка. Если взять показатели констант диссоциации: р. КСООН < р. КNH 2 Состояние белка, когда заряд равен нулю, называется изоэлектрическим состоянием белка [ИЭС]. Значение р. Н, при котором белок находится в изоэлектрическом состоянии, называется изоэлектрической точкой белка [ИЭТ]. • • •

• Методы определения иэоэлектрической точки белков. • Изоэлектрическая точка белков может быть определена следующими методами: • 1. По величине набухания- Наименьшее набухание будет в изоэлектрической точке. • 2. По скорости желатинирования. Быстрее всего желатинирование происходит в изоэлектрической точке. • 3. По степени коагуляции -Наиболее выраженное помутнение раствора будет в изоэлектрической точке. • 4. По электрофоретической неподвижности -В растворе, где р. Н соответствует изоэлектрической точке белка, белок будет электронейтральным и перемещаться в электрическом поле не будет. • 5. Потенциометрическое титрование в сочетании с определением максимальной степени коагуляции.

• • • Свойства белка в ИЭТ. Минимальны: 1/ вязкость; 2/ гидратация; 3/ набухание; 4/ растворимость; 5/ осмотическое давление; 6/ электропроводность; 7/ дзета-потенциал. Максимальны: 1/ степень коагуляции; 2/ желатинирование.

• Нарушение устойчивости растворов полимеров • Кройт - схему осаждения коллоидов: • а/ удаление водной оболочки частиц водоотнимающим средством [например, спиртом]; • б/ снятие заряда частиц при добавлении электролита, • главным фактором устойчивости у них является водная оболочка

Дегидратировать частицу можно двумя путями: 1. Лишить частицу свойства гидрофильности, изменив структуру. Таким процессом является денатурация. 2. Отнять у частицы гидратационную воду, не лишая частицу свойства гидрофильности. Таким процессом является высаливание белков. Денатурация — это любое негидролитическое нарушение структуры нативного белка, которое приводит к изменению физических, химических и биологических свойств, присущих данному белку. Гидролитическое нарушение – разрушение первичной структуры.

При денатурации наблюдается: 1. Изменение вторичной, третичной и четвертичной структуры белка 2. Уменьшение растворимости [за счет развертывания молекул и появления снаружи гидрофобных гомополярных группировок]. 3. Изменение формы и размеров молекул. 5. Изменение реактивности некоторых химических группировок [например, сульфгидрильных групп, образующихся вместо дисульфидных групп]. 6. Уменьшение или потеря биологической активности [в образовании активных центров ферментов участвует третичная структура, а при денатурации эта структура нарушается]. 7. При денатурации увеличивается вязкость и утрачивается способность к набуханию.
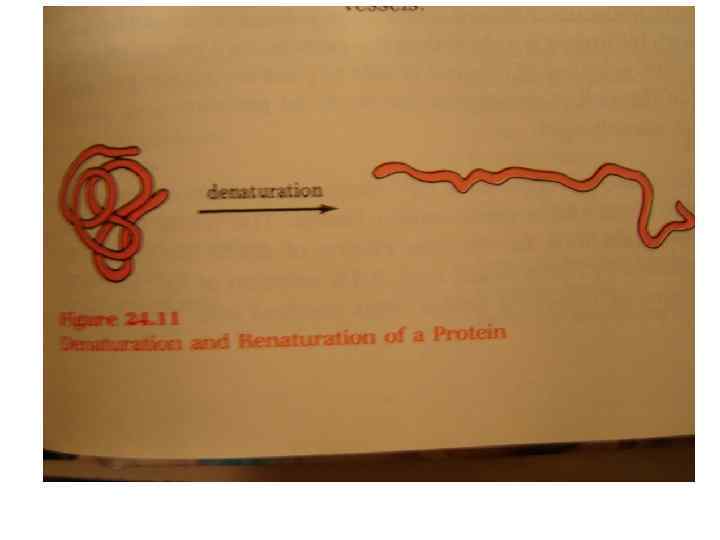

• • • Денатурацию могут вызвать факторы: а/ нагревание свыше 60°; б/ ультразвук; в/ многократное замораживание и оттаивание; г/ высокое давление; д/ ультрафиолетовое и ионизирующее излучения; е/ действие солей тяжелых металлов; ж/ изменение р. Н среды; з/ действие кислот; и/ действие алкалоидных реактивов; к/ действие мочевины и т. д. Денатурации обычно сопровождается коагуляцией и седиментацией.

• В клинике для обнаружения белков - денатурирующее действие органических и неорганических кислот. -Чувствительной реакцией на белок является реакция с сульфосалициловой кислотой, • -на втором месте по чувствительности стоит реакция с концентрированной азотной кислотой. • -Алкалоидные реактивы [например, танин] т. к. в белках содержатся гетероциклы, характерные для алкалоидов. • - действием солей тяжелых металлов • -не применяют концентрированную соляную и концентрированную серную кислоту, так как образующиеся осадки растворяются в избытке растворителя.

• Высаливание. - выделение белков путем добавления высоких концентраций нейтральных солей (не подвергающихся гидролизу) • Отличие от коагуляции - при высаливании частицы осаждаются не укрупняясь. К высаживанию совершенно неприменимо правило Шульце-Гарди.

• Высаливание зависит от: • 1) степени гидратации высаливающего иона ( ряд Гофмейстера) • 2) р. Н среды, в ИЭТ - макисмально • 3) от концентрации электролита ( разделение альбуминов и глобулинов сыворотки крови) • 4) температуры
Аминокислоты.ppt