Аминокислоты.pptx
- Количество слайдов: 25

Аминокислоты.

Аминокислоты – Гетерофункциональные соединения, которые обязательно содержат две функциональные группы: аминогруппу –NH 2 и карбоксильную группу –СООН, связанные с углеводородным радикалом. NH 2—CH—COOH | R
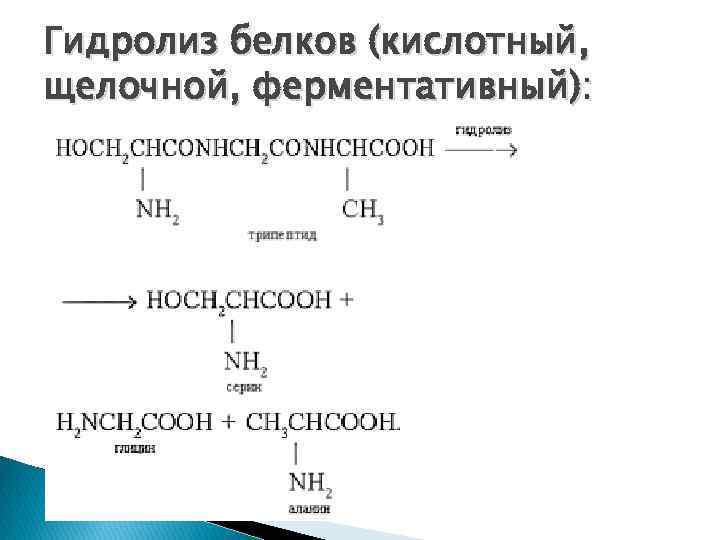
Гидролиз белков (кислотный, щелочной, ферментативный):

Амфотерность аминокислот Одновременное наличие в молекулах аминокислот двух функциональных групп определяет их своеобразные химические свойства. Карбоксильная группа – СООН в аминокислотах определяет их кислотные свойства. Аминогруппа – NH 2 определяет основные свойства вещества, так как способна присоединять к себе катион водорода за счёт наличия свободной электронной пары у атома азота:

Реакция поликонденсации, результат - полипептид: Благодаря наличию кислотной и основной групп молекулы аминокислот способны взаимодействовать друг с другом и образовывать полимеры – белки. …+ HNH-CH 2 -COOH + HNH-CH 2 -COOH +… …-NH-CH 2 CO-… + n. H 2 O
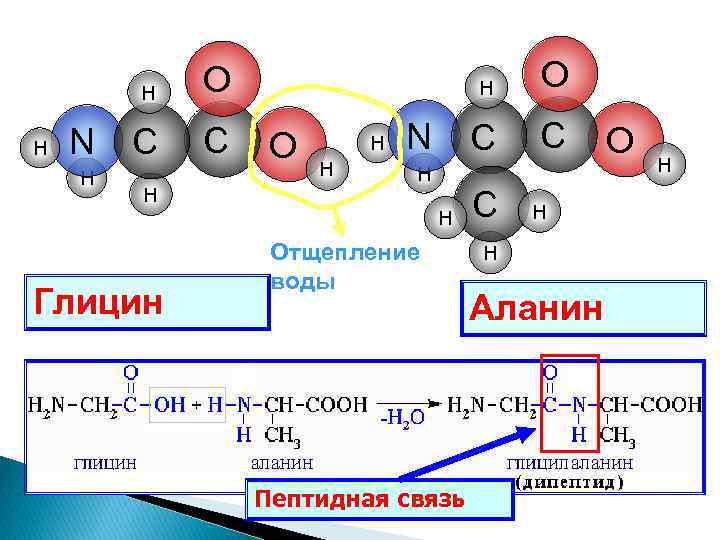
H H N H C C H H O H H N H H Глицин Отщепление воды Пептидная связь O C C H H Аланин O H

Физические свойства: Бесцветные кристаллические вещества; t кип (разложения)= 200 ◦С; Растворяются в воде, не растворяются в эфире; В зависимости от —R – горькие, сладкие, безвкусные.

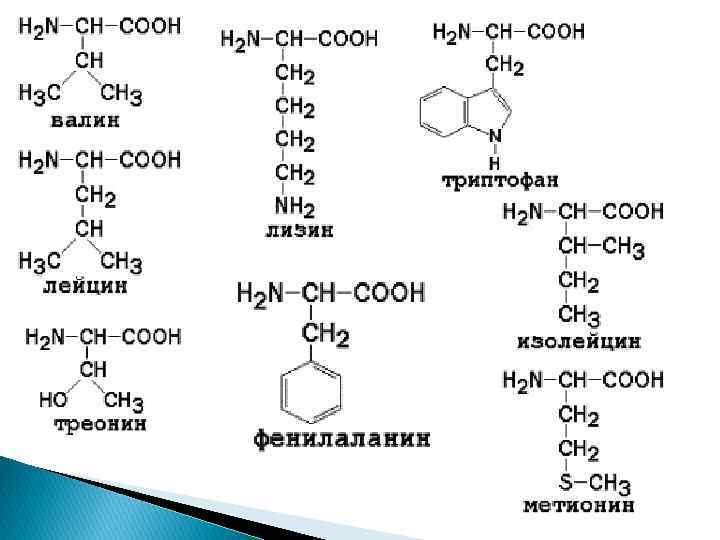
Незаменимые аминокислоты Незаменимыми называются аминокислоты, которые не могут быть синтезированы организмом из веществ, поступающих с пищей, в количествах, достаточных для того, чтобы удовлетворить физиологические потребности организма. Следующие аминокислоты принято считать незаменимыми для организма человека: изолейцин, лизин, метионин, фенилаланин, треонин, триптофан и валин. 8

Серповидно-клеточная анемия возникает в результате замены одного аминокислотного остатка глутаминовой кислоты на остаток валина в полипептидной цепи молекулы гемоглобина. Фрагмент цепи нормального гемоглобина: –Глу–Лиз–. Фрагмент цепи аномального гемоглобина: –Вал–Глу–Лиз–.

Белки – это природные полимеры, обладающие высокими значениями молекулярной массы, молекулы которых построены из остатков аминокислот, соединенных пептидной связью. Белковая молекула – это полимер, в котором пептидная связь повторяется многократно, поэтому полимер называется полипептидом.
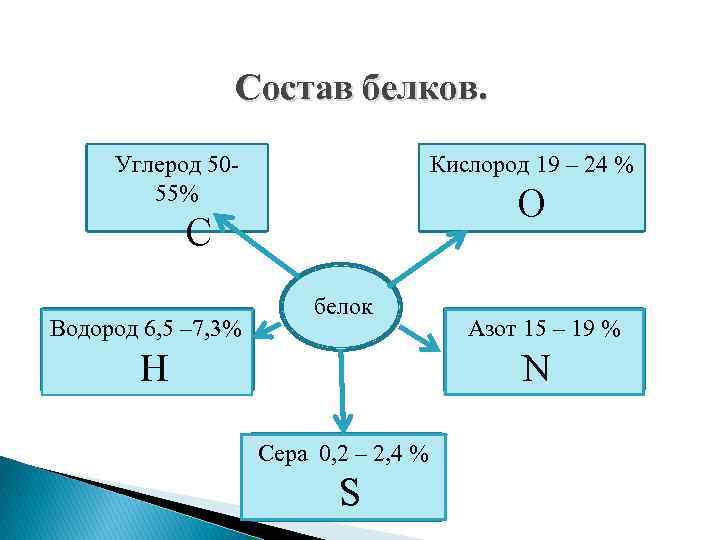
Состав белков. Углерод 5055% Кислород 19 – 24 % О С Водород 6, 5 – 7, 3% белок Н Азот 15 – 19 % N Сера 0, 2 – 2, 4 % S
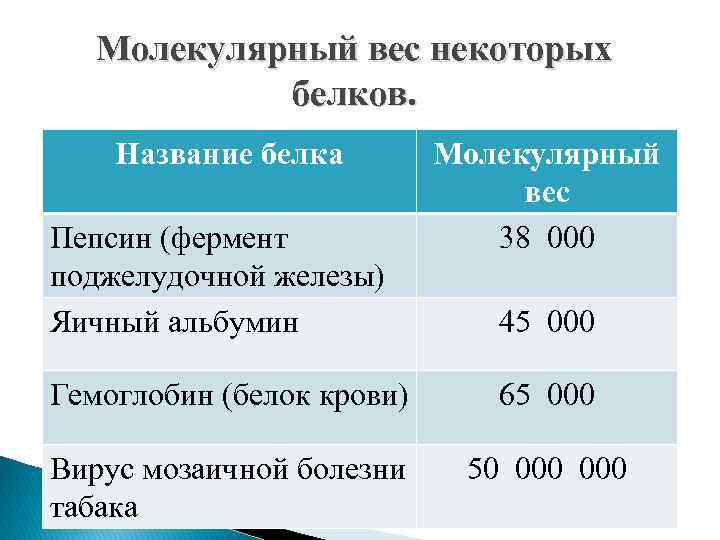
Молекулярный вес некоторых белков. Название белка Пепсин (фермент поджелудочной железы) Яичный альбумин Молекулярный вес 38 000 45 000 Гемоглобин (белок крови) 65 000 Вирус мозаичной болезни табака 50 000
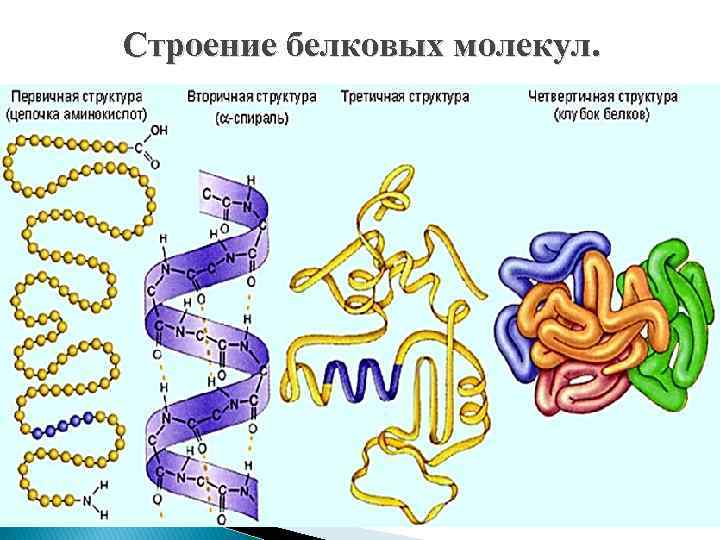
Строение белковых молекул.

Первичная структура белка. Специфическая аминокислотная последовательность, т. е. порядок чередования α- аминокислотных остатков в полипептидной цепи. Представляет собой вытянутую нить; определяется тремя факторами: • природой аминокислот, входящих в состав белков; • количеством аминокислот; • последовательностью аминокислот.
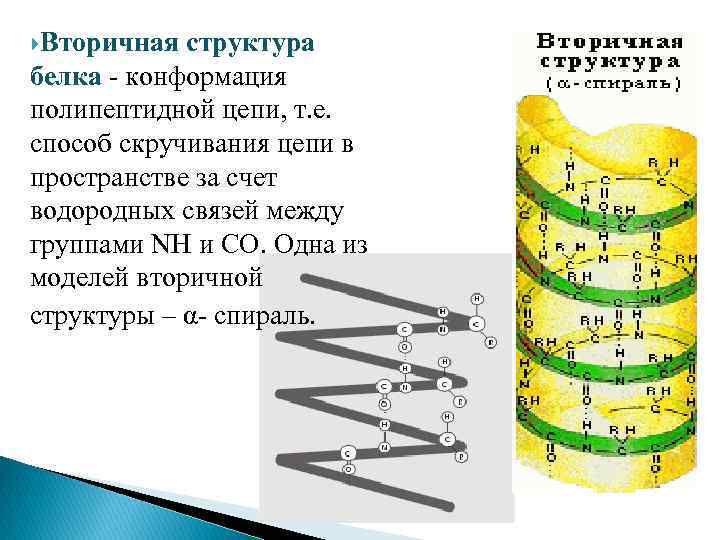
Вторичная структура белка - конформация полипептидной цепи, т. е. способ скручивания цепи в пространстве за счет водородных связей между группами NH и CO. Одна из моделей вторичной структуры – α- спираль.

Третичная структура белка - форма закрученной спирали в пространстве, образованная главным образом за счет дисульфидных мостиков -S-S-, водородных связей, гидрофобных и ионных взаимодействий.

Четвертичная структура белка – агрегаты нескольких белковых макромолекул (белковые комплексы), образованные за счет взаимодействия разных полипептидных цепей

Свойства белков. 1. Гидролиз( разрушение первичной структуры белка по пептидным связям):

2. Денатурация. Условия прохождения процесса: нагревание; действие сильных кислот и оснований; действие солей тяжелых металлов. При денатурации происходят изменения во вторичной и третичной структурах белка. Первичная структура сохраняется. Де- и ренатурация белка: К 2– 3 мл раствора белка добавить несколько кристалликов поваренной соли, размешать. Появление белого мутного осадка будет свидетельствовать о денатурации белка. Если к полученному осадку добавить несколько миллилитров воды и снова размешать, осадок растворяется, т. е. происходит ренатурация белка.

Свойства белков. 3. Горение. При горении белков образуется характерный запах «жженного рога» ( определяется содержанием серы в белках). Продукты горения: азот, диоксид углерода и вода.

Свойства белков. 4. Цветные реакции: 1. Биуретовая реакция: Взаимодействие с солями Cu в щелочной среде 2 Na. OH + Cu. SO 4 Cu(OH)2 + Na 2 SO 4 Все белки дают фиолетовое окрашивание. 2. Ксантопротеиновая реакция. Эта реакция на циклические аминокислоты: нагревание фенилаланин + НОNО 2 нитрофенилаланин - Н 2 О желтый цвет 3. Сульфгидрильная реакция. На серосодержащие аминокислоты , при нагревании белка с уксуснокислым свинцом образуется черный осадок

Функции белков: 1) Структурная (пластическая) – белками образованы многие клеточные компоненты, а в комплексе с липидами они входят в состав клеточных мембран. 2) Каталитическая – все биологические катализаторы – ферменты по своей химической природе являются белками. 3) Транспортная – белок гемоглобин транспортирует кислород, ряд других белков образуя комплекс с липидами транспортируют их по крови и лимфе (пример: миоглобин, сывороточный альбумин). 4) Механохимическая – мышечная работа и иные формы движения в организме осуществляются при непосредственном участии сократительных белков с использованием энергии макроэргических связей (пример: актин, миозин)

5) Регуляторная – ряд гормонов и других биологически активных веществ имеют белковую природу (пр. : инсулин, АКТГ). 6) Защитная – антитела (иммуноглобулины) являются белками, кроме того основу кожи составляет белок коллаген, а волос – креатин. Кожа и волосы защищают внутреннюю среду организма от внешних воздействий. В состав слизи и синовиальной жидкости входят мукопротеиды. 7) Опорная – сухожилия, поверхности суставов соединения костей образованы в значительной степени белковыми веществами (пр. : коллаген, эластин). 8) Энергетическая – аминокислоты белков могут поступать на путь гликолиза, который обеспечивает клетку энергией. 9) Рецепторная – многие белки участвуют в процесса избирательного узнавания(рецепторы).

Домашнее задание: § 38, № 4, с. 232
Аминокислоты.pptx