АМИНОКИСЛОТЫ (А/К) Функц. группы– NН 2






Презентация Аминок-т+ПЕПТИДЫ.ppt
- Количество слайдов: 28
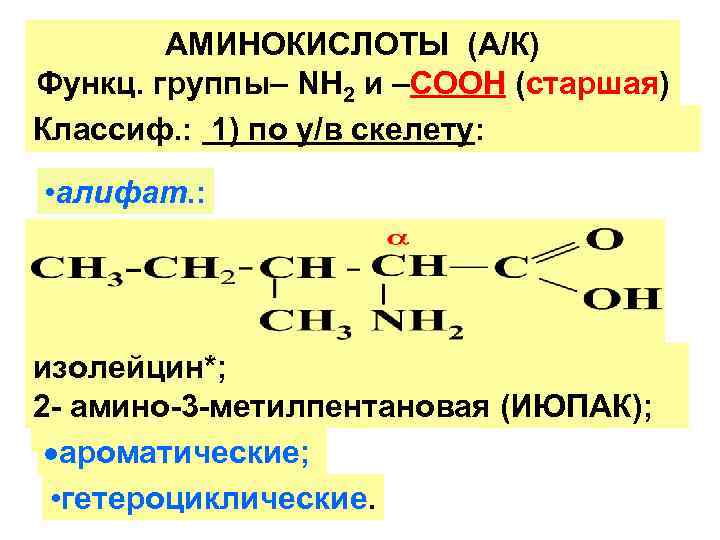
 АМИНОКИСЛОТЫ (А/К) Функц. группы– NН 2 и –СООН (старшая) Классиф. : 1) по у/в скелету: • алифат. : изолейцин*; 2 - амино-3 -метилпентановая (ИЮПАК); ароматические; • гетероциклические.
АМИНОКИСЛОТЫ (А/К) Функц. группы– NН 2 и –СООН (старшая) Классиф. : 1) по у/в скелету: • алифат. : изолейцин*; 2 - амино-3 -метилпентановая (ИЮПАК); ароматические; • гетероциклические.
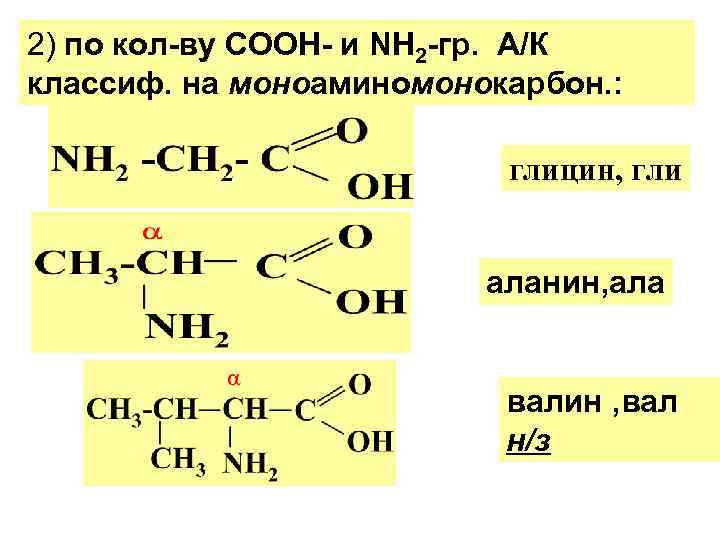
 2) по кол-ву СООН- и NH 2 -гр. А/К классиф. на моноаминомонокарбон. : глицин, гли аланин, ала валин , вал н/з
2) по кол-ву СООН- и NH 2 -гр. А/К классиф. на моноаминомонокарбон. : глицин, гли аланин, ала валин , вал н/з
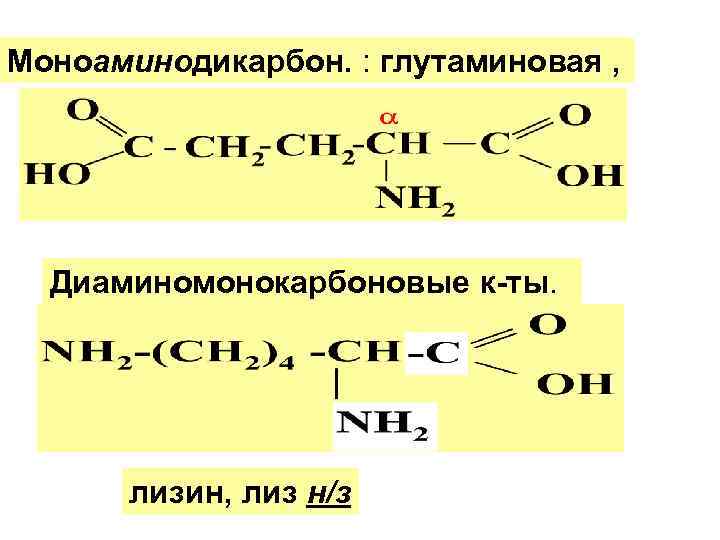
 Моноаминодикарбон. : глутаминовая , Диаминомонокарбоновые к-ты. лизин, лиз н/з
Моноаминодикарбон. : глутаминовая , Диаминомонокарбоновые к-ты. лизин, лиз н/з
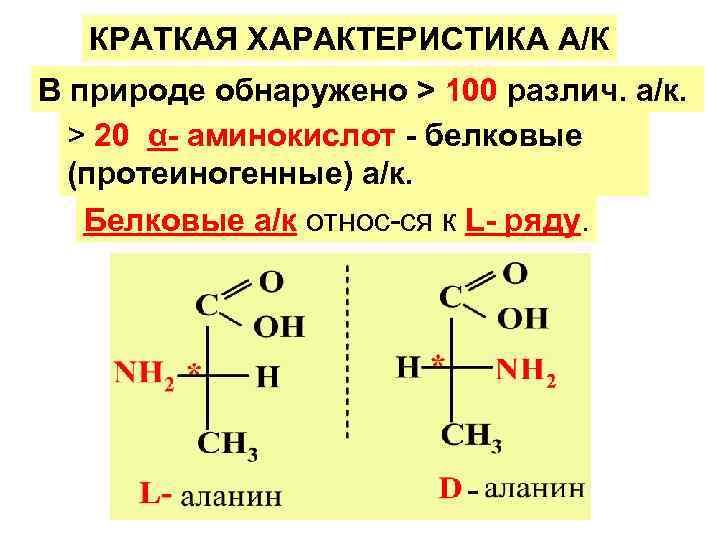
 КРАТКАЯ ХАРАКТЕРИСТИКА А/К В природе обнаружено > 100 различ. а/к. > 20 α- аминокислот - белковые (протеиногенные) а/к. Белковые а/к относ-ся к L- ряду.
КРАТКАЯ ХАРАКТЕРИСТИКА А/К В природе обнаружено > 100 различ. а/к. > 20 α- аминокислот - белковые (протеиногенные) а/к. Белковые а/к относ-ся к L- ряду.
 Из 20 протеиногенных а/к 8 (восемь) – незаменимые (н/з) для человека (все L-ряда) : валин, лейцин, изолейцин, лизин, метионин, треонин, триптофан, фенилаланин.
Из 20 протеиногенных а/к 8 (восемь) – незаменимые (н/з) для человека (все L-ряда) : валин, лейцин, изолейцин, лизин, метионин, треонин, триптофан, фенилаланин.
 ФИЗИЧ. СВ-ВА А/К 1. Кристалл. вещ-ва с аном. высок. Т пл. ; 2. Раств-мы в воде, р-ры –электролиты; 3. В ИК-спектрах отсутст. полосы поглощ-я, характер. для – NН 2 и –СООН групп т. е по св-вам напоминают соли
ФИЗИЧ. СВ-ВА А/К 1. Кристалл. вещ-ва с аном. высок. Т пл. ; 2. Раств-мы в воде, р-ры –электролиты; 3. В ИК-спектрах отсутст. полосы поглощ-я, характер. для – NН 2 и –СООН групп т. е по св-вам напоминают соли
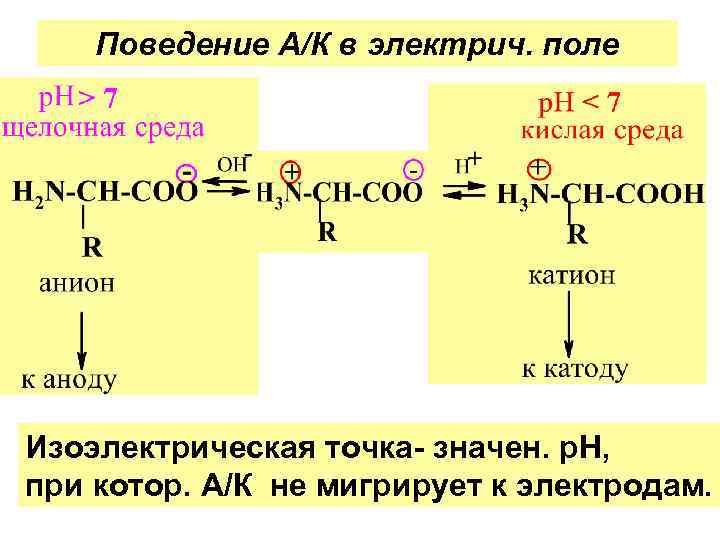
 Поведение А/К в электрич. поле Изоэлектрическая точка- значен. р. Н, при котор. А/К не мигрирует к электродам.
Поведение А/К в электрич. поле Изоэлектрическая точка- значен. р. Н, при котор. А/К не мигрирует к электродам.
 ХИМ. СВ-ВА А/К I. Амфотерность а/к II. Качеств. р-ции на α-аминок-ты III. Р-ции по NН 2 -гр. , IV. Р-ции по СООН- гр. V. Специфические св-ва (взаимное влияние функц. гр. )
ХИМ. СВ-ВА А/К I. Амфотерность а/к II. Качеств. р-ции на α-аминок-ты III. Р-ции по NН 2 -гр. , IV. Р-ции по СООН- гр. V. Специфические св-ва (взаимное влияние функц. гр. )
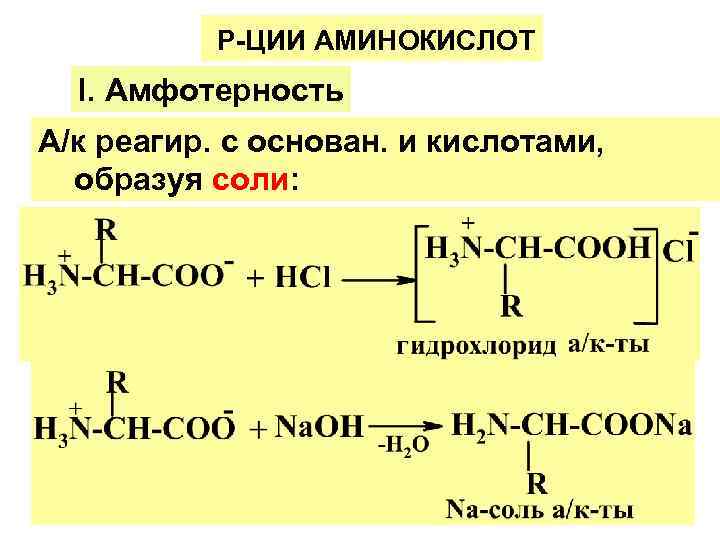
 Р-ЦИИ АМИНОКИСЛОТ l. Амфотерность А/к реагир. с основан. и кислотами, образуя соли:
Р-ЦИИ АМИНОКИСЛОТ l. Амфотерность А/к реагир. с основан. и кислотами, образуя соли:
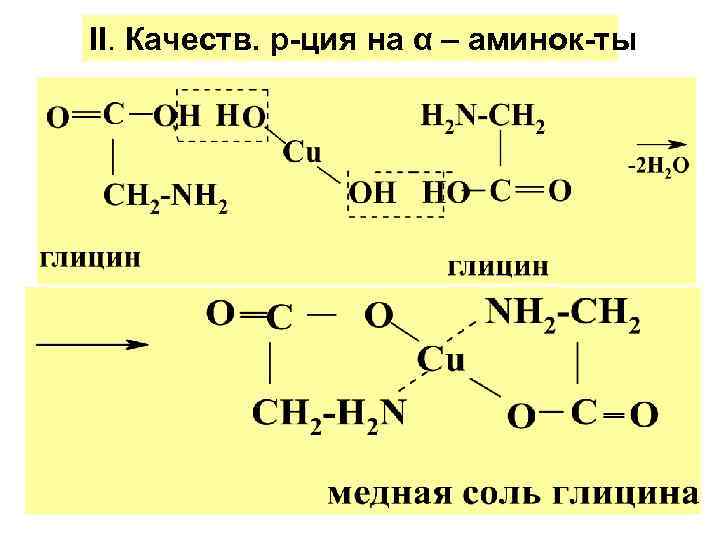
 II. Качеств. р-ция на α – аминок-ты
II. Качеств. р-ция на α – аминок-ты
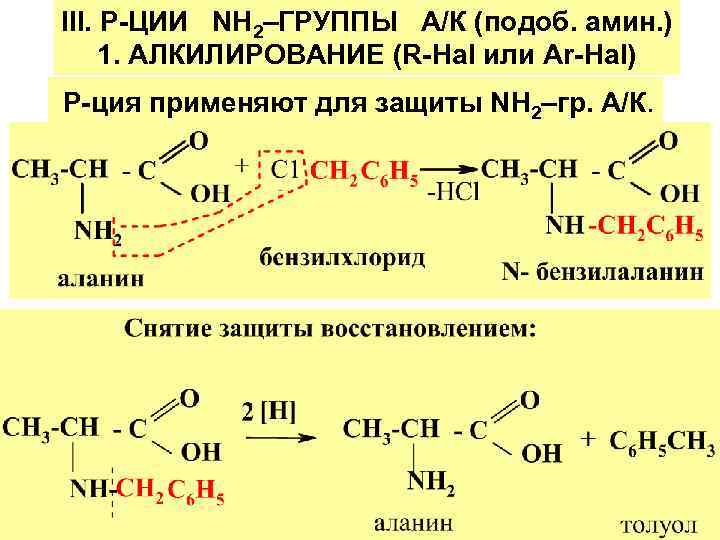
 III. Р-ЦИИ NН 2–ГРУППЫ А/К (подоб. амин. ) 1. АЛКИЛИРОВАНИЕ (R-Наl или Аr-Наl) Р-ция применяют для защиты NН 2–гр. А/К.
III. Р-ЦИИ NН 2–ГРУППЫ А/К (подоб. амин. ) 1. АЛКИЛИРОВАНИЕ (R-Наl или Аr-Наl) Р-ция применяют для защиты NН 2–гр. А/К.
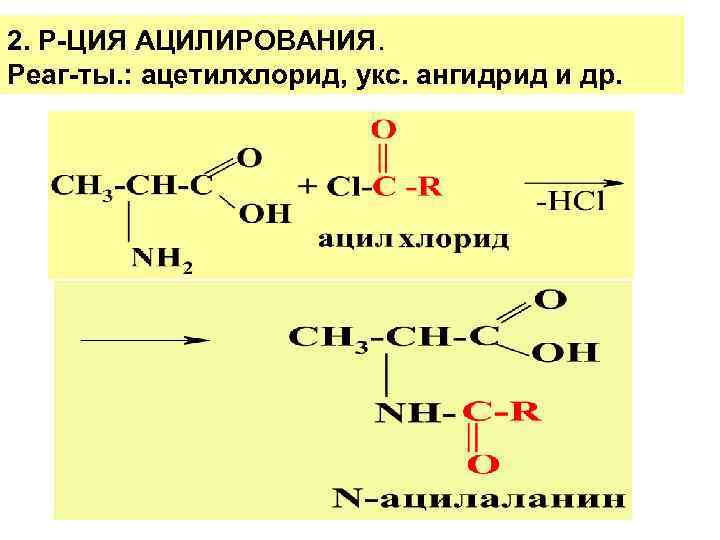
 2. Р-ЦИЯ АЦИЛИРОВАНИЯ. Реаг-ты. : ацетилхлорид, укс. ангидрид и др.
2. Р-ЦИЯ АЦИЛИРОВАНИЯ. Реаг-ты. : ацетилхлорид, укс. ангидрид и др.
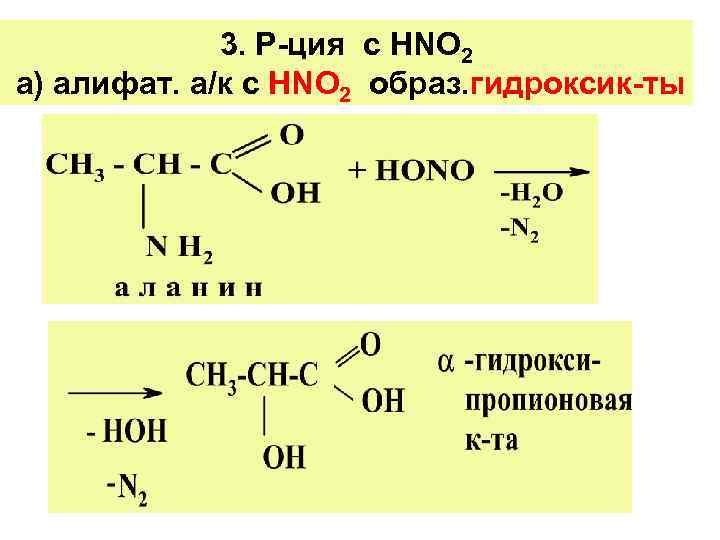
 3. Р-ция с НNО 2 а) алифат. а/к с НNО 2 образ. гидроксик-ты
3. Р-ция с НNО 2 а) алифат. а/к с НNО 2 образ. гидроксик-ты
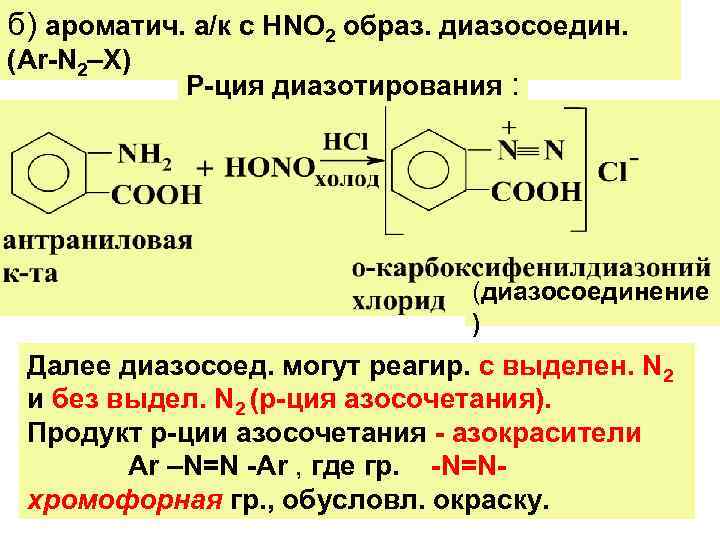
 б) ароматич. а/к с НNО 2 образ. диазосоедин. (Ar-N 2–X) Р-ция диазотирования : (диазосоединение ) Далее диазосоед. могут реагир. с выделен. N 2 и без выдел. N 2 (р-ция азосочетания). Продукт р-ции азосочетания - азокрасители Ar –N=N -Ar , где гр. -N=N- хромофорная гр. , обусловл. окраску.
б) ароматич. а/к с НNО 2 образ. диазосоедин. (Ar-N 2–X) Р-ция диазотирования : (диазосоединение ) Далее диазосоед. могут реагир. с выделен. N 2 и без выдел. N 2 (р-ция азосочетания). Продукт р-ции азосочетания - азокрасители Ar –N=N -Ar , где гр. -N=N- хромофорная гр. , обусловл. окраску.
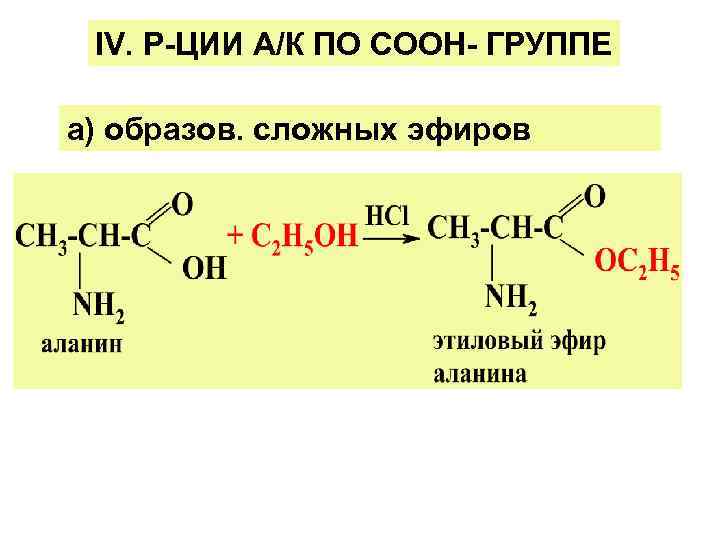
 IV. Р-ЦИИ А/К ПО СООН- ГРУППЕ а) образов. сложных эфиров
IV. Р-ЦИИ А/К ПО СООН- ГРУППЕ а) образов. сложных эфиров
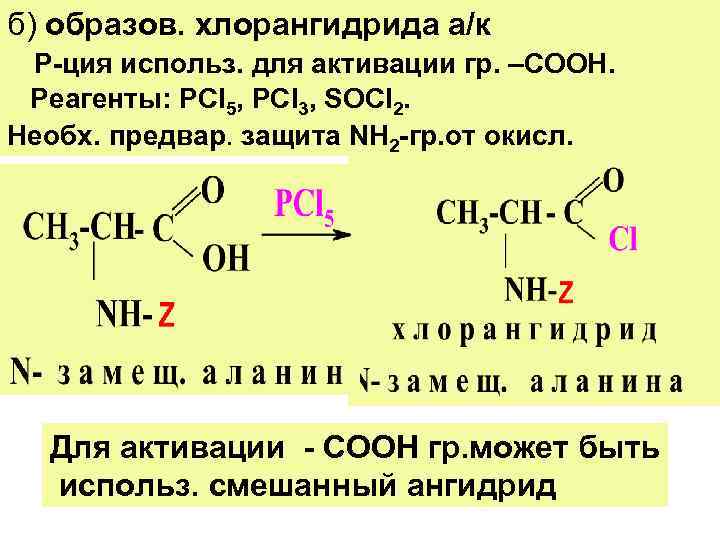
 б) образов. хлорангидрида а/к Р-ция использ. для активации гр. –СООН. Реагенты: РСl 5, РСl 3, SOСI 2. Необх. предвар. защита NН 2 -гр. от окисл. Для активации - СООН гр. может быть использ. смешанный ангидрид
б) образов. хлорангидрида а/к Р-ция использ. для активации гр. –СООН. Реагенты: РСl 5, РСl 3, SOСI 2. Необх. предвар. защита NН 2 -гр. от окисл. Для активации - СООН гр. может быть использ. смешанный ангидрид
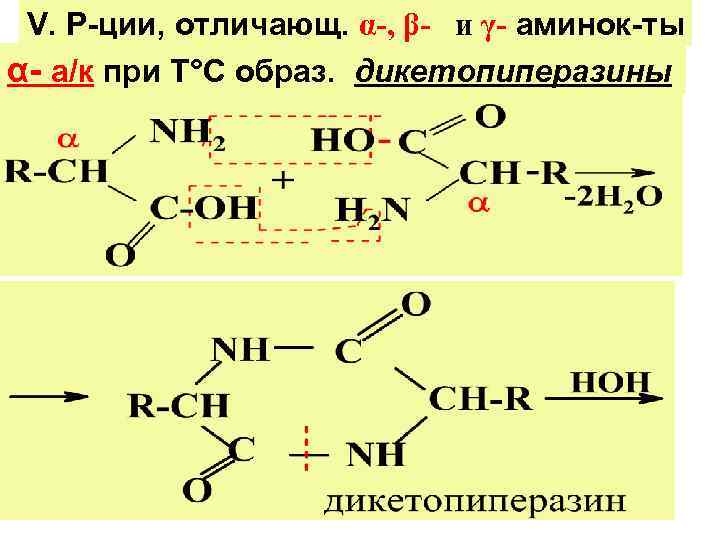
 V. Р-ции, отличающ. α-, β- и γ- аминок-ты α- а/к при Т°С образ. дикетопиперазины
V. Р-ции, отличающ. α-, β- и γ- аминок-ты α- а/к при Т°С образ. дикетопиперазины
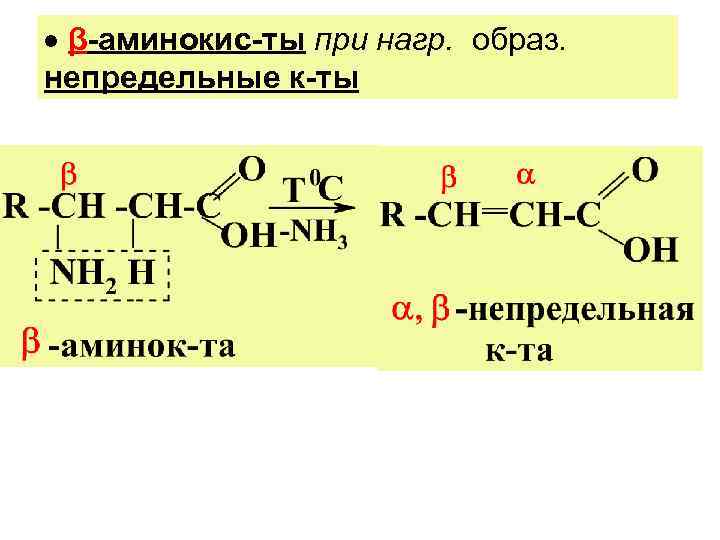
 β-аминокис-ты при нагр. образ. непредельные к-ты
β-аминокис-ты при нагр. образ. непредельные к-ты
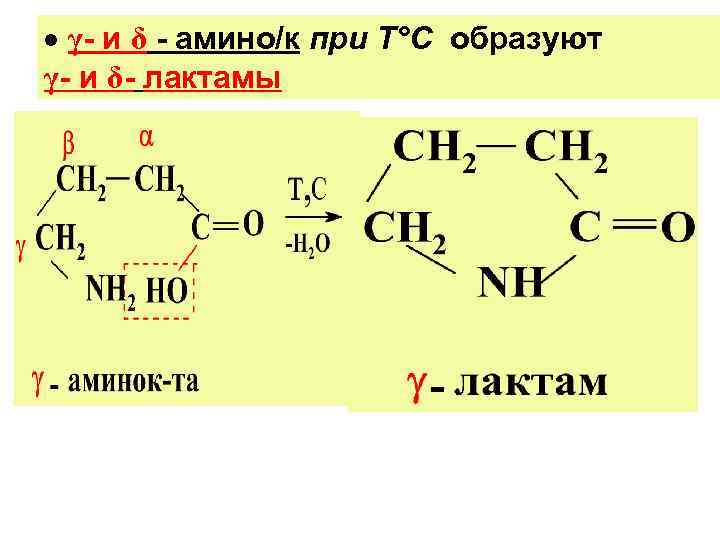
 γ- и δ - амино/к при Т°С образуют γ- и δ- лактамы
γ- и δ - амино/к при Т°С образуют γ- и δ- лактамы
 ПОЛУЧЕНИЕ АМИНОКИСЛОТ 1. Биотехнологические методы: а) гидролиз белков (смесь , L-а/к) б) микробиолог. синтез 2. Химические синтезы а) аммонолиз -галогензамещ. к-т Br-CH 2 -COOH+2 NH 3 H 2 N-CH 2 -COOH +NH 4 Br -бромуксусная к-та глицин
ПОЛУЧЕНИЕ АМИНОКИСЛОТ 1. Биотехнологические методы: а) гидролиз белков (смесь , L-а/к) б) микробиолог. синтез 2. Химические синтезы а) аммонолиз -галогензамещ. к-т Br-CH 2 -COOH+2 NH 3 H 2 N-CH 2 -COOH +NH 4 Br -бромуксусная к-та глицин
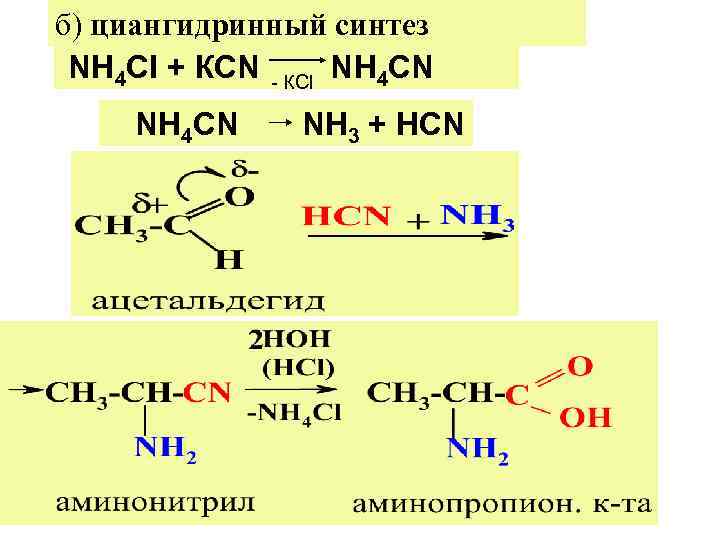
 б) циангидринный синтез NH 4 СI + КСN - КСl NH 4 СN NH 3 + HСN
б) циангидринный синтез NH 4 СI + КСN - КСl NH 4 СN NH 3 + HСN
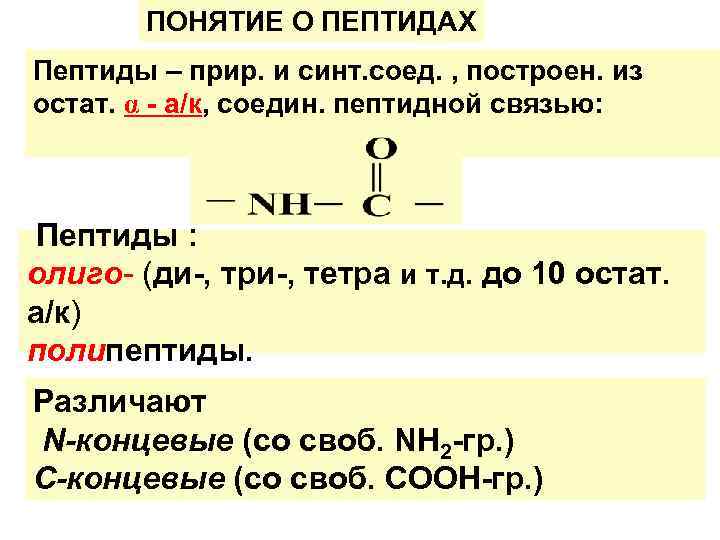
 ПОНЯТИЕ О ПЕПТИДАХ Пептиды – прир. и синт. соед. , построен. из остат. α - а/к, соедин. пептидной связью: Пептиды : олиго- (ди-, три-, тетра и т. д. до 10 остат. а/к) полипептиды. Различают N-концевые (со своб. NН 2 -гр. ) С-концевые (со своб. СООН-гр. )
ПОНЯТИЕ О ПЕПТИДАХ Пептиды – прир. и синт. соед. , построен. из остат. α - а/к, соедин. пептидной связью: Пептиды : олиго- (ди-, три-, тетра и т. д. до 10 остат. а/к) полипептиды. Различают N-концевые (со своб. NН 2 -гр. ) С-концевые (со своб. СООН-гр. )
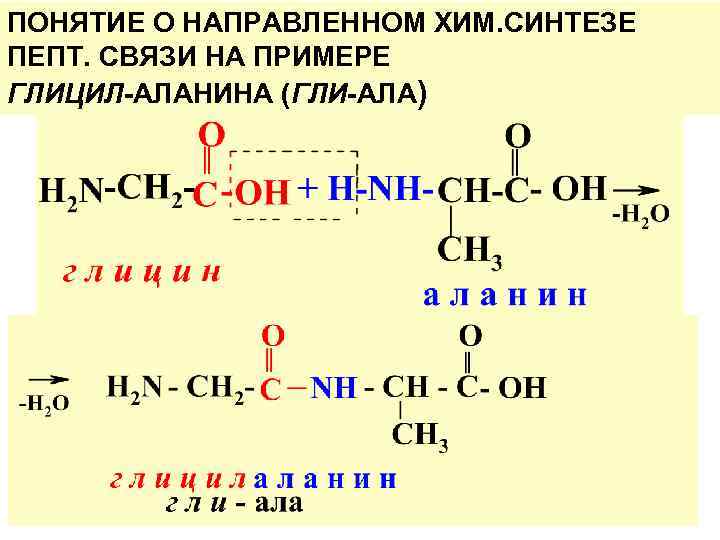
 ПОНЯТИЕ О НАПРАВЛЕННОМ ХИМ. СИНТЕЗЕ ПЕПТ. СВЯЗИ НА ПРИМЕРЕ ГЛИЦИЛ-АЛАНИНА (ГЛИ-АЛА)
ПОНЯТИЕ О НАПРАВЛЕННОМ ХИМ. СИНТЕЗЕ ПЕПТ. СВЯЗИ НА ПРИМЕРЕ ГЛИЦИЛ-АЛАНИНА (ГЛИ-АЛА)
 При взаимодейст. глицина и аланина возможны след. варианты дипептидов : гли-ала ала-гли гли-гли ала-ала Для исключ. получ. побочных дипептидов проводят последоват-ную защиту функц. гр. : NН 2 –гр. в глицине и СООН-гр. в аланине.
При взаимодейст. глицина и аланина возможны след. варианты дипептидов : гли-ала ала-гли гли-гли ала-ала Для исключ. получ. побочных дипептидов проводят последоват-ную защиту функц. гр. : NН 2 –гр. в глицине и СООН-гр. в аланине.
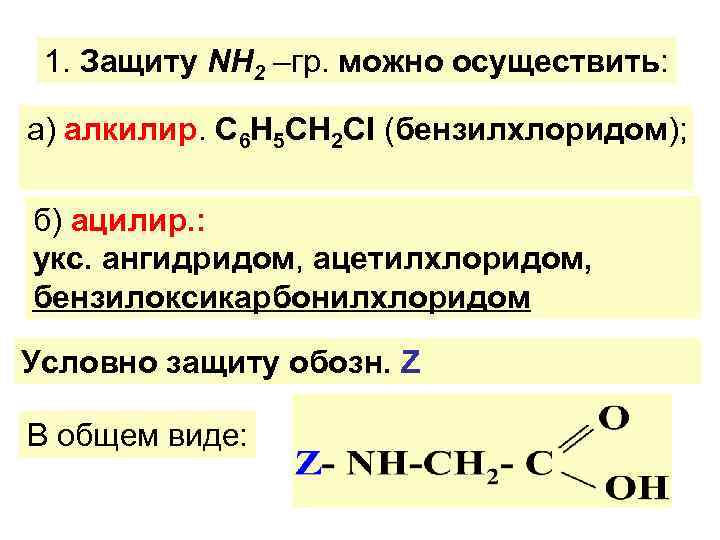
 1. Защиту NН 2 –гр. можно осуществить: а) алкилир. С 6 Н 5 СН 2 СI (бензилхлоридом); б) ацилир. : укс. ангидридом, ацетилхлоридом, бензилоксикарбонилхлоридом Условно защиту обозн. Z В общем виде:
1. Защиту NН 2 –гр. можно осуществить: а) алкилир. С 6 Н 5 СН 2 СI (бензилхлоридом); б) ацилир. : укс. ангидридом, ацетилхлоридом, бензилоксикарбонилхлоридом Условно защиту обозн. Z В общем виде:
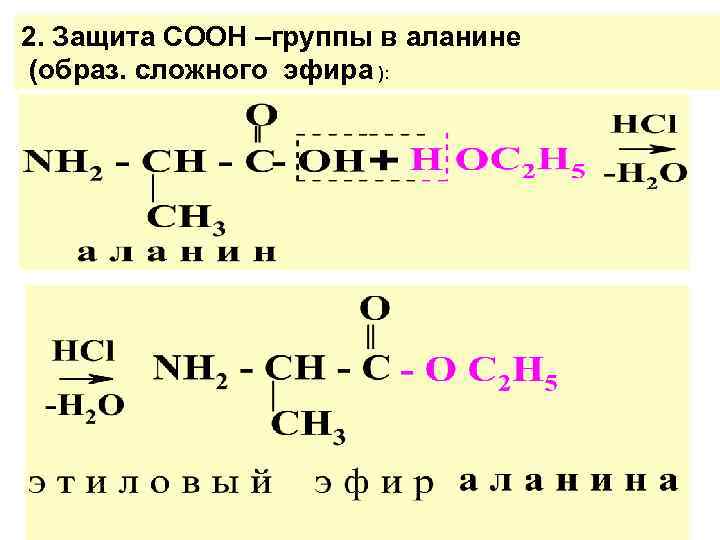
 2. Защита СООН –группы в аланине (образ. сложного эфира ):
2. Защита СООН –группы в аланине (образ. сложного эфира ):
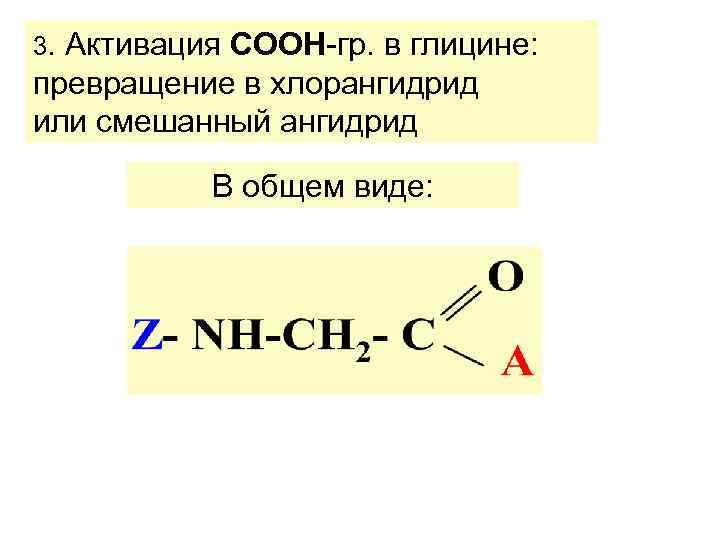
 3. Активация СООН-гр. в глицине: превращение в хлорангидрид или смешанный ангидрид В общем виде:
3. Активация СООН-гр. в глицине: превращение в хлорангидрид или смешанный ангидрид В общем виде:
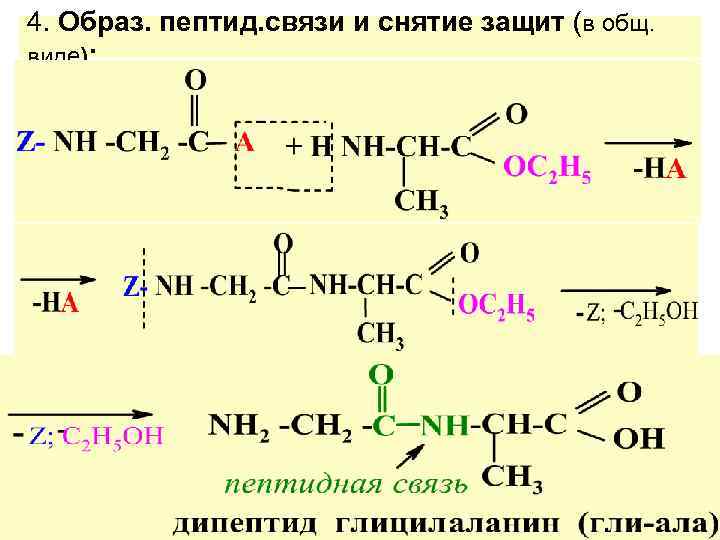
 4. Образ. пептид. связи и снятие защит (в общ. виде):
4. Образ. пептид. связи и снятие защит (в общ. виде):

