биофизика 006.ppt
- Количество слайдов: 6
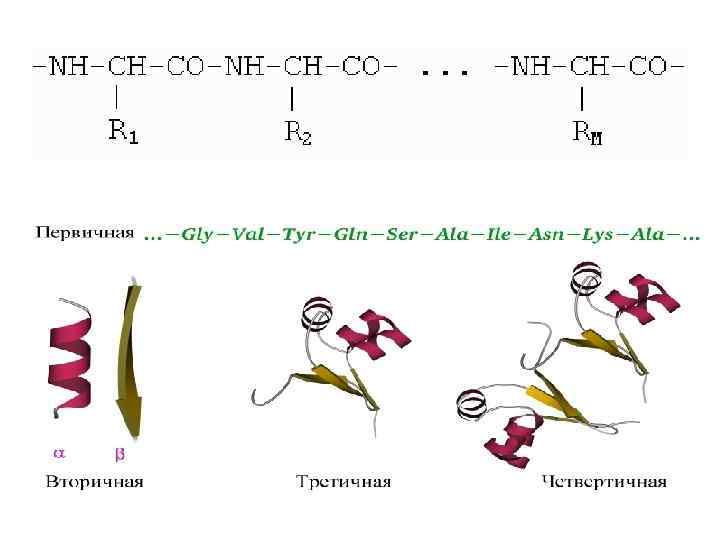
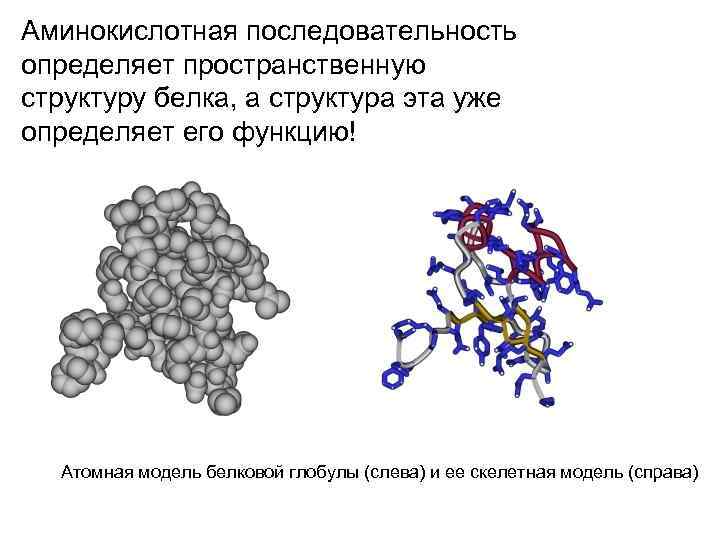
Аминокислотная последовательность определяет пространственную структуру белка, а структура эта уже определяет его функцию! Атомная модель белковой глобулы (слева) и ее скелетная модель (справа)

ЭЛЕМЕНТАРНЫЕ ВЗАИМОДЕЙСТВИЯ В БЕЛКОВЫХ МОЛЕКУЛАХ * КОВАЛЕНТНЫЕ связи - обычные прочные химические связи. а) пептидная связь б) дисульфидная связь * НЕКОВАЛЕНТНЫЕ (СЛАБЫЕ) ТИПЫ СВЯЗЕЙ - физико-химические взаимодействия родственных структур. а) Ионная связь б) Взаимодействие Вандер-Ваальса. в) Водородная связь г) Гидрофобное взаимодействие
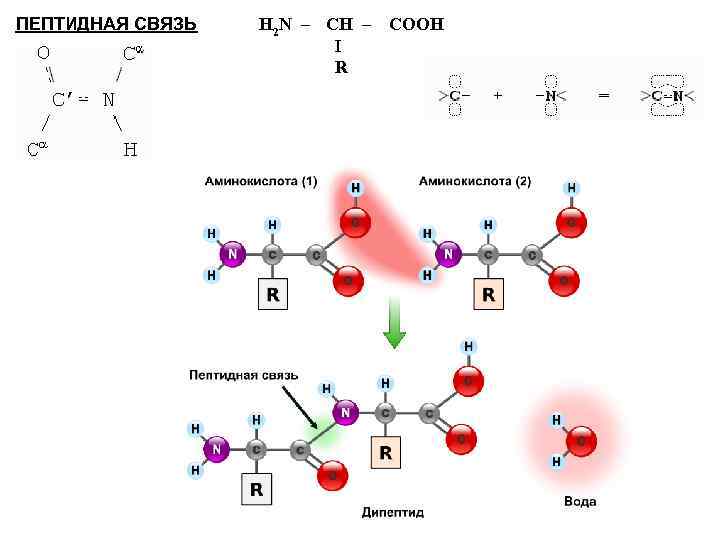
ПЕПТИДНАЯ СВЯЗЬ H 2 N – CH – COOH I R

ДИСУЛЬФИДНАЯ СВЯЗЬ (S-S) Дисульфидные связи образуются цистеиновыми аминокислотными остатками. Цистеин - аминокислота, которая в радикале имеет SHгруппу, за счет которой и образуются дисульфидные связи. В клетке глутатион: 1) в мономерной тиольной форме (GSH) - восстановленная 2) в димерной дисульфидной (GSSG) форме - окисленная Фермент - глутатионредуктаза Белок + GS-SG белок + GSH белок + 2 GSH I I I I SH HS SH S-SG S - S Фермент дисульфидизомераза
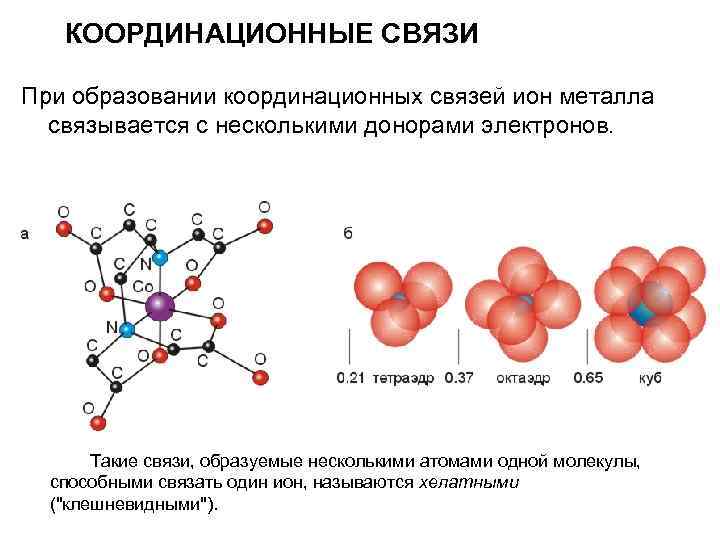
КООРДИНАЦИОННЫЕ СВЯЗИ При образовании координационных связей ион металла связывается с несколькими донорами электронов. Такие связи, образуемые несколькими атомами одной молекулы, способными связать один ион, называются хелатными ("клешневидными").
биофизика 006.ppt