Alkilamini-09.ppt
- Количество слайдов: 10
 АМІНИ АЛІФАТИЧНОГО РЯДУ Аміни можна розглядати як похідні амоніаку, у молекулі якого атоми Гідрогену заміщені на вуглеводневі залишки. Класифікація. 1. Залежно від того, скільки атомів Гідрогену заміщено на вуглеводневі залишки (скільки залишків сполучено з атомом Нітрогену), розрізняють первинні R–NH 2, вторинні – NHRR’ і третинні – NRR’R’’ аміни. Первинні аміни містять аміногрупу –NH 2, вторинні – іміногрупу –NH–, а третинні — третинний атом Нітрогену >N–. Відомі також сполуки з четвертинним атомом Нітрогену >N+<, наприклад: 1. Залежно від будови карбонового ланцюга розрізняють аліфатичні (насичені і ненасичені), аліциклічні, ароматичні (такі, що містять аміногрупу, сполучену з кільцем або у бічному ланцюгу), гетероциклічні аміни, наприклад: 3. Залежно від кількості аміногруп –NH 2 (або ж алкіламіногруп –NHR чи діалкіламіногруп —NR 2) у молекулі розрізняють моноаміни, діаміни тощо. Номенклатура. За рекомендаціями IUPAC (1993 р. ) для назв амінів можливі три підходи: 1) за принципами систематичної номенклатури (заміщення, найменших локантів, алфавітного порядку замісників); 2) за радикально-функціональною номенклатурою; 3) аміни розглядають як заміщені азану (систематична назва амоніаку).
АМІНИ АЛІФАТИЧНОГО РЯДУ Аміни можна розглядати як похідні амоніаку, у молекулі якого атоми Гідрогену заміщені на вуглеводневі залишки. Класифікація. 1. Залежно від того, скільки атомів Гідрогену заміщено на вуглеводневі залишки (скільки залишків сполучено з атомом Нітрогену), розрізняють первинні R–NH 2, вторинні – NHRR’ і третинні – NRR’R’’ аміни. Первинні аміни містять аміногрупу –NH 2, вторинні – іміногрупу –NH–, а третинні — третинний атом Нітрогену >N–. Відомі також сполуки з четвертинним атомом Нітрогену >N+<, наприклад: 1. Залежно від будови карбонового ланцюга розрізняють аліфатичні (насичені і ненасичені), аліциклічні, ароматичні (такі, що містять аміногрупу, сполучену з кільцем або у бічному ланцюгу), гетероциклічні аміни, наприклад: 3. Залежно від кількості аміногруп –NH 2 (або ж алкіламіногруп –NHR чи діалкіламіногруп —NR 2) у молекулі розрізняють моноаміни, діаміни тощо. Номенклатура. За рекомендаціями IUPAC (1993 р. ) для назв амінів можливі три підходи: 1) за принципами систематичної номенклатури (заміщення, найменших локантів, алфавітного порядку замісників); 2) за радикально-функціональною номенклатурою; 3) аміни розглядають як заміщені азану (систематична назва амоніаку).
 За раціональною номенклатурою для утворення назви аліфатичних амінів перераховують вуглеводневі залишки, сполучені з атомом Нітрогену, додаючи в кінці суфікс -амін. Для утворення назв амінів різної будови за систематичною номенклатурою використовують наступну схему: у префікси виносять алкільні замісники в алфавітному порядку; назва родоначальної структури містить корінь, що включає головний ланцюг або основну циклічну структуру та суфікс, який вказує ступінь насиченості (-ан; -ен чи -єн; -ин або -ін, -їн), старша характеристична група (-амін) завершує назву сполуки. Утворення назв первинних амінів розгалуженої будови проводять у такій послідовності: а) визначають старшу характеристичну групу; б) вибирають родоначальну структуру; в) нумерують атоми Карбону головного карбонового ланцюга (нумерацію проводять таким чином, щоб положення аміногрупи було позначено найменшим локантом); г) визначають алкільні замісники та їх локанти (алкільні замісники перелічують в алфавітному порядку з локантами та множинними префіксами (ди- (ді), три-, тетратощо), але при визначенні алфавітного порядку множинні префікси не враховують, а назву останнього замісника пишуть разом з назвою родоначальної структури), наприклад: Назви вторинних амінів несиметричної будови утворюють шляхом додавання префікса Ν-алкіл до назви алканамін, яку визначає головний карбоновий ланцюг, сполучений з ΝН-групою. Назви третинних амінів несиметричної будови утворюють шляхом додавання префікса Ν-алкіл-Ν-алкіл до назви алканамін, яку визначає головний карбоновий ланцюг, сполучений з атомом Нітрогену, наприклад:
За раціональною номенклатурою для утворення назви аліфатичних амінів перераховують вуглеводневі залишки, сполучені з атомом Нітрогену, додаючи в кінці суфікс -амін. Для утворення назв амінів різної будови за систематичною номенклатурою використовують наступну схему: у префікси виносять алкільні замісники в алфавітному порядку; назва родоначальної структури містить корінь, що включає головний ланцюг або основну циклічну структуру та суфікс, який вказує ступінь насиченості (-ан; -ен чи -єн; -ин або -ін, -їн), старша характеристична група (-амін) завершує назву сполуки. Утворення назв первинних амінів розгалуженої будови проводять у такій послідовності: а) визначають старшу характеристичну групу; б) вибирають родоначальну структуру; в) нумерують атоми Карбону головного карбонового ланцюга (нумерацію проводять таким чином, щоб положення аміногрупи було позначено найменшим локантом); г) визначають алкільні замісники та їх локанти (алкільні замісники перелічують в алфавітному порядку з локантами та множинними префіксами (ди- (ді), три-, тетратощо), але при визначенні алфавітного порядку множинні префікси не враховують, а назву останнього замісника пишуть разом з назвою родоначальної структури), наприклад: Назви вторинних амінів несиметричної будови утворюють шляхом додавання префікса Ν-алкіл до назви алканамін, яку визначає головний карбоновий ланцюг, сполучений з ΝН-групою. Назви третинних амінів несиметричної будови утворюють шляхом додавання префікса Ν-алкіл-Ν-алкіл до назви алканамін, яку визначає головний карбоновий ланцюг, сполучений з атомом Нітрогену, наприклад:
 Діаміни за раціональною номенклатурою називають як відповідні двовалентні вуглеводневі залишки, додаючи закінчення –діамін. Діаміни з нерозгалуженим карбоновим ланцюгом здебільшого називають поліметилендіамінами. Для деяких амінів широко вживані і тривіальні назви, наприклад: Ізомерія амінів визначається, по-перше, ізомерією вуглеводневих залишків. По-друге, для амінів можлива метамерія. Для діамінів також розрізняють взаємне розміщення аміногруп. Наприклад, ізомерами бутанаміну є:
Діаміни за раціональною номенклатурою називають як відповідні двовалентні вуглеводневі залишки, додаючи закінчення –діамін. Діаміни з нерозгалуженим карбоновим ланцюгом здебільшого називають поліметилендіамінами. Для деяких амінів широко вживані і тривіальні назви, наприклад: Ізомерія амінів визначається, по-перше, ізомерією вуглеводневих залишків. По-друге, для амінів можлива метамерія. Для діамінів також розрізняють взаємне розміщення аміногруп. Наприклад, ізомерами бутанаміну є:
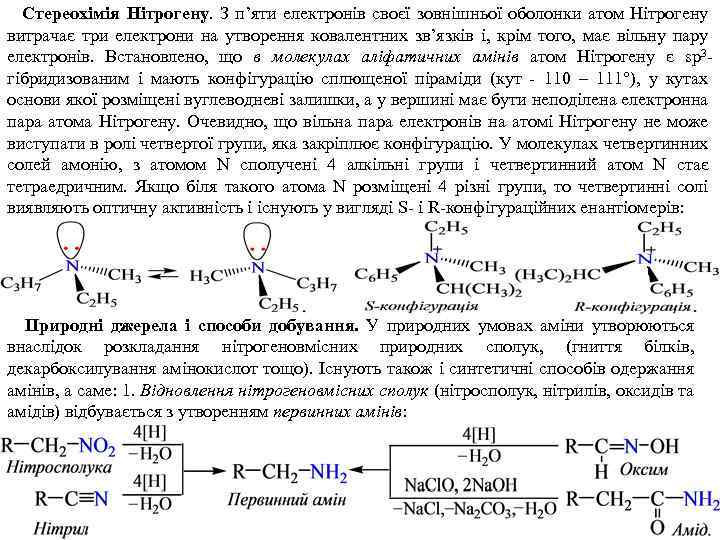 Стереохімія Нітрогену. З п’яти електронів своєї зовнішньої оболонки атом Нітрогену витрачає три електрони на утворення ковалентних зв’язків і, крім того, має вільну пару електронів. Встановлено, що в молекулах аліфатичних амінів атом Нітрогену є sp 3 гібридизованим і мають конфігурацію сплющеної піраміди (кут - 110 – 111°), у кутах основи якої розміщені вуглеводневі залишки, а у вершині має бути неподілена електронна пара атома Нітрогену. Очевидно, що вільна пара електронів на атомі Нітрогену не може виступати в ролі четвертої групи, яка закріплює конфігурацію. У молекулах четвертинних солей амонію, з атомом N сполучені 4 алкільні групи і четвертинний атом N стає тетраедричним. Якщо біля такого атома N розміщені 4 різні групи, то четвертинні солі виявляють оптичну активність і існують у вигляді S- i R-конфігураційних енантіомерів: Природні джерела і способи добування. У природних умовах аміни утворюються внаслідок розкладання нітрогеновмісних природних сполук, (гниття білків, декарбоксилування амінокислот тощо). Існують також і синтетичні способів одержання амінів, а саме: 1. Відновлення нітрогеновмісних сполук (нітросполук, нітрилів, оксидів та амідів) відбувається з утворенням первинних амінів:
Стереохімія Нітрогену. З п’яти електронів своєї зовнішньої оболонки атом Нітрогену витрачає три електрони на утворення ковалентних зв’язків і, крім того, має вільну пару електронів. Встановлено, що в молекулах аліфатичних амінів атом Нітрогену є sp 3 гібридизованим і мають конфігурацію сплющеної піраміди (кут - 110 – 111°), у кутах основи якої розміщені вуглеводневі залишки, а у вершині має бути неподілена електронна пара атома Нітрогену. Очевидно, що вільна пара електронів на атомі Нітрогену не може виступати в ролі четвертої групи, яка закріплює конфігурацію. У молекулах четвертинних солей амонію, з атомом N сполучені 4 алкільні групи і четвертинний атом N стає тетраедричним. Якщо біля такого атома N розміщені 4 різні групи, то четвертинні солі виявляють оптичну активність і існують у вигляді S- i R-конфігураційних енантіомерів: Природні джерела і способи добування. У природних умовах аміни утворюються внаслідок розкладання нітрогеновмісних природних сполук, (гниття білків, декарбоксилування амінокислот тощо). Існують також і синтетичні способів одержання амінів, а саме: 1. Відновлення нітрогеновмісних сполук (нітросполук, нітрилів, оксидів та амідів) відбувається з утворенням первинних амінів:
 2. Ізонітрили при гідролізі утворюють первинні аміни і форміатну кислоту, а при відновленні – вторинні аміни: 3. Алкілування амоніаку галогеналканами (Гофман, 1849 p. ) полягає в тому, що під час нагрівання спиртового розчину амоніаку з галогеналканами атоми H в молекулі амоніаку поступово заміщуються на R (за SN-механізмом з утворенням суміші солей різних (первинних, вторинних і третинних) амінів, або четвертинної амонійної солі: 4. Алкілування амоніаку спиртами застосовується для синтезу лише нижчих алкіламінів (С 1–С 4): Фізичні властивості. Метиламін, диметиламін і три метиламін – гази, інші нижчі аміни – рідини. Нижчі аміни мають амоніачний запах і подібно до амоніаку добре розчиняються у воді. Більш складні аміни – рідини з неприємним запахом зіпсованої риби.
2. Ізонітрили при гідролізі утворюють первинні аміни і форміатну кислоту, а при відновленні – вторинні аміни: 3. Алкілування амоніаку галогеналканами (Гофман, 1849 p. ) полягає в тому, що під час нагрівання спиртового розчину амоніаку з галогеналканами атоми H в молекулі амоніаку поступово заміщуються на R (за SN-механізмом з утворенням суміші солей різних (первинних, вторинних і третинних) амінів, або четвертинної амонійної солі: 4. Алкілування амоніаку спиртами застосовується для синтезу лише нижчих алкіламінів (С 1–С 4): Фізичні властивості. Метиламін, диметиламін і три метиламін – гази, інші нижчі аміни – рідини. Нижчі аміни мають амоніачний запах і подібно до амоніаку добре розчиняються у воді. Більш складні аміни – рідини з неприємним запахом зіпсованої риби.
 Хімічні властивості. Властивості амінів визначаються в першу чергу наявністю в їх молекулах аміногрупи. Кислотно-основні властивості амінів. Атом N аміногрупи має вільну пару електронів. Тому аміни, подібно до амоніаку, виявляють основні властивості і вступають у різні реакції як нуклеофільні реагенти. Так, у водних розчинах аміни приєднують протон води і утворюють гідроксиди амонійних сполук: R–NH 2 + HOH → [R–NH 3]+ + OH–. Аміни виявляють основні властивості в реакціях з мінеральними кислотами, утворюючи алкілзаміщені амонійні солі, наприклад: R–NH 2 + HCl → [R–NH 3]+Cl–. У молекулах первинних і вторинних аліфатичних амінів унаслідок зміщення електронної густини зв'язку N–H до атома Нітрогену атом Гідрогену частково протонізується і може виявляти слабкі кислотні властивості. Вони полягають у тому, що первинні і вторинні аміни взаємодіють зі сполуками лужного характеру (лужними металами, металорганічними сполуками), утворюючи солеподібні сполуки – алкіл- і діалкіламіди: 2 R–NH 2 + 2 Na → R–NH–Na +H 2. 2 R 2 NH + 2 Na → R 2 N–Na +H 2. Алкіл- і діалкіламіди легко гідролізуються водою: R–NH–Na + HOH→ R–NH 2 + Na. OH. R 2 N–Na + HOH → R 2 NH + Na. OH. Алкілування амінів. Аміни легко вступають у реакцію з галогеналканами, в результаті якої відбувається поступове заміщення атомів водню біля амінного Нітрогену на алкільні радикали. Такого типу взаємодію було названо реакціями алкілування. Алкілуванням можна з первинних амінів добути вторинні, а з вторинних – третинні аміни (див. реакція Гофмана).
Хімічні властивості. Властивості амінів визначаються в першу чергу наявністю в їх молекулах аміногрупи. Кислотно-основні властивості амінів. Атом N аміногрупи має вільну пару електронів. Тому аміни, подібно до амоніаку, виявляють основні властивості і вступають у різні реакції як нуклеофільні реагенти. Так, у водних розчинах аміни приєднують протон води і утворюють гідроксиди амонійних сполук: R–NH 2 + HOH → [R–NH 3]+ + OH–. Аміни виявляють основні властивості в реакціях з мінеральними кислотами, утворюючи алкілзаміщені амонійні солі, наприклад: R–NH 2 + HCl → [R–NH 3]+Cl–. У молекулах первинних і вторинних аліфатичних амінів унаслідок зміщення електронної густини зв'язку N–H до атома Нітрогену атом Гідрогену частково протонізується і може виявляти слабкі кислотні властивості. Вони полягають у тому, що первинні і вторинні аміни взаємодіють зі сполуками лужного характеру (лужними металами, металорганічними сполуками), утворюючи солеподібні сполуки – алкіл- і діалкіламіди: 2 R–NH 2 + 2 Na → R–NH–Na +H 2. 2 R 2 NH + 2 Na → R 2 N–Na +H 2. Алкіл- і діалкіламіди легко гідролізуються водою: R–NH–Na + HOH→ R–NH 2 + Na. OH. R 2 N–Na + HOH → R 2 NH + Na. OH. Алкілування амінів. Аміни легко вступають у реакцію з галогеналканами, в результаті якої відбувається поступове заміщення атомів водню біля амінного Нітрогену на алкільні радикали. Такого типу взаємодію було названо реакціями алкілування. Алкілуванням можна з первинних амінів добути вторинні, а з вторинних – третинні аміни (див. реакція Гофмана).
 Ацилування амінів. Взаємодія первинних і вторинних амінів з органічними кислотами, їх ангідридами, галогенангідридами та естерами є реакцією ацилування. При цьому атом Гідрогену аміногрупи заміщується на ацильний залишок органічної кислоти: Взаємодія з нітритною кислотою є характерною реакцією на аміни, що дає змогу розрізнити первинні, вторинні і третинні аміни. Вважають, що діючим реагентом у реакції амінів з нітритною кислотою є нітроген(ІІІ) оксид N 2 O 3, який утворюється з нітритної кислоти: 2 HO–N=O ↔ O=N–O–N=O + H 2 O. А. Первинні аміни аліфатичного ряду на холоді утворюють нетривкі похідні алкілдіазонію, що розщеплюються з виділенням нітрогену діазогрупи, наприклад: Етиламін в умовах цієї реакції утворює етанол (60%), пропіламін – пропіловий спирт (7%) (ізопропіловий – 32%), а також пропілен та інші продукти. Б. Вторинні аміни з нітритною кислотою утворюють N-нітрозаміни, наприклад з дипропіламіну – N–нітрозодипропіламін: (C 3 H 7)2 NH + HO–N=O ↔ (C 3 H 7)2 N –N=O + HOH. N-Нітрозопохідні вторинних аліфатичних амінів при нагріванні з розбавленою хлоридною кислотою гідролізуються з утворенням вторинного аміну і нітритної кислоти. З третинними амінами на холоді нітритна кислота не реагує.
Ацилування амінів. Взаємодія первинних і вторинних амінів з органічними кислотами, їх ангідридами, галогенангідридами та естерами є реакцією ацилування. При цьому атом Гідрогену аміногрупи заміщується на ацильний залишок органічної кислоти: Взаємодія з нітритною кислотою є характерною реакцією на аміни, що дає змогу розрізнити первинні, вторинні і третинні аміни. Вважають, що діючим реагентом у реакції амінів з нітритною кислотою є нітроген(ІІІ) оксид N 2 O 3, який утворюється з нітритної кислоти: 2 HO–N=O ↔ O=N–O–N=O + H 2 O. А. Первинні аміни аліфатичного ряду на холоді утворюють нетривкі похідні алкілдіазонію, що розщеплюються з виділенням нітрогену діазогрупи, наприклад: Етиламін в умовах цієї реакції утворює етанол (60%), пропіламін – пропіловий спирт (7%) (ізопропіловий – 32%), а також пропілен та інші продукти. Б. Вторинні аміни з нітритною кислотою утворюють N-нітрозаміни, наприклад з дипропіламіну – N–нітрозодипропіламін: (C 3 H 7)2 NH + HO–N=O ↔ (C 3 H 7)2 N –N=O + HOH. N-Нітрозопохідні вторинних аліфатичних амінів при нагріванні з розбавленою хлоридною кислотою гідролізуються з утворенням вторинного аміну і нітритної кислоти. З третинними амінами на холоді нітритна кислота не реагує.
 Діаміни. Сполуки, в молекулах яких є дві аміногрупи, називають діамінами. Стійкими є тільки такі діаміни, в молекулах яких аміногрупи розміщені біля різних вуглецевих атомів. Тому метилендіамін у вільному стані не існує. Найпростішим з первинних діамінів є етилендіамін, або етан-1, 2 -діамін – NH 2–CH 2–NH 2. Його гомологами є триметилендіамін (пропан-1, 3 -діамін) – NH 2–(СН 2)3–NH 2; тетраметилендіамін (бутан-1, 4 діамін) – NH 2–(CH 2)4–NH 2; пентаметилендіамін (пентан-1, 5 -діамін) – NH 2–(CH 2)5–NH 2; гексаметилендіамін (гексан-1, 6 -діамін) – NH 2–(CH 2)6–NH 2 та ін. Бутан-1, 4 -діамін, або путресцин (від лат. putrescere – той, що гниє), і пентан-1, 5 -діамін, або кадаверин (від лат. cadaverosus – трупний), відомі під назвою „трупні отрути”, які утворюються при гнитті білків (трупів тварин), зокрема при декарбоксилуванні амінокислоти орнітину. Вони належать до птомаїнів – органічних основ, що утворюються під час гниття тваринних продуктів. Кадаверин у невеликих кількостях знайдений у мухоморах, пивних дріжджах, а також у сечі і екскрементах людей, хворих на холеру і цистинурію. Нижчі діаміни розчинні у воді і є більш сильними основами, ніж моноаміни. Діаміни утворюють солі з двома еквівалентами кислот, можуть алкілуватися і ацилуватися за участі як однієї, так і обох аміногруп. Окремі представники. Моноаміни аліфатичного ряду використовуються в синтезі фармацевтичних препаратів і барвників. Етиламін також має застосування як компонент ракетного палива. Ди- і триметиламін мають запах оселедців. Цікаво, що в концентрованому стані запах триметиламіну нагадує запах амоніаку і не є неприємним, а в розбавленому стані стає надзвичайно неприємним і дуже довго утримується шкірою і волоссям. Солі вищих амінів з мінеральними кислотами дістали назву „катіонних” (кислих) мил. На відміну від звичайних мил – натрієвих або калієвих солей карбонових кислот (аніонних мил), – ці синтетичні мийні засоби нечутливі до твердої води.
Діаміни. Сполуки, в молекулах яких є дві аміногрупи, називають діамінами. Стійкими є тільки такі діаміни, в молекулах яких аміногрупи розміщені біля різних вуглецевих атомів. Тому метилендіамін у вільному стані не існує. Найпростішим з первинних діамінів є етилендіамін, або етан-1, 2 -діамін – NH 2–CH 2–NH 2. Його гомологами є триметилендіамін (пропан-1, 3 -діамін) – NH 2–(СН 2)3–NH 2; тетраметилендіамін (бутан-1, 4 діамін) – NH 2–(CH 2)4–NH 2; пентаметилендіамін (пентан-1, 5 -діамін) – NH 2–(CH 2)5–NH 2; гексаметилендіамін (гексан-1, 6 -діамін) – NH 2–(CH 2)6–NH 2 та ін. Бутан-1, 4 -діамін, або путресцин (від лат. putrescere – той, що гниє), і пентан-1, 5 -діамін, або кадаверин (від лат. cadaverosus – трупний), відомі під назвою „трупні отрути”, які утворюються при гнитті білків (трупів тварин), зокрема при декарбоксилуванні амінокислоти орнітину. Вони належать до птомаїнів – органічних основ, що утворюються під час гниття тваринних продуктів. Кадаверин у невеликих кількостях знайдений у мухоморах, пивних дріжджах, а також у сечі і екскрементах людей, хворих на холеру і цистинурію. Нижчі діаміни розчинні у воді і є більш сильними основами, ніж моноаміни. Діаміни утворюють солі з двома еквівалентами кислот, можуть алкілуватися і ацилуватися за участі як однієї, так і обох аміногруп. Окремі представники. Моноаміни аліфатичного ряду використовуються в синтезі фармацевтичних препаратів і барвників. Етиламін також має застосування як компонент ракетного палива. Ди- і триметиламін мають запах оселедців. Цікаво, що в концентрованому стані запах триметиламіну нагадує запах амоніаку і не є неприємним, а в розбавленому стані стає надзвичайно неприємним і дуже довго утримується шкірою і волоссям. Солі вищих амінів з мінеральними кислотами дістали назву „катіонних” (кислих) мил. На відміну від звичайних мил – натрієвих або калієвих солей карбонових кислот (аніонних мил), – ці синтетичні мийні засоби нечутливі до твердої води.
 Солі третинних амінів або четвертинні амонієві солі, які містять залишки з великою кількістю атомів Карбону, мають сильну бактерицидну і бактеріостатичну дії. Гексаметилендіамін (гексан-1, 6 -діамін) має найбільше практичне значення серед діамінів. Його синтезують з адипінової кислоти за наступною схемою: Гексаметилендіамін використовується у виробництві поліамідних синтетичних волокон, наприклад найлону, що синтезується поліконденсацією зазначеного діаміну з адипіновою кислотою: Натрій (або кальцій) цикламат в деяких країнах застосовується як штучна підсолоджуюча речовина, але в організмі він може легко перетворитись на канцерогенний циклогексиламін: Ідентифікація амінів. Найширше для ідентифікації амінів використовуються ІЧспектри. Валентним коливанням вільної NH 2 -гpyпи відповідає вузька смуга при 3500 см– 1. У первинних і вторинних амінів спостерігається широка смуга в області 3300– 3500 см– 1 і в області 1100– 1300 см– 1 (νС–N). У спектрах ариламінів - смуги в області 650– 900 см– 1 (δNH 2). Солі амінів характеризуються широкою смугою ν(NH) і δ(NH 2) ~ 1600– 1500 см– 1. Віднесення ЯМР-спектрів можливі для протонів біля α-карбонового атома, тобто –СН–N –(7– 8 м. ч. ) для ароматичних амінів. Циклічні вторинні аміни мають смуги, зумовлені протонами –СН 2– груп (7, 2– 7, 5 м. ч. ), а третинні циклічні аміни >N– при 7, 6— 8, 1 м. ч.
Солі третинних амінів або четвертинні амонієві солі, які містять залишки з великою кількістю атомів Карбону, мають сильну бактерицидну і бактеріостатичну дії. Гексаметилендіамін (гексан-1, 6 -діамін) має найбільше практичне значення серед діамінів. Його синтезують з адипінової кислоти за наступною схемою: Гексаметилендіамін використовується у виробництві поліамідних синтетичних волокон, наприклад найлону, що синтезується поліконденсацією зазначеного діаміну з адипіновою кислотою: Натрій (або кальцій) цикламат в деяких країнах застосовується як штучна підсолоджуюча речовина, але в організмі він може легко перетворитись на канцерогенний циклогексиламін: Ідентифікація амінів. Найширше для ідентифікації амінів використовуються ІЧспектри. Валентним коливанням вільної NH 2 -гpyпи відповідає вузька смуга при 3500 см– 1. У первинних і вторинних амінів спостерігається широка смуга в області 3300– 3500 см– 1 і в області 1100– 1300 см– 1 (νС–N). У спектрах ариламінів - смуги в області 650– 900 см– 1 (δNH 2). Солі амінів характеризуються широкою смугою ν(NH) і δ(NH 2) ~ 1600– 1500 см– 1. Віднесення ЯМР-спектрів можливі для протонів біля α-карбонового атома, тобто –СН–N –(7– 8 м. ч. ) для ароматичних амінів. Циклічні вторинні аміни мають смуги, зумовлені протонами –СН 2– груп (7, 2– 7, 5 м. ч. ), а третинні циклічні аміни >N– при 7, 6— 8, 1 м. ч.
 Аміноспирти – біфункціональні сполуки, молекули яких містять одночасно як спиртову, так і аміногрупу. Існують також четвертинні амонійні солі цих спиртів. Спиртова група в молекулах аміноспиртів може бути первинною, вторинною і третинною. Гомологічний ряд первинних аміноспиртів починається з аміноетилового спирту H 2 N– CH 2–OH, який називають β-етаноламіном, або коламіном. За систематичною номенклатурою назви аміноспиртів утворюють з назв відповідних спиртів, додаючи слово аміно- і зазначаючи номер атома Карбону, біля якого розміщена ця група, наприклад 2 амінопропан-1 -ол: СH 3–CH(NH 2)–CH 2–OH. α-Аміноспирти добувають приєднанням амоніаку до α-оксидів, наприклад: Важливу біологічну активність виявляє гідроксид триметил-β-гідроксіетиламонію – холін, який є складовою частиною жироподібних речовин – фосфатидів. Холін можна синтезувати взаємодією гідроксиду триетиламонію з оксидом етилену. Він знижує тиск крові в організмі. При ацетилуванні холін перетворюється на ацетилхолін: Ацетилхолін відіграє важливу роль у діяльності центральної нервової системи, оскільки бере участь у передачі нервового збудження. Він синтезується в закінченнях нервових клітин з холіну і ацетатної кислоти під впливом ферменту холінестерази. Проникнення холіну в місце контакту нервового волокна і інервуючої клітини приводить до її збудження (гальмування). За допомогою холінестерази він гідролізується на холін і ацетатну кислоту.
Аміноспирти – біфункціональні сполуки, молекули яких містять одночасно як спиртову, так і аміногрупу. Існують також четвертинні амонійні солі цих спиртів. Спиртова група в молекулах аміноспиртів може бути первинною, вторинною і третинною. Гомологічний ряд первинних аміноспиртів починається з аміноетилового спирту H 2 N– CH 2–OH, який називають β-етаноламіном, або коламіном. За систематичною номенклатурою назви аміноспиртів утворюють з назв відповідних спиртів, додаючи слово аміно- і зазначаючи номер атома Карбону, біля якого розміщена ця група, наприклад 2 амінопропан-1 -ол: СH 3–CH(NH 2)–CH 2–OH. α-Аміноспирти добувають приєднанням амоніаку до α-оксидів, наприклад: Важливу біологічну активність виявляє гідроксид триметил-β-гідроксіетиламонію – холін, який є складовою частиною жироподібних речовин – фосфатидів. Холін можна синтезувати взаємодією гідроксиду триетиламонію з оксидом етилену. Він знижує тиск крові в організмі. При ацетилуванні холін перетворюється на ацетилхолін: Ацетилхолін відіграє важливу роль у діяльності центральної нервової системи, оскільки бере участь у передачі нервового збудження. Він синтезується в закінченнях нервових клітин з холіну і ацетатної кислоти під впливом ферменту холінестерази. Проникнення холіну в місце контакту нервового волокна і інервуючої клітини приводить до її збудження (гальмування). За допомогою холінестерази він гідролізується на холін і ацетатну кислоту.


