Лекция 3. Белки - 2011.ppt
- Количество слайдов: 34
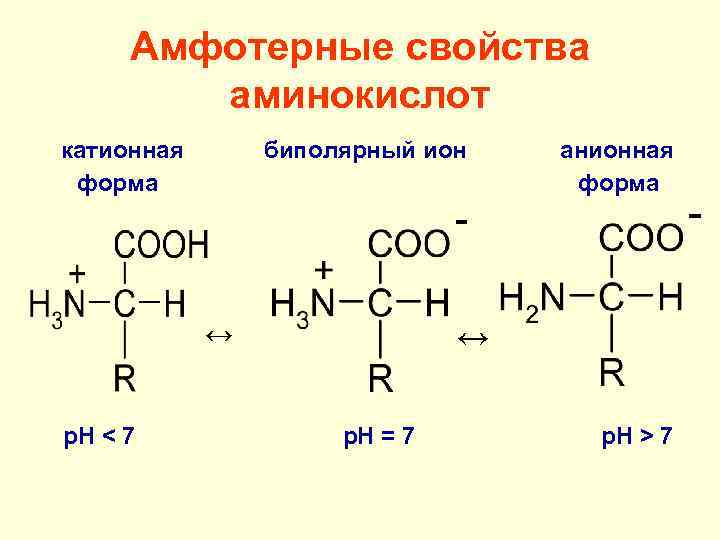
Амфотерные свойства аминокислот катионная форма биполярный ион ↔ p. H < 7 анионная форма ↔ p. H = 7 p. H > 7

Изоэлектрическая точка (p. I) значение р. Н среды, при котором заряд аминокислоты (пептида, белка) равен нулю. для нейтральных аминокислот p. I ≈ 7, для кислых (глу, асп) < 7, для основных (лиз, арг, гис) > 7. Задание: определить величину заряда лизина при различных значениях р. Н среды
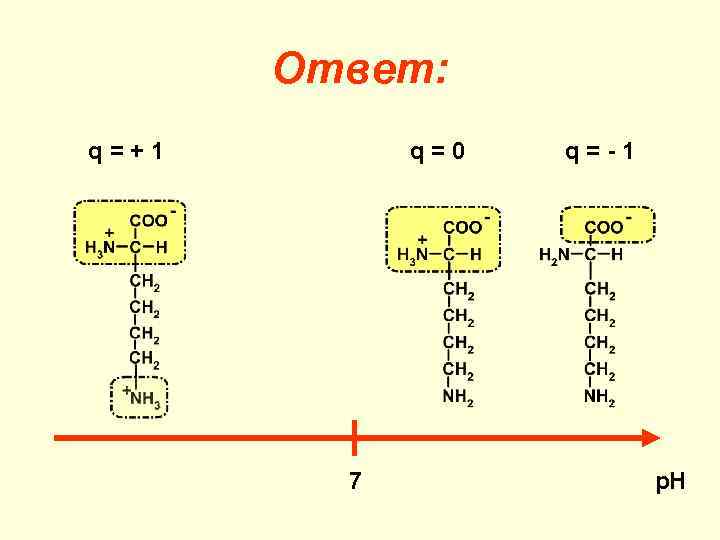
Ответ: q=+1 q=0 7 q=-1 р. Н

ФГАОУ ВПО «Уральский федеральный университет имени первого Президента России Б. Н. Ельцина» БИОХИМИЯ Лекция 3 СТРОЕНИЕ И ФУНКЦИИ БЕЛКОВ лектор - к. м. н. , доцент Емельянов В. В.
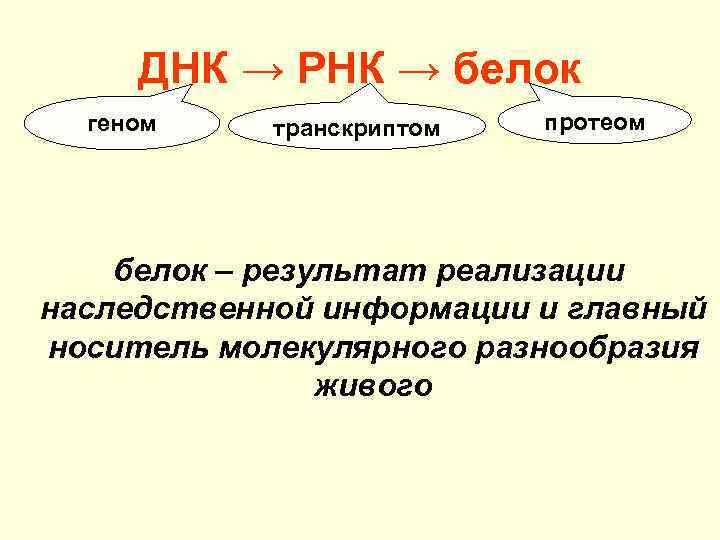
ДНК → РНК → белок геном транскриптом протеом белок – результат реализации наследственной информации и главный носитель молекулярного разнообразия живого
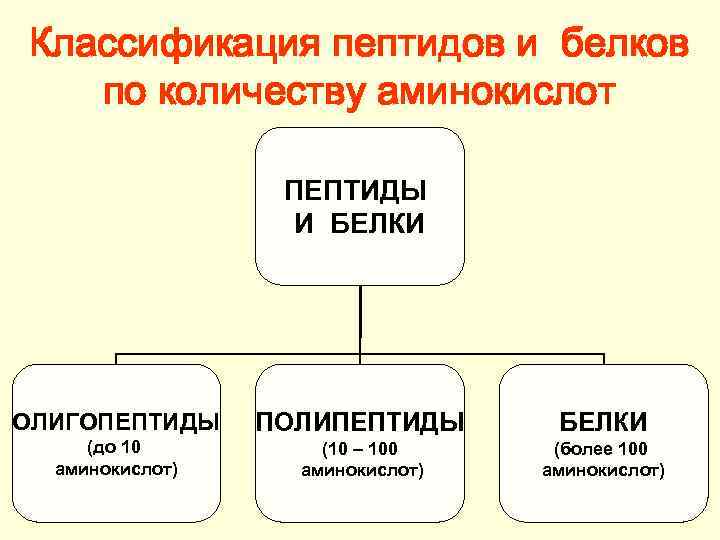
Классификация пептидов и белков по количеству аминокислот ПЕПТИДЫ И БЕЛКИ ОЛИГОПЕПТИДЫ ПОЛИПЕПТИДЫ БЕЛКИ (до 10 аминокислот) (10 – 100 аминокислот) (более 100 аминокислот)

Классификация белков по строению 1. Простые 2. Сложные: а) хромопротеины б) гликопротеины в) липопротеины г) нуклеопротеины д) металлопротеины е) фосфопротеины
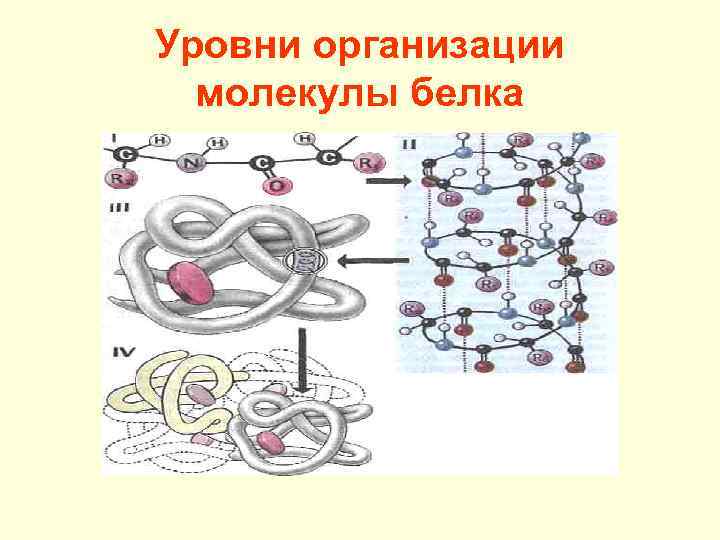
Уровни организации молекулы белка
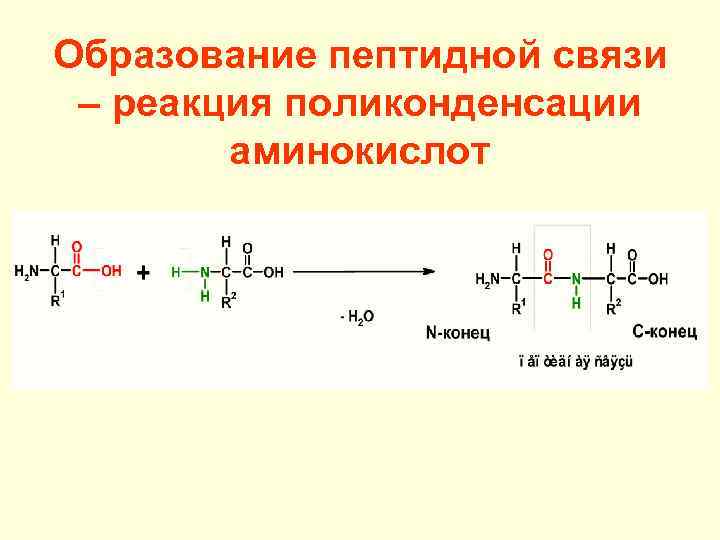
Образование пептидной связи – реакция поликонденсации аминокислот

Свойства пептидной группы 1. Прочная ковалентная связь, приобретающая частично двойной характер. 2. Все атомы группы лежат в одной плоскости. 3. Атомы О и Н находятся в трансконфигурации и вращение вокруг связи С-N невозможно.
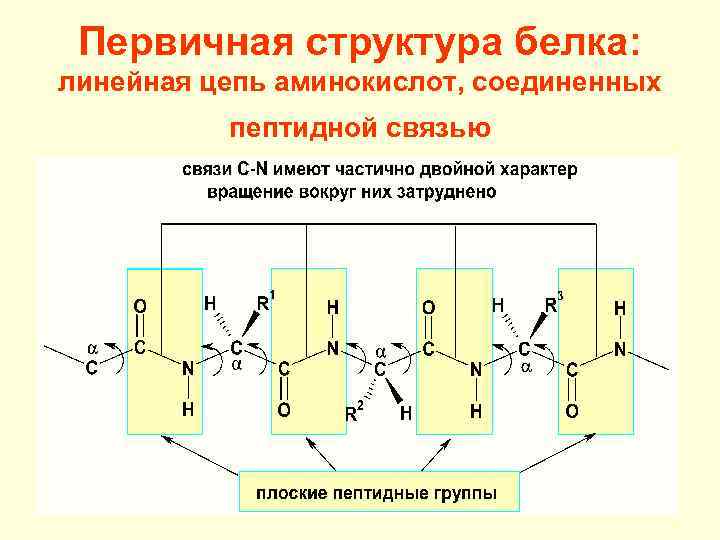
Первичная структура белка: линейная цепь аминокислот, соединенных пептидной связью
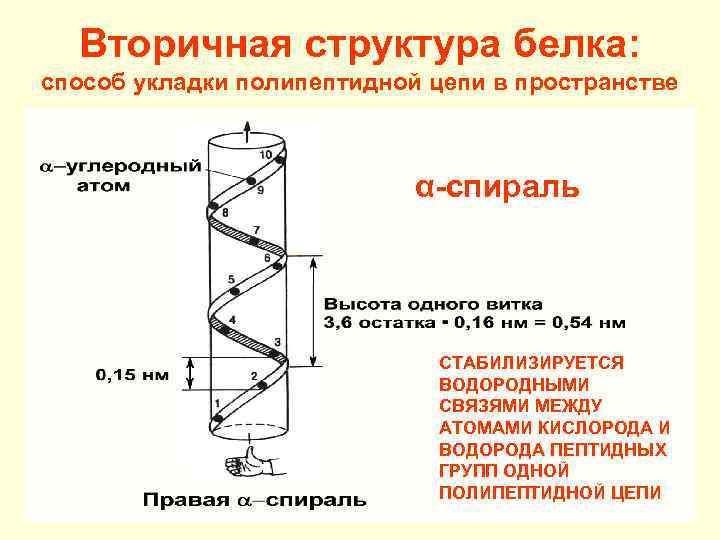
Вторичная структура белка: способ укладки полипептидной цепи в пространстве α-спираль СТАБИЛИЗИРУЕТСЯ ВОДОРОДНЫМИ СВЯЗЯМИ МЕЖДУ АТОМАМИ КИСЛОРОДА И ВОДОРОДА ПЕПТИДНЫХ ГРУПП ОДНОЙ ПОЛИПЕПТИДНОЙ ЦЕПИ
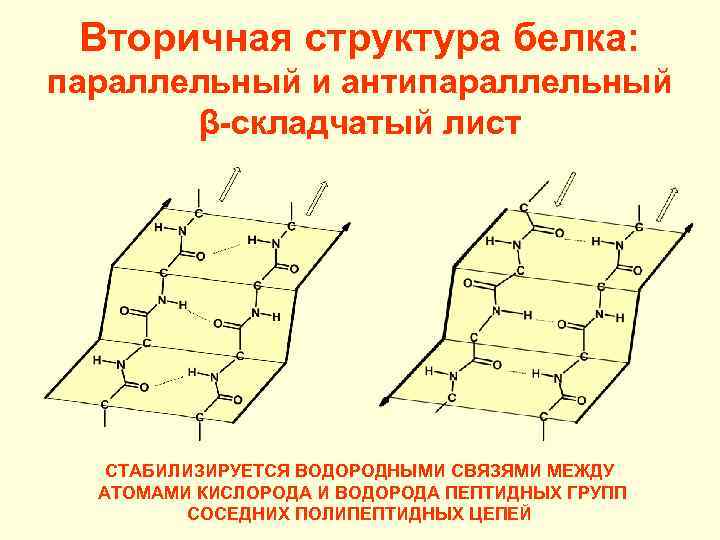
Вторичная структура белка: параллельный и антипараллельный β-складчатый лист СТАБИЛИЗИРУЕТСЯ ВОДОРОДНЫМИ СВЯЗЯМИ МЕЖДУ АТОМАМИ КИСЛОРОДА И ВОДОРОДА ПЕПТИДНЫХ ГРУПП СОСЕДНИХ ПОЛИПЕПТИДНЫХ ЦЕПЕЙ
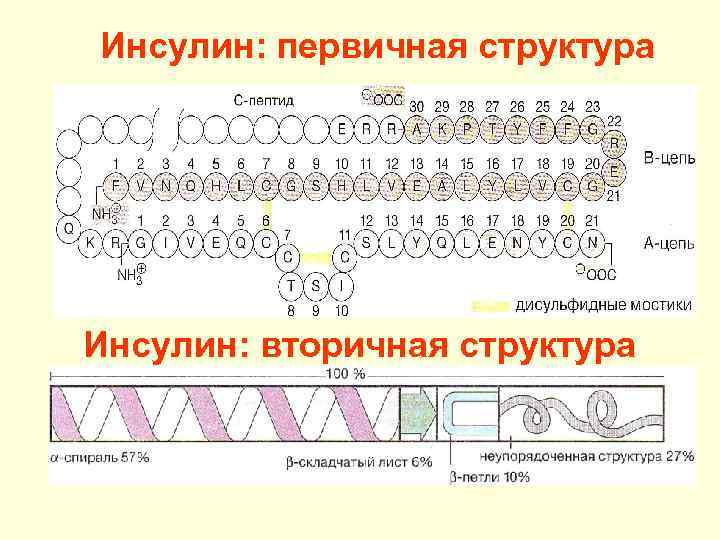
Инсулин: первичная структура Инсулин: вторичная структура
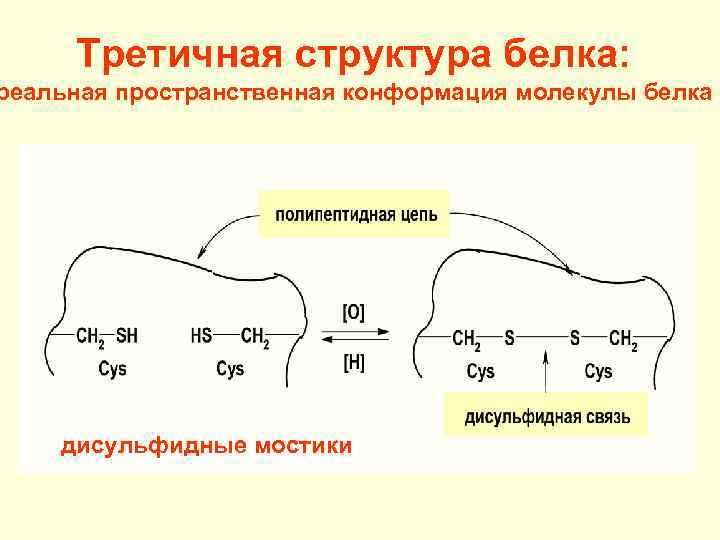
Третичная структура белка: реальная пространственная конформация молекулы белка дисульфидные мостики
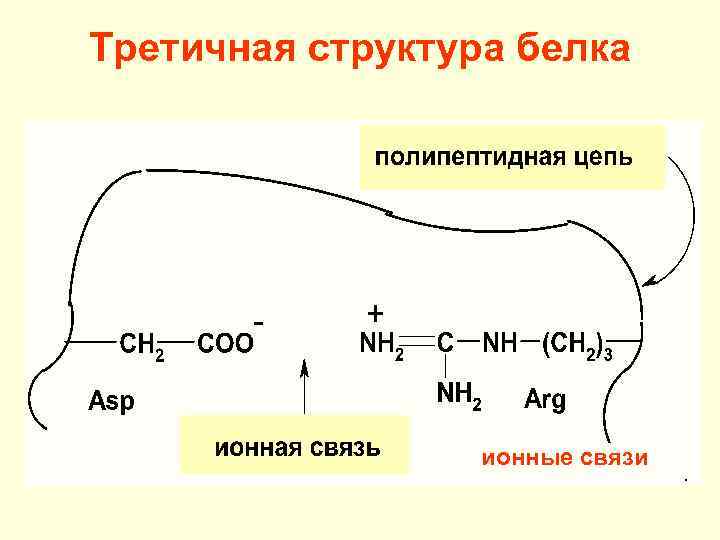
Третичная структура белка ионные связи
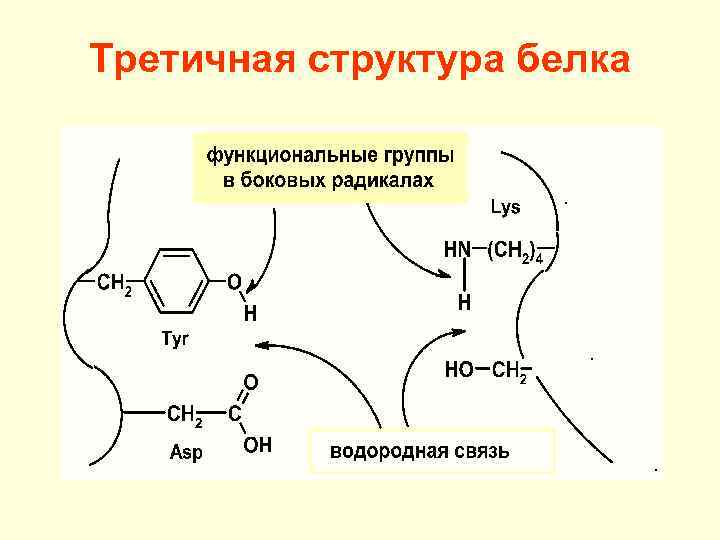
Третичная структура белка
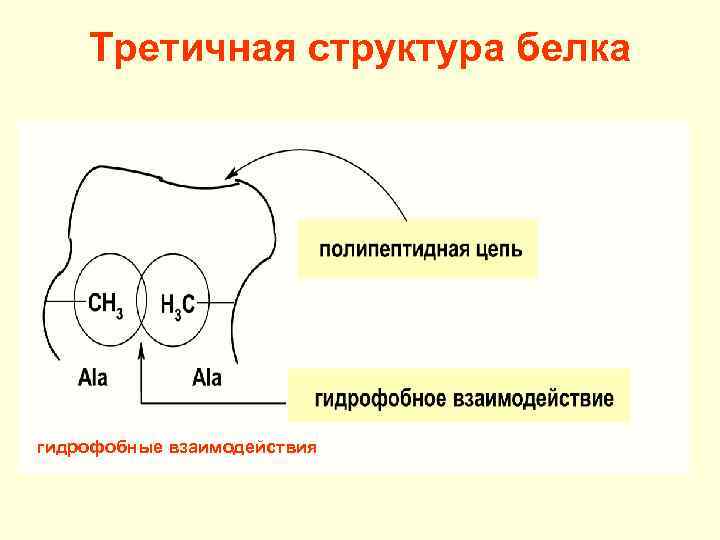
Третичная структура белка гидрофобные взаимодействия
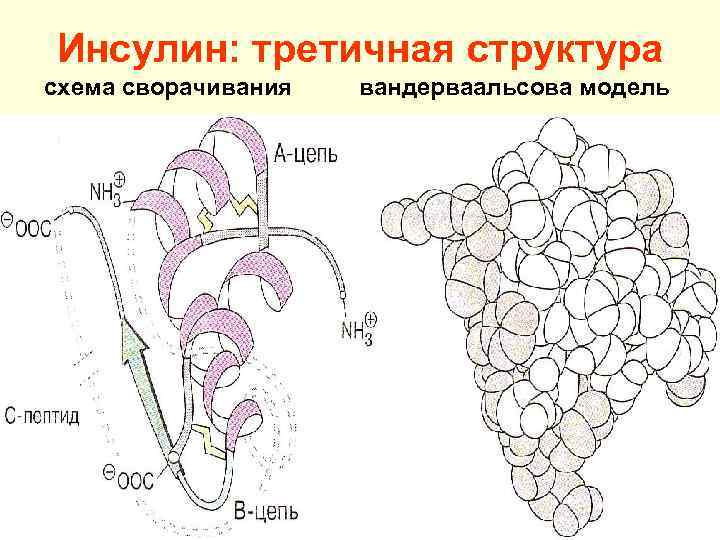
Инсулин: третичная структура схема сворачивания вандерваальсова модель

Глобулярные и фибриллярные белки Параметр Глобулярные Фибриллярные Форма молекулы Сферическая Вытянутая Растворимость в воде Чаще растворимы Чаще нерастворимы α-спираль β–складчатый лист Преобладает вторичная структура
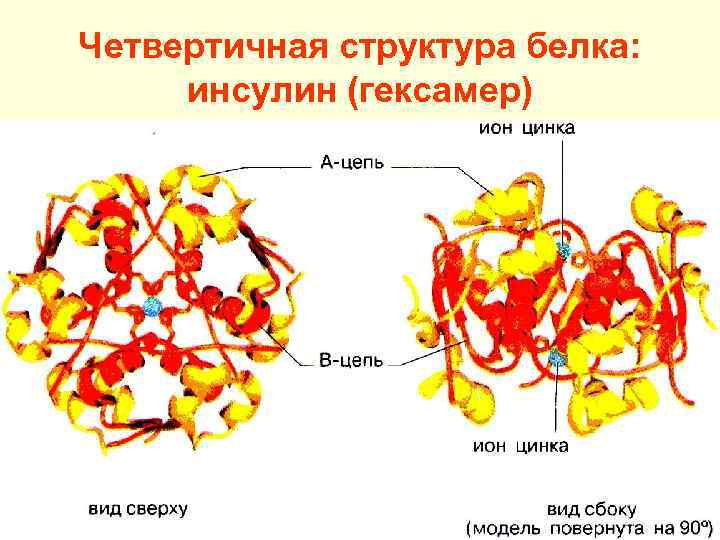
Четвертичная структура белка: инсулин (гексамер)

Особенности белков четвертичной структуры 1. Имеют олигомерное строение (состоят из субъединиц - протомеров). 2. Являются сложными белками (содержат небелковый компонент – простетическую группу). 3. Характерны кооперативные взаимодействия (изменение структуры и функции одного протомера вызывает то же в остальных протомерах).

Физико-химические свойства белков 1. Способность к денатурации – разрушению высших структур белковой молекулы. 2. Способность к растворению в воде. 3. Молекула белка имеет заряд и движется в электрическом поле. 4. Растворы белков способны к образованию гелей.
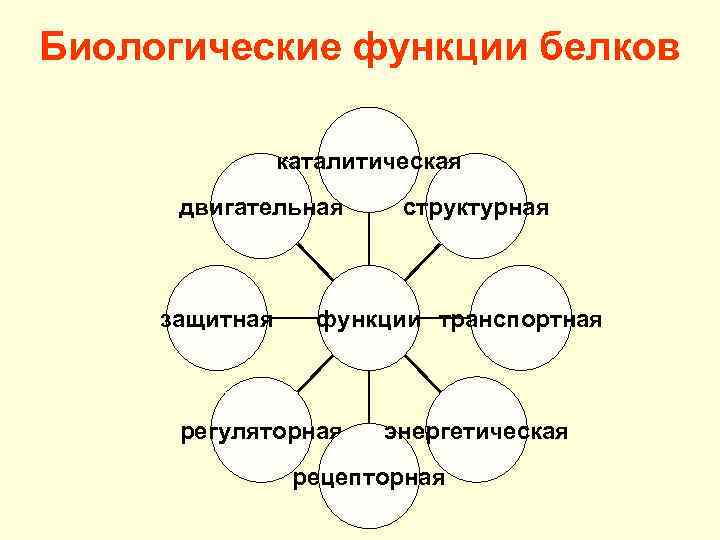
Биологические функции белков каталитическая двигательная защитная структурная функции транспортная регуляторная энергетическая рецепторная
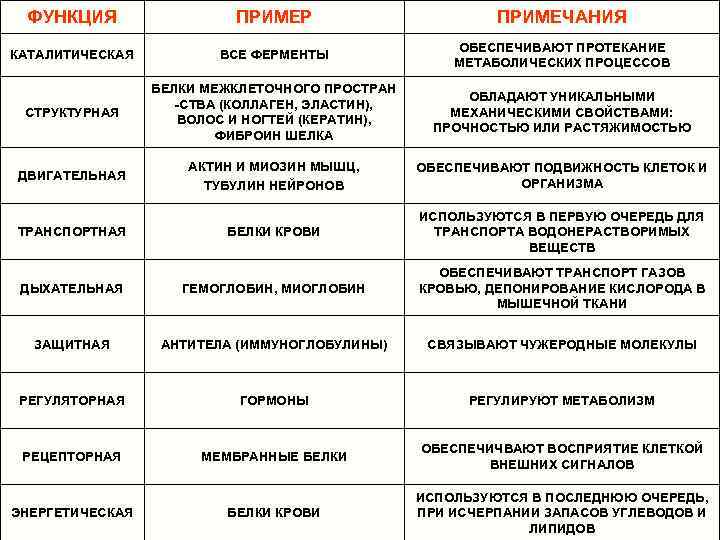
ФУНКЦИЯ ПРИМЕР ПРИМЕЧАНИЯ КАТАЛИТИЧЕСКАЯ ВСЕ ФЕРМЕНТЫ ОБЕСПЕЧИВАЮТ ПРОТЕКАНИЕ МЕТАБОЛИЧЕСКИХ ПРОЦЕССОВ СТРУКТУРНАЯ БЕЛКИ МЕЖКЛЕТОЧНОГО ПРОСТРАН -СТВА (КОЛЛАГЕН, ЭЛАСТИН), ВОЛОС И НОГТЕЙ (КЕРАТИН), ФИБРОИН ШЕЛКА ОБЛАДАЮТ УНИКАЛЬНЫМИ МЕХАНИЧЕСКИМИ СВОЙСТВАМИ: ПРОЧНОСТЬЮ ИЛИ РАСТЯЖИМОСТЬЮ ДВИГАТЕЛЬНАЯ АКТИН И МИОЗИН МЫШЦ, ТУБУЛИН НЕЙРОНОВ ОБЕСПЕЧИВАЮТ ПОДВИЖНОСТЬ КЛЕТОК И ОРГАНИЗМА БЕЛКИ КРОВИ ИСПОЛЬЗУЮТСЯ В ПЕРВУЮ ОЧЕРЕДЬ ДЛЯ ТРАНСПОРТА ВОДОНЕРАСТВОРИМЫХ ВЕЩЕСТВ ДЫХАТЕЛЬНАЯ ГЕМОГЛОБИН, МИОГЛОБИН ОБЕСПЕЧИВАЮТ ТРАНСПОРТ ГАЗОВ КРОВЬЮ, ДЕПОНИРОВАНИЕ КИСЛОРОДА В МЫШЕЧНОЙ ТКАНИ ЗАЩИТНАЯ АНТИТЕЛА (ИММУНОГЛОБУЛИНЫ) СВЯЗЫВАЮТ ЧУЖЕРОДНЫЕ МОЛЕКУЛЫ РЕГУЛЯТОРНАЯ ГОРМОНЫ РЕГУЛИРУЮТ МЕТАБОЛИЗМ РЕЦЕПТОРНАЯ МЕМБРАННЫЕ БЕЛКИ ОБЕСПЕЧИЧВАЮТ ВОСПРИЯТИЕ КЛЕТКОЙ ВНЕШНИХ СИГНАЛОВ БЕЛКИ КРОВИ ИСПОЛЬЗУЮТСЯ В ПОСЛЕДНЮЮ ОЧЕРЕДЬ, ПРИ ИСЧЕРПАНИИ ЗАПАСОВ УГЛЕВОДОВ И ЛИПИДОВ ТРАНСПОРТНАЯ ЭНЕРГЕТИЧЕСКАЯ
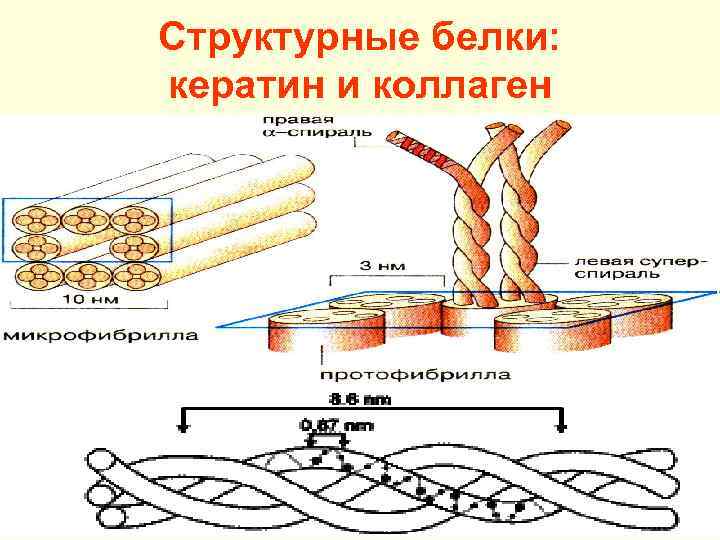
Структурные белки: кератин и коллаген
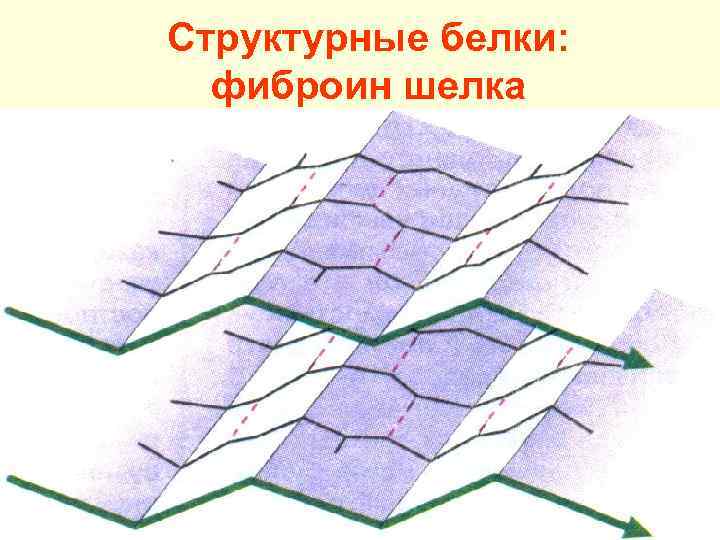
Структурные белки: фиброин шелка
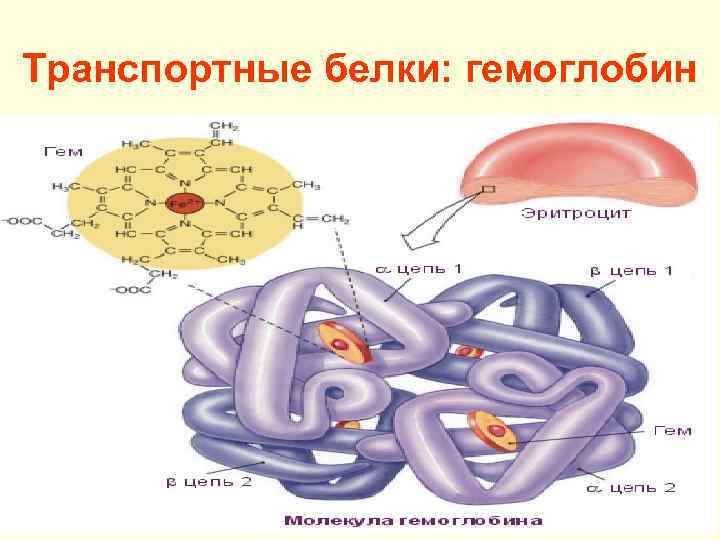
Транспортные белки: гемоглобин
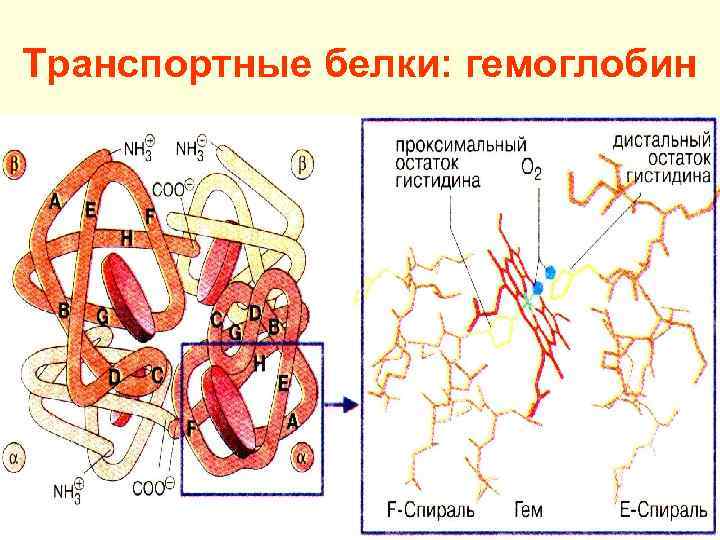
Транспортные белки: гемоглобин
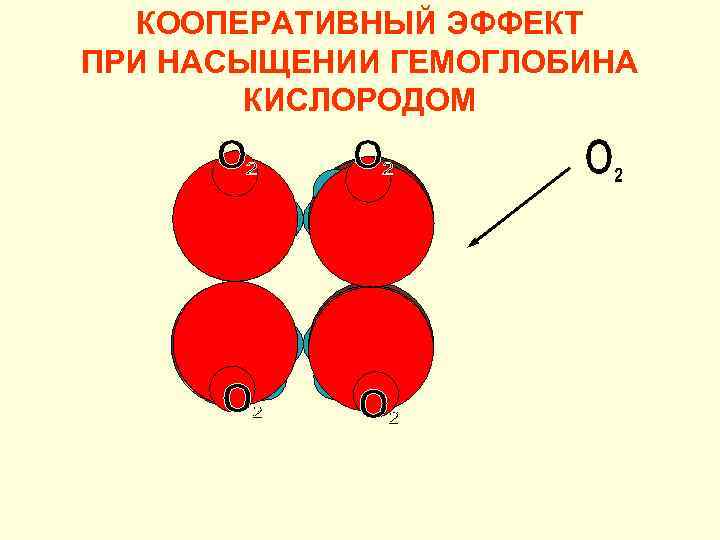
КООПЕРАТИВНЫЙ ЭФФЕКТ ПРИ НАСЫЩЕНИИ ГЕМОГЛОБИНА КИСЛОРОДОМ
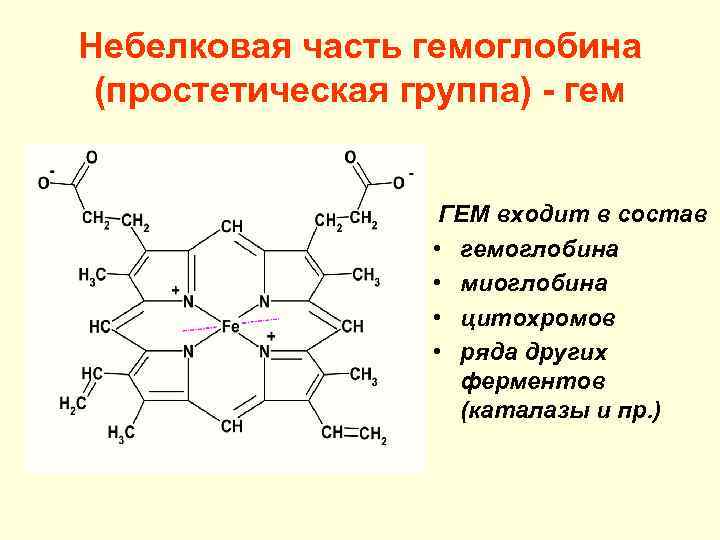
Небелковая часть гемоглобина (простетическая группа) - гем ГЕМ входит в состав • гемоглобина • миоглобина • цитохромов • ряда других ферментов (каталазы и пр. )
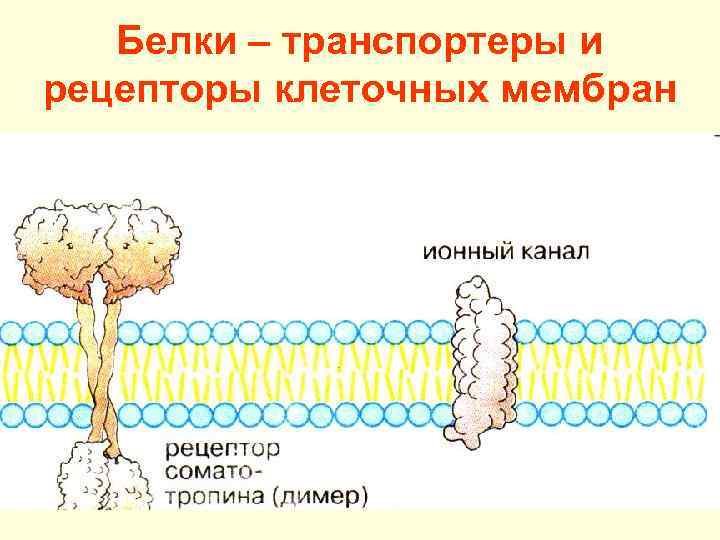
Белки – транспортеры и рецепторы клеточных мембран
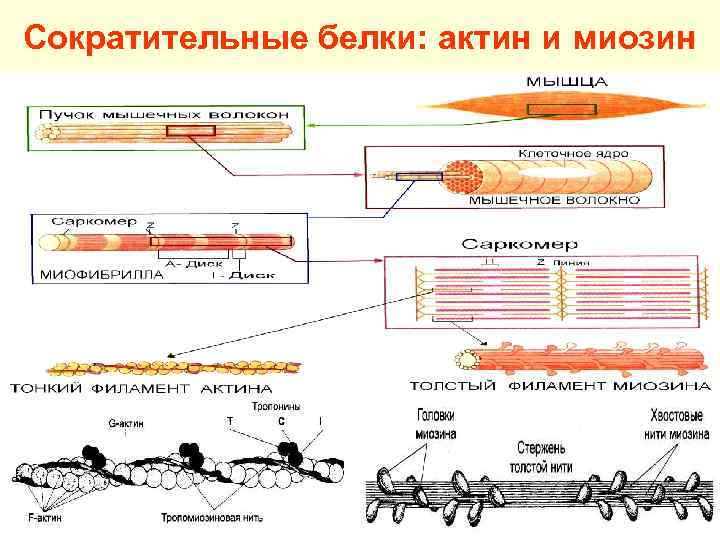
Сократительные белки: актин и миозин
Лекция 3. Белки - 2011.ppt