 АМФОТЕРНЫЕ ОКСИДЫ И ГИДРОКСИДЫ.
АМФОТЕРНЫЕ ОКСИДЫ И ГИДРОКСИДЫ.
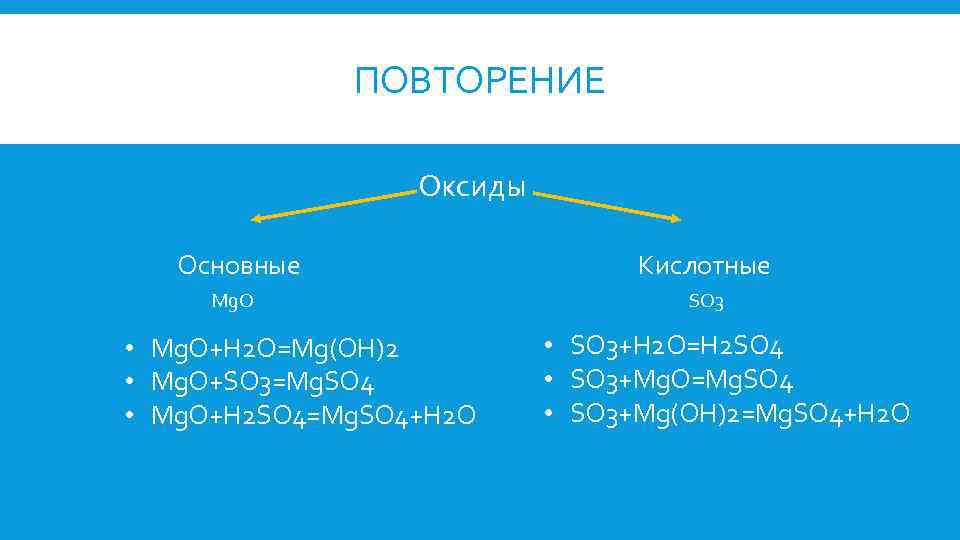 ПОВТОРЕНИЕ Оксиды Основные Mg. O • Mg. O+H 2 O=Mg(OH)2 • Mg. O+SO 3=Mg. SO 4 • Mg. O+H 2 SO 4=Mg. SO 4+H 2 O Кислотные SO 3 • SO 3+H 2 O=H 2 SO 4 • SO 3+Mg. O=Mg. SO 4 • SO 3+Mg(OH)2=Mg. SO 4+H 2 O
ПОВТОРЕНИЕ Оксиды Основные Mg. O • Mg. O+H 2 O=Mg(OH)2 • Mg. O+SO 3=Mg. SO 4 • Mg. O+H 2 SO 4=Mg. SO 4+H 2 O Кислотные SO 3 • SO 3+H 2 O=H 2 SO 4 • SO 3+Mg. O=Mg. SO 4 • SO 3+Mg(OH)2=Mg. SO 4+H 2 O
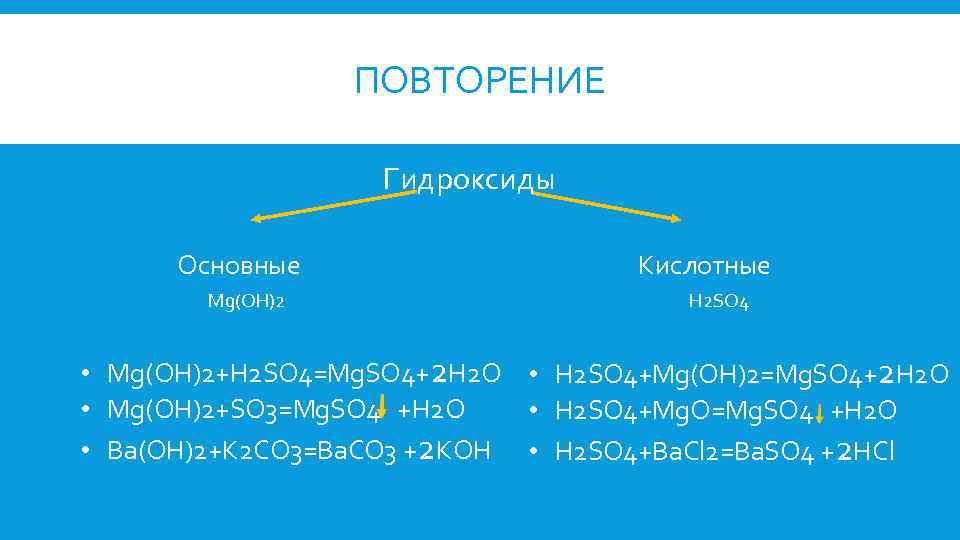 ПОВТОРЕНИЕ Гидроксиды Основные Mg(OH)2 Кислотные H 2 SO 4 • Mg(OH)2+H 2 SO 4=Mg. SO 4+2 H 2 O • H 2 SO 4+Mg(OH)2=Mg. SO 4+2 H 2 O • Mg(OH)2+SO 3=Mg. SO 4 +H 2 O • H 2 SO 4+Mg. O=Mg. SO 4 +H 2 O • Ba(OH)2+K 2 CO 3=Ba. CO 3 +2 KOH • H 2 SO 4+Ba. Cl 2=Ba. SO 4 +2 HCl
ПОВТОРЕНИЕ Гидроксиды Основные Mg(OH)2 Кислотные H 2 SO 4 • Mg(OH)2+H 2 SO 4=Mg. SO 4+2 H 2 O • H 2 SO 4+Mg(OH)2=Mg. SO 4+2 H 2 O • Mg(OH)2+SO 3=Mg. SO 4 +H 2 O • H 2 SO 4+Mg. O=Mg. SO 4 +H 2 O • Ba(OH)2+K 2 CO 3=Ba. CO 3 +2 KOH • H 2 SO 4+Ba. Cl 2=Ba. SO 4 +2 HCl
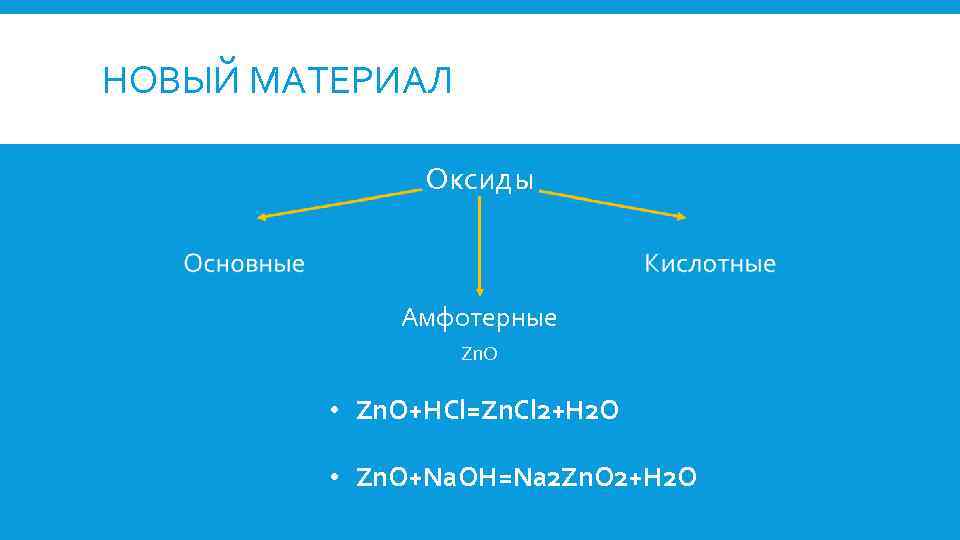 НОВЫЙ МАТЕРИАЛ Оксиды Амфотерные Zn. O • Zn. O+HCl=Zn. Cl 2+H 2 O • Zn. O+Na. OH=Na 2 Zn. O 2+H 2 O
НОВЫЙ МАТЕРИАЛ Оксиды Амфотерные Zn. O • Zn. O+HCl=Zn. Cl 2+H 2 O • Zn. O+Na. OH=Na 2 Zn. O 2+H 2 O
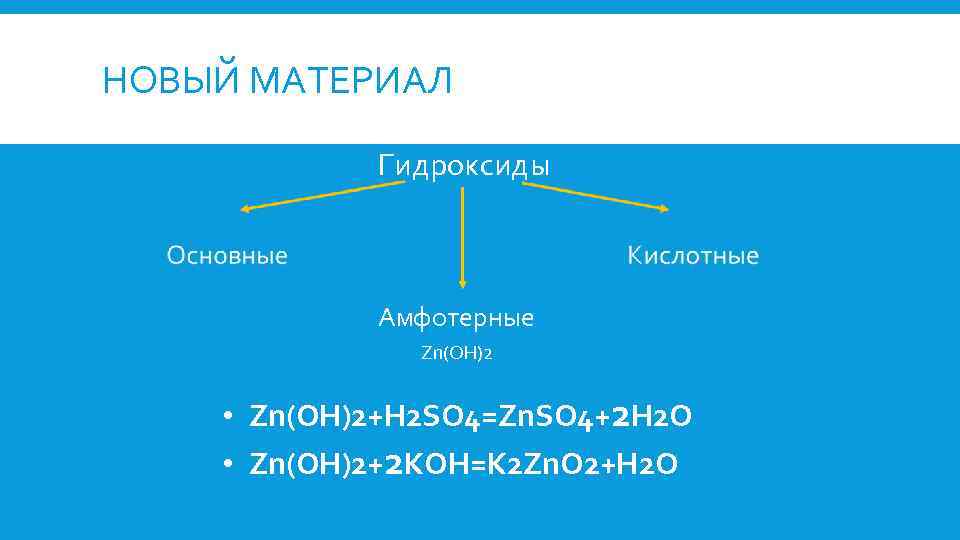 НОВЫЙ МАТЕРИАЛ Гидроксиды Амфотерные Zn(OH)2 • Zn(OH)2+H 2 SO 4=Zn. SO 4+2 H 2 O • Zn(OH)2+2 KOH=K 2 Zn. O 2+H 2 O
НОВЫЙ МАТЕРИАЛ Гидроксиды Амфотерные Zn(OH)2 • Zn(OH)2+H 2 SO 4=Zn. SO 4+2 H 2 O • Zn(OH)2+2 KOH=K 2 Zn. O 2+H 2 O
 ТАКИМ ОБРАЗОМ Амфотерными называются вещества, которые в зависимости от условий реакции проявляют кислотные или основные свойства.
ТАКИМ ОБРАЗОМ Амфотерными называются вещества, которые в зависимости от условий реакции проявляют кислотные или основные свойства.
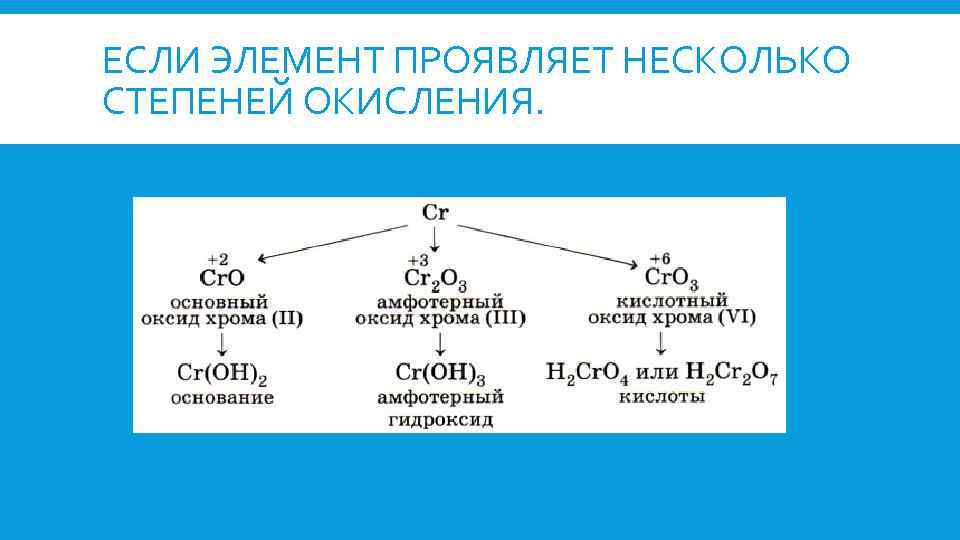 ЕСЛИ ЭЛЕМЕНТ ПРОЯВЛЯЕТ НЕСКОЛЬКО СТЕПЕНЕЙ ОКИСЛЕНИЯ.
ЕСЛИ ЭЛЕМЕНТ ПРОЯВЛЯЕТ НЕСКОЛЬКО СТЕПЕНЕЙ ОКИСЛЕНИЯ.
 ЗАКРЕПЛЕНИЕ ИЗУЧЕННОГО
ЗАКРЕПЛЕНИЕ ИЗУЧЕННОГО
 ДОМАШНЯЯ РАБОТА § 2, упр. 2, 3. Решить задачу: При сплавлении оксида алюминия с гидроксидом калия образовалось 98 г. метаалюмината калия (KAl. O 2). Определите массу оксида, вступившего в реакцию.
ДОМАШНЯЯ РАБОТА § 2, упр. 2, 3. Решить задачу: При сплавлении оксида алюминия с гидроксидом калия образовалось 98 г. метаалюмината калия (KAl. O 2). Определите массу оксида, вступившего в реакцию.