
Амфотерность

СПЛАВЫ (без воды) 2 KOH(тв. ) + H 2 Zn. O 2(тв. ) (t, сплавление)→ K 2 Zn. O 2 + 2 H 2 O Be(OH)2(тв. ) + 2 Na. OH(тв. ) (t, сплавление)→ 2 H 2 O + Na 2 Be. O 2 (метабериллат натрия, или бериллат) Pb(OH)2(тв. ) + 2 Na. OH(тв. ) (t, сплавление)→ 2 H 2 O + Na 2 Pb. O 2 (метаплюмбат натрия, или плюмбат)

H 3 Al. O 3 – H 2 O → HAl. O 2 + H 2 O Al(OH)3(тв. ) + KOH(тв. ) (t, сплавление)→ 2 H 2 O + KAl. O 2(метаалюминат калия) Cr(OH)3 → H 3 Cr. O 3 → HCr. O 2 Cr(OH)3(тв. ) + KOH(тв. ) (t, сплавление)→ 2 H 2 O + KCr. O 2(метахромат калия).
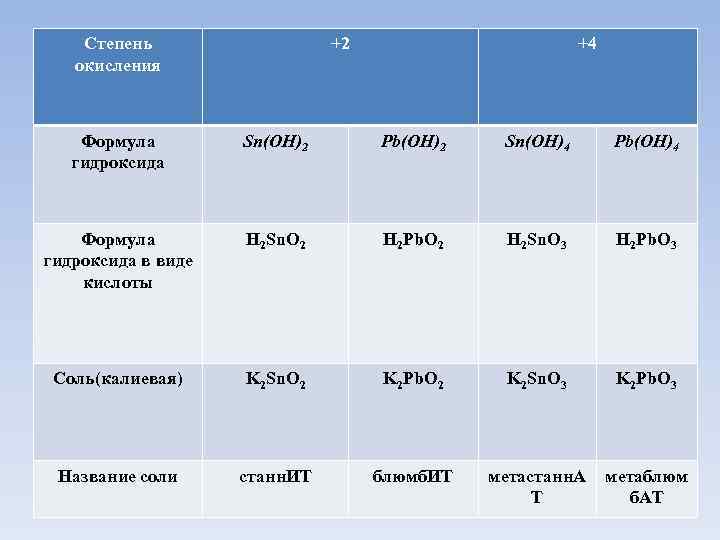
Степень окисления +2 +4 Формула гидроксида Sn(OH)2 Pb(OH)2 Sn(OH)4 Pb(OH)4 Формула гидроксида в виде кислоты H 2 Sn. O 2 H 2 Pb. O 2 H 2 Sn. O 3 H 2 Pb. O 3 Соль(калиевая) K 2 Sn. O 2 K 2 Pb. O 2 K 2 Sn. O 3 K 2 Pb. O 3 Название соли станн. ИТ блюмб. ИТ метастанн. А Т метаблюм б. АТ
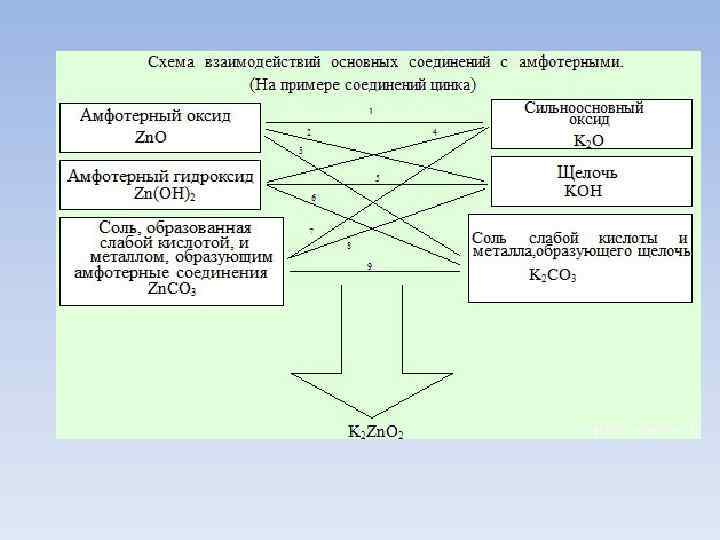

СПЛАВЛЕНИЕ!!! 1. Амфотерного оксида с сильноосновным оксидом: Zn. O(тв. ) + K 2 O(тв. ) (t, сплавление)→ K 2 Zn. O 2 (метацинкат калия/цинкат калия) 2. Амфотерного оксида со щелочью: Zn. O(тв. ) + 2 KOH(тв. ) (t, сплавление)→ K 2 Zn. O 2 + H 2 O↑ 3. Амфотерного оксида с солью слабой кислоты и металла, образующего щелочь: Zn. O(тв. ) + K 2 CO 3(тв. ) (t, сплавление)→ K 2 Zn. O 2 + CO 2↑ 4. Амфотерного гидроксида с сильноосновным оксидом: Zn(OH)2(тв. ) + K 2 O(тв. ) (t, сплавление)→ K 2 Zn. O 2 + H 2 O↑ 5. Амфотерного гидроксида со щелочью: Zn(OH)2(тв. ) + 2 KOH(тв. ) (t, сплавление)→ K 2 Zn. O 2 + 2 H 2 O↑ 6. Амфотерного гидроксида с солью слабой кислоты и металла, образующего щелочь: Zn(OH)2(тв. ) + K 2 CO 3(тв. ) (t, сплавление)→ K 2 Zn. O 2 + CO 2↑ + H 2 O↑ 7. Соли слабой кислоты и металла, образующего амфотерные соединение с сильноосновным оксидом: Zn. CO 3(тв. ) + K 2 O(тв. ) (t, сплавление)→ K 2 Zn. O 2 + CO 2↑ 8. Соли слабой кислоты и металла, образующего амфотерные соединение со щелочью: Zn. CO 3(тв. ) + 2 KOH(тв. ) (t, сплавление)→ K 2 Zn. O 2 + CO 2↑ + H 2 O↑ 9. Соли слабой кислоты и металла, образующего амфотерные соединение с солью слабой кислоты и металла, образующего щелочь: Zn. CO 3(тв. ) + K 2 CO 3(тв. ) (t, сплавление)→ K 2 Zn. O 2 + 2 CO 2↑

РАСТВОРЫ!! Al 2 O 3 + 2 Na. OH + 3 H 2 O → 2 Na[Al(OH)4] Al 2 O 3 + 6 Na. OH + 3 H 2 O → 2 Na 3[Al(OH)6] 2 Al + 2 Na. OH + 6 H 2 O → 2 Na[Al(OH)4] + 3 H 2↑ 2 Al + 6 Na. OH + 6 H 2 O → 2 Na 3[Al(OH)6] + 3 H 2↑
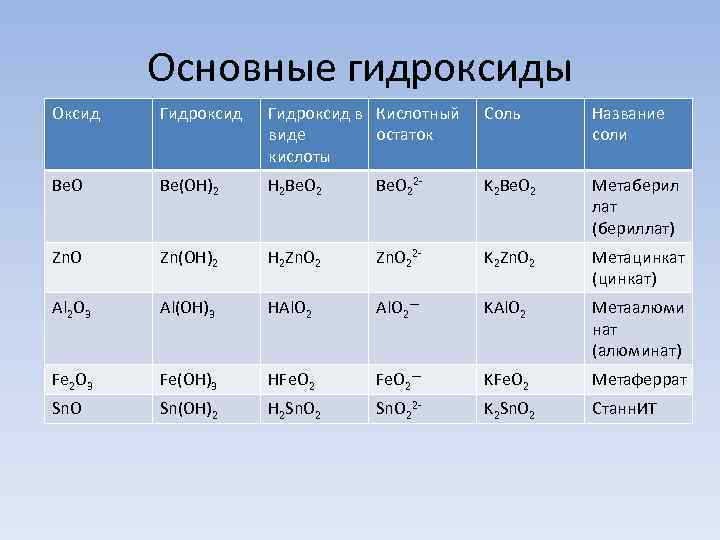
Основные гидроксиды Оксид Гидроксид в Кислотный виде остаток кислоты Соль Название соли Be. O Be(OH)2 H 2 Be. O 22 - K 2 Be. O 2 Метаберил лат (бериллат) Zn. O Zn(OH)2 H 2 Zn. O 22 - K 2 Zn. O 2 Метацинкат (цинкат) Al 2 O 3 Al(OH)3 HAl. O 2— KAl. O 2 Метаалюми нат (алюминат) Fe 2 O 3 Fe(OH)3 HFe. O 2— KFe. O 2 Метаферрат Sn. O Sn(OH)2 H 2 Sn. O 22 - K 2 Sn. O 2 Станн. ИТ
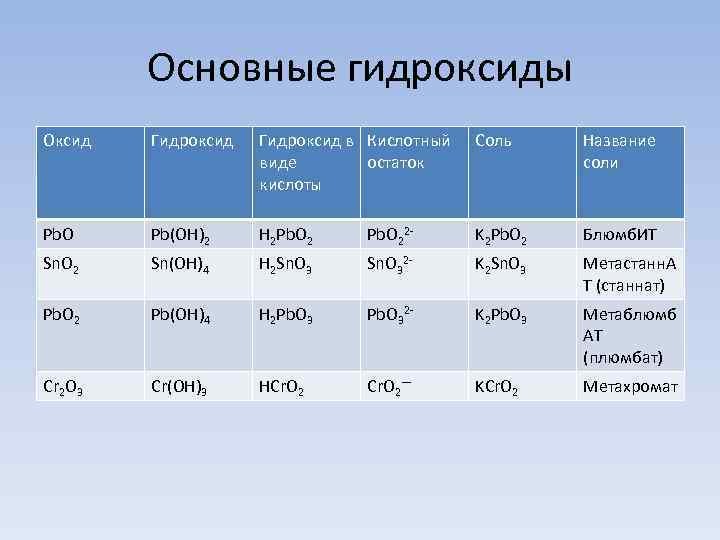
Основные гидроксиды Оксид Гидроксид в Кислотный виде остаток кислоты Соль Название соли Pb. O Pb(OH)2 H 2 Pb. O 22 - K 2 Pb. O 2 Блюмб. ИТ Sn. O 2 Sn(OH)4 H 2 Sn. O 32 - K 2 Sn. O 3 Метастанн. А Т (станнат) Pb. O 2 Pb(OH)4 H 2 Pb. O 32 - K 2 Pb. O 3 Метаблюмб АТ (плюмбат) Cr 2 O 3 Cr(OH)3 HCr. O 2— KCr. O 2 Метахромат
![1. Na[Al(OH)4] - Тетрагидроксоалюминат натрия Al(OH)3 + Na. OH → Na[Al(OH)4] Al 2 O 1. Na[Al(OH)4] - Тетрагидроксоалюминат натрия Al(OH)3 + Na. OH → Na[Al(OH)4] Al 2 O](https://present5.com/presentation/458769076_457384533/image-10.jpg)
1. Na[Al(OH)4] - Тетрагидроксоалюминат натрия Al(OH)3 + Na. OH → Na[Al(OH)4] Al 2 O 3 + 2 Na. OH + 3 H 2 O → 2 Na[Al(OH)4] 2 Al + 2 Na. OH + 6 H 2 O → 2 Na[Al(OH)4] + 3 H 2↑ 2. Na 3[Al(OH)6] -Гексагидроксоалюминат натрия Al(OH)3 + 3 Na. OH → Na 3[Al(OH)6] Al 2 O 3 + 6 Na. OH + 3 H 2 O → 2 Na 3[Al(OH)6] 2 Al + 6 Na. OH + 6 H 2 O → 2 Na 3[Al(OH)6] + 3 H 2↑
![3. K 2[Zn(OH)4] -тетрагидроксоцинкат натрия Zn(OH)2 + 2 Na. OH → Na 2[Zn(OH)4] Zn. 3. K 2[Zn(OH)4] -тетрагидроксоцинкат натрия Zn(OH)2 + 2 Na. OH → Na 2[Zn(OH)4] Zn.](https://present5.com/presentation/458769076_457384533/image-11.jpg)
3. K 2[Zn(OH)4] -тетрагидроксоцинкат натрия Zn(OH)2 + 2 Na. OH → Na 2[Zn(OH)4] Zn. O + 2 Na. OH + H 2 O → Na 2[Zn(OH)4] Zn + 2 Na. OH + 2 H 2 O → Na 2[Zn(OH)4]+ H 2↑ 4. K 4[Zn(OH)6] -гексагидроксоцинкат натрия Zn(OH)2 + 4 Na. OH → Na 4[Zn(OH)6] Zn. O + 4 Na. OH + H 2 O → Na 4[Zn(OH)6] Zn + 4 Na. OH + 2 H 2 O → Na 4[Zn(OH)6]+ H 2↑
![5. Li 2[Be(OH)4] -тетрагидроксобериллат лития Be(OH)2 + 2 Li. OH → Li 2[Be(OH)4] Be. 5. Li 2[Be(OH)4] -тетрагидроксобериллат лития Be(OH)2 + 2 Li. OH → Li 2[Be(OH)4] Be.](https://present5.com/presentation/458769076_457384533/image-12.jpg)
5. Li 2[Be(OH)4] -тетрагидроксобериллат лития Be(OH)2 + 2 Li. OH → Li 2[Be(OH)4] Be. O + 2 Li. OH + H 2 O → Li 2[Be(OH)4] Be + 2 Li. OH + 2 H 2 O → Li 2[Be(OH)4]+ H 2↑ 6. Li 4[Be(OH)6] -гексагидроксобериллат лития Be(OH)2 + 4 Li. OH → Li 4[Be(OH)6] Be. O + 4 Li. OH + H 2 O → Li 4[Be(OH)6] Be + 4 Li. OH + 2 H 2 O → Li 4[Be(OH)6]+ H 2↑
![7. Na[Cr(OH)4] -тетрагидроксохромат натрия Cr(OH)3 + Na. OH → Na[Cr(OH)4] Cr 2 O 3 7. Na[Cr(OH)4] -тетрагидроксохромат натрия Cr(OH)3 + Na. OH → Na[Cr(OH)4] Cr 2 O 3](https://present5.com/presentation/458769076_457384533/image-13.jpg)
7. Na[Cr(OH)4] -тетрагидроксохромат натрия Cr(OH)3 + Na. OH → Na[Cr(OH)4] Cr 2 O 3 + 2 Na. OH + 3 H 2 O → 2 Na[Cr(OH)4] 8. Na 3[Cr(OH)6] - гексагидроксохромат натрия Cr(OH)3 + 3 Na. OH → Na 3[Cr(OH)6] Cr 2 O 3 + 6 Na. OH + 3 H 2 O → 2 Na 3[Cr(OH)6] 9. Na[Fe(OH)4] - тетрагидроксоферрат натрия Fe(OH)3 + Na. OH → Na[Fe(OH)4] Fe 2 O 3 + 2 Na. OH + 3 H 2 O → 2 Na[Fe(OH)4] 10. Na 3[Fe(OH)6] -гексагидроксоферрат натрия Fe(OH)3 + 3 Na. OH → Na 3[Fe(OH)6] Fe 2 O 3 + 6 Na. OH + 3 H 2 O → 2 Na 3[Fe(OH)6]

Полученные в этих взаимодействиях соли реагируют с кислотами, образуя две другие соли (соли данной кислоты и двух металлов): 2 Na 3[Al(OH)6] + 6 H 2 SO 4 → 3 Na 2 SO 4 + Al 2(SO 4)3 + 12 H 2 O