алкены.pptx
- Количество слайдов: 26

Алкены Хайрутдинов Р. И. Учитель химии ГБОУ гимназия № 1565 отделение Школа-297 Москва 2014
Номенклатура Строение молекулы Изомерия Физические свойства Cn. H 2 n Химические свойства Получение Проверка знаний Применение 2

Cn. H 2 n Алкены – ациклические углеводороды, в молекуле которых кроме одинарных связей содержится одна двойная связь между атомами углерода. Общая формула: Сn. H 2 n 3
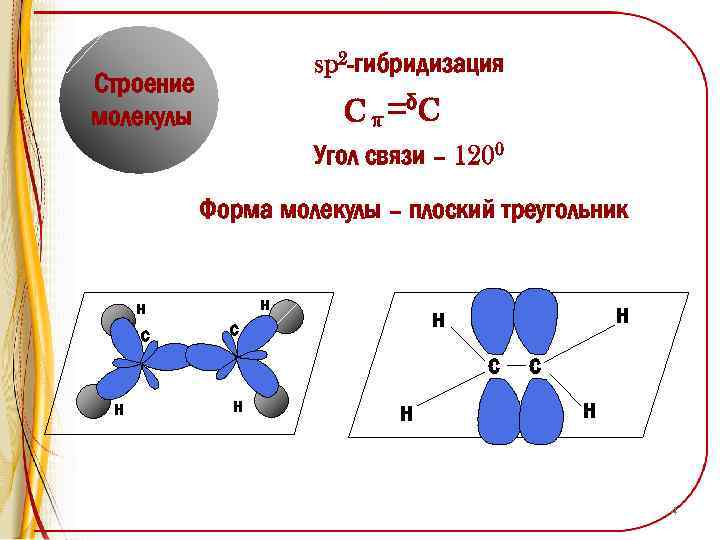
sp 2 -гибридизация Строение молекулы Cπ δC Угол связи – 1200 Форма молекулы – плоский треугольник н с н н н с н 4

Гомологический ряд C 2 H 4 этен C 3 H 6 пропен C 4 H 8 бутен C 5 H 10 пентен - амилен C 6 H 12 гексен C 7 H 14 гептен C 8 H 16 октен C 9 H 18 нонен C 10 H 20 децен Гомологи – вещества, имеющие одинаковый качественный состав, содержащие одинаковые функциональные группы и отличающиеся одно от другого на одну или несколько групп -CН 2 -.
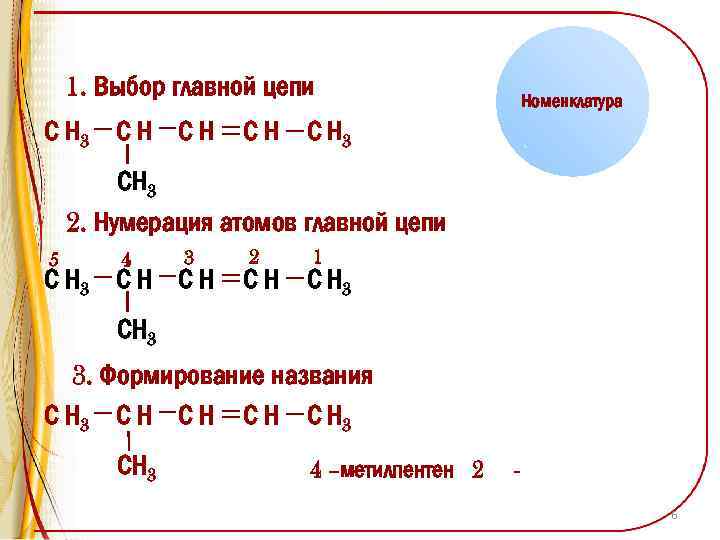
1. Выбор главной цепи С Н 3 С Н Номенклатура С Н 3 СН 3 2. Нумерация атомов главной цепи 5 4 3 С Н С Н 2 1 С Н 3 СН 3 3. Формирование названия С Н 3 С Н С Н 3 СН 3 4 –метилпентен 2 6
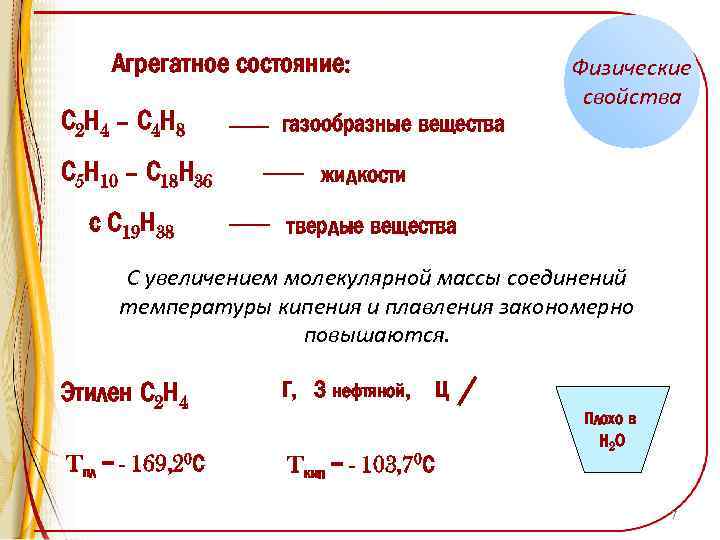
Агрегатное состояние: С 2 Н 4 – С 4 Н 8 С 5 Н 10 – С 18 Н 36 с С 19 Н 38 газообразные вещества Физические свойства жидкости твердые вещества С увеличением молекулярной массы соединений температуры кипения и плавления закономерно повышаются. Этилен С 2 Н 4 Г, З нефтяной, Tпл = - 169, 20 С Tкип = - 103, 70 С Ц Плохо в Н 2 О 7
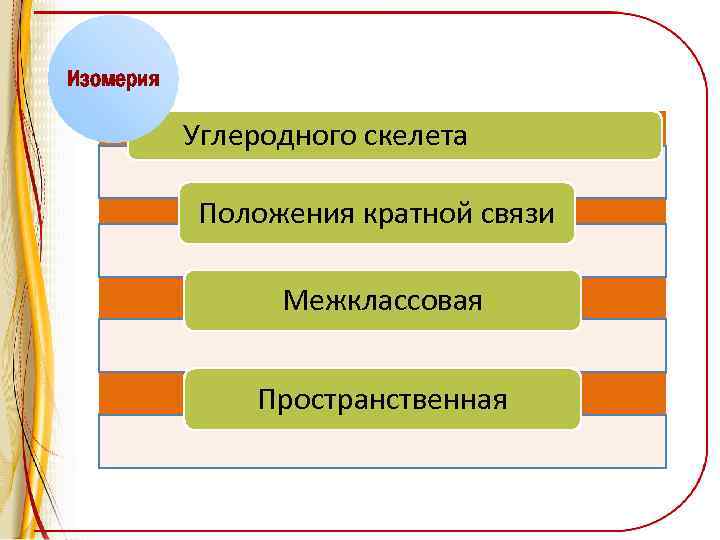
Изомерия Углеродного скелета Положения кратной связи Межклассовая Пространственная

СН 3 СН 2 СН СН 2 бутен - 1 СН 3 2 -метилпропен С СН 2 СН 3 1. Структурная изомерия: изомерия углеродного скелета Изомеры – вещества, имеющие одинаковый количественный и качественный состав, но разное расположение атомов в молекуле (разное строение) => различные свойства. 9

2. Структурная изомерия: положения двойной связи CH 2=CH-CH 2 -CH 3 бутен-1 CH 3 -CH=CH-CH 3 бутен -2
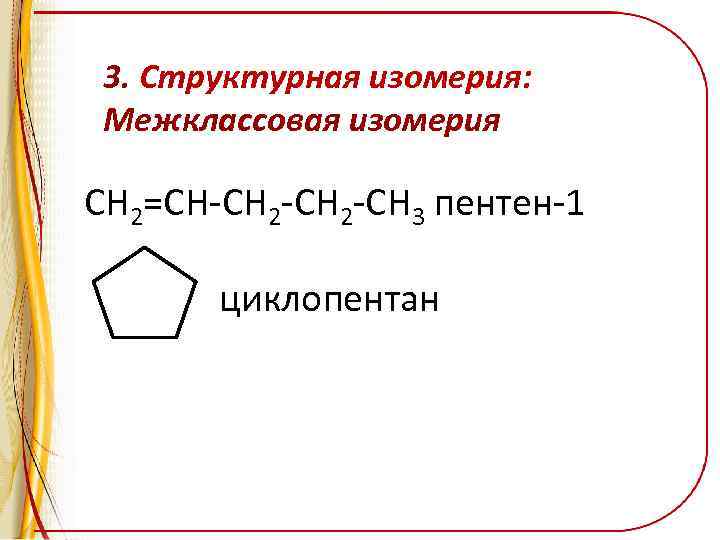
3. Структурная изомерия: Межклассовая изомерия CH 2=CH-CH 2 -CH 3 пентен-1 циклопентан
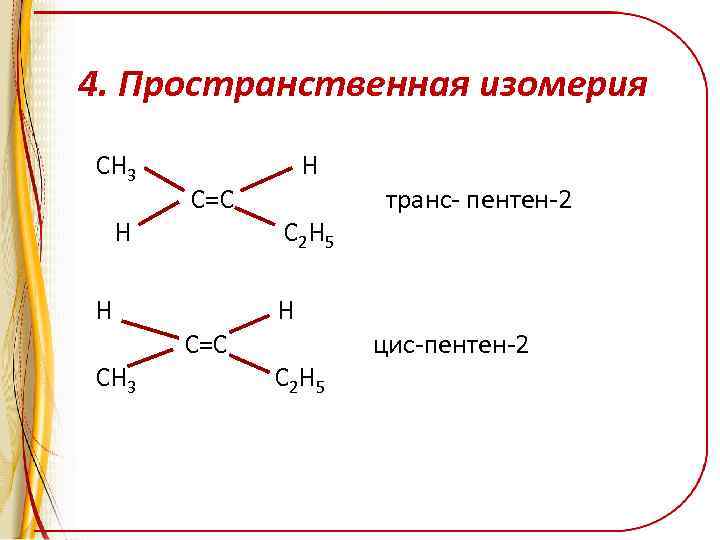
4. Пространственная изомерия CH 3 H H CH 3 C=C H C 2 H 5 транс- пентен-2 цис-пентен-2
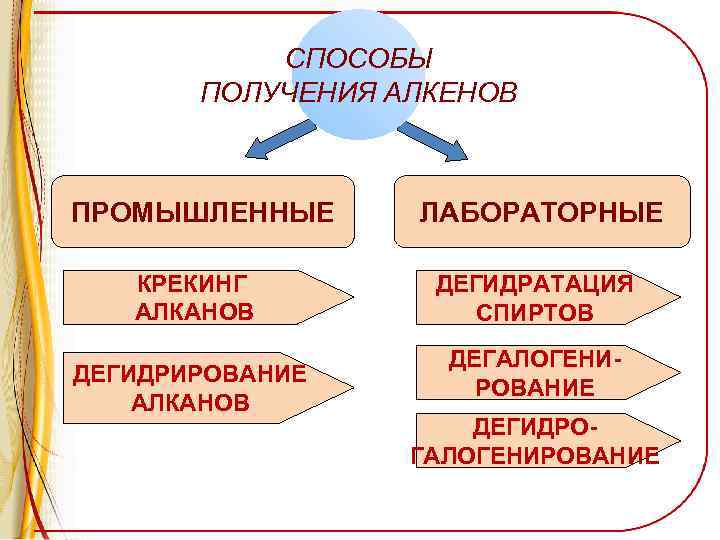
СПОСОБЫ ПОЛУЧЕНИЯ АЛКЕНОВ ПРОМЫШЛЕННЫЕ КРЕКИНГ АЛКАНОВ ДЕГИДРИРОВАНИЕ АЛКАНОВ ЛАБОРАТОРНЫЕ ДЕГИДРАТАЦИЯ СПИРТОВ ДЕГАЛОГЕНИРОВАНИЕ ДЕГИДРОГАЛОГЕНИРОВАНИЕ
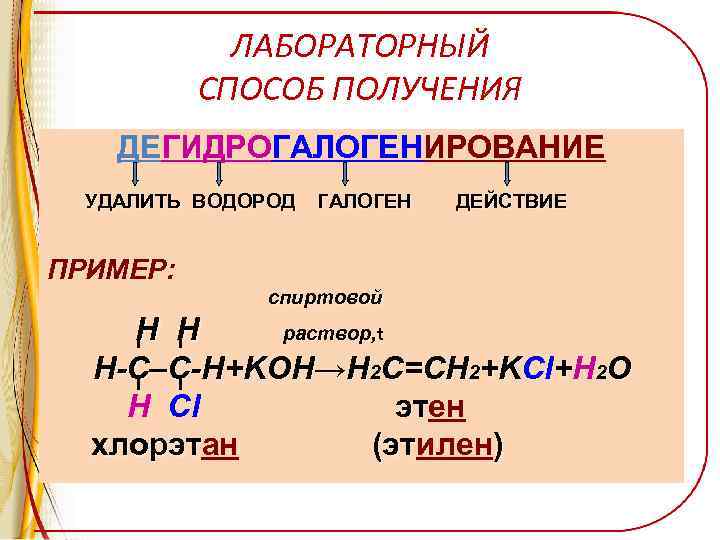
ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГИДРОГАЛОГЕНИРОВАНИЕ УДАЛИТЬ ВОДОРОД ГАЛОГЕН ДЕЙСТВИЕ ПРИМЕР: спиртовой H H раствор, t раствор, Н-С–С-Н+KOH→Н 2 С=СН 2+KCl+H 2 O +K Н Cl этен эт хлорэтан (этилен) хлорэт (эт

ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГАЛОГЕНИРОВАНИЕ ПРИМЕР: t Н 2 С – СН 2 + Zn → Н 2 С = СН 2 + Zn. Br 2 Zn Br Br этен эт 1, 2 -дибромэтан (этилен) 1, 2 -дибромэт (эт
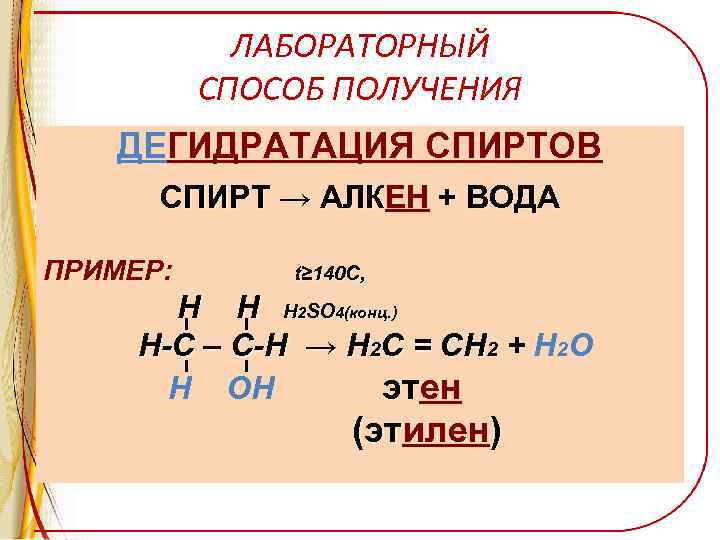
ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГИДРАТАЦИЯ СПИРТОВ СПИРТ → АЛКЕН + ВОДА АЛК ПРИМЕР: t≥ 140 C, Н Н Н 2 SO 4(конц. ) Н-С – С-Н → Н 2 С = СН 2 + Н 2 О Н ОН этен эт (этилен) (эт

ПРОМЫШЛЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ КРЕКИНГ АЛКАНОВ АЛКАН → АЛКАН + АЛКЕН АЛК АЛК С БОЛЕЕ ДЛИННОЙ С МЕНЕЕ ДЛИННОЙ УГЛЕРОДНОЙ ЦЕПЬЮ ПРИМЕР: С 10 t=400 -700 C Н 22→ С 5 Н 12+ С 5 Н 10 декан дек пентан пентен пент

ПРОМЫШЛЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГИДРИРОВАНИЕ АЛКАНОВ АЛКАН → АЛКЕН + ВОДОРОД АЛК ПРИМЕР: Ni, t=500 C Н 3 С - СН 3 → Н 2 С = СН 2 + Н 2 этан этен эт эт (этилен) (эт
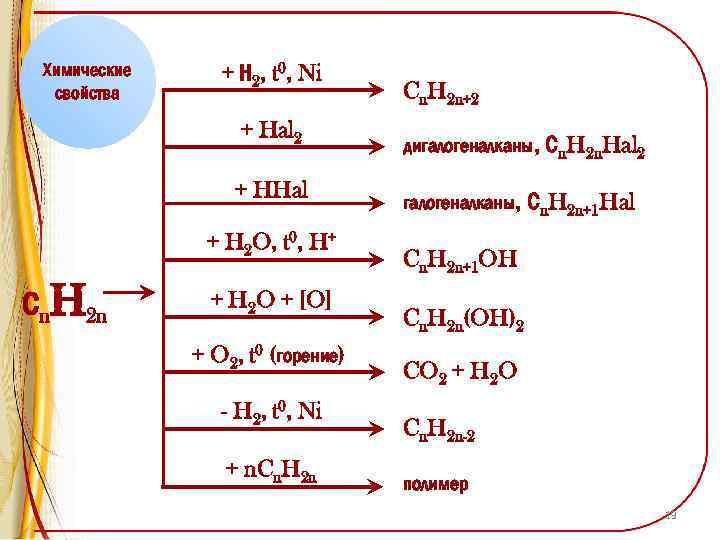
Химические свойства + Н 2, t 0, Ni + Hal 2 + HHal + H 2 O, t 0, H+ Сn. H 2 n + H 2 O + [O] + O 2, t 0 (горение) - H 2, t 0, Ni + n. Cn. H 2 n+2 дигалогеналканы, Сn. H 2 n. Hal 2 Сn. H 2 n+1 Hal Cn. H 2 n+1 OH Cn. H 2 n(OH)2 CO 2 + H 2 O Cn. H 2 n-2 полимер 19

1. Гидрирование: СН 2 2. Галогенирование: СН 2 3. Гидрогалогенирование: СН 2 4. Гидратация: СН 2 Pt, t + Br 2 СН 2 + Н 2 О СН 3 СН 2 Вr СН 2 + НСl t, Н 3 РО 4 СН 3 CН 3 СН 2 Вr СН 3 СН 2 Сl СН 2 ОН I. Реакции присоединения 20

II. РЕАКЦИИ ОКИСЛЕНИЯ ГОРЕНИЕ АЛКЕНОВ ПРИМЕР: С 2 Н 4 + 3 О 2 2 СО 2 + 2 Н 2 О

РЕАКЦИИ ОКИСЛЕНИЯ МЯГКОЕ ОКИСЛЕНИЕ – ВЗАИМОДЕЙСТВИЕ С РАСТВОРОМ ПЕРМАНГАНАТА КАЛИЯ (реакция Е. Е. Вагнера) Н 2 С=СН 2 + [O] + H 2 O H 2 C - CH 2 OH OH этиленгликоль (этандиол-1, 2) ! Качественная реакция на непредельность углеводорода – на кратную связь

III. РЕАКЦИЯ ПОЛИМЕРИЗАЦИИ Это процесс соединения одинаковых молекул в более крупные. ПРИМЕР: n CH 2=CH 2 этилен (мономер) (-CH 2 -)n полиэтилен (полимер) n – степень полимеризации, показывает число молекул, вступивших в реакцию -CH 2 - структурное звено
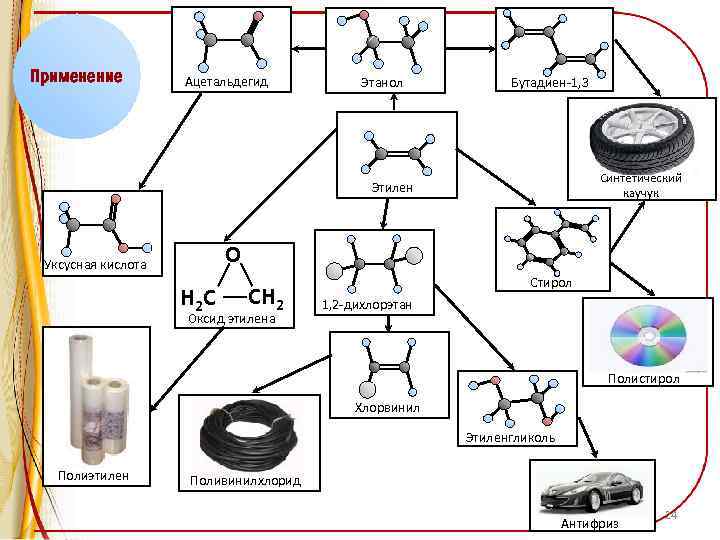
Применение Ацетальдегид Этанол Бутадиен-1, 3 Синтетический каучук Этилен О Уксусная кислота Н 2 С СН 2 Оксид этилена Стирол 1, 2 -дихлорэтан Полистирол Хлорвинил Этиленгликоль Полиэтилен Поливинилхлорид Антифриз 24

Применение этилена Свойство 1. Полимеризация 2. Галогенирование 3. Гидрогалогенирование Применение Производство полиэтилена, пластмасс Получение растворителей Для местная анестезия, получения растворителей, в с/х для обеззараживания зернохранилищ Пример
Свойство 4. Гидратация 5. Окисление раствором KMn. O 4 6. Особое свойство этилена: Применение Получение этилового спирта, используемого как растворитель, анти-септик в медицине , в производстве синтетического каучука Получение антифризов, тормозных жидкостей, в производстве пластмасс Этилен ускоряет созревание плодов Пример
алкены.pptx