Третья лекция (алкены).ppt
- Количество слайдов: 59
 АЛКЕНЫ: СТРОЕНИЕ, МЕТОДЫ ПОЛУЧЕНИЯ И ХИМИЧЕСКИЕ СВОЙСТВА 1
АЛКЕНЫ: СТРОЕНИЕ, МЕТОДЫ ПОЛУЧЕНИЯ И ХИМИЧЕСКИЕ СВОЙСТВА 1
 Алкены Алкенами называются углеводороды, содержащие одну двойную связь С=С. Являются ненасыщенными соединениями. Формула гомологического ряда Сn. Н 2 n 2
Алкены Алкенами называются углеводороды, содержащие одну двойную связь С=С. Являются ненасыщенными соединениями. Формула гомологического ряда Сn. Н 2 n 2
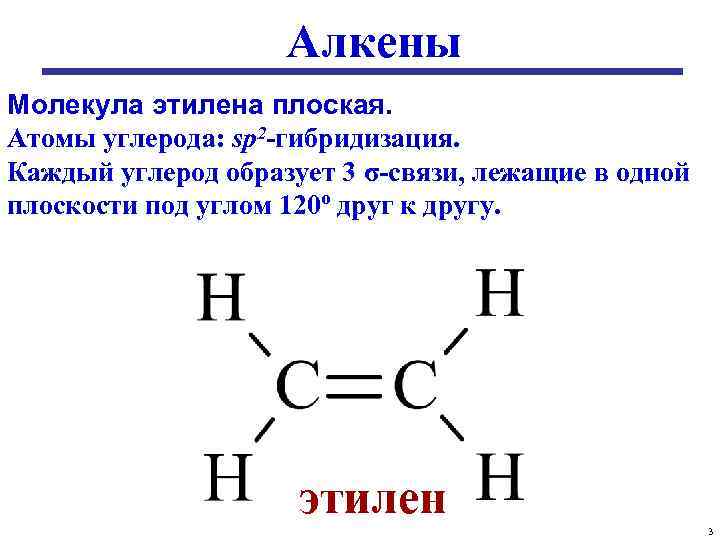 Алкены Молекула этилена плоская. Атомы углерода: sp 2 -гибридизация. Каждый углерод образует 3 σ-связи, лежащие в одной плоскости под углом 120º друг к другу. этилен 3
Алкены Молекула этилена плоская. Атомы углерода: sp 2 -гибридизация. Каждый углерод образует 3 σ-связи, лежащие в одной плоскости под углом 120º друг к другу. этилен 3
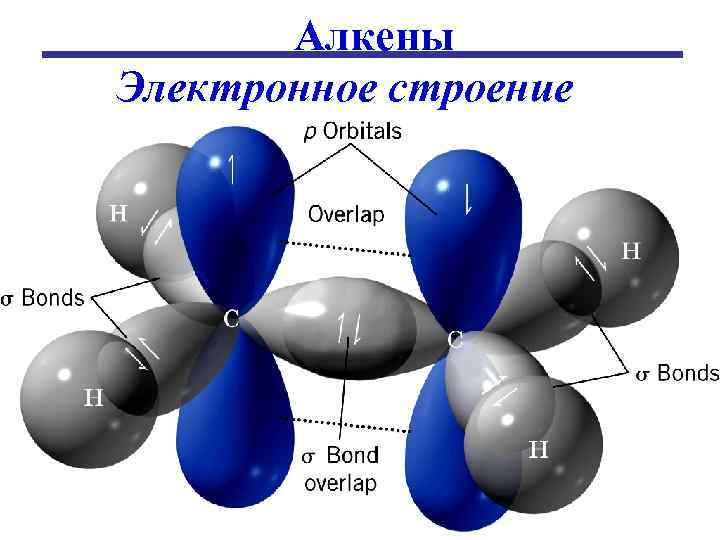 Алкены Электронное строение 4
Алкены Электронное строение 4
 π-связь более слабая связь, чем σсвязь Связь длина (нм) Е (к. Кал/моль) С-С 0, 154 82 С=С 0, 134 147 Е (π-связи) = 147 -82 = или 65 ккал/моль 5
π-связь более слабая связь, чем σсвязь Связь длина (нм) Е (к. Кал/моль) С-С 0, 154 82 С=С 0, 134 147 Е (π-связи) = 147 -82 = или 65 ккал/моль 5
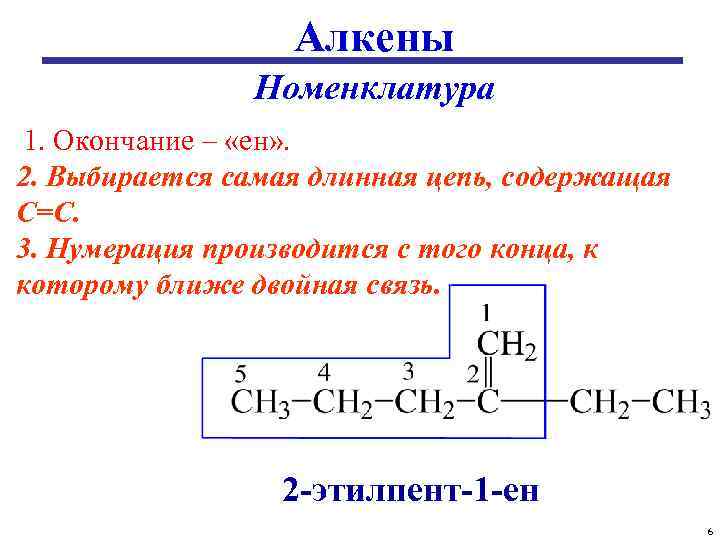 Алкены Номенклатура 1. Окончание – «ен» . 2. Выбирается самая длинная цепь, содержащая С=С. 3. Нумерация производится с того конца, к которому ближе двойная связь. 2 -этилпент-1 -ен 6
Алкены Номенклатура 1. Окончание – «ен» . 2. Выбирается самая длинная цепь, содержащая С=С. 3. Нумерация производится с того конца, к которому ближе двойная связь. 2 -этилпент-1 -ен 6
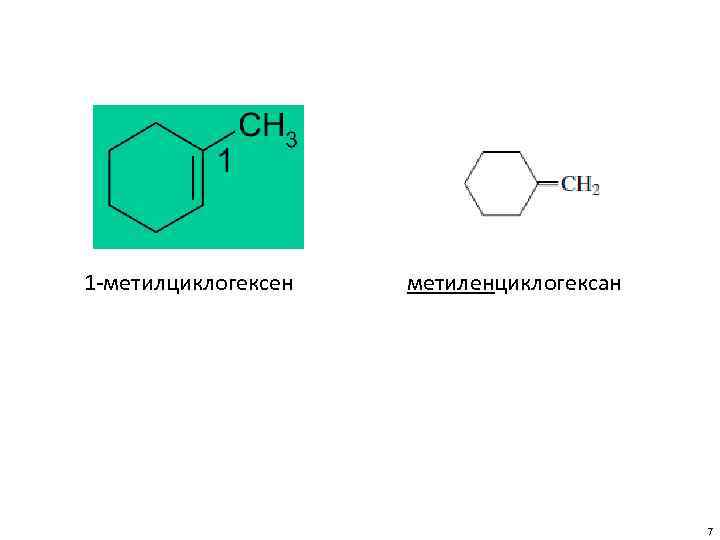 1 -метилциклогексен метиленциклогексан 7
1 -метилциклогексен метиленциклогексан 7
 Алкены Изомерия. Структурная изомерия. 8
Алкены Изомерия. Структурная изомерия. 8
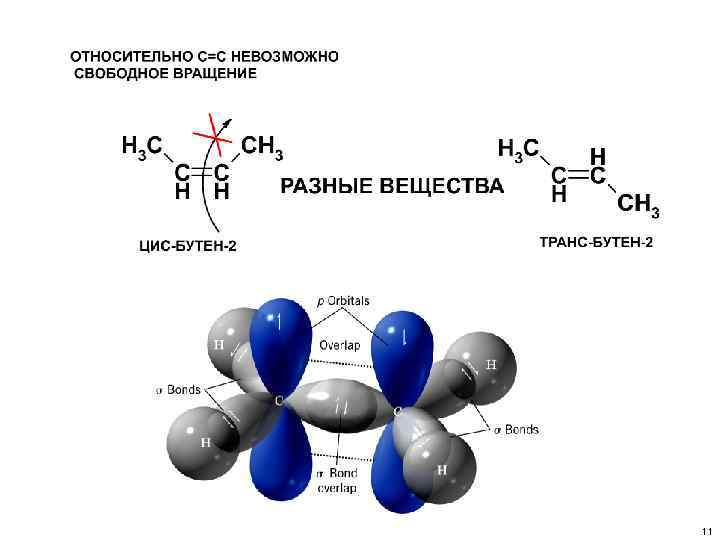
 Алкены Геометрическая изомерия (π-диастереомерия). Связана с разным расположением заместителей относительно двойной связи. Цис- и транс-изомеры бут-2 -ена 9
Алкены Геометрическая изомерия (π-диастереомерия). Связана с разным расположением заместителей относительно двойной связи. Цис- и транс-изомеры бут-2 -ена 9
 10
10
 11
11
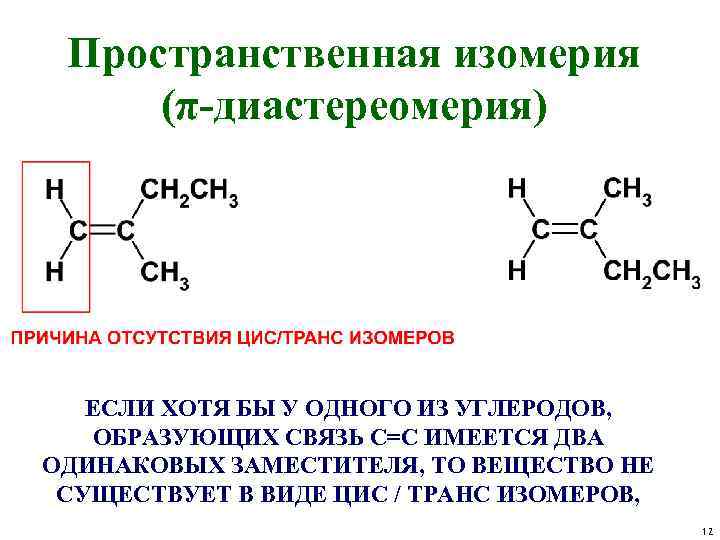 Пространственная изомерия (π-диастереомерия) ЕСЛИ ХОТЯ БЫ У ОДНОГО ИЗ УГЛЕРОДОВ, ОБРАЗУЮЩИХ СВЯЗЬ С=С ИМЕЕТСЯ ДВА ОДИНАКОВЫХ ЗАМЕСТИТЕЛЯ, ТО ВЕЩЕСТВО НЕ СУЩЕСТВУЕТ В ВИДЕ ЦИС / ТРАНС ИЗОМЕРОВ, 12
Пространственная изомерия (π-диастереомерия) ЕСЛИ ХОТЯ БЫ У ОДНОГО ИЗ УГЛЕРОДОВ, ОБРАЗУЮЩИХ СВЯЗЬ С=С ИМЕЕТСЯ ДВА ОДИНАКОВЫХ ЗАМЕСТИТЕЛЯ, ТО ВЕЩЕСТВО НЕ СУЩЕСТВУЕТ В ВИДЕ ЦИС / ТРАНС ИЗОМЕРОВ, 12
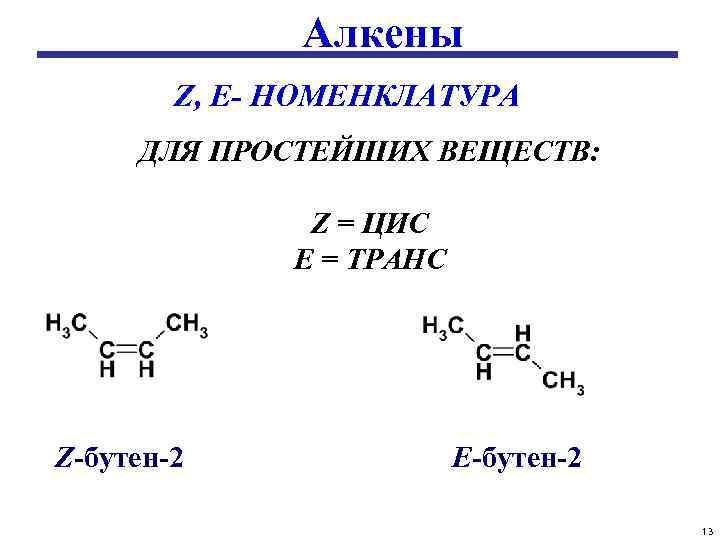 Алкены Z, E- НОМЕНКЛАТУРА ДЛЯ ПРОСТЕЙШИХ ВЕЩЕСТВ: Z = ЦИС E = ТРАНС Z-бутен-2 E-бутен-2 13
Алкены Z, E- НОМЕНКЛАТУРА ДЛЯ ПРОСТЕЙШИХ ВЕЩЕСТВ: Z = ЦИС E = ТРАНС Z-бутен-2 E-бутен-2 13
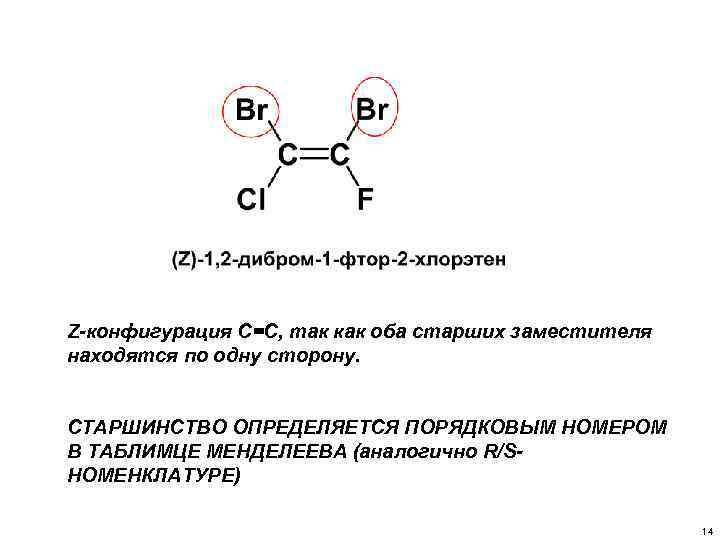 Z-конфигурация С=С, так как оба старших заместителя находятся по одну сторону. СТАРШИНСТВО ОПРЕДЕЛЯЕТСЯ ПОРЯДКОВЫМ НОМЕРОМ В ТАБЛИМЦЕ МЕНДЕЛЕЕВА (аналогично R/SНОМЕНКЛАТУРЕ) 14
Z-конфигурация С=С, так как оба старших заместителя находятся по одну сторону. СТАРШИНСТВО ОПРЕДЕЛЯЕТСЯ ПОРЯДКОВЫМ НОМЕРОМ В ТАБЛИМЦЕ МЕНДЕЛЕЕВА (аналогично R/SНОМЕНКЛАТУРЕ) 14
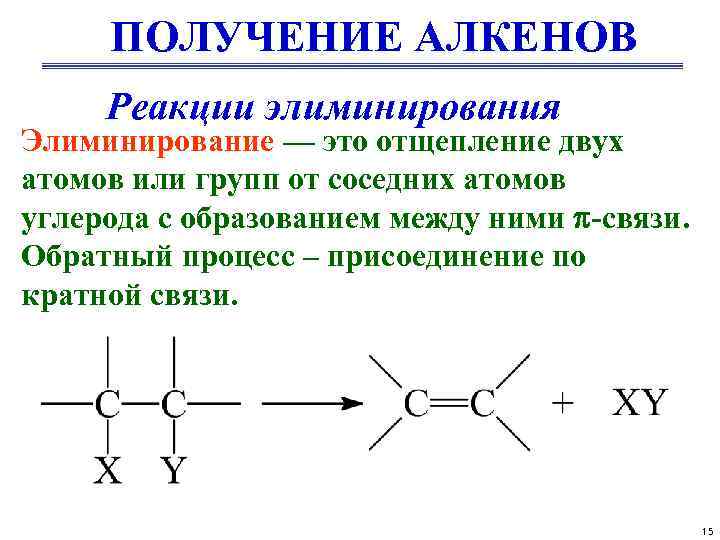 ПОЛУЧЕНИЕ АЛКЕНОВ Реакции элиминирования Элиминирование — это отщепление двух атомов или групп от соседних атомов углерода с образованием между ними -связи. Обратный процесс – присоединение по кратной связи. 15
ПОЛУЧЕНИЕ АЛКЕНОВ Реакции элиминирования Элиминирование — это отщепление двух атомов или групп от соседних атомов углерода с образованием между ними -связи. Обратный процесс – присоединение по кратной связи. 15
 Алкены 16
Алкены 16
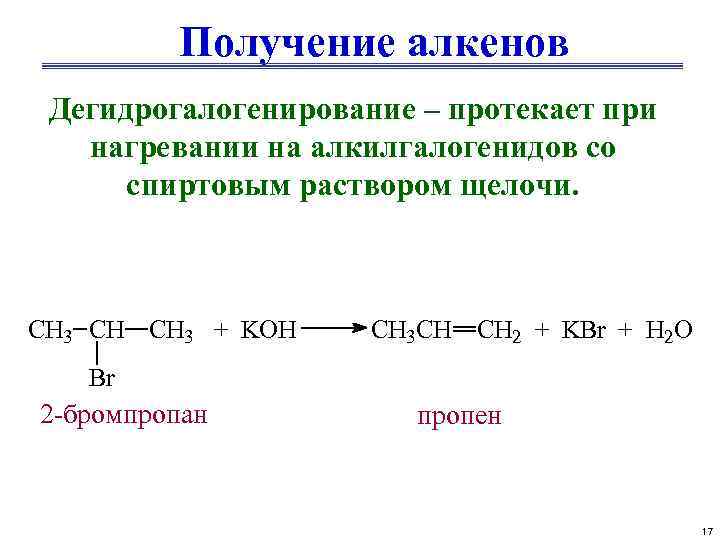 Получение алкенов Дегидрогалогенирование – протекает при нагревании на алкилгалогенидов со спиртовым раствором щелочи. CH 3 CH CH 3 + KOH CH 3 CH CH 2 + KBr + H 2 O Br 2 -бромпропан пропен 17
Получение алкенов Дегидрогалогенирование – протекает при нагревании на алкилгалогенидов со спиртовым раствором щелочи. CH 3 CH CH 3 + KOH CH 3 CH CH 2 + KBr + H 2 O Br 2 -бромпропан пропен 17
 Реакция дегидрогалогенирования Правило Зайцева – преимущественно отщепляется третичный атом водорода, хуже – вторичный, еще хуже – первичный. 18
Реакция дегидрогалогенирования Правило Зайцева – преимущественно отщепляется третичный атом водорода, хуже – вторичный, еще хуже – первичный. 18
 Реакция дегидрогалогенирования Правило Зайцева – преимущественно образуется тот алкен, при двойной связи которого имеется больше заместителей (то есть более замещенный алкен). 19
Реакция дегидрогалогенирования Правило Зайцева – преимущественно образуется тот алкен, при двойной связи которого имеется больше заместителей (то есть более замещенный алкен). 19
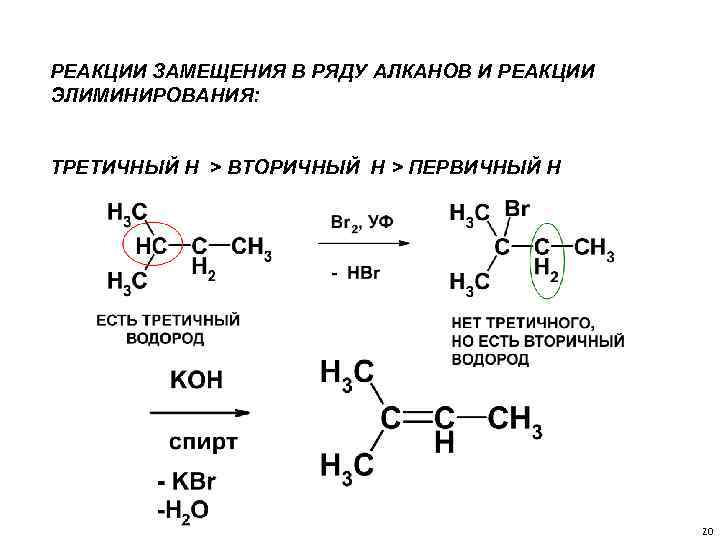 РЕАКЦИИ ЗАМЕЩЕНИЯ В РЯДУ АЛКАНОВ И РЕАКЦИИ ЭЛИМИНИРОВАНИЯ: ТРЕТИЧНЫЙ Н > ВТОРИЧНЫЙ Н > ПЕРВИЧНЫЙ Н 20
РЕАКЦИИ ЗАМЕЩЕНИЯ В РЯДУ АЛКАНОВ И РЕАКЦИИ ЭЛИМИНИРОВАНИЯ: ТРЕТИЧНЫЙ Н > ВТОРИЧНЫЙ Н > ПЕРВИЧНЫЙ Н 20
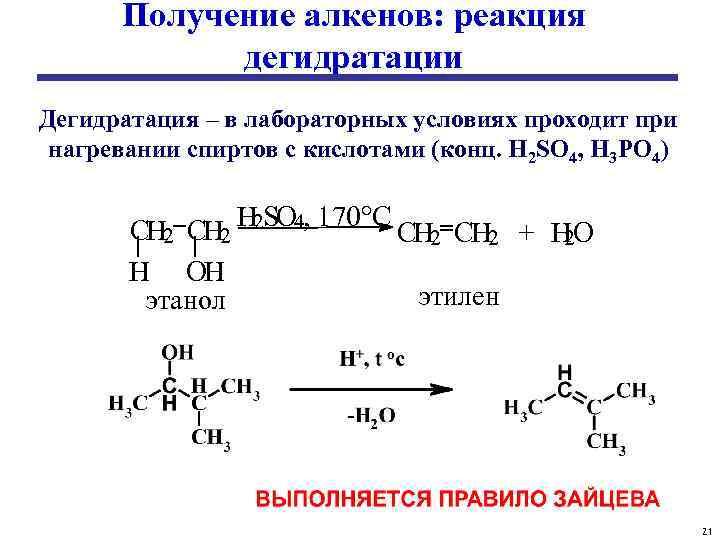 Получение алкенов: реакция дегидратации Дегидратация – в лабораторных условиях проходит при нагревании спиртов с кислотами (конц. H 2 SO 4, H 3 PO 4) H 2 SO 4, 170°C CH 2 + H O 2 H OH этилен этанол 21
Получение алкенов: реакция дегидратации Дегидратация – в лабораторных условиях проходит при нагревании спиртов с кислотами (конц. H 2 SO 4, H 3 PO 4) H 2 SO 4, 170°C CH 2 + H O 2 H OH этилен этанол 21
 Получение алкенов: дегидратация В промышленных условиях дегидратацию проводят пропуская пары спиртов над такими катализаторами, как Al 2 O 3, при высокой температуре. 22
Получение алкенов: дегидратация В промышленных условиях дегидратацию проводят пропуская пары спиртов над такими катализаторами, как Al 2 O 3, при высокой температуре. 22
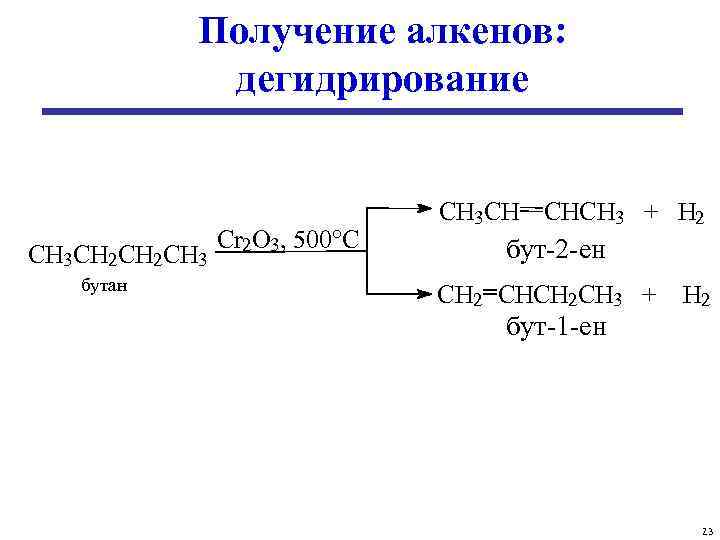 Получение алкенов: дегидрирование CH 3 CH 2 CH 3 бутан Cr 2 O 3, 500°C CH 3 CH CHCH 3 + H 2 бут-2 -ен CH 2 CHCH 2 CH 3 + H 2 бут-1 -ен 23
Получение алкенов: дегидрирование CH 3 CH 2 CH 3 бутан Cr 2 O 3, 500°C CH 3 CH CHCH 3 + H 2 бут-2 -ен CH 2 CHCH 2 CH 3 + H 2 бут-1 -ен 23
 ХИМИЧЕСКИЕ СВОЙСТВА АЛКЕНОВ АЛКЕНАМ ХАРАКТЕРНЫ РЕАКЦИИ ПРИСОЕДИНЕНИЯ 24
ХИМИЧЕСКИЕ СВОЙСТВА АЛКЕНОВ АЛКЕНАМ ХАРАКТЕРНЫ РЕАКЦИИ ПРИСОЕДИНЕНИЯ 24
 25
25
 • Наиболее характерные реакции – реакции электрофильного присоединения (Аd. E , от английских addition electrophilic). 26
• Наиболее характерные реакции – реакции электрофильного присоединения (Аd. E , от английских addition electrophilic). 26
 Электрофилы (Е+) – частицы с вакантной орбиталью. Простейший пример: протон Н+. Нуклеофилы (Nu-) – частицы с неподеленной электронной парой. Обычно – анионы (Cl-, Br- OH-), хотя нуклеофилом может быть и нейтральная молекула, содержащая кислород или азот (Н 2 О, NH 3, CH 3 OH). 27
Электрофилы (Е+) – частицы с вакантной орбиталью. Простейший пример: протон Н+. Нуклеофилы (Nu-) – частицы с неподеленной электронной парой. Обычно – анионы (Cl-, Br- OH-), хотя нуклеофилом может быть и нейтральная молекула, содержащая кислород или азот (Н 2 О, NH 3, CH 3 OH). 27
 28
28
 29
29
 • ПРИМЕРЫ РЕАКЦИЙ ЭЛЕКТРОФИЛНОГО ПРИСОЕДИНЕНИЯ: • ПРИСОЕДИНЕНИЕ ГАЛОГЕНОВОДОРОДОВ, ВОДЫ, ГАЛОГЕНОВ. 30
• ПРИМЕРЫ РЕАКЦИЙ ЭЛЕКТРОФИЛНОГО ПРИСОЕДИНЕНИЯ: • ПРИСОЕДИНЕНИЕ ГАЛОГЕНОВОДОРОДОВ, ВОДЫ, ГАЛОГЕНОВ. 30
 31
31
 Механизм электрофильного присоединения галогеноводородов 32
Механизм электрофильного присоединения галогеноводородов 32
 33
33
 Пояснение первой стадии 34
Пояснение первой стадии 34
 Пояснение первой стадии 35
Пояснение первой стадии 35
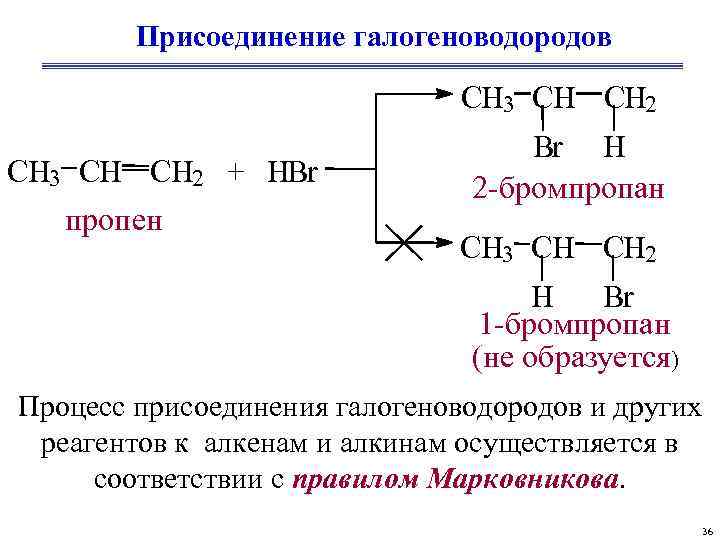 Присоединение галогеноводородов CH 3 CH CH 2 + HBr пропен Br H 2 -бромпропан CH 3 CH CH 2 H Br 1 -бромпропан (не образуется) Процесс присоединения галогеноводородов и других реагентов к алкенам и алкинам осуществляется в соответствии с правилом Марковникова. 36
Присоединение галогеноводородов CH 3 CH CH 2 + HBr пропен Br H 2 -бромпропан CH 3 CH CH 2 H Br 1 -бромпропан (не образуется) Процесс присоединения галогеноводородов и других реагентов к алкенам и алкинам осуществляется в соответствии с правилом Марковникова. 36
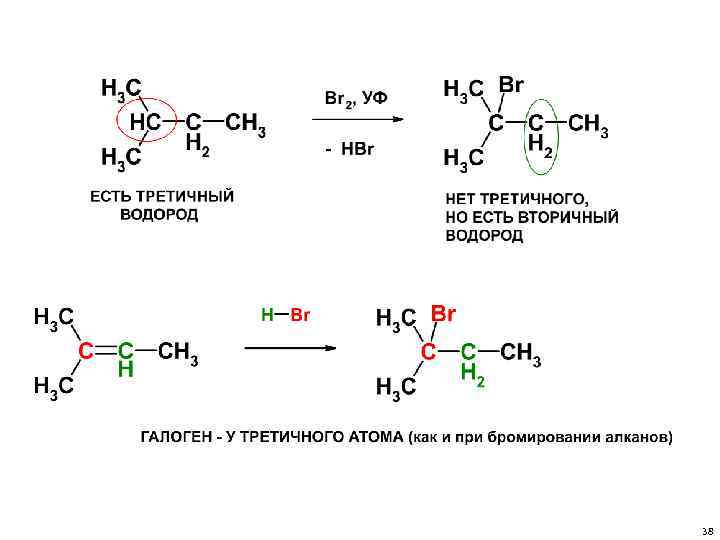
 • Правило Марковникова: в реакциях присоединения водород присоединяется к более гидрогенизированному атому углероду. • Иными словами: водород преимущественно оказывается у первичного атома углерода, а галоген (или другая группа) – у третичного атома углерода. 37
• Правило Марковникова: в реакциях присоединения водород присоединяется к более гидрогенизированному атому углероду. • Иными словами: водород преимущественно оказывается у первичного атома углерода, а галоген (или другая группа) – у третичного атома углерода. 37
 38
38
 Теоретическая интерпретация правила Марковникова 39
Теоретическая интерпретация правила Марковникова 39
 40
40
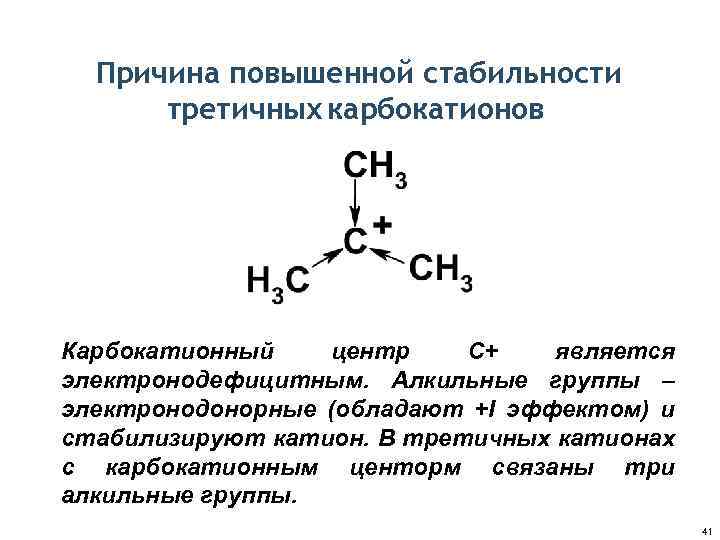 Причина повышенной стабильности третичных карбокатионов Карбокатионный центр С+ является электронодефицитным. Алкильные группы – электронодонорные (обладают +I эффектом) и стабилизируют катион. В третичных катионах с карбокатионным центорм связаны три алкильные группы. 41
Причина повышенной стабильности третичных карбокатионов Карбокатионный центр С+ является электронодефицитным. Алкильные группы – электронодонорные (обладают +I эффектом) и стабилизируют катион. В третичных катионах с карбокатионным центорм связаны три алкильные группы. 41
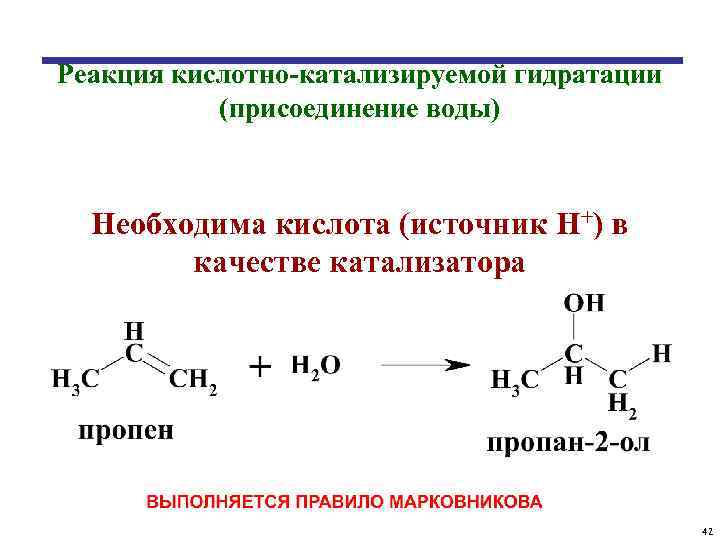 Реакция кислотно-катализируемой гидратации (присоединение воды) Необходима кислота (источник Н+) в качестве катализатора 42
Реакция кислотно-катализируемой гидратации (присоединение воды) Необходима кислота (источник Н+) в качестве катализатора 42
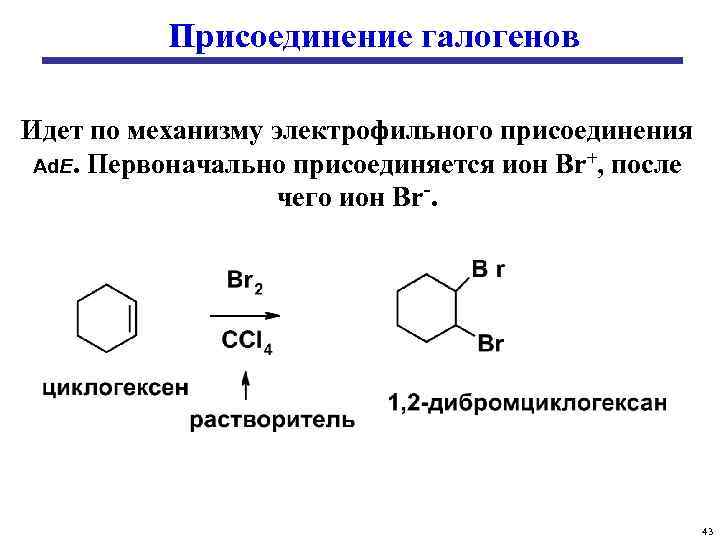 Присоединение галогенов Идет по механизму электрофильного присоединения Аd. Е. Первоначально присоединяется ион Br+, после чего ион Br-. 43
Присоединение галогенов Идет по механизму электрофильного присоединения Аd. Е. Первоначально присоединяется ион Br+, после чего ион Br-. 43
 КАЧЕСТВЕННАЯ РЕАКЦИЯ НА НЕНАСЫЩЕННЫЕ СОЕДИНЕНИЯ • ОБЕСЦВЕЧИВАНИЕ РАСТВОРА БРОМА (В ВОДЕ, CCl 4 и др. РАСТВОРИТЕЛЯХ) 44
КАЧЕСТВЕННАЯ РЕАКЦИЯ НА НЕНАСЫЩЕННЫЕ СОЕДИНЕНИЯ • ОБЕСЦВЕЧИВАНИЕ РАСТВОРА БРОМА (В ВОДЕ, CCl 4 и др. РАСТВОРИТЕЛЯХ) 44
 • РЕАКЦИИ АЛКЕНОВ, НЕ ОТНОСЯЩИЕСЯ К ЭЛЕКТРОФИЛЬНОМУ ПРИСОЕДИНЕНИЮ 45
• РЕАКЦИИ АЛКЕНОВ, НЕ ОТНОСЯЩИЕСЯ К ЭЛЕКТРОФИЛЬНОМУ ПРИСОЕДИНЕНИЮ 45
 КАТАЛИТИЧЕСКОЕ ГИДРИРОВАНИЕ 46
КАТАЛИТИЧЕСКОЕ ГИДРИРОВАНИЕ 46
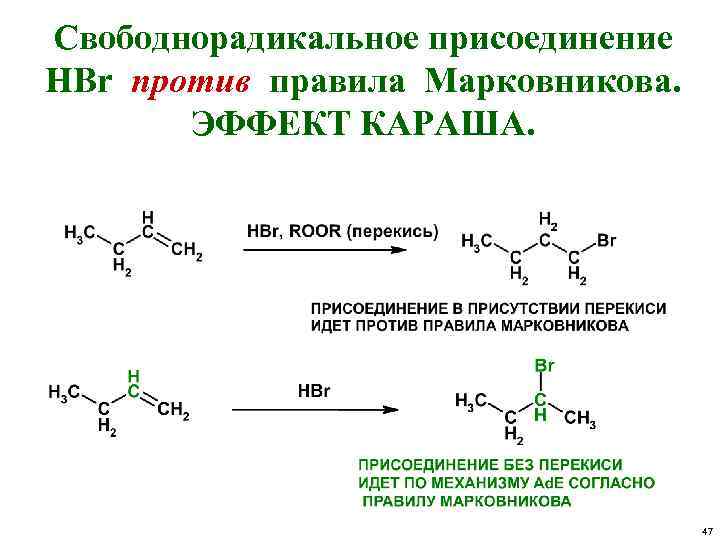 Свободнорадикальное присоединение HBr против правила Марковникова. ЭФФЕКТ КАРАША. 47
Свободнорадикальное присоединение HBr против правила Марковникова. ЭФФЕКТ КАРАША. 47
 ПРИМЕР ПЕРЕКИСИ 48
ПРИМЕР ПЕРЕКИСИ 48
 РЕАКЦИЯ ВАГНЕРА Окисление алкенов в цис-гликоли действием перманганата калия в щелочной среде. Реакция служит качественной реакцией на кратную связь (включая тройную). Признак протекания реакции – обесцвечивание розового раствора KMn. O 4 и выпадение бурого осадка Mn. O 2. ВАГНЕР Егорович (9. XII. 1849 – 27. XI. 1903) 49
РЕАКЦИЯ ВАГНЕРА Окисление алкенов в цис-гликоли действием перманганата калия в щелочной среде. Реакция служит качественной реакцией на кратную связь (включая тройную). Признак протекания реакции – обесцвечивание розового раствора KMn. O 4 и выпадение бурого осадка Mn. O 2. ВАГНЕР Егорович (9. XII. 1849 – 27. XI. 1903) 49
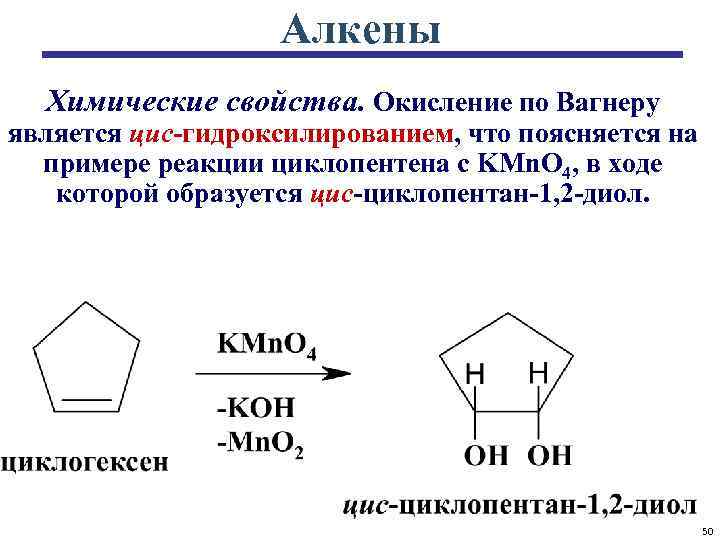 Алкены Химические свойства. Окисление по Вагнеру является цис-гидроксилированием, что поясняется на примере реакции циклопентена с KMn. O 4, в ходе которой образуется цис-циклопентан-1, 2 -диол. 50
Алкены Химические свойства. Окисление по Вагнеру является цис-гидроксилированием, что поясняется на примере реакции циклопентена с KMn. O 4, в ходе которой образуется цис-циклопентан-1, 2 -диол. 50
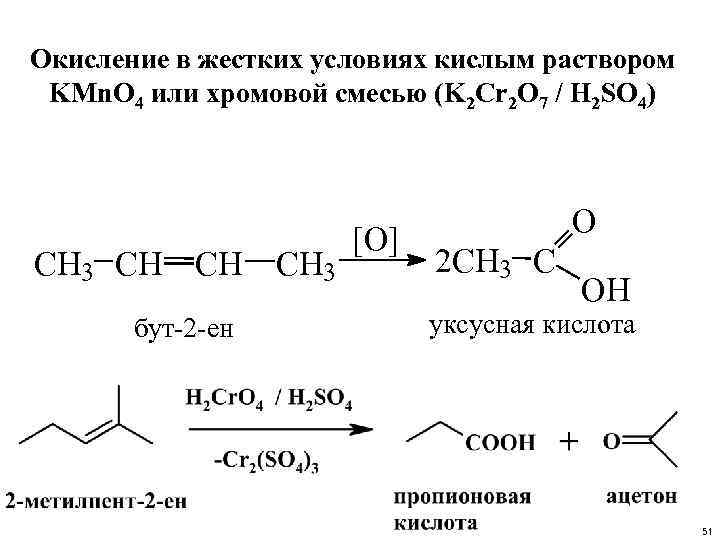 Окисление в жестких условиях кислым раствором KMn. O 4 или хромовой смесью (K 2 Cr 2 O 7 / H 2 SO 4) CH 3 CH CH CH 3 бут-2 -ен [O] O 2 CH 3 C OH уксусная кислота 51
Окисление в жестких условиях кислым раствором KMn. O 4 или хромовой смесью (K 2 Cr 2 O 7 / H 2 SO 4) CH 3 CH CH CH 3 бут-2 -ен [O] O 2 CH 3 C OH уксусная кислота 51
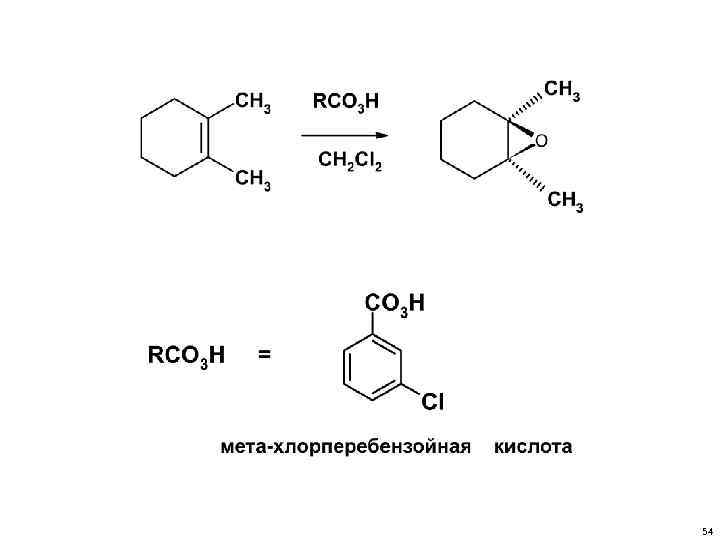
 Реакция эпоксидирования – окисление алкена до эпоксида Окись этилена производят путем каталитического окисления этилена воздухом на серебряной сетке. 52
Реакция эпоксидирования – окисление алкена до эпоксида Окись этилена производят путем каталитического окисления этилена воздухом на серебряной сетке. 52
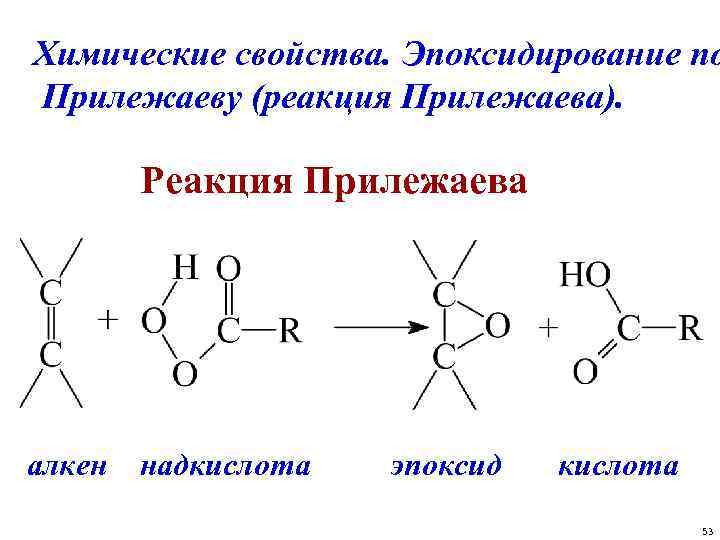 Химические свойства. Эпоксидирование по Прилежаеву (реакция Прилежаева). Реакция Прилежаева алкен надкислота эпоксид кислота 53
Химические свойства. Эпоксидирование по Прилежаеву (реакция Прилежаева). Реакция Прилежаева алкен надкислота эпоксид кислота 53
 54
54
 Гидрирование алкенов Происходит в присутствии катализаторов на основе Ni, Pd, Pt 55
Гидрирование алкенов Происходит в присутствии катализаторов на основе Ni, Pd, Pt 55
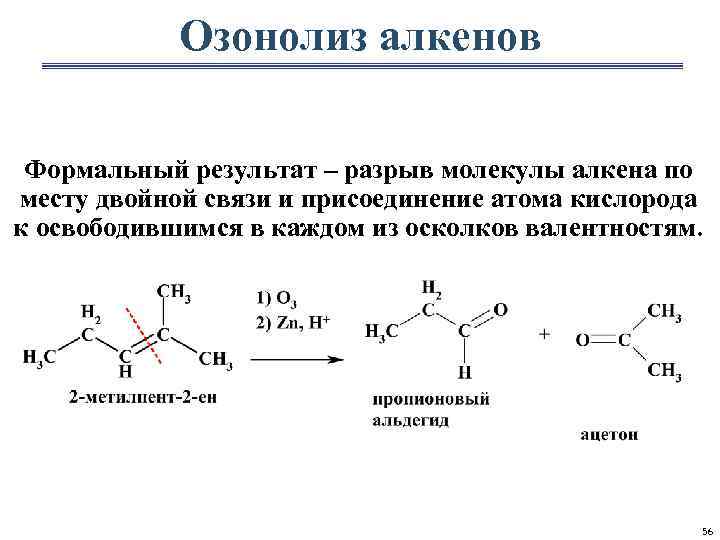 Озонолиз алкенов Формальный результат – разрыв молекулы алкена по месту двойной связи и присоединение атома кислорода к освободившимся в каждом из осколков валентностям. 56
Озонолиз алкенов Формальный результат – разрыв молекулы алкена по месту двойной связи и присоединение атома кислорода к освободившимся в каждом из осколков валентностям. 56
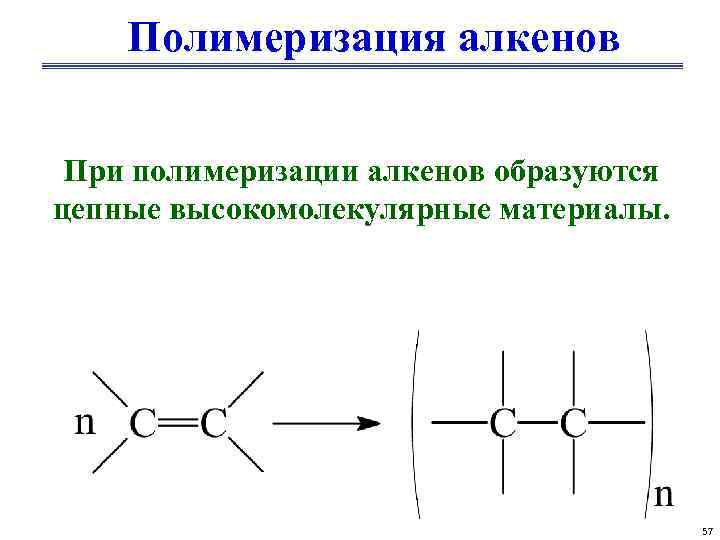 Полимеризация алкенов При полимеризации алкенов образуются цепные высокомолекулярные материалы. 57
Полимеризация алкенов При полимеризации алкенов образуются цепные высокомолекулярные материалы. 57
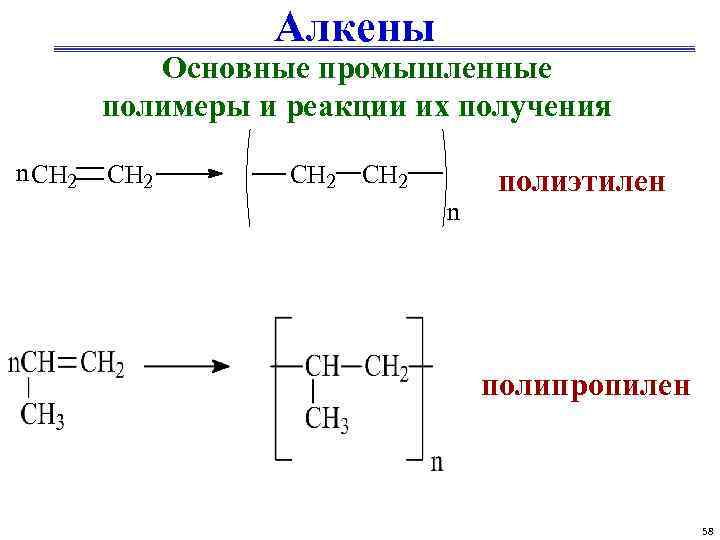 Алкены Основные промышленные полимеры и реакции их получения n CH 2 n полиэтилен полипропилен 58
Алкены Основные промышленные полимеры и реакции их получения n CH 2 n полиэтилен полипропилен 58
 59
59


