алкены 1..ppt
- Количество слайдов: 20
 АЛКЕНЫ – НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ. ПОЛУЧЕНИЕ, ХИМИЧЕСКИЕ СВОЙСТВА И ПРИМЕНЕНИЕ.
АЛКЕНЫ – НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ. ПОЛУЧЕНИЕ, ХИМИЧЕСКИЕ СВОЙСТВА И ПРИМЕНЕНИЕ.
 Учебная цель: изучить способы получения; химические свойства; применение алкенов на примере непредельного углеводорода этилена
Учебная цель: изучить способы получения; химические свойства; применение алкенов на примере непредельного углеводорода этилена
 Эпиграф к уроку «Границ научному познанию и предсказанию предвидеть невозможно» Д. И. Менделеев
Эпиграф к уроку «Границ научному познанию и предсказанию предвидеть невозможно» Д. И. Менделеев
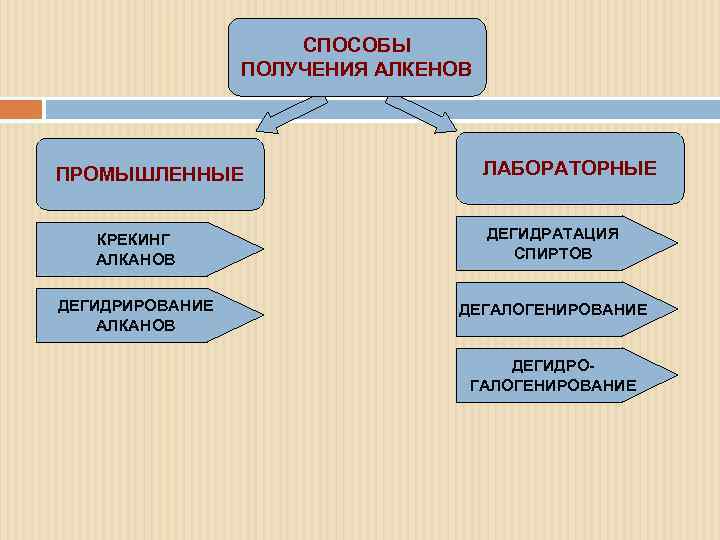 СПОСОБЫ ПОЛУЧЕНИЯ АЛКЕНОВ ПРОМЫШЛЕННЫЕ ЛАБОРАТОРНЫЕ КРЕКИНГ АЛКАНОВ ДЕГИДРАТАЦИЯ СПИРТОВ ДЕГИДРИРОВАНИЕ АЛКАНОВ ДЕГАЛОГЕНИРОВАНИЕ ДЕГИДРОГАЛОГЕНИРОВАНИЕ
СПОСОБЫ ПОЛУЧЕНИЯ АЛКЕНОВ ПРОМЫШЛЕННЫЕ ЛАБОРАТОРНЫЕ КРЕКИНГ АЛКАНОВ ДЕГИДРАТАЦИЯ СПИРТОВ ДЕГИДРИРОВАНИЕ АЛКАНОВ ДЕГАЛОГЕНИРОВАНИЕ ДЕГИДРОГАЛОГЕНИРОВАНИЕ
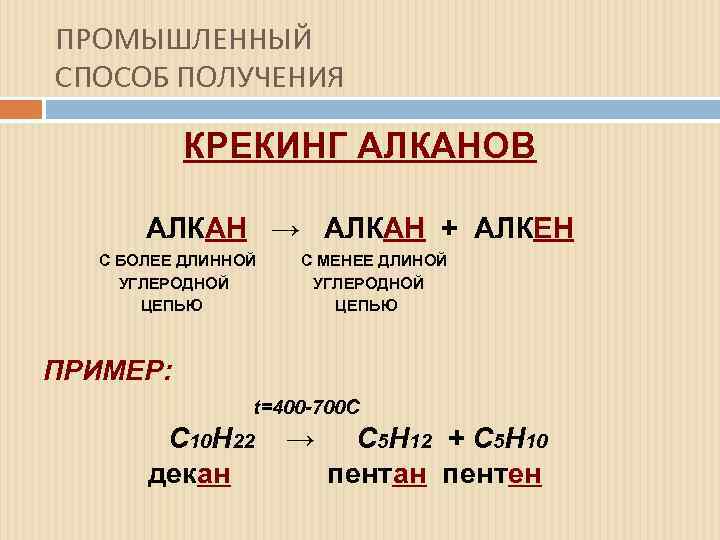 ПРОМЫШЛЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ КРЕКИНГ АЛКАНОВ АЛКАН → АЛКАН + АЛКЕН АЛК АЛК С БОЛЕЕ ДЛИННОЙ УГЛЕРОДНОЙ ЦЕПЬЮ С МЕНЕЕ ДЛИНОЙ УГЛЕРОДНОЙ ЦЕПЬЮ ПРИМЕР: t=400 -700 C С 10 Н 22 декан дек → C 5 H 12 + C 5 H 10 пентан пентен пент
ПРОМЫШЛЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ КРЕКИНГ АЛКАНОВ АЛКАН → АЛКАН + АЛКЕН АЛК АЛК С БОЛЕЕ ДЛИННОЙ УГЛЕРОДНОЙ ЦЕПЬЮ С МЕНЕЕ ДЛИНОЙ УГЛЕРОДНОЙ ЦЕПЬЮ ПРИМЕР: t=400 -700 C С 10 Н 22 декан дек → C 5 H 12 + C 5 H 10 пентан пентен пент
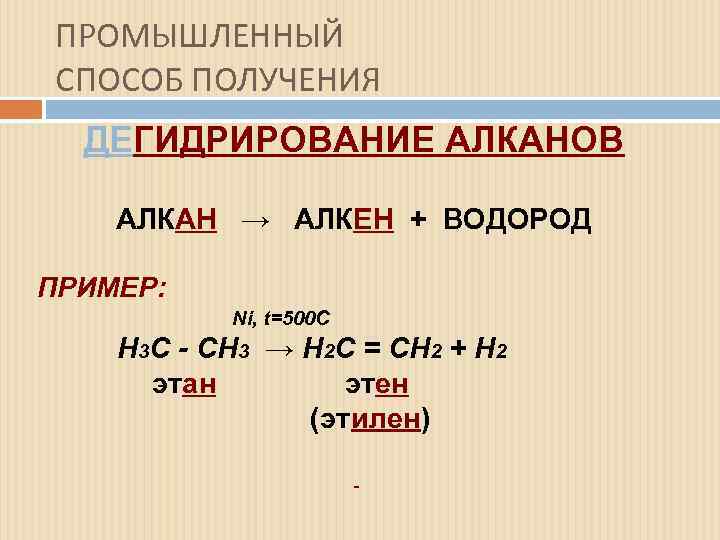 ПРОМЫШЛЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГИДРИРОВАНИЕ АЛКАНОВ АЛКАН → АЛКЕН + ВОДОРОД АЛК ПРИМЕР: Ni, t=500 C Н 3 С - СН 3 → Н 2 С = СН 2 + Н 2 этан этен эт эт (этилен) (эт
ПРОМЫШЛЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГИДРИРОВАНИЕ АЛКАНОВ АЛКАН → АЛКЕН + ВОДОРОД АЛК ПРИМЕР: Ni, t=500 C Н 3 С - СН 3 → Н 2 С = СН 2 + Н 2 этан этен эт эт (этилен) (эт
 ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГИДРАТАЦИЯ СПИРТОВ СПИРТ → АЛКЕН + ВОДА АЛК ПРИМЕР: t≥ 140 C, Н Н Н 2 SO 4(конц. ) Н-С – С-Н → Н 2 С = СН 2 + Н 2 О Н ОН этен эт (этилен) (эт
ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГИДРАТАЦИЯ СПИРТОВ СПИРТ → АЛКЕН + ВОДА АЛК ПРИМЕР: t≥ 140 C, Н Н Н 2 SO 4(конц. ) Н-С – С-Н → Н 2 С = СН 2 + Н 2 О Н ОН этен эт (этилен) (эт
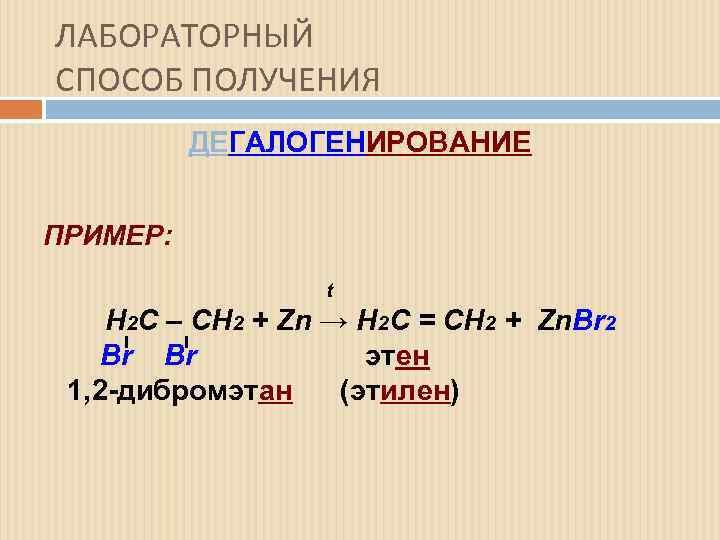 ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГАЛОГЕНИРОВАНИЕ ПРИМЕР: t Н 2 С – СН 2 + Zn → Н 2 С = СН 2 + Zn. Br 2 Zn Br Br этен эт 1, 2 -дибромэтан (этилен) 1, 2 -дибромэт (эт
ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГАЛОГЕНИРОВАНИЕ ПРИМЕР: t Н 2 С – СН 2 + Zn → Н 2 С = СН 2 + Zn. Br 2 Zn Br Br этен эт 1, 2 -дибромэтан (этилен) 1, 2 -дибромэт (эт
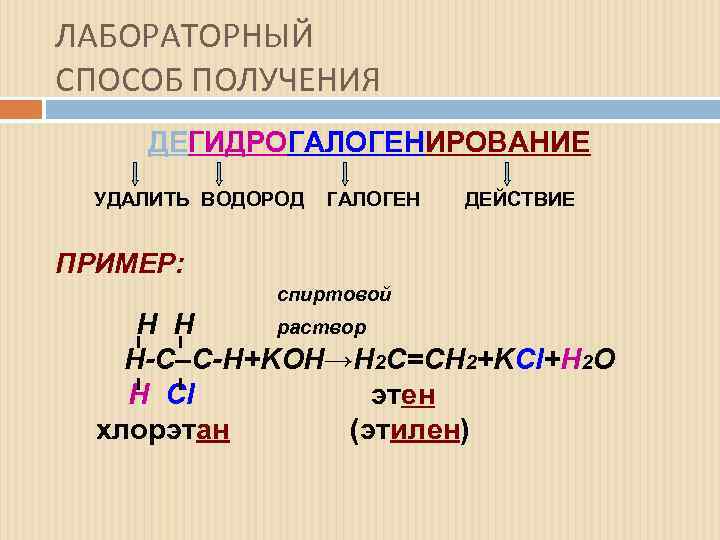 ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГИДРОГАЛОГЕНИРОВАНИЕ УДАЛИТЬ ВОДОРОД ГАЛОГЕН ДЕЙСТВИЕ ПРИМЕР: спиртовой H H раствор Н-С–С-Н+KOH→Н 2 С=СН 2+KCl+H 2 O +K Н Cl этен эт хлорэтан (этилен) хлорэт (эт
ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГИДРОГАЛОГЕНИРОВАНИЕ УДАЛИТЬ ВОДОРОД ГАЛОГЕН ДЕЙСТВИЕ ПРИМЕР: спиртовой H H раствор Н-С–С-Н+KOH→Н 2 С=СН 2+KCl+H 2 O +K Н Cl этен эт хлорэтан (этилен) хлорэт (эт
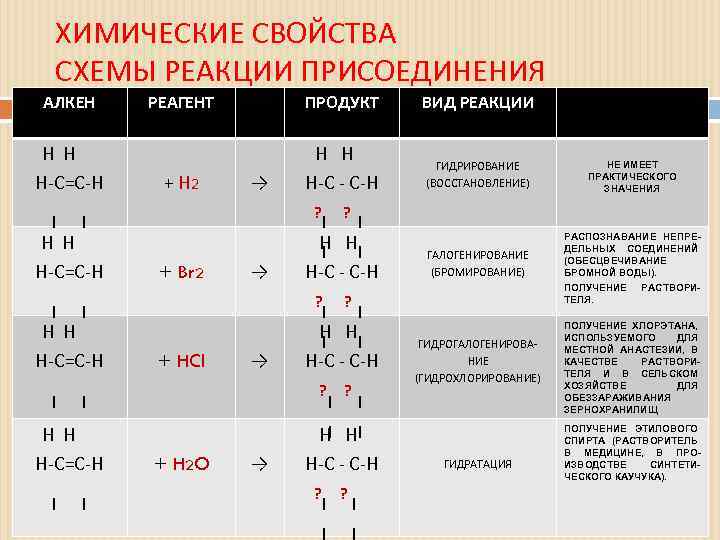 ХИМИЧЕСКИЕ СВОЙСТВА СХЕМЫ РЕАКЦИИ ПРИСОЕДИНЕНИЯ АЛКЕН Н Н Н-С=С-Н РЕАГЕНТ ПРОДУКТ ВИД РЕАКЦИИ Применение реродуктов + Н 2 Н Н Н-С - С-Н ГИДРИРОВАНИЕ (ВОССТАНОВЛЕНИЕ) НЕ ИМЕЕТ ПРАКТИЧЕСКОГО ЗНАЧЕНИЯ ГАЛОГЕНИРОВАНИЕ (БРОМИРОВАНИЕ) РАСПОЗНАВАНИЕ НЕПРЕДЕЛЬНЫХ СОЕДИНЕНИЙ (ОБЕСЦВЕЧИВАНИЕ БРОМНОЙ ВОДЫ). ПОЛУЧЕНИЕ РАСТВОРИТЕЛЯ. → ? Н Н Н-С=С-Н + Br 2 → Н Н Н-С - С-Н ? Н Н Н-С=С-Н + HCl → + H 2 O → ? Н Н Н-С - С-Н ? Н Н Н-С=С-Н ? ? Н Н Н-С - С-Н ? ? ГИДРОГАЛОГЕНИРОВАНИЕ (ГИДРОХЛОРИРОВАНИЕ) ГИДРАТАЦИЯ ПОЛУЧЕНИЕ ХЛОРЭТАНА, ИСПОЛЬЗУЕМОГО ДЛЯ МЕСТНОЙ АНАСТЕЗИИ, В КАЧЕСТВЕ РАСТВОРИТЕЛЯ И В СЕЛЬСКОМ ХОЗЯЙСТВЕ ДЛЯ ОБЕЗЗАРАЖИВАНИЯ ЗЕРНОХРАНИЛИЩ ПОЛУЧЕНИЕ ЭТИЛОВОГО СПИРТА (РАСТВОРИТЕЛЬ В МЕДИЦИНЕ, В ПРОИЗВОДСТВЕ СИНТЕТИЧЕСКОГО КАУЧУКА).
ХИМИЧЕСКИЕ СВОЙСТВА СХЕМЫ РЕАКЦИИ ПРИСОЕДИНЕНИЯ АЛКЕН Н Н Н-С=С-Н РЕАГЕНТ ПРОДУКТ ВИД РЕАКЦИИ Применение реродуктов + Н 2 Н Н Н-С - С-Н ГИДРИРОВАНИЕ (ВОССТАНОВЛЕНИЕ) НЕ ИМЕЕТ ПРАКТИЧЕСКОГО ЗНАЧЕНИЯ ГАЛОГЕНИРОВАНИЕ (БРОМИРОВАНИЕ) РАСПОЗНАВАНИЕ НЕПРЕДЕЛЬНЫХ СОЕДИНЕНИЙ (ОБЕСЦВЕЧИВАНИЕ БРОМНОЙ ВОДЫ). ПОЛУЧЕНИЕ РАСТВОРИТЕЛЯ. → ? Н Н Н-С=С-Н + Br 2 → Н Н Н-С - С-Н ? Н Н Н-С=С-Н + HCl → + H 2 O → ? Н Н Н-С - С-Н ? Н Н Н-С=С-Н ? ? Н Н Н-С - С-Н ? ? ГИДРОГАЛОГЕНИРОВАНИЕ (ГИДРОХЛОРИРОВАНИЕ) ГИДРАТАЦИЯ ПОЛУЧЕНИЕ ХЛОРЭТАНА, ИСПОЛЬЗУЕМОГО ДЛЯ МЕСТНОЙ АНАСТЕЗИИ, В КАЧЕСТВЕ РАСТВОРИТЕЛЯ И В СЕЛЬСКОМ ХОЗЯЙСТВЕ ДЛЯ ОБЕЗЗАРАЖИВАНИЯ ЗЕРНОХРАНИЛИЩ ПОЛУЧЕНИЕ ЭТИЛОВОГО СПИРТА (РАСТВОРИТЕЛЬ В МЕДИЦИНЕ, В ПРОИЗВОДСТВЕ СИНТЕТИЧЕСКОГО КАУЧУКА).
 РЕАКЦИЯ ПОЛИМЕРИЗАЦИИ Это процесс соединения одинаковых молекул в более крупные. ПРИМЕР: n CH 2=CH 2 (-CH 2 -)n этилен полиэтилен (мономер) (полимер) n – степень полимеризации, показывает число молекул, вступивших в реакцию -CH 2 - структурное звено
РЕАКЦИЯ ПОЛИМЕРИЗАЦИИ Это процесс соединения одинаковых молекул в более крупные. ПРИМЕР: n CH 2=CH 2 (-CH 2 -)n этилен полиэтилен (мономер) (полимер) n – степень полимеризации, показывает число молекул, вступивших в реакцию -CH 2 - структурное звено
 РЕАКЦИИ ОКИСЛЕНИЯ ГОРЕНИЕ АЛКЕНОВ ПРИМЕР: 2 С 2 Н 6 + 7 О 2 4 СО 2 + 6 Н 2 О
РЕАКЦИИ ОКИСЛЕНИЯ ГОРЕНИЕ АЛКЕНОВ ПРИМЕР: 2 С 2 Н 6 + 7 О 2 4 СО 2 + 6 Н 2 О
 РЕАКЦИИ ОКИСЛЕНИЯ МЯГКОЕ ОКИСЛЕНИЕ – ВЗАИМОДЕЙСТВИЕ С РАСТВОРОМ ПЕРМАНАГАНАТА КАЛИЯ (реакция Е. Е. Вагнера) Н 2 С=СН 2 + [O] + H 2 O H 2 C - CH 2 OH OH этиленгликоль (этандиол-1, 2) ! Качественная реакция на непредельность углеводорода – на кратную связь.
РЕАКЦИИ ОКИСЛЕНИЯ МЯГКОЕ ОКИСЛЕНИЕ – ВЗАИМОДЕЙСТВИЕ С РАСТВОРОМ ПЕРМАНАГАНАТА КАЛИЯ (реакция Е. Е. Вагнера) Н 2 С=СН 2 + [O] + H 2 O H 2 C - CH 2 OH OH этиленгликоль (этандиол-1, 2) ! Качественная реакция на непредельность углеводорода – на кратную связь.
 Применение этилена Свойство 1. Полимеризация 2. Галогенирование 3. Гидрогалогенирование Применение Производство полиэтилена, пластмасс Получение растворителей Для местная анестезия, получения растворителей, в с/х для обеззараживания зернохранилищ Пример
Применение этилена Свойство 1. Полимеризация 2. Галогенирование 3. Гидрогалогенирование Применение Производство полиэтилена, пластмасс Получение растворителей Для местная анестезия, получения растворителей, в с/х для обеззараживания зернохранилищ Пример
 Свойство 4. Гидратация 5. Окисление раствором KMn. O 4 6. Особое свойство этилена: Применение Получение этилового спирта, используемого как растворитель, анти-септик в медицине , в производстве синтетического каучука Получение антифризов, тормозных жидкостей, в производстве пластмасс Этилен ускоряет созревание плодов Пример
Свойство 4. Гидратация 5. Окисление раствором KMn. O 4 6. Особое свойство этилена: Применение Получение этилового спирта, используемого как растворитель, анти-септик в медицине , в производстве синтетического каучука Получение антифризов, тормозных жидкостей, в производстве пластмасс Этилен ускоряет созревание плодов Пример
 СИНКВЕЙН 1 строка – имя существительное (тема синквейна) 2 строка – два прилагательных (раскрывающие тему синквейна) 3 строка – три глагола (описывают действия) 4 строка – фраза или предложение (высказывают своё отношение к теме) 5 строка – синоним (слово-резюме)
СИНКВЕЙН 1 строка – имя существительное (тема синквейна) 2 строка – два прилагательных (раскрывающие тему синквейна) 3 строка – три глагола (описывают действия) 4 строка – фраза или предложение (высказывают своё отношение к теме) 5 строка – синоним (слово-резюме)
 Ответьте, пожалуйста, на следующие вопросы: 1. 2. 3. 4. 5. 6. 7. Какие углеводороды называются алкенами? Какова общая формула алкенов? Какова структурная формула первого представителя гомологического ряда алкенов? Назовите его. Почему в отличие от алканов алкены в природе практически не встречаются? Какие способы получения алкенов вы знаете? Каким лабораторным способом можно получить алкены? Какие химические свойства обуславливает наличие кратной (двойной) связи в молекулах алкенов? Для чего используют алкены?
Ответьте, пожалуйста, на следующие вопросы: 1. 2. 3. 4. 5. 6. 7. Какие углеводороды называются алкенами? Какова общая формула алкенов? Какова структурная формула первого представителя гомологического ряда алкенов? Назовите его. Почему в отличие от алканов алкены в природе практически не встречаются? Какие способы получения алкенов вы знаете? Каким лабораторным способом можно получить алкены? Какие химические свойства обуславливает наличие кратной (двойной) связи в молекулах алкенов? Для чего используют алкены?
 1. 2. 3. 4. 5. Этилен Ненасыщенный, активный Горит, обесцвечивает, присоединяет Этилен – представитель непредельных углеводородов Алкен
1. 2. 3. 4. 5. Этилен Ненасыщенный, активный Горит, обесцвечивает, присоединяет Этилен – представитель непредельных углеводородов Алкен
 ДОМАШНЕЕ ЗАДАНИЕ параграф 4, № 5 -7 Оценка « 5» : Составить цепочку превращений, используя материал по темам «Алканы» и «Алкены»
ДОМАШНЕЕ ЗАДАНИЕ параграф 4, № 5 -7 Оценка « 5» : Составить цепочку превращений, используя материал по темам «Алканы» и «Алкены»
 СПАСИБО ЗА РАБОТУ!
СПАСИБО ЗА РАБОТУ!


