 АЛКЕНЫ
АЛКЕНЫ
 Гомологический ряд этилена: Cn. H 2 n - общая формула C 2 H 4 – этен (этилен) C 3 H 6 – пропен (пропилен) C 4 H 8 - бутен C 5 H 10 - пентен C 6 H 12 - гексен C 7 H 14 - гептен C 8 H 16 - октен C 9 H 18 - нонен
Гомологический ряд этилена: Cn. H 2 n - общая формула C 2 H 4 – этен (этилен) C 3 H 6 – пропен (пропилен) C 4 H 8 - бутен C 5 H 10 - пентен C 6 H 12 - гексен C 7 H 14 - гептен C 8 H 16 - октен C 9 H 18 - нонен
 Изомерия:
Изомерия:
 Получение алкенов 1) ДЕГИДРИРОВАНИЕ АЛКАНОВ АЛКАН → АЛКЕН + ВОДОРОД Ni, t=500 C Н 3 С - СН 3 → Н 2 С = СН 2 + Н 2 этан этен (этилен) 2) Деполимеризация этилена: t (-CH 2 -)n → n CH 2=CH 2 полиэтилен (мономер) (полимер)
Получение алкенов 1) ДЕГИДРИРОВАНИЕ АЛКАНОВ АЛКАН → АЛКЕН + ВОДОРОД Ni, t=500 C Н 3 С - СН 3 → Н 2 С = СН 2 + Н 2 этан этен (этилен) 2) Деполимеризация этилена: t (-CH 2 -)n → n CH 2=CH 2 полиэтилен (мономер) (полимер)
 ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ 3) ДЕГИДРАТАЦИЯ СПИРТОВ СПИРТ → АЛКЕН + ВОДА Н Н Н 2 SO 4(конц. ) t≥ 140 C, Н-С – С-Н Н → Н 2 С = СН 2 + Н 2 О этилен ОН 4) ДЕГАЛОГЕНИРОВАНИЕ дигалогензамещенных алканов t Н 2 С – СН 2 + Zn → Н 2 С = СН 2 + Zn. Br 2 (этилен) Br Br 1, 2 -дибромэтан
ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ 3) ДЕГИДРАТАЦИЯ СПИРТОВ СПИРТ → АЛКЕН + ВОДА Н Н Н 2 SO 4(конц. ) t≥ 140 C, Н-С – С-Н Н → Н 2 С = СН 2 + Н 2 О этилен ОН 4) ДЕГАЛОГЕНИРОВАНИЕ дигалогензамещенных алканов t Н 2 С – СН 2 + Zn → Н 2 С = СН 2 + Zn. Br 2 (этилен) Br Br 1, 2 -дибромэтан
 5) ДЕГИДРОГАЛОГЕНИРОВАНИЕ H H Н-С –С-Н+KOH→Н 2 С=СН 2+KCl+H 2 O Спирт. р-р этен Н Cl (этилен) хлорэтан
5) ДЕГИДРОГАЛОГЕНИРОВАНИЕ H H Н-С –С-Н+KOH→Н 2 С=СН 2+KCl+H 2 O Спирт. р-р этен Н Cl (этилен) хлорэтан
 Крекинг нефтепродуктов:
Крекинг нефтепродуктов:
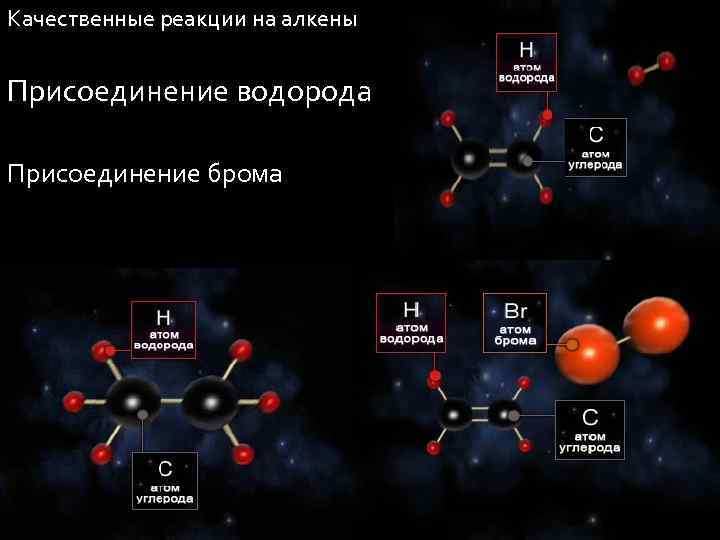 Качественные реакции на алкены Присоединение водорода Присоединение брома Клок Г. Д. учитель химии г. Нижневартовск
Качественные реакции на алкены Присоединение водорода Присоединение брома Клок Г. Д. учитель химии г. Нижневартовск
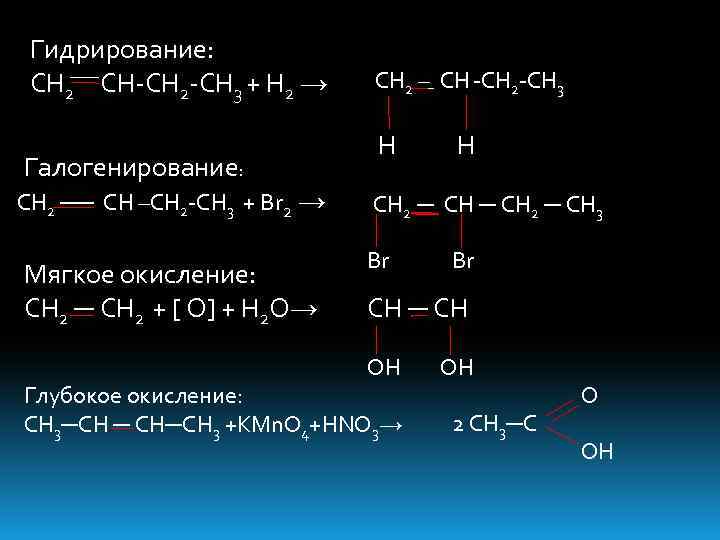 Гидрирование: CH 2 CH-CH 2 -CH 3 + H 2 → Галогенирование: CH 2 ── CH –CH 2 -CH 3 + Br 2 → Мягкое окисление: CH 2 ─ CH 2 + [ O] + H 2 O→ CH 2 – CH -CH 2 -CH 3 Н Н CH 2 ─ CH 3 Br Br CH ─ CH OH Глубокое окисление: CH 3─CH ─ CH─CH 3 +KMn. O 4+HNO 3→ OH 2 CH 3─C O OH
Гидрирование: CH 2 CH-CH 2 -CH 3 + H 2 → Галогенирование: CH 2 ── CH –CH 2 -CH 3 + Br 2 → Мягкое окисление: CH 2 ─ CH 2 + [ O] + H 2 O→ CH 2 – CH -CH 2 -CH 3 Н Н CH 2 ─ CH 3 Br Br CH ─ CH OH Глубокое окисление: CH 3─CH ─ CH─CH 3 +KMn. O 4+HNO 3→ OH 2 CH 3─C O OH
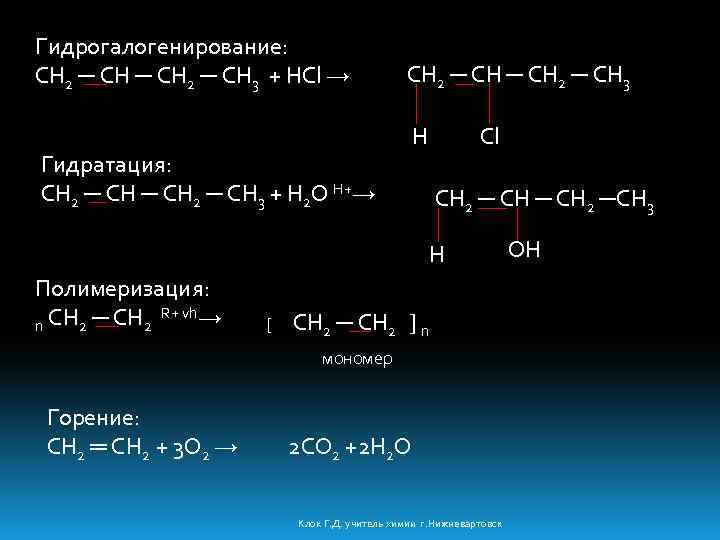 Гидрогалогенирование: CH 2 ─ CH 3 + HCl → CH 2 ─ CH 3 Гидратация: CH 2 ─ CH 3 + H 2 O H+→ H Cl CH 2 ─CH 3 H Полимеризация: R+ vh→ n CH 2 ─ CH 2 [ CH 2 ─ CH 2 ] n мономер Горение: CH 2 ═ CH 2 + 3 O 2 → 2 CO 2 +2 H 2 O Клок Г. Д. учитель химии г. Нижневартовск OH
Гидрогалогенирование: CH 2 ─ CH 3 + HCl → CH 2 ─ CH 3 Гидратация: CH 2 ─ CH 3 + H 2 O H+→ H Cl CH 2 ─CH 3 H Полимеризация: R+ vh→ n CH 2 ─ CH 2 [ CH 2 ─ CH 2 ] n мономер Горение: CH 2 ═ CH 2 + 3 O 2 → 2 CO 2 +2 H 2 O Клок Г. Д. учитель химии г. Нижневартовск OH
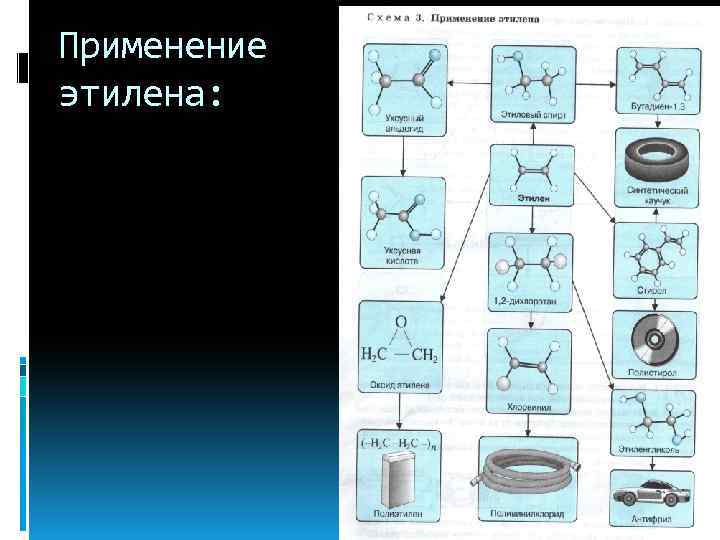 Применение этилена:
Применение этилена:
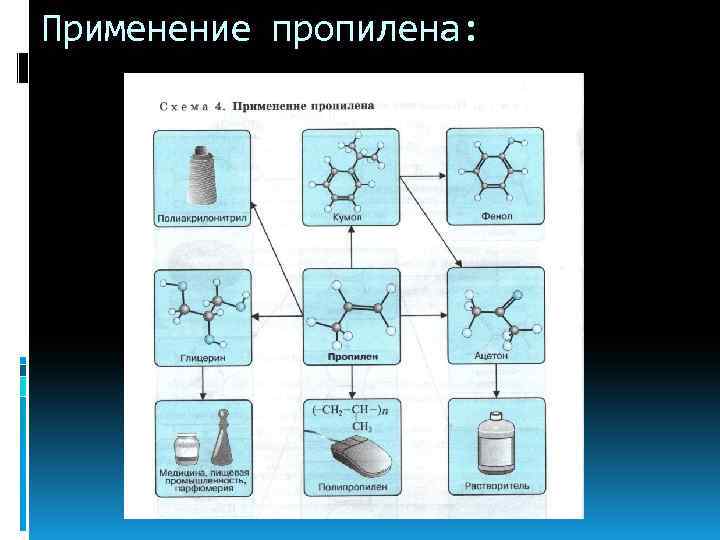 Применение пропилена:
Применение пропилена: