Алкены_ОБщая характеристика_Методы получения.pptx
- Количество слайдов: 20
 Алкены – это непредельные ациклические углеводороды, в молекуле которых содержится одна двойная связь этиленовые углеводороды, олефины
Алкены – это непредельные ациклические углеводороды, в молекуле которых содержится одна двойная связь этиленовые углеводороды, олефины
 Два атома углерода в молекуле алкена, которые участвует в образовании двойной связи, – атомы sp 2−C; Все атомы углерода в молекуле алкена, которые не участвуют в образовании двойной связи, – атомы sp 3−C; Простейший представитель – этилен или этен: развернутая структурная формула, построенная с учетом реальной геометрии молекулы Н sp 2 Н 120° Н 0, 134 нм Н краткая структурная формула СН 2= СН 2, брутто-формула С 2 Н 4; Общая формула – Cn. H 2 n, где n ≥ 2
Два атома углерода в молекуле алкена, которые участвует в образовании двойной связи, – атомы sp 2−C; Все атомы углерода в молекуле алкена, которые не участвуют в образовании двойной связи, – атомы sp 3−C; Простейший представитель – этилен или этен: развернутая структурная формула, построенная с учетом реальной геометрии молекулы Н sp 2 Н 120° Н 0, 134 нм Н краткая структурная формула СН 2= СН 2, брутто-формула С 2 Н 4; Общая формула – Cn. H 2 n, где n ≥ 2
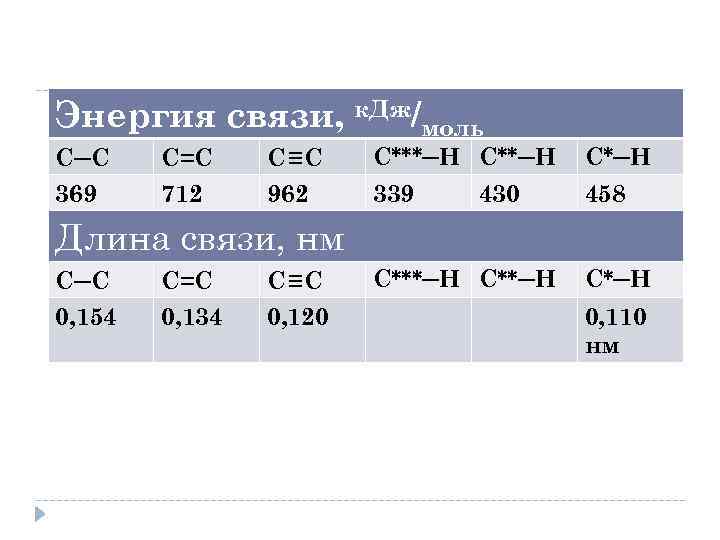 Энергия связи, к. Дж/моль С─С 369 С=С 712 С≡С 962 С***─Н С*─Н 339 458 430 Длина связи, нм С─С 0, 154 С=С 0, 134 С≡С 0, 120 С***─Н С*─Н 0, 110 нм
Энергия связи, к. Дж/моль С─С 369 С=С 712 С≡С 962 С***─Н С*─Н 339 458 430 Длина связи, нм С─С 0, 154 С=С 0, 134 С≡С 0, 120 С***─Н С*─Н 0, 110 нм
 Изомерия, номенклатура I. Структурная изомерия 1. Изомерия углеродного скелета (С 4 Н 8) СН 2=СН─СН 2─СН 3 бутен-1 СН 2=С─СН 3 │ СН 3 2 -метилпропен или изобутен СН 2=СН─СН 2─СН 3 пентен-1 СН 2=СН─СН─СН 3 СН 2=С─СН 2─СН 3 │ │ СН 3 3 -метилбутен-1 2 -метилбутен-1
Изомерия, номенклатура I. Структурная изомерия 1. Изомерия углеродного скелета (С 4 Н 8) СН 2=СН─СН 2─СН 3 бутен-1 СН 2=С─СН 3 │ СН 3 2 -метилпропен или изобутен СН 2=СН─СН 2─СН 3 пентен-1 СН 2=СН─СН─СН 3 СН 2=С─СН 2─СН 3 │ │ СН 3 3 -метилбутен-1 2 -метилбутен-1
 Изомерия, номенклатура I. Структурная изомерия 2. Изомерия положения двойной связи (С 4 Н 8) СН 2=СН─СН 2─СН 3 бутен-1 СН 3─СН=СН─СН 3 бутен-2 СН 2=СН─СН 2─СН 3 пентен-1 СН 3─СН=СН─СН 2─СН 3 пентен-2
Изомерия, номенклатура I. Структурная изомерия 2. Изомерия положения двойной связи (С 4 Н 8) СН 2=СН─СН 2─СН 3 бутен-1 СН 3─СН=СН─СН 3 бутен-2 СН 2=СН─СН 2─СН 3 пентен-1 СН 3─СН=СН─СН 2─СН 3 пентен-2
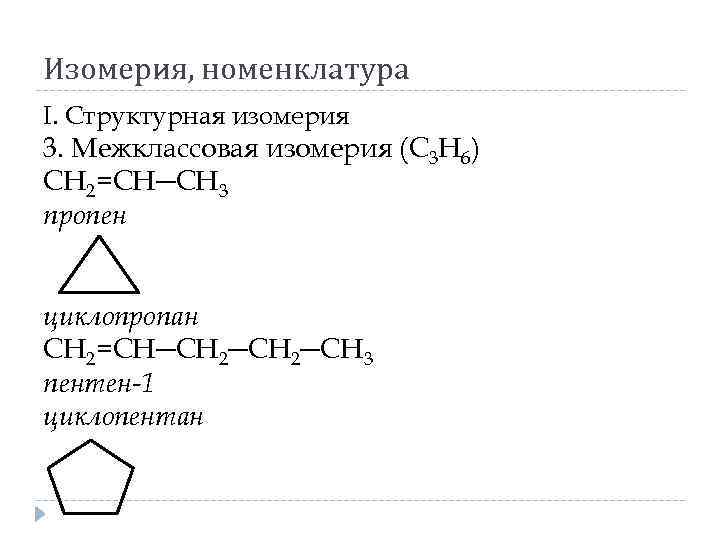 Изомерия, номенклатура I. Структурная изомерия 3. Межклассовая изомерия (С 3 Н 6) СН 2=СН─СН 3 пропен циклопропан СН 2=СН─СН 2─СН 3 пентен-1 циклопентан
Изомерия, номенклатура I. Структурная изомерия 3. Межклассовая изомерия (С 3 Н 6) СН 2=СН─СН 3 пропен циклопропан СН 2=СН─СН 2─СН 3 пентен-1 циклопентан
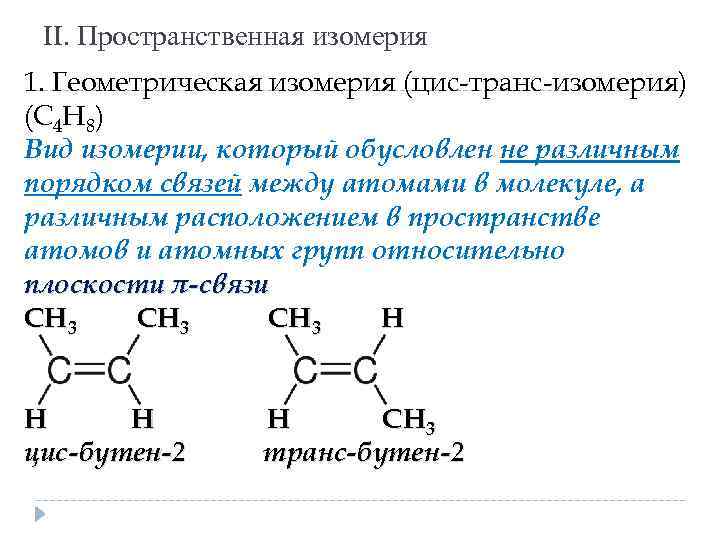 II. Пространственная изомерия 1. Геометрическая изомерия (цис-транс-изомерия) (С 4 Н 8) Вид изомерии, который обусловлен не различным порядком связей между атомами в молекуле, а различным расположением в пространстве атомов и атомных групп относительно плоскости π-связи СН 3 Н Н Н цис-бутен-2 Н СН 3 транс-бутен-2
II. Пространственная изомерия 1. Геометрическая изомерия (цис-транс-изомерия) (С 4 Н 8) Вид изомерии, который обусловлен не различным порядком связей между атомами в молекуле, а различным расположением в пространстве атомов и атомных групп относительно плоскости π-связи СН 3 Н Н Н цис-бутен-2 Н СН 3 транс-бутен-2
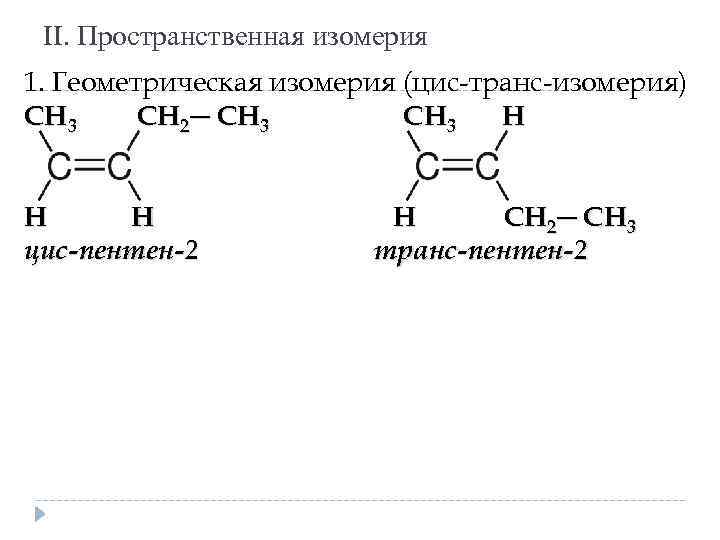 II. Пространственная изомерия 1. Геометрическая изомерия (цис-транс-изомерия) СН 3 СН 2─ СН 3 Н Н Н цис-пентен-2 Н СН 2─ СН 3 транс-пентен-2
II. Пространственная изомерия 1. Геометрическая изомерия (цис-транс-изомерия) СН 3 СН 2─ СН 3 Н Н Н цис-пентен-2 Н СН 2─ СН 3 транс-пентен-2
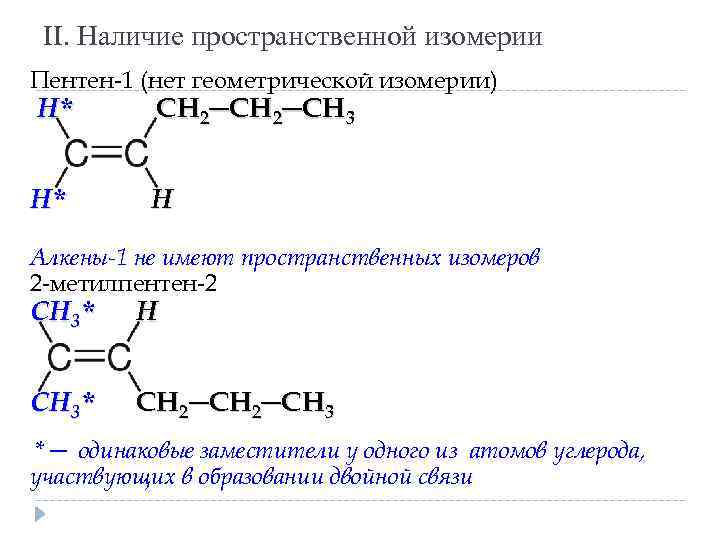 II. Наличие пространственной изомерии Пентен-1 (нет геометрической изомерии) Н* СН 2─СН 3 Н* Н Алкены-1 не имеют пространственных изомеров 2 -метилпентен-2 СН 3* Н СН 3* СН 2─СН 3 * ─ одинаковые заместители у одного из атомов углерода, участвующих в образовании двойной связи
II. Наличие пространственной изомерии Пентен-1 (нет геометрической изомерии) Н* СН 2─СН 3 Н* Н Алкены-1 не имеют пространственных изомеров 2 -метилпентен-2 СН 3* Н СН 3* СН 2─СН 3 * ─ одинаковые заместители у одного из атомов углерода, участвующих в образовании двойной связи
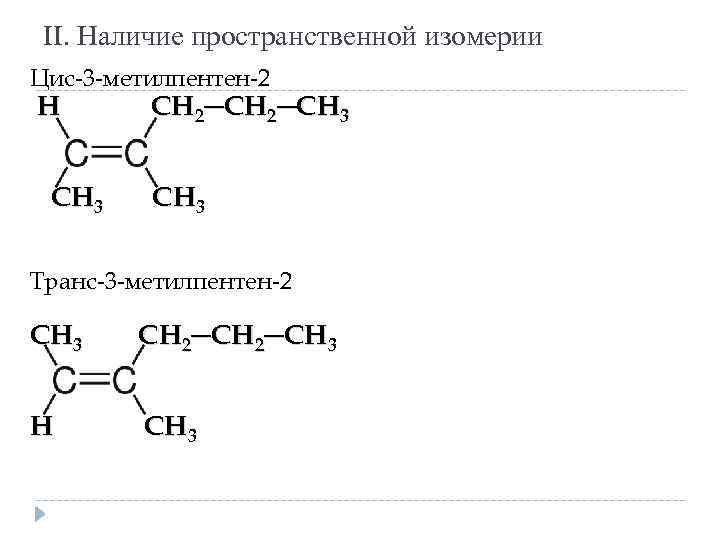 II. Наличие пространственной изомерии Цис-3 -метилпентен-2 Н СН 3 СН 2─СН 3 Транс-3 -метилпентен-2 СН 3 СН 2─СН 3 Н СН 3
II. Наличие пространственной изомерии Цис-3 -метилпентен-2 Н СН 3 СН 2─СН 3 Транс-3 -метилпентен-2 СН 3 СН 2─СН 3 Н СН 3
 Алгоритм 1. Показать атомы углерода двойной связи, соблюдая реальную геометрию молекулы 2. «Пристроить» все остальные атомы и атомные группы 3. Назвать полученный изомер или указать, что цис-транс-изомерия невозможна
Алгоритм 1. Показать атомы углерода двойной связи, соблюдая реальную геометрию молекулы 2. «Пристроить» все остальные атомы и атомные группы 3. Назвать полученный изомер или указать, что цис-транс-изомерия невозможна
 Методы получения алкенов Промышленные (I) и лабораторные (II)
Методы получения алкенов Промышленные (I) и лабораторные (II)
 I. Промышленные методы получения алкенов. 1. Дегидрирование алканов 450°C− 500°C СН 3−СН 3 ⇄ СН 2=СН 2 + H 2 этан Cr 2 O 3* этен или этилен * – другие катализаторы – Ni, Pd, Pt 450°C− 500°C СH 3−СН−СН 3 ⇄ │ Cr 2 O 3 СН 3 СH 2=С−СН 3 + H 2 (☻) │ СН 3 2 -метилпропан 2 -метилпропен изобутан изобутен (☻) – метод получения индивидуального вещества 450°C− 500°C СH 3−СН−СН 2−СН 3 ⇄ СH 3−С=СН−СН 2−СН 3+ H 2 │ Cr 2 O 3 │ СН 3 2 -метилпентан 2 -метилпентен-2
I. Промышленные методы получения алкенов. 1. Дегидрирование алканов 450°C− 500°C СН 3−СН 3 ⇄ СН 2=СН 2 + H 2 этан Cr 2 O 3* этен или этилен * – другие катализаторы – Ni, Pd, Pt 450°C− 500°C СH 3−СН−СН 3 ⇄ │ Cr 2 O 3 СН 3 СH 2=С−СН 3 + H 2 (☻) │ СН 3 2 -метилпропан 2 -метилпропен изобутан изобутен (☻) – метод получения индивидуального вещества 450°C− 500°C СH 3−СН−СН 2−СН 3 ⇄ СH 3−С=СН−СН 2−СН 3+ H 2 │ Cr 2 O 3 │ СН 3 2 -метилпентан 2 -метилпентен-2
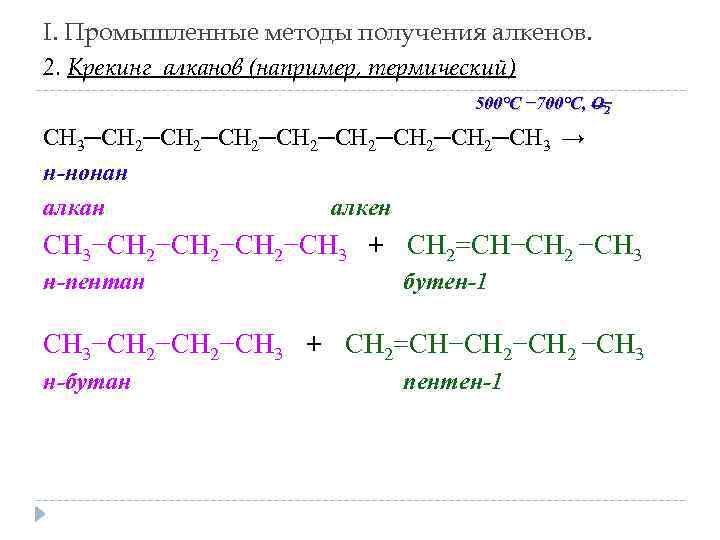 I. Промышленные методы получения алкенов. 2. Крекинг алканов (например, термический) 500°C − 700°C, О 2 СН 3─СН 2─СН 2─СН 3 → н-нонан алкен СН 3−СН 2−СН 3 + СН 2=СН−СН 2 −СН 3 н-пентан бутен-1 СН 3−СН 2−СН 3 + СН 2=СН−СН 2 −СН 3 н-бутан пентен-1
I. Промышленные методы получения алкенов. 2. Крекинг алканов (например, термический) 500°C − 700°C, О 2 СН 3─СН 2─СН 2─СН 3 → н-нонан алкен СН 3−СН 2−СН 3 + СН 2=СН−СН 2 −СН 3 н-пентан бутен-1 СН 3−СН 2−СН 3 + СН 2=СН−СН 2 −СН 3 н-бутан пентен-1
 II. Лабораторные методы получения алкенов. Все лабораторные методы получения алкенов основаны на реакциях отщепления или элиминирования (Е) 1. Дегалогенирование дигалогеналканов, в молекуле которых оба атома галогена связаны с двумя соседними атомами углерода – атомами углерода «будущей» двойной связи Zn, C 2 H 5 OH* СН 2−СН−СН 3 → CH 2=CH−СН 2−CH−CH 3 + Zn. Br 2* │ │ Br Br СН 3 1, 2 -дибром-4 -метилпентан 4 -метилпентен-1 *Mg, C 2 H 5−O−C 2 H 5 (Mg. Br 2) Условия проведения реакции дегалогенирования: Znпыль, спирт или Zn, C 2 H 5 OH* Mgстружка, абсолютный эфир или Mg, C 2 H 5−O−C 2 H 5
II. Лабораторные методы получения алкенов. Все лабораторные методы получения алкенов основаны на реакциях отщепления или элиминирования (Е) 1. Дегалогенирование дигалогеналканов, в молекуле которых оба атома галогена связаны с двумя соседними атомами углерода – атомами углерода «будущей» двойной связи Zn, C 2 H 5 OH* СН 2−СН−СН 3 → CH 2=CH−СН 2−CH−CH 3 + Zn. Br 2* │ │ Br Br СН 3 1, 2 -дибром-4 -метилпентан 4 -метилпентен-1 *Mg, C 2 H 5−O−C 2 H 5 (Mg. Br 2) Условия проведения реакции дегалогенирования: Znпыль, спирт или Zn, C 2 H 5 OH* Mgстружка, абсолютный эфир или Mg, C 2 H 5−O−C 2 H 5
 Правило Зайцева При отщеплении несимметричной молекулы H─X, (где H─X ⇔ H─Hal, H─OH, H─NH 2), группа ─X отщепляется «по месту» , т. е. от того атома С, с которым связана, атом ─H отщепляется от соседнего атома углерода, с которым связано наименьшее число атомов водорода; такой атом углерода – наименее гидрогенизированный.
Правило Зайцева При отщеплении несимметричной молекулы H─X, (где H─X ⇔ H─Hal, H─OH, H─NH 2), группа ─X отщепляется «по месту» , т. е. от того атома С, с которым связана, атом ─H отщепляется от соседнего атома углерода, с которым связано наименьшее число атомов водорода; такой атом углерода – наименее гидрогенизированный.
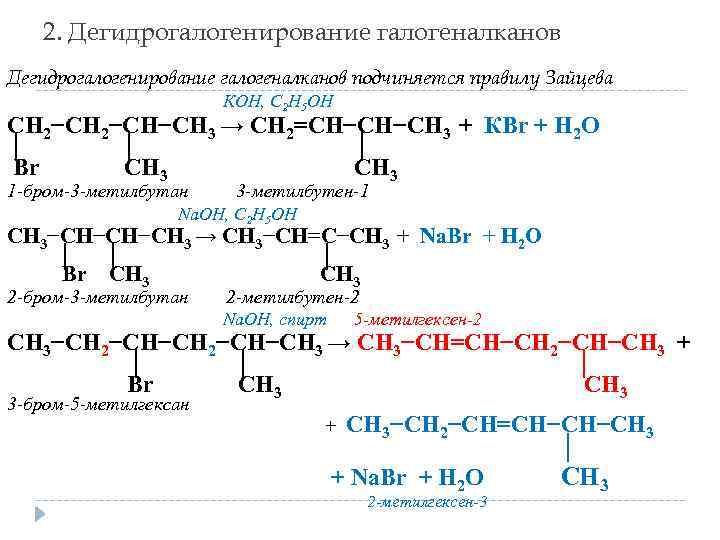 2. Дегидрогалогенирование галогеналканов подчиняется правилу Зайцева КОН, C 2 H 5 OH СН 2−СН−СН 3 → CH 2=CH−CH−CH 3 + КBr + H 2 O │ │ │ Br СН 3 1 -бром-3 -метилбутан 3 -метилбутен-1 Na. ОН, C 2 H 5 OH СН 3−СН−СН−СН 3 → CH 3−CH=C−CH 3 + Na. Br + H 2 O │ │ │ Br СН 3 2 -бром-3 -метилбутан 2 -метилбутен-2 Na. ОН, спирт 5 -метилгексен-2 СН 3−СН 2−СН−СН 3 → CH 3−CH=CН−CH 2−СН−СН 3 + │ │ │ Br СН 3 3 -бром-5 -метилгексан CH 3−CH 2−CН=CH−СН−СН 3 │ + Na. Br + H 2 O СН 3 + 2 -метилгексен-3
2. Дегидрогалогенирование галогеналканов подчиняется правилу Зайцева КОН, C 2 H 5 OH СН 2−СН−СН 3 → CH 2=CH−CH−CH 3 + КBr + H 2 O │ │ │ Br СН 3 1 -бром-3 -метилбутан 3 -метилбутен-1 Na. ОН, C 2 H 5 OH СН 3−СН−СН−СН 3 → CH 3−CH=C−CH 3 + Na. Br + H 2 O │ │ │ Br СН 3 2 -бром-3 -метилбутан 2 -метилбутен-2 Na. ОН, спирт 5 -метилгексен-2 СН 3−СН 2−СН−СН 3 → CH 3−CH=CН−CH 2−СН−СН 3 + │ │ │ Br СН 3 3 -бром-5 -метилгексан CH 3−CH 2−CН=CH−СН−СН 3 │ + Na. Br + H 2 O СН 3 + 2 -метилгексен-3
 3. Дегидратация (внутримолекулярная) предельных одноатомных спиртов подчиняется правилу Зайцева H 2 SO 4 конц. , t°>150°C* СН 2−СН−СН 3 → CH 2=CH−CH−CH 3 + H 2 O │ │ │ ОН СН 3 3 -метилбутанол-1 3 -метилбутен-1 H 2 SO 4 конц. , t°=180°C СН 3−СН−СН−СН 3 → CH 3−CH=C−CH 3 + H 2 O │ │ │ ОН СН 3 3 -метилбутанол-2 2 -метилбутен-2 Al 2 O 3, t°>350°C 5 -метилгексен-2 СН 3−СН 2−СН−СН 3 → CH 3−CH=CН−CH 2−СН−СН 3 + │ │ │ ОН СН 3 5 -метилгексанол-3 + H 2 O + CH 3−CH 2−CН=CH−СН−СН 3 │ * Другие условия проведения реакции: 2 -метилгексен-3 H 2 SO 4 конц. , t°=180°C; Al 2 O 3, t°>350°C; Al 2 O 3, t°=400°C СН 3
3. Дегидратация (внутримолекулярная) предельных одноатомных спиртов подчиняется правилу Зайцева H 2 SO 4 конц. , t°>150°C* СН 2−СН−СН 3 → CH 2=CH−CH−CH 3 + H 2 O │ │ │ ОН СН 3 3 -метилбутанол-1 3 -метилбутен-1 H 2 SO 4 конц. , t°=180°C СН 3−СН−СН−СН 3 → CH 3−CH=C−CH 3 + H 2 O │ │ │ ОН СН 3 3 -метилбутанол-2 2 -метилбутен-2 Al 2 O 3, t°>350°C 5 -метилгексен-2 СН 3−СН 2−СН−СН 3 → CH 3−CH=CН−CH 2−СН−СН 3 + │ │ │ ОН СН 3 5 -метилгексанол-3 + H 2 O + CH 3−CH 2−CН=CH−СН−СН 3 │ * Другие условия проведения реакции: 2 -метилгексен-3 H 2 SO 4 конц. , t°=180°C; Al 2 O 3, t°>350°C; Al 2 O 3, t°=400°C СН 3
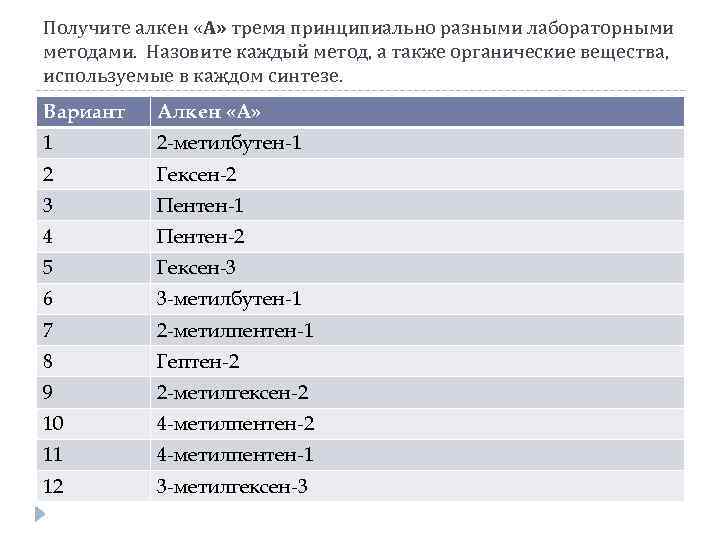 Получите алкен «А» тремя принципиально разными лабораторными методами. Назовите каждый метод, а также органические вещества, используемые в каждом синтезе. Вариант Алкен «А» 1 2 -метилбутен-1 2 Гексен-2 3 Пентен-1 4 Пентен-2 5 Гексен-3 6 3 -метилбутен-1 7 2 -метилпентен-1 8 Гептен-2 9 2 -метилгексен-2 10 4 -метилпентен-2 11 4 -метилпентен-1 12 3 -метилгексен-3
Получите алкен «А» тремя принципиально разными лабораторными методами. Назовите каждый метод, а также органические вещества, используемые в каждом синтезе. Вариант Алкен «А» 1 2 -метилбутен-1 2 Гексен-2 3 Пентен-1 4 Пентен-2 5 Гексен-3 6 3 -метилбутен-1 7 2 -метилпентен-1 8 Гептен-2 9 2 -метилгексен-2 10 4 -метилпентен-2 11 4 -метилпентен-1 12 3 -метилгексен-3
 Приведите структурную формулу алкена «А» , а также структурную формулу и название одного межклассового изомера алкена «А» . Получите алкен «А» тремя принципиально разными лабораторными методами. Назовите каждый метод, а также органические вещества, используемые в каждом синтезе. Вариант Алкен «А» 1 2 -метилбутен-1 9 2 -метилгексен-2 2 Гексен-2 10 4 -метилпентен-2 3 3 -метилпентен-2 11 4 -метилпентен-1 4 Пентен-2 12 3 -метилгексен-3 5 3 -метилгексен-2 13 2 -метилгексен-2 6 3 -метилбутен-1 14 4 -метилпентен-2 7 2 -метилпентен-1 15 4 -метилпентен-1 8 Гептен-2 16 Пентен-1
Приведите структурную формулу алкена «А» , а также структурную формулу и название одного межклассового изомера алкена «А» . Получите алкен «А» тремя принципиально разными лабораторными методами. Назовите каждый метод, а также органические вещества, используемые в каждом синтезе. Вариант Алкен «А» 1 2 -метилбутен-1 9 2 -метилгексен-2 2 Гексен-2 10 4 -метилпентен-2 3 3 -метилпентен-2 11 4 -метилпентен-1 4 Пентен-2 12 3 -метилгексен-3 5 3 -метилгексен-2 13 2 -метилгексен-2 6 3 -метилбутен-1 14 4 -метилпентен-2 7 2 -метилпентен-1 15 4 -метилпентен-1 8 Гептен-2 16 Пентен-1


