Алкены.ppt
- Количество слайдов: 19

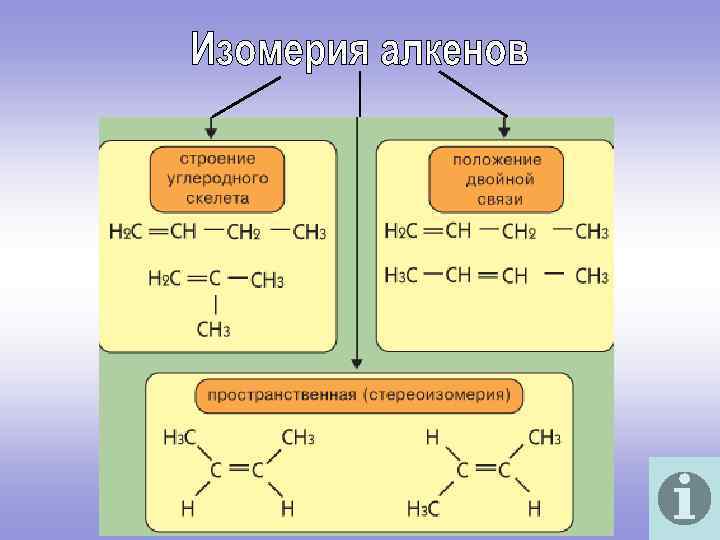
 Алкены (этиленовые углеводороды, олефины) – непредельные алифатические углеводороды, молекулы которых содержат двойную связь. Общая формула ряда алкенов Сn. H 2 n Простейшие представители: С 2 Н 4 С 3 Н 6 СН 2=СН 2=СН–СН 3 этилен (этен) пропилен (пропен) С 4 Н 8 СН 2=СН–СН 2–СН 3 бутилен-1 (бутен-1)
Алкены (этиленовые углеводороды, олефины) – непредельные алифатические углеводороды, молекулы которых содержат двойную связь. Общая формула ряда алкенов Сn. H 2 n Простейшие представители: С 2 Н 4 С 3 Н 6 СН 2=СН 2=СН–СН 3 этилен (этен) пропилен (пропен) С 4 Н 8 СН 2=СН–СН 2–СН 3 бутилен-1 (бутен-1)
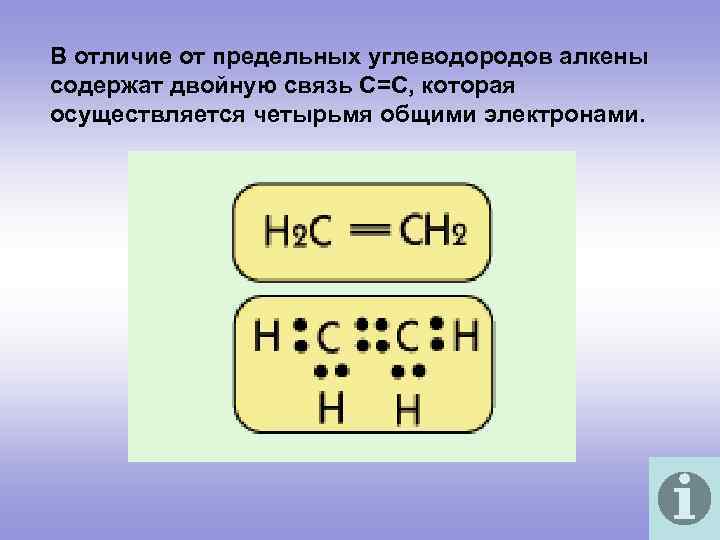 В отличие от предельных углеводородов алкены содержат двойную связь С=С, которая осуществляется четырьмя общими электронами.
В отличие от предельных углеводородов алкены содержат двойную связь С=С, которая осуществляется четырьмя общими электронами.
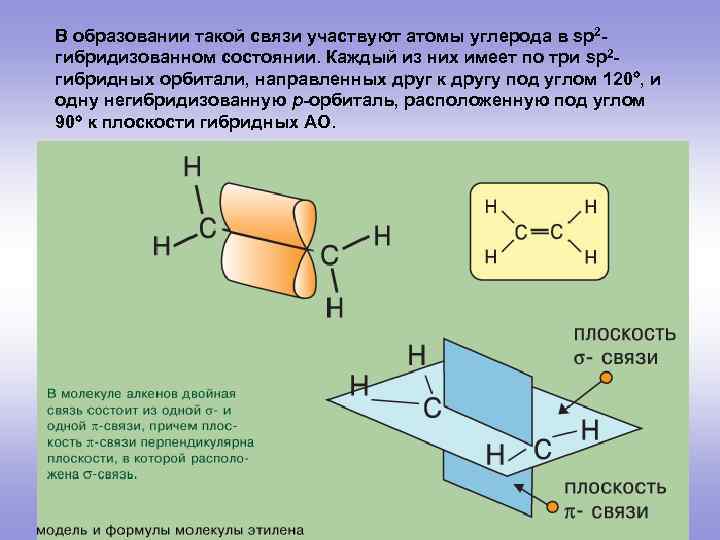 В образовании такой связи участвуют атомы углерода в sp 2 гибридизованном состоянии. Каждый из них имеет по три sp 2 гибридных орбитали, направленных друг к другу под углом 120 , и одну негибридизованную р-орбиталь, расположенную под углом 90 к плоскости гибридных АО.
В образовании такой связи участвуют атомы углерода в sp 2 гибридизованном состоянии. Каждый из них имеет по три sp 2 гибридных орбитали, направленных друг к другу под углом 120 , и одну негибридизованную р-орбиталь, расположенную под углом 90 к плоскости гибридных АО.
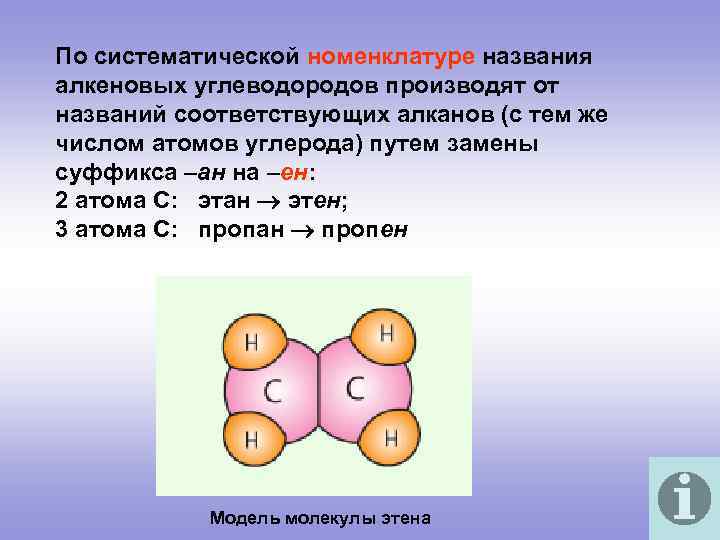 По систематической номенклатуре названия алкеновых углеводородов производят от названий соответствующих алканов (с тем же числом атомов углерода) путем замены суффикса –ан на –ен: 2 атома С: этан этен; 3 атома С: пропан пропен Модель молекулы этена
По систематической номенклатуре названия алкеновых углеводородов производят от названий соответствующих алканов (с тем же числом атомов углерода) путем замены суффикса –ан на –ен: 2 атома С: этан этен; 3 атома С: пропан пропен Модель молекулы этена
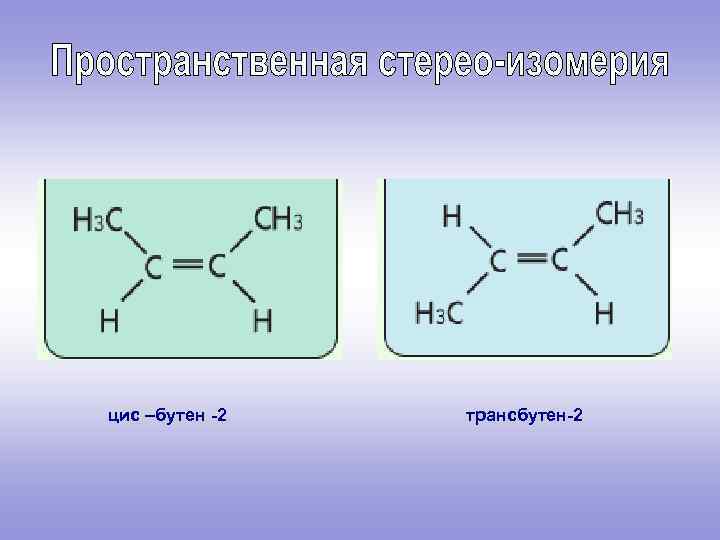 цис –бутен -2 трансбутен-2
цис –бутен -2 трансбутен-2
 Физические свойства алкенов закономерно изменяются в гомологическом ряду: от С 2 Н 4 до С 4 Н 8 – газы, начиная с С 5 Н 10 –жидкости, с С 18 Н 36 – твердые вещества. Алкены практически нерастворимы в воде, но хорошо растворяются в органических растворителях.
Физические свойства алкенов закономерно изменяются в гомологическом ряду: от С 2 Н 4 до С 4 Н 8 – газы, начиная с С 5 Н 10 –жидкости, с С 18 Н 36 – твердые вещества. Алкены практически нерастворимы в воде, но хорошо растворяются в органических растворителях.
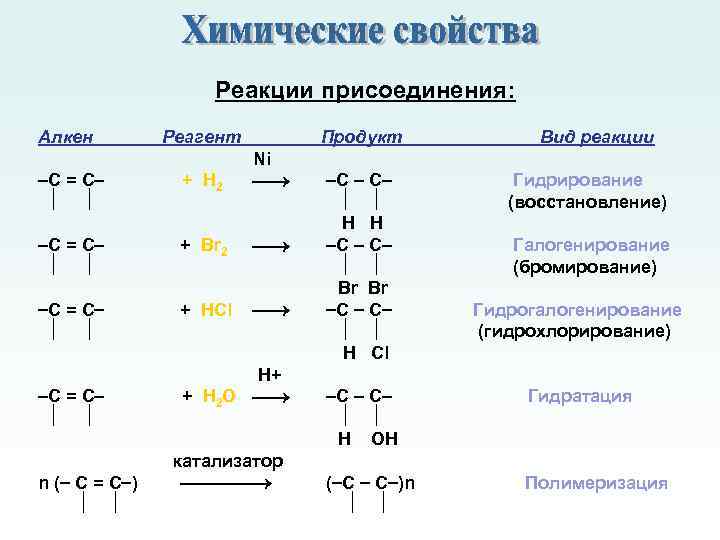 Реакции присоединения: Алкен Реагент Продукт С = С + Н 2 Ni С = С + Br 2 С = С + HCl С = С n ( С = С ) H+ + H 2 О катализатор С С Н Н С С Br Br С С H Cl Вид реакции Гидрирование (восстановление) Галогенирование (бромирование) Гидрогалогенирование (гидрохлорирование) С С H ОН Гидратация ( С С )n Полимеризация
Реакции присоединения: Алкен Реагент Продукт С = С + Н 2 Ni С = С + Br 2 С = С + HCl С = С n ( С = С ) H+ + H 2 О катализатор С С Н Н С С Br Br С С H Cl Вид реакции Гидрирование (восстановление) Галогенирование (бромирование) Гидрогалогенирование (гидрохлорирование) С С H ОН Гидратация ( С С )n Полимеризация
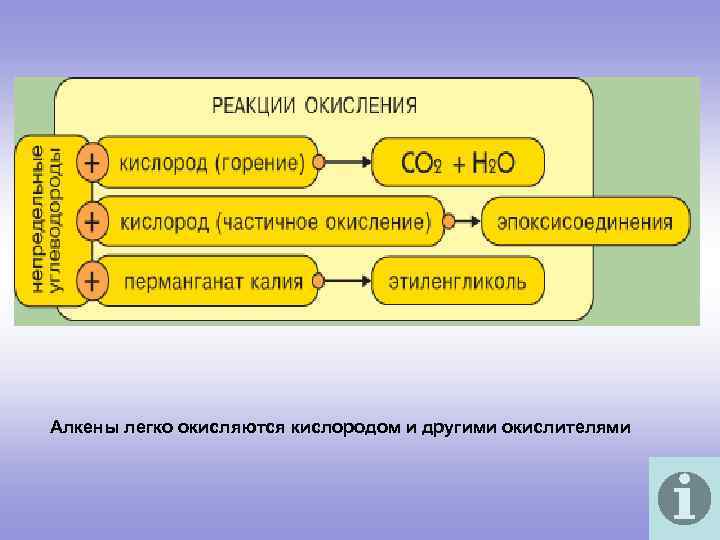 Алкены легко окисляются кислородом и другими окислителями
Алкены легко окисляются кислородом и другими окислителями
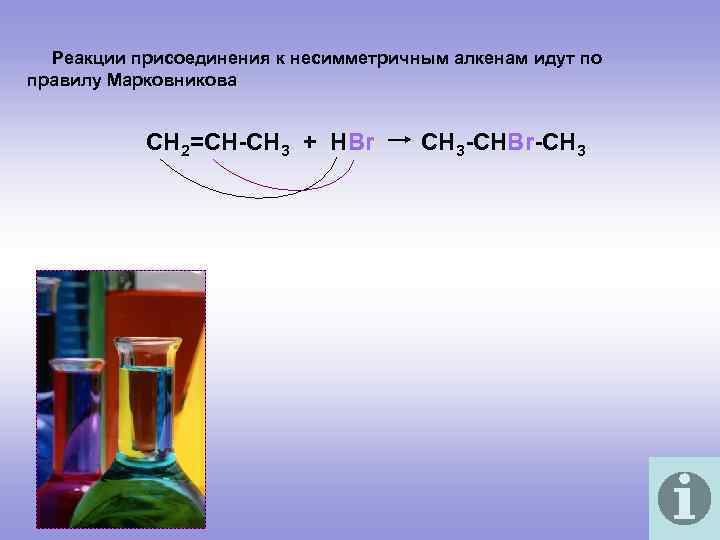 Реакции присоединения к несимметричным алкенам идут по правилу Марковникова СН 2=СН-СН 3 + НВr CH 3 -CHBr-CH 3
Реакции присоединения к несимметричным алкенам идут по правилу Марковникова СН 2=СН-СН 3 + НВr CH 3 -CHBr-CH 3
 Важнейшей реакцией непредельных углеводородов является реакция полимеризации –соединение молекул углеводородов друг с другом с образованием длинных цепей. С 2 Н 4 +… (-СН 2 -)n Полимеризация этилена
Важнейшей реакцией непредельных углеводородов является реакция полимеризации –соединение молекул углеводородов друг с другом с образованием длинных цепей. С 2 Н 4 +… (-СН 2 -)n Полимеризация этилена
 Реакции изомеризации Алкены вступают в реакцию изомеризации при нагревании в присутствии катализаторов (Al 2 O 3). Изомеризация алкенов приводит или к перемещению – связи: катализатор, t СН 2=СН СН 2 СН 3 СН =СН СН 3 бутен-1 бутен-2 или к перестройке углеродного скелета: катализатор, t СН 2=СН СН 2 СН 3 СН 2=С СН 3 бутен-1 2 -метилпропен (изобутилен)
Реакции изомеризации Алкены вступают в реакцию изомеризации при нагревании в присутствии катализаторов (Al 2 O 3). Изомеризация алкенов приводит или к перемещению – связи: катализатор, t СН 2=СН СН 2 СН 3 СН =СН СН 3 бутен-1 бутен-2 или к перестройке углеродного скелета: катализатор, t СН 2=СН СН 2 СН 3 СН 2=С СН 3 бутен-1 2 -метилпропен (изобутилен)
 Крекинг алканов: Cn. H 2 n+2 Cm. H 2 m + Cp. H 2 p+2, (где m + p = n) Например: С 7 Н 16 СН 3 СН=СН 2 + С 4 Н 10
Крекинг алканов: Cn. H 2 n+2 Cm. H 2 m + Cp. H 2 p+2, (где m + p = n) Например: С 7 Н 16 СН 3 СН=СН 2 + С 4 Н 10
 Дегидратация спиртов (лабораторный способ) при t > 150 C в присутствии водоотнимающих реагентов H 2 SO 4 CH 3 CH 2 OH CH 2=CH 2 + H 2 O H 2 SO 4 СH 3 CHOH CH 2 CH 3 CH=CH CH 3 + H 2 O
Дегидратация спиртов (лабораторный способ) при t > 150 C в присутствии водоотнимающих реагентов H 2 SO 4 CH 3 CH 2 OH CH 2=CH 2 + H 2 O H 2 SO 4 СH 3 CHOH CH 2 CH 3 CH=CH CH 3 + H 2 O
 Дегидрогалогенирование моногалогеналканов при действии спиртового_раствора щелочи : СН 3 СНBr CH 3 + KOH (спирт) CH 3 CH=CH 2 + KBr + H 2 O Дегалогенирование дигалогеналканов, имеющих атомы галогена у соседних атомов углерода, при действии активных металлов: СH 2 Br CH 3 + Mg CH 2=CH CH 3 + Mg. Br 2 Дегидрирование алканов при 500 С Cr 2 O 3 СH 3 CH CH 2 CH 3 CH =CH 2 + Н 2 Н Н
Дегидрогалогенирование моногалогеналканов при действии спиртового_раствора щелочи : СН 3 СНBr CH 3 + KOH (спирт) CH 3 CH=CH 2 + KBr + H 2 O Дегалогенирование дигалогеналканов, имеющих атомы галогена у соседних атомов углерода, при действии активных металлов: СH 2 Br CH 3 + Mg CH 2=CH CH 3 + Mg. Br 2 Дегидрирование алканов при 500 С Cr 2 O 3 СH 3 CH CH 2 CH 3 CH =CH 2 + Н 2 Н Н
 Получение спиртов, альдегидов, кислот Этилен –для ускорения созревания плодов Получение полимеров и пластмасс Получение СК (резины)
Получение спиртов, альдегидов, кислот Этилен –для ускорения созревания плодов Получение полимеров и пластмасс Получение СК (резины)
 Почему алкены относят к непредельным углеводородам? Чем алкены отличаются от алканов (по составу и строению молекул) ? Какие виды изомерии есть у алкенов? Какие химические свойства характерны для алкенов? Сформулируйте правило Марковникова и правило Зайцева. Как получают алкены в промышленности? Каковы лабораторные способы получения алкенов? Назовите основные области применения алкенов. ТЕСТ
Почему алкены относят к непредельным углеводородам? Чем алкены отличаются от алканов (по составу и строению молекул) ? Какие виды изомерии есть у алкенов? Какие химические свойства характерны для алкенов? Сформулируйте правило Марковникова и правило Зайцева. Как получают алкены в промышленности? Каковы лабораторные способы получения алкенов? Назовите основные области применения алкенов. ТЕСТ
 ОТВЕТЫ: 1) 1 2) 3 3) 3 4) 2 5) 2 6) 1 7) 4 8) 2 9) 2 10)2
ОТВЕТЫ: 1) 1 2) 3 3) 3 4) 2 5) 2 6) 1 7) 4 8) 2 9) 2 10)2


